Opti kurs fizike hemije I Fond asova 44




























- Slides: 32

Opšti kurs fizičke hemije I Fond časova: 4+4 Profesor: Ivanka Holclajtner-Antunović Soba 374, prizemlje, blok C Email: ivanka@ffh. bg. ac. yu Website Fakulteta: www. ffh. bg. ac. yu/OKFH Asistenti: Isidora Cekić, Miroslav Ristić i Igor Pašti Konsultacije: Svaki dan, posle 9 h uz usmeni dogovor ili putem e-maila Predavanje: Utorak, 12: 00 -14: 00, Amfiteatar za Fakulteta, Blok C, prizemlje Interaktivna nastava: Ponedeljak, 14: 00 -16: 00, Amfiteatar za Fakulteta Vežbe: Po grupama po rasporedu, vežbaonica 263, I podrum

Cilj predmeta Opšti kurs fizičke hemije: Eksperimentalno i teorijski proučava rezličite oblike materije preko njihovih makroskopskih osobina i njihovu interakciju sa energijom # Ovaj kurs služi kao uvod hemijskoj termodinamici, omogućavajući razumevanje bazičnih principa, zakona i teorija fizičke hemije uopšte, odnosno pojedinih njenih disciplina kao što su hemijska kinetika, elektrohemija, spektrohemija, fizička hemija fluida, biofizička hemija i dr. # Kroz ovaj kurs treba da naučite da koristite sopstvenu logiku i zaključivanje pri rešavanju problema i izvođenju jednačina prema postavljenom modelu, tako da jednačine daju jasnu sliku fizičkih pojava koje proučavate. # Pored toga treba da razvijete sposobnost da rešavate kvantitativne probleme. Treba da naučite kako da primenjujete matematiku u hemiji i fizičkoj hemiji. To ćemo činiti kroz računske zadatke.

Sadržaj predmeta Opšti kurs fizičke hemije I GASOVITO STANJE: IDEALNO GASNO STANJE REALNO GASNO STANJE KINETIČKA TEORIJA GASOVA n OSNOVI TERMODINAMIKEosnovni pojmovi hemijske termodinamike n

Kolokvijumi: I kolokvijum: Osnovna merenja 1. Određivanje gustine tečnosti 2. Određivanje indeksa prelamanja 3. Određivanje viskoznosti tečnosti 4. Određivanje površinskog napona 5. Određivanje ugla skretanja optički aktivnih supstancija II kolokvijum: Gasovi 6. Određivanje molarne mase Viktor-Majerovom metodom III kolokvijum: Termodinamika i ravnoteža 7. Određivanje toplote rastvaranja 8. Određivanje toplote sagorevanja 9. Određivanje toplote topljenja leda 10. Određivanje konstante ravnoteže mutarotacije glukoze Radna sveska!

Polaganje ispita-usmeno Način ocenjivanja Posećivanje predavanja 5 bodova: 50 -60% -1, 60 -70%-2, 70 -80 -3, 80 -90%-4 i 90 -100 -5 Interakt. nastava i domaći: 5 bodova Kolokvijumi vežbe: 15, svaki po 5 (1 bod-6, 2 b. -7, 3 b. -8, 4 b. -9, 5 b. -10)-Minimalno 3 boda Vežbe: 5, svaka po 0, 5 Nastavni kolokv. 40, svaki po 20 Ocena Ispit 30 51 -60 bodova 6 61 -70 bodova 7 71 -80 bodova 8 81 -90 bodova 9 91 -100 bodova 10 70

Literatura Udžbenici: 1. Holclajtner-Antrunović Ivanka, Opšti kurs fizičke hemije, Zavod za izdavanje udžbenika, Beograd, 2000. 2. S. Đorđević, V. Dražić, Fizička hemija, Beograd, Fizička hemija, Tehnološko-metalurški fakultet, Beograd, 2002. 3. Atkins, P. W. & de Paula, J. Physical Chemistry, 7 th Edition. W. H. Freeman & Co. , New York, 2002. (6. i ostala izdanja Atkinsovog udžbenika) 4. I. Levine, Physical Chemistry, New York, 1995. 5. 6. 7. 8. 9. F. Daniels, R. Alberty, Physical Chemistry, New York, 1975. S. Gledston, Udžbenik fizičke hemije, Beograd, 1967. W. Moore, Fizička hemija, Beograd, 1967. J. Egert, I. Hok, G. M. Švab, Udžbenik fizičke hemije, Beograd, 1966. R. Brdička, Osnove fizičke hemije, Zagreb, 1969. Praktikumi i Zbirke: 1. R. Konjević i sar. , Praktikum iz fizičke hemije za studente hemije 2. U. Mioč, R. Hercigonja, Zbirka zadataka iz opšteg kursa fizičke hemije


Šta je fizička hemija? FIZIČKA HEMIJA proučava fizičke osnove i definiše fizičke principe koji određuju osobine i ponašanje materije u različitim agregatnim stanjima u zavisnosti od hemijskih osobina i uslova pod kojim se materija nalazi kao i njihovo uzajamno dejstvo. Izvodeći na egzaktnoj osnovi najopštije relacije, fizička hemija sa ostalim posebno prirodnim naukama doprinosi jedinstvenom pogledu na suštinu sveta, a razvija se uporedo sa razvojem eksperimentalnih tehnika, metoda i tehnologije.

ATOMISTIKA HEMIJSKA I STATISTIČKA TERMODINAMIKA SPEKTROHEMIJA

ELEKTROHEMIJA RADIOHEMIJA HEMIJSKA KINETIKA

FIZIČKA HEMIJA FLUIDA FIZIČKA HEMIJA ČVRSTOG STANJA KVANTNA HEMIJA I MOLEKULSKE STRUKTURE

BIOFIZIČKA HEMIJA ŽIVOTNE SREDINE

FIZIČKA HEMIJA PLAZME FIZIČKA HEMIJA MATERIJALA…

Počeci fizičke hemije u svetu 1887. Zeitschrift fur physikalische Chemie Wilhelm Ostwald Svante Arrhenius Jacobus Van’t Hoff

Robert Boyle (1627 -1691) Physico-Chemical Doubts and Paradoxes (XVII v. ) I. Newton (XVIII v. ) J. Black, A. Lavoisier (XIX v. ) M. Faraday, W. Allen Miller, Chemical Physics

M. V. Lomonosov • 1741 - Elementi matematičke hemije • 1752 - Uvod u pravu fizičku hemiju ”Fizička hemija je nauka koja objašnjava, na osnovu postavki i iskustava fizike, uzroke onoga čto se dečava u hemijskim operacijama u složenim telima” (1711 -1765)

Počeci visokog školstva u Srbiji • 1838 -juna meseca osnovan Licej u Kragujevcu • 1844 -Licej se seli u Konak knjeginje Ljubice u Beogradu

1863 -Licej prerasta u Veliku školu 1903. god. početkom septembra dr. Miloje Stojiljković postavljen za docenta fizičke hemije Velika pijaca ispred Kapetan Mišinog zdanja

Velika škola je prerasla 1905. godine u Univerzitet u Beogradu

Prof. Stojiljković je bio upravnik Zavoda sa ratnim prekidima čitavih četrdeset godina. Prof. Miloje Stojiljković (1873 -1962)

Fizičkohemijski zavod 1908. Radomir Veljković u Zavodu 1922. Prof. Stojiljković ispred konduktometra

Prof. Pavle Savić rukovodi Zavodom od 1947. do 1966. (1909 -1994)

Nastavni plan Fizičkohemijske grupe iz 1947. Opšta fizika I Opšti kurs fizičke hemije Opšta fizika II Atomistika Radioaktivnost i fizika jezgr Matematika I Termohemija Matematika II Elektrohemija Neorganska hemija Specijalni kurs Organska hemija sa stereohemijom Analitička hemija Osnovni kurs mineralogije Diplomski rad Osnovi marksizma-lenjinizm Predvojnička obuka Strani jezik

1961. USELJENJE U NOVU ZGRADU

Obrazuju se katedre Instituta: n n n Katedra za opštu fizičku hemiju Katedra za radiohemiju Katedra za spektrohemiju (kasnije i fizičku hemiju plazme) Katedra za elektrohemiju i hemijsku kinetiku Katedra za molekulske sutrukture (kasnije Katedra za strukturu i dinamiku materije) 1990. nastaje Fakultet za fizičku hemiju

danas. . .

Agregatna stanja materije Četiri agregatna stanja materije: Gas: Ispunjava i zauzima oblik suda u kome se nalazi, slično tečnostima, sem što su čestice na tako velikim rastojanjima pa su interakcije između čestica minimalne. Prosečna energija po čestici reda 1 e. V. Gasovi su mešljivi i kompresibilni. Tečnosti: Ne ispunjavaju sud, ali uzimaju njegov oblik. Interakcije izražene, prosečna energija reda 10 -1 e. V, rastojanje između čestica nešto veće od njihovih dimenzija. Čvrsto: Ne ispunjava i ne uzima oblik suda. Čestice na rastojanjima vrlo bliskim njihovim dimenzijama. Interakcije vrlo izražene. Prosečna energija po čestici reda 10 -2 e. V. Gasna plazma: Više ili manje jonizovani gas gde je prosečna energija po čestici reda 10 e. V pa dolazi do neelastičnih sudara.

Stanje gasova Stanje svake supstancije se opisuje osobinama stanja. Osobine stanja izražavaju se parametrima stanja: V zapremina P pritisak T temperatura n količina supstancije (mol) Veza između parametara stanja predstavlja jednačinu stanja:

Pritisak predstavlja odnos između sile (u N) i površine (u m 2) na koju sila deluje: Pritisak gasa je rezultat ogromnog broja sudara molekula gasa sa zidom suda

Jedinice pritiska Ime Simbol Vrednost paskal bar atmosfera Torr mm živinog stuba funta po kvadratnom inču 1 1 1 1 N m-2, 1 kg m 1 s-2 105 Pa 101 325 Pa 133, 322 Pa 6, 894757 k. Pa Pa bar atm Torr mm. Hg psi

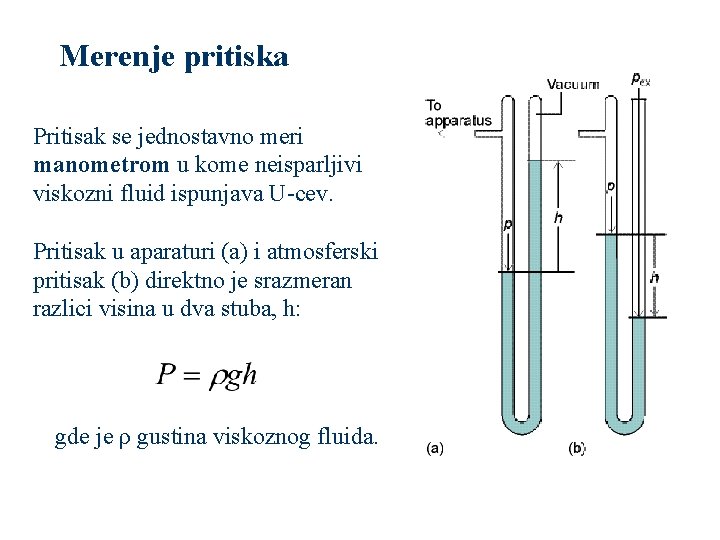
Merenje pritiska Pritisak se jednostavno meri manometrom u kome neisparljivi viskozni fluid ispunjava U-cev. Pritisak u aparaturi (a) i atmosferski pritisak (b) direktno je srazmeran razlici visina u dva stuba, h: gde je ρ gustina viskoznog fluida.

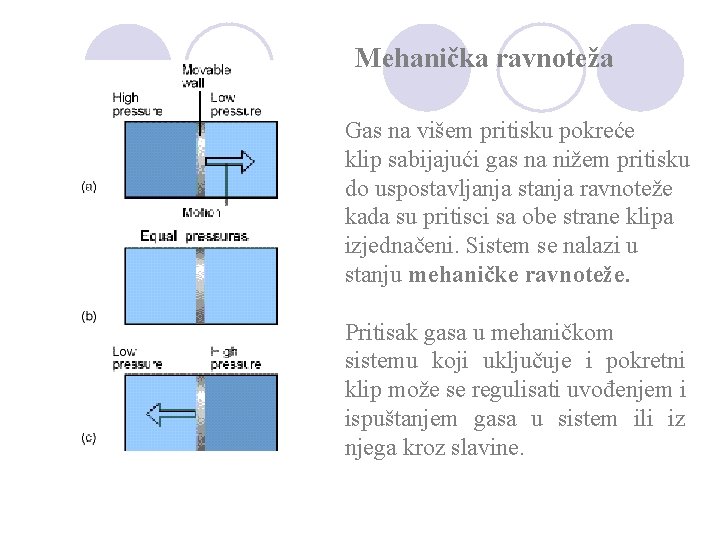
Mehanička ravnoteža Gas na višem pritisku pokreće klip sabijajući gas na nižem pritisku do uspostavljanja stanja ravnoteže kada su pritisci sa obe strane klipa izjednačeni. Sistem se nalazi u stanju mehaničke ravnoteže. Pritisak gasa u mehaničkom sistemu koji uključuje i pokretni klip može se regulisati uvođenjem i ispuštanjem gasa u sistem ili iz njega kroz slavine.