Opakovn z minula AO MO SD Kvantov chemick



























- Slides: 37

Opakování z minula

AO → MO → SD Kvantově chemický výpočet: 1) zvolíme vhodné atomové orbitály (tzv. bázi atomových orbitalů, basis set) 2) vypočítáme koeficienty v MO = Σci AO 3) zkonstruujeme výslednou vlnovou funkci z jednoelektronových MO jako Slaterův determinant

• množině AO se říká báze (basis set), z něj konstruujeme výsledné jednoelektronové MO • STO vs. GTO • kvalita báze – minimální báze – double zeta (triple, quadruple) – split valence double zeta – polarizační funkce

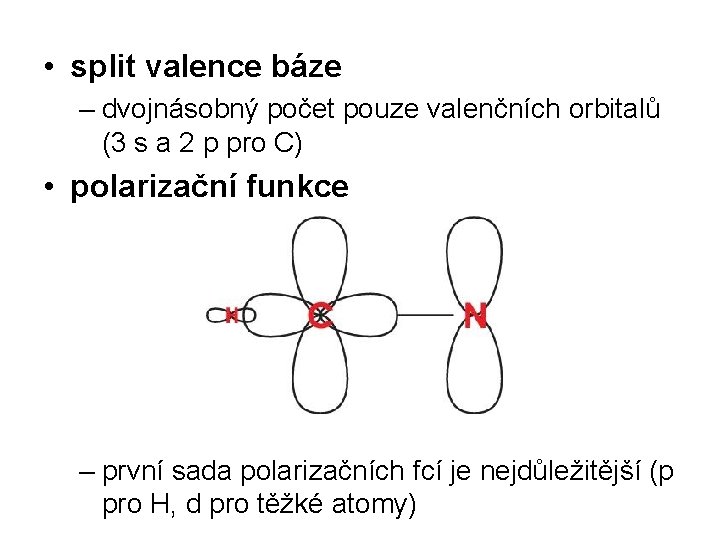
• split valence báze – dvojnásobný počet pouze valenčních orbitalů (3 s a 2 p pro C) • polarizační funkce – první sada polarizačních fcí je nejdůležitější (p pro H, d pro těžké atomy)

Nový materiál

• double zeta a polarizační – DZP – polarizační fce jsou ale jenom jednou – ano/ne na vodíky • difuzní funkce – malé exponenty – hodně rozprostřeny – potřeba když • volně vázané elektrony (např. anionty) • vlastnost závisí na „chvostu“ funkce (polarizovatelnost)

Optimalizace bází • míněno jak získám zeta exponenty • s a p funkce – variační HF výpočty atomů, optimalizace energie • polarizační fce jsou z definice neobsazené, proto není možno použít HF atomů – HF molekul – nebo korelační metody na atomech (vhodnější přístup)

Kontrakce bází • mnoho bázových fcí je použito pro popis energeticky důležitého core regionu, který je ale nedůležitý chemicky • zkonstantnit koeficienty před inner-core bázemi – už tedy nebudou v průběhu HF měněny • kontrakce vždy zvýší energii, ale zredukuje výpočetní náročnost • (10 s 4 p 1 d/4 s 1 p) → [3 s 2 p 1 d/2 s 1 p]

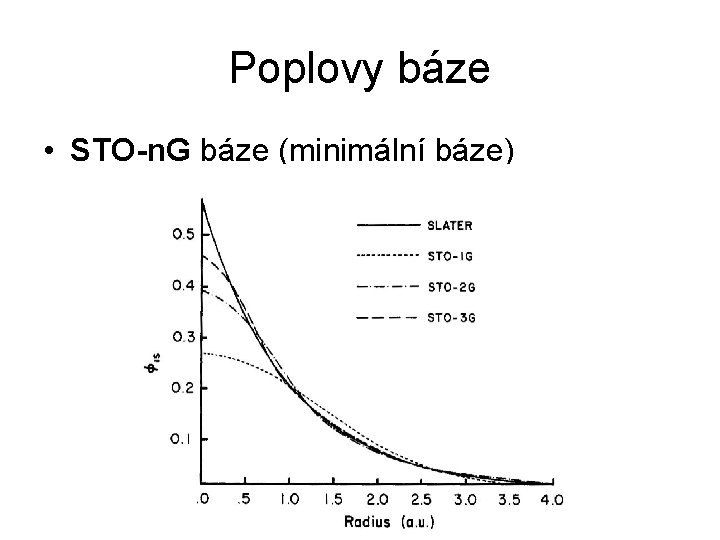
Poplovy báze • STO-n. G báze (minimální báze)

• k-nlm. G báze – split valence – k. . . kolik PGTO reprezentuje core orbitály – nlm. . . dvě čísla nl – double-valence, nlm – triple valence – hodnoty nlm udávají s- a p- fce v bázi, polarizační fce se píšou za G – omezení: s- a p- mají stejné exponenty !! – 3 -21 G • core je ze 3 PGTO • valence je popsán dvěma orbitály, jedním ze dvou PGTO a dalším samotným PGTO

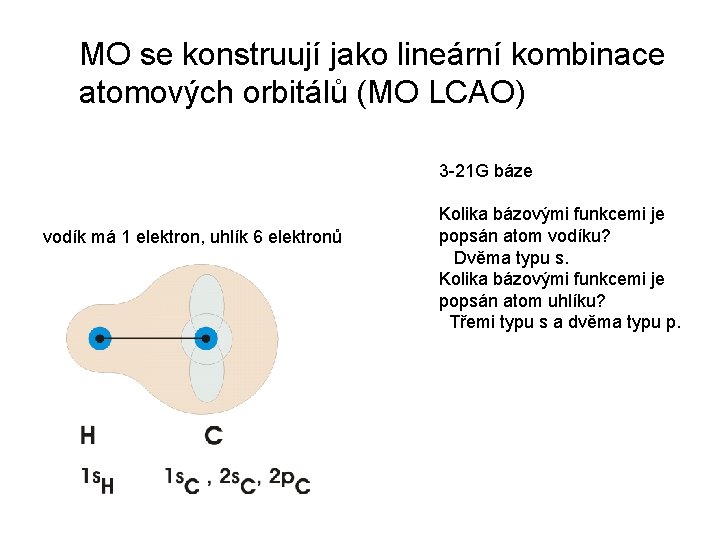
MO se konstruují jako lineární kombinace atomových orbitálů (MO LCAO) 3 -21 G báze vodík má 1 elektron, uhlík 6 elektronů Kolika bázovými funkcemi je popsán atom vodíku? Dvěma typu s. Kolika bázovými funkcemi je popsán atom uhlíku? Třemi typu s a dvěma typu p.

3 -21 G … vodík – 2 s, uhlík – 3 s a 2 p split-valence double zeta: ψ = c 11 s‘H+c 21 s‘‘H+c 31 s‘C+c 42 s‘C+c 52 s‘‘C+c 62 p‘C+c 72 p‘‘C spinorbitaly •

ψ = c 11 s‘H+c 21 s‘‘H+c 31 s‘C+c 42 s‘C+c 52 s‘‘C+c 62 p‘C+c 72 p‘‘C • a nyní se podíváme na atomové orbitály, tedy s. H, s. C a p. C • AO jsou řešením atomu vodíku a jsou funkcí, , STO • v praxi se však z výpočetních důvodů nepracuje přímo s STO, ale s GTO, které jsou funkcí

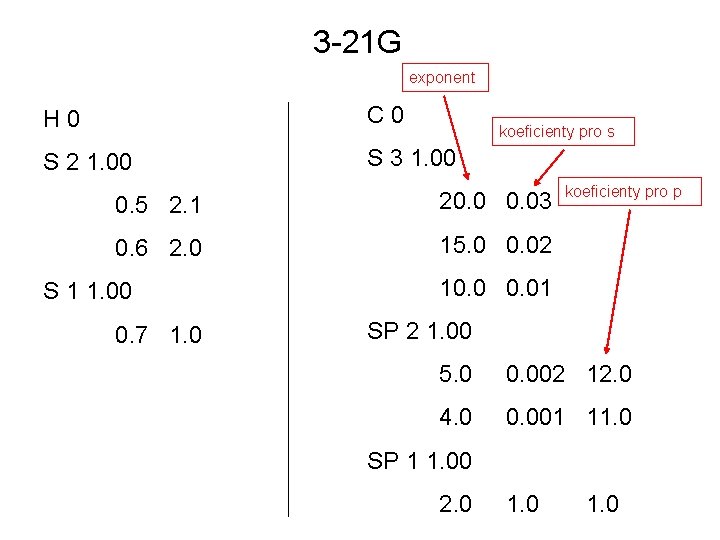
3 -21 G exponent H 0 C 0 S 2 1. 00 S 3 1. 00 koeficienty pro s 0. 5 2. 1 20. 0 0. 03 0. 6 2. 0 15. 0 0. 02 S 1 1. 00 0. 7 1. 0 koeficienty pro p 10. 0 0. 01 SP 2 1. 00 5. 0 0. 002 12. 0 4. 0 0. 001 11. 0 SP 1 1. 00 2. 0 1. 0

ψ = c 11 s‘H+c 21 s‘‘H+c 31 s‘C+c 42 s‘C+c 52 s‘‘C+c 62 p‘C+c 72 p‘‘C 1 s‘H = 2. 1 e-0. 5 + 2. 0 e-0. 6 1 s‘‘H = 1. 0 e-0. 7 1 s‘C = 0. 03 e-20 + 0. 02 e-15 + 0. 01 e-10 2 s‘C = 0. 002 e-5 + 0. 001 e-4 2 s‘‘C = 1. 0 e-2 2 p‘C = 12 e-5 + 11 e-4 2 p‘‘C = 1. 0 e-2

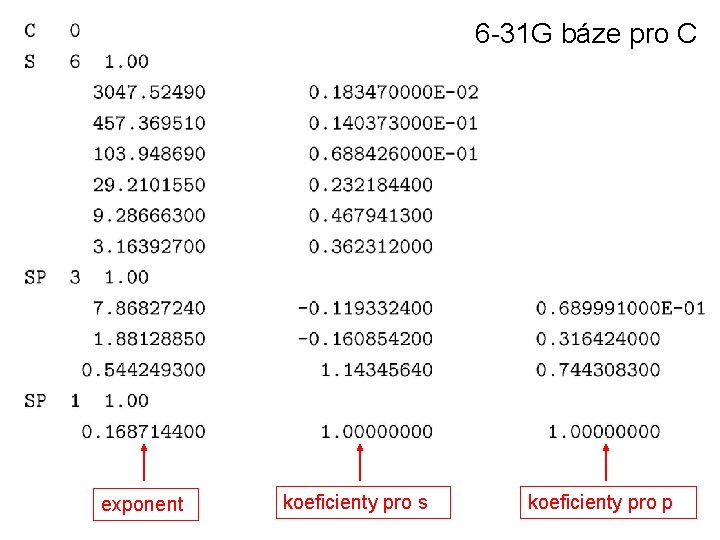
6 -31 G báze pro C exponent koeficienty pro s koeficienty pro p

• difuzní fce s pro H, s a p pro těžké atomy + či ++ před G 6 -31+G • polarizační fce v závorce za G (těžký atom, vodík) 6 -311++G(2 df, 2 pd) alternativně pro jednu sadu polarizačních fcí se používá *, **: 6 -31+G* = 6 -31+G(d)

6 -31 G pro uhlík exponent koeficienty pro s 6 -31+G* pro uhlík diffuse polarization koeficienty pro p

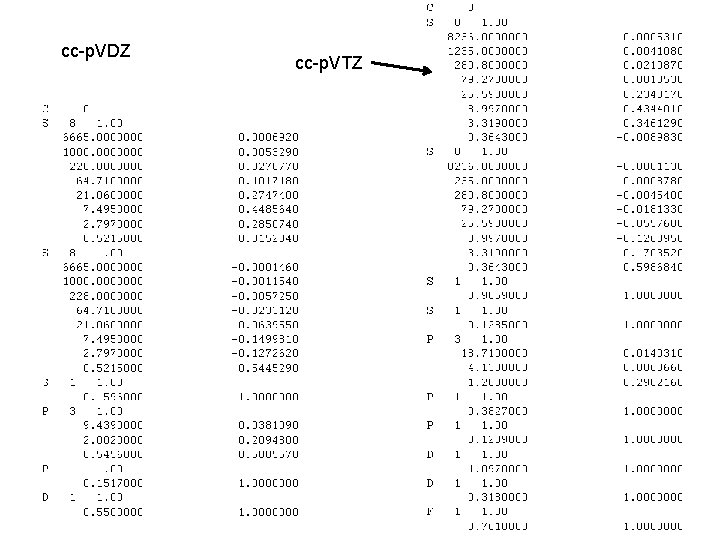
Dunningovy cc báze • cc. . . korelačně konzistentní • optimalizované za použití korelované (CISD) funkce • cc-p. VXZ korelačně konzistentní valence polarizovaná X-zeta báze – cc-p. VDZ, cc-p. VTZ, cc-p. VQZ, cc-p. V 5 Z, . . . • funkce jsou dodávány ve slupkách (shells) – cc-p. VDZ pro C je 3 s 2 p 1 d, cc-p. VTZ je 4 s 3 p 2 d 1 f

cc-p. VDZ cc-p. VTZ

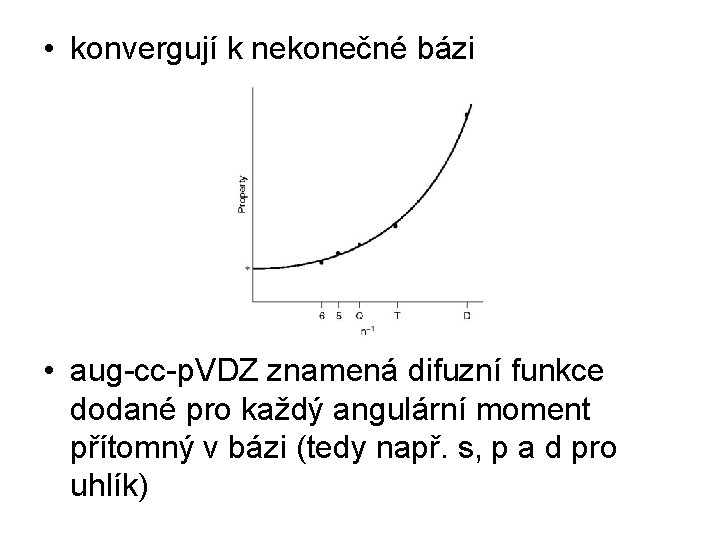
• konvergují k nekonečné bázi • aug-cc-p. VDZ znamená difuzní funkce dodané pro každý angulární moment přítomný v bázi (tedy např. s, p a d pro uhlík)

Báze prakticky • větší = lepší – obvykle, třeba vybalancovat s použitou metodou, cc-p. VQZ je overkill pro HF • STO-3 G nepoužívat • difuzní fce pro anionty • cc-p. VDZ není vždy lepší než 6 -31 G(d, p), ale cc-p. VTZ vždy lepší než 6 -311 G(d, p) • Basis set exchange – https: //bse. pnl. gov/bse/portal

Variační princip • existují různé funkce které splňují podmínky kladené na vlnovou funkci • kvalitu těchto funkcí je možno posoudit na základě energií jim příslušejících • čím nižší, tím lepší

Hartree-Fockova metoda

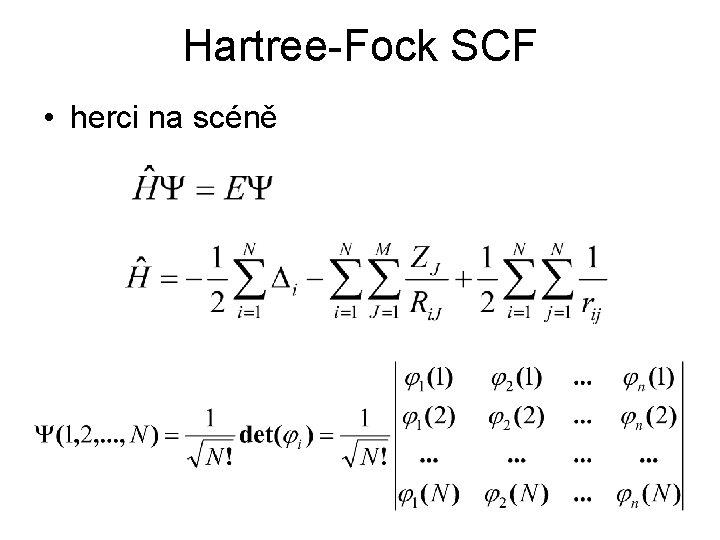
Hartree-Fock SCF • herci na scéně

• z determinantu a Hamiltoniánu sestrojíme N-elektronovou Schrödingerovu rovnici • odvodíme Hartree-Fockovy rovnice • N-el Schr. se rozpadá na N 1 -el Fockových rovnic • Fockián je „ 1 -D Hamiltonián“, Vi{j} je interakční potenciál mezi jedním elektronem a všemi ostatními (zprůměrováno) • háček: Fockián obsahuje spinorbitaly, na které působí (neboť ρ=φ2)

• elektrony se pohybují v potenciálu který samy vytvořily, mluvíme o self-konzistentním poli SCF • M – počet bázových funkcí • při řešení Fockových rovnic je tedy potřeba iterovat – – volba počátečních MO - φi zkonstruuji z nich Fockián vyřeším Fockovy rovnice, tak získám nové φi pokračuji až do dosažení konvergenčního kritéria

• Čili výsledkem řešení HF rovnic jsou jednoelektronové molekulové vlnové funkce – MO • Při velikosti báze M získám iterativním řešením Fockových rovnic M Hartree. Fockových orbitalů • N energeticky nejníže ležících spinorbitalů obsadím elektrony a sestavím z nich Slaterův determinant – obsazené vs. virtuální orbitály

• HF energie • obsahuje tyto složky 1) kinetická energie elektronů 2) elektrostatické (Coulombovo) přitahování jader a elektronů 3) elektrostatická repulze elektronu od ostatních elektronů 4) výměnná energie • • • neodpovídá žádné klasické síle, čistě kvantový původ exchange and correlation energy plyne z Pauliho vylučovacího principu, elektrony se stejným spinem nemohou okupovat stejnou část v prostoru (Fermiho díra)

• konvergence SCF procesu ke stabilnímu řešení není zaručena • oscilace SCF energie nebo ještě horší patologické neodhadnutelné změny v energii • dva možné způsoby vyřešení problému: 1) matematicky • extrapolace, damping, level shifting, DIIS

2) chemicky • často je probémem iniciální odhad vlnové fce • • • obvykle je snadnější dokonvergova HF v malé bázi než ve velké takže nejprve získat vlnovou fci v minimální bázi STO-3 G pak ji použít jako odhad pro lepší bázi, atd. častým důvodem je i špatná geometrie – mezera mezi HOMO a LUMO (HOMO LUMO gap) je malá • optimalizovat geometrii v malé bázi

HF prakticky • Ecorr = Eexact – EHF • • formálně škáluje jako M 4 v praxi je situace málokdy tak špatná, linearscaling metody direct SCF – výpočet integrálů jak jsou potřeba je rychlejší než je ukládat na disk a později vybírat zpět molekulová symetrie – významné urychlení • •

BSSE basis set superposition error • podstatný problém, výrazně vyšší interakční energie • komplex je více stabilnější než monomery díky větší (flexibilnější) bázi • counterpoise-correction (CP) by Boys, Bernardi, ghost atoms (G 03: Counterpoise) deformační energie

• CP BSSE přeceňuje • v některých případech BSSE kompenzuje nekompletnost báze, nedělat !!! • i optimalizace geometrie by měla být BSSE corrected • v limitě nekonečné báze CBS vymizí • některé metody mají nižší BSSE • intramolekulární BSSE – CBS • není jasné jak opravovat BSSE při výpočtu reakcí

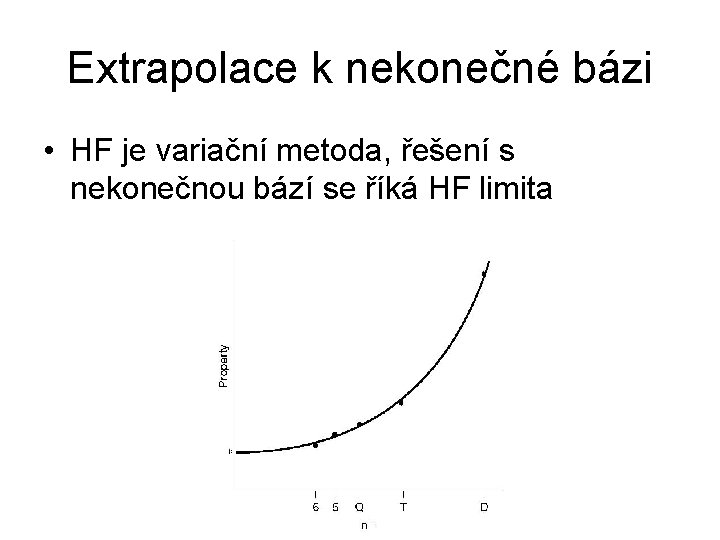
Extrapolace k nekonečné bázi • HF je variační metoda, řešení s nekonečnou bází se říká HF limita

• CBS extrapolation (complete basis set limit) • je potřeba použít konzistentní sadu bází (Dunningovy cc-p. Vn. Z báze) • z praktických důvodů se počítají dvě báze • mnoho schémat, nejčastěji používané (Helgaker): • v nekonečné bázi efektivně zrušíme BSSE

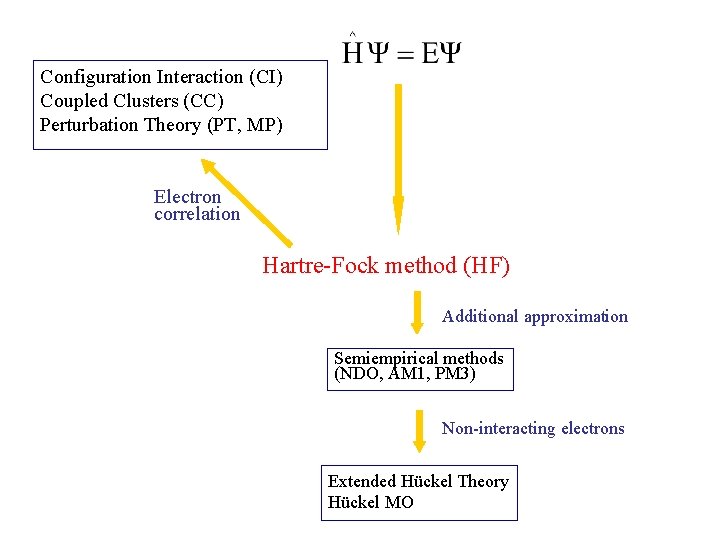
Configuration Interaction (CI) Coupled Clusters (CC) Perturbation Theory (PT, MP) Electron correlation Hartre-Fock method (HF) Additional approximation Semiempirical methods (NDO, AM 1, PM 3) Non-interacting electrons Extended Hückel Theory Hückel MO