Onderverdeling stoffen 4 categorin metalen bestaan uit metaalatomen

Onderverdeling stoffen 4 categoriën: - metalen: bestaan uit metaalatomen (bv. Fe) - moleculaire stoffen: bestaan uit niet metaalatomen (bv. CH 4) - atomaire stoffen: bestaan uit niet metaalatomen (bv. diamant) - zouten: bestaan uit metaal- en niet metaalatomen (bv. Na. Cl) Al deze stoffen hebben in de vaste fase een bepaalde structuur, ze zitten vast in een rooster.

Kristalroosters Verreweg de meeste stoffen bestaan in vaste toestand uit kristallen: ze zijn kristallijn en hebben kristalroosters. diamant keukenzout koper Voorbeelden van stoffen die niet kristallijn zijn glas, plastics en rubber. Dit noemen we amorf.

Soorten kristalroosters We onderscheiden 4 soorten kristalroosters: - Metaalroosters (bij metalen) Molecuulroosters (bij moleculaire stoffen) Atoomroosters (bij atomaire stoffen) Ionroosters (bij zouten)
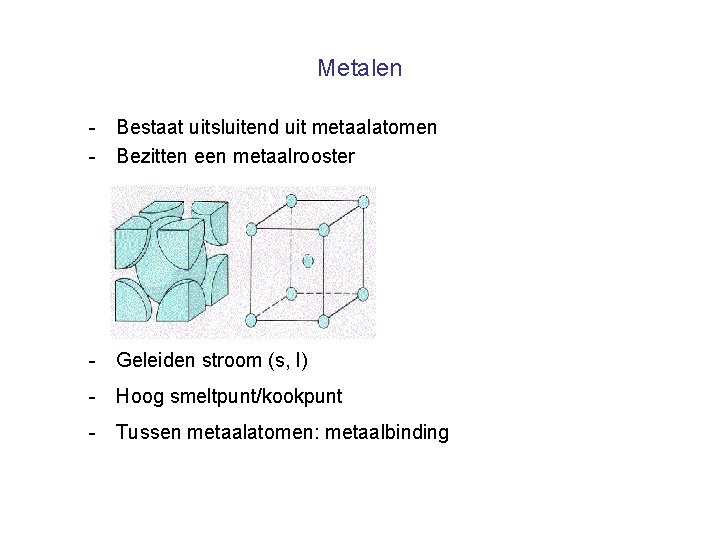
Metalen - Bestaat uitsluitend uit metaalatomen - Bezitten een metaalrooster - Geleiden stroom (s, l) - Hoog smeltpunt/kookpunt - Tussen metaalatomen: metaalbinding
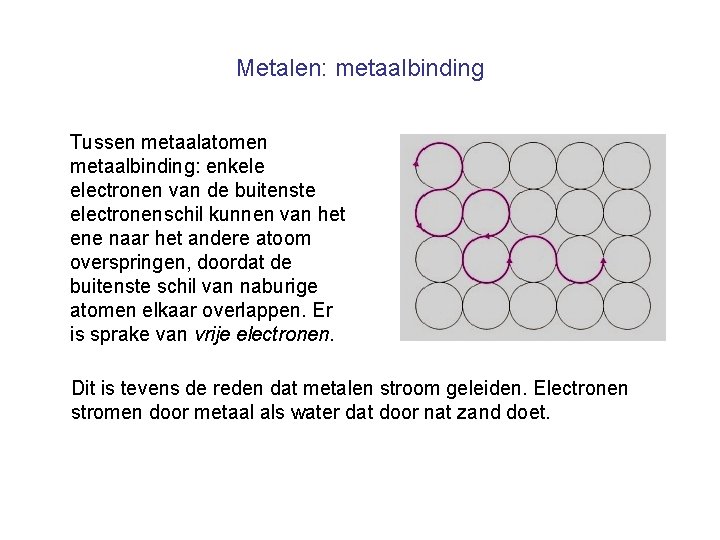
Metalen: metaalbinding Tussen metaalatomen metaalbinding: enkele electronen van de buitenste electronenschil kunnen van het ene naar het andere atoom overspringen, doordat de buitenste schil van naburige atomen elkaar overlappen. Er is sprake van vrije electronen. Dit is tevens de reden dat metalen stroom geleiden. Electronen stromen door metaal als water dat door nat zand doet.

Metalen: metaalbinding Metaalbinding: positieve atoomresten worden bijeen gehouden door negatieve vrije electronen. De vrije electronen werken als ‘vloeibare lijm’. Atoomlagen kunnen over elkaar schuiven, zonder dat de samenhang verbroken wordt. Daardoor zijn metalen buigzaam en smeedbaar.
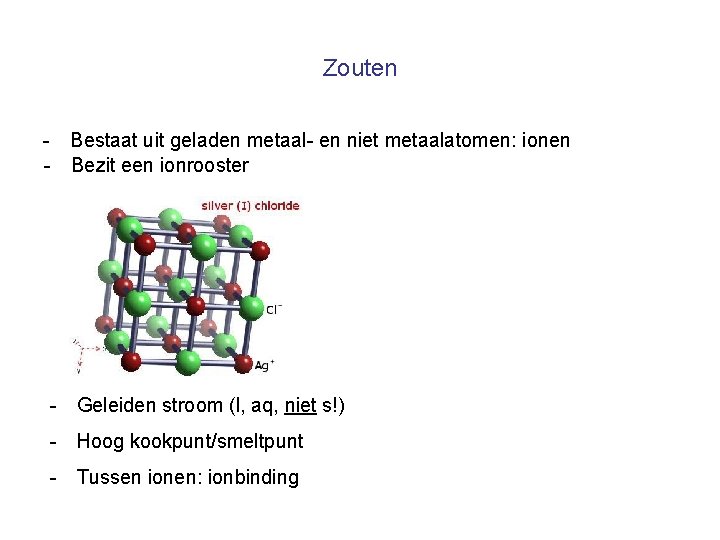
Zouten - Bestaat uit geladen metaal- en niet metaalatomen: ionen - Bezit een ionrooster - Geleiden stroom (l, aq, niet s!) - Hoog kookpunt/smeltpunt - Tussen ionen: ionbinding
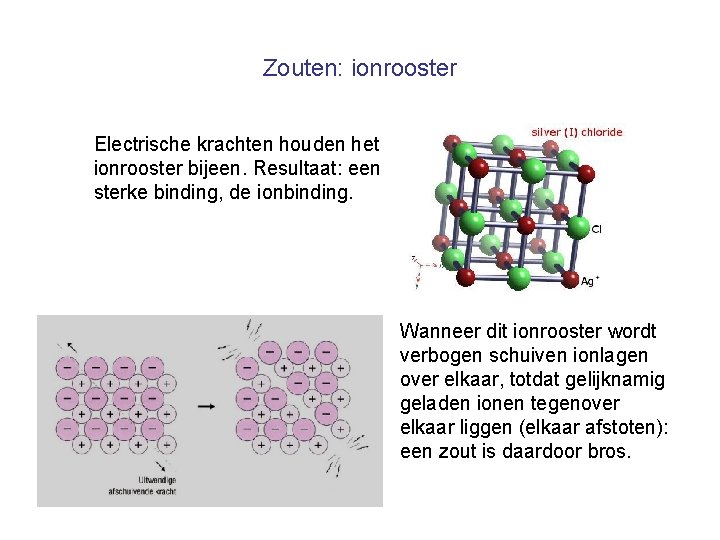
Zouten: ionrooster Electrische krachten houden het ionrooster bijeen. Resultaat: een sterke binding, de ionbinding. Wanneer dit ionrooster wordt verbogen schuiven ionlagen over elkaar, totdat gelijknamig geladen ionen tegenover elkaar liggen (elkaar afstoten): een zout is daardoor bros.

Moleculaire stoffen - Bestaan uitsluitend uit niet-metaalatomen - Bezitten een molecuulrooster - Geleiden geen stroom - Laag smeltpunt - Bindingen: -tussen moleculen: vanderwaalsbinding -binnen molecuul: atoombinding
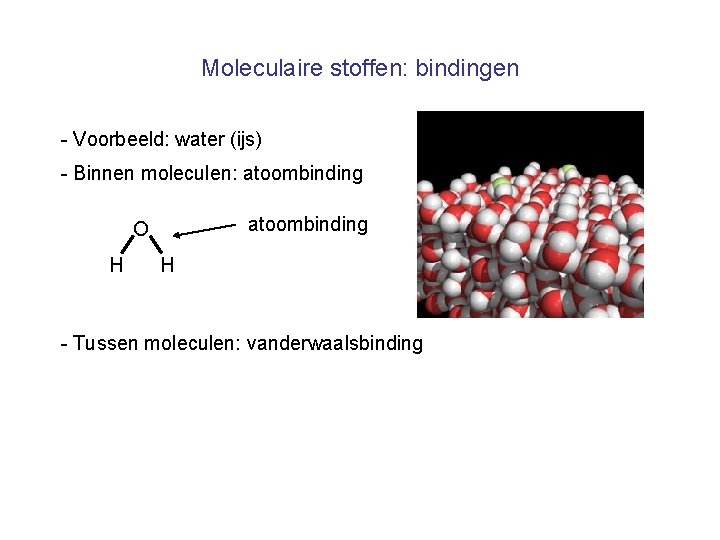
Moleculaire stoffen: bindingen - Voorbeeld: water (ijs) - Binnen moleculen: atoombinding O H H - Tussen moleculen: vanderwaalsbinding
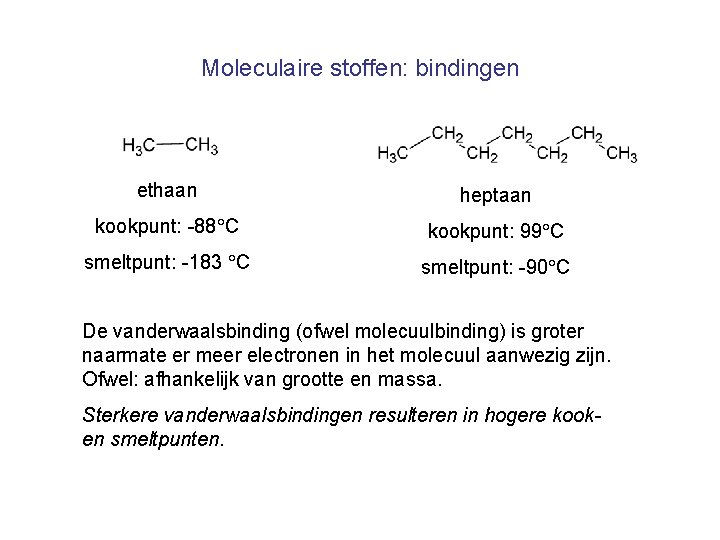
Moleculaire stoffen: bindingen ethaan heptaan kookpunt: -88 C kookpunt: 99 C smeltpunt: -183 C smeltpunt: -90 C De vanderwaalsbinding (ofwel molecuulbinding) is groter naarmate er meer electronen in het molecuul aanwezig zijn. Ofwel: afhankelijk van grootte en massa. Sterkere vanderwaalsbindingen resulteren in hogere kooken smeltpunten.
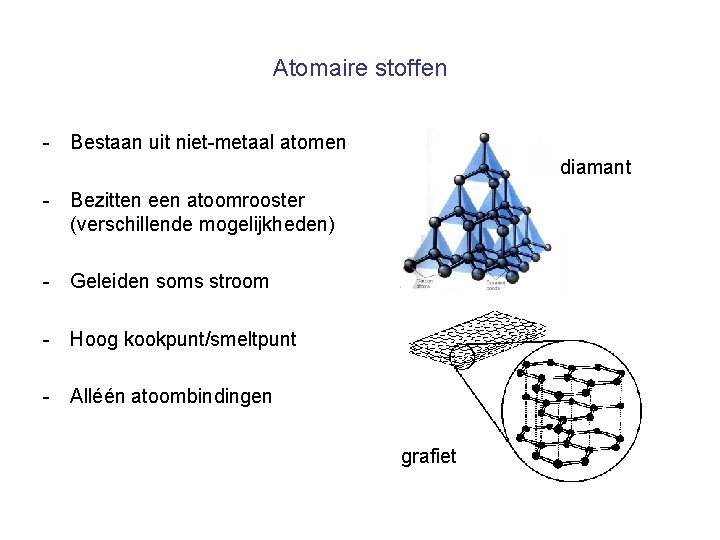
Atomaire stoffen - Bestaan uit niet-metaal atomen diamant - Bezitten een atoomrooster (verschillende mogelijkheden) - Geleiden soms stroom - Hoog kookpunt/smeltpunt - Alléén atoombindingen grafiet
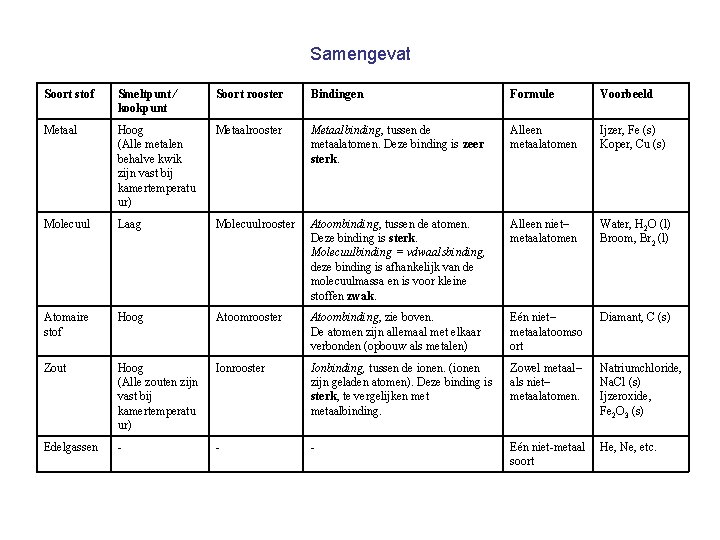
Samengevat Soort stof Smeltpunt ⁄ kookpunt Soort rooster Bindingen Formule Voorbeeld Metaal Hoog (Alle metalen behalve kwik zijn vast bij kamertemperatu ur) Metaalrooster Metaalbinding, tussen de metaalatomen. Deze binding is zeer sterk. Alleen metaalatomen Ijzer, Fe (s) Koper, Cu (s) Molecuul Laag Molecuulrooster Atoombinding, tussen de atomen. Deze binding is sterk. Molecuulbinding = vdwaalsbinding, deze binding is afhankelijk van de molecuulmassa en is voor kleine stoffen zwak. Alleen niet– metaalatomen Water, H 2 O (l) Broom, Br 2 (l) Atomaire stof Hoog Atoomrooster Atoombinding, zie boven. De atomen zijn allemaal met elkaar verbonden (opbouw als metalen) Eén niet– metaalatoomso ort Diamant, C (s) Zout Hoog (Alle zouten zijn vast bij kamertemperatu ur) Ionrooster Ionbinding, tussen de ionen. (ionen zijn geladen atomen). Deze binding is sterk, te vergelijken metaalbinding. Zowel metaal– als niet– metaalatomen. Natriumchloride, Na. Cl (s) Ijzeroxide, Fe 2 O 3 (s) Edelgassen - - - Eén niet-metaal soort He, Ne, etc.
- Slides: 13