Oldatok Savak s bzisok Tartalomjegyzk Oldatok 1 Az

Oldatok Savak és bázisok

Tartalomjegyzék • Oldatok 1. Az oldatok jellemzői 2. Oldódás 3. Oldékonyság 4. A koncentráció • Savak és bázisok 1. Meghatározás és osztályozás 2. Ionizáció vizes közegben 3. p. H 4. Savak és bázisok hatása indikátorokra 5. Semlegesítési reakció

I. Oldatok 1. Az oldatok jellemzői: • homogén keverékek • oldott anyagból (mf) és oldószerből állnak
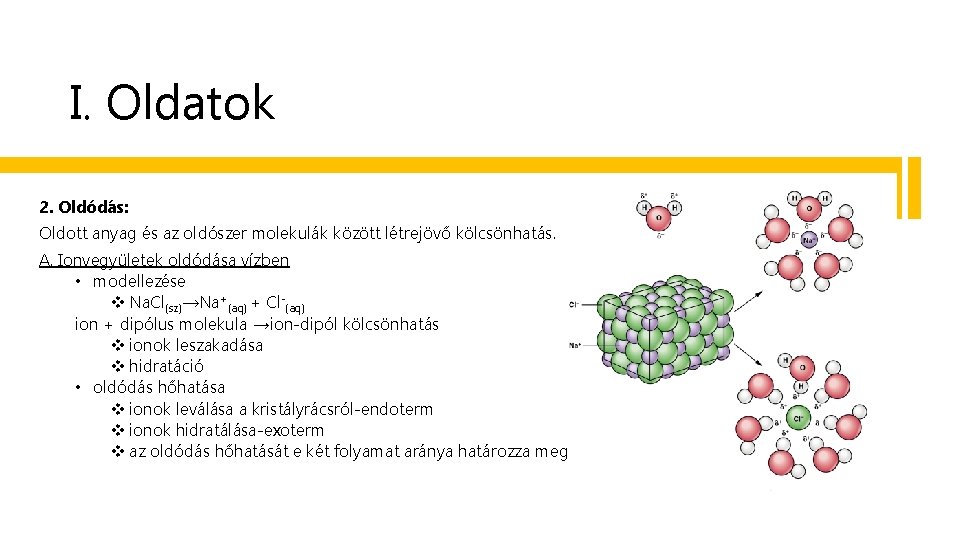
I. Oldatok 2. Oldódás: Oldott anyag és az oldószer molekulák között létrejövő kölcsönhatás. A. Ionvegyületek oldódása vízben • modellezése v Na. Cl(sz)→Na+(aq) + Cl-(aq) ion + dipólus molekula →ion-dipól kölcsönhatás v ionok leszakadása v hidratáció • oldódás hőhatása v ionok leválása a kristályrácsról-endoterm v ionok hidratálása-exoterm v az oldódás hőhatását e két folyamat aránya határozza meg
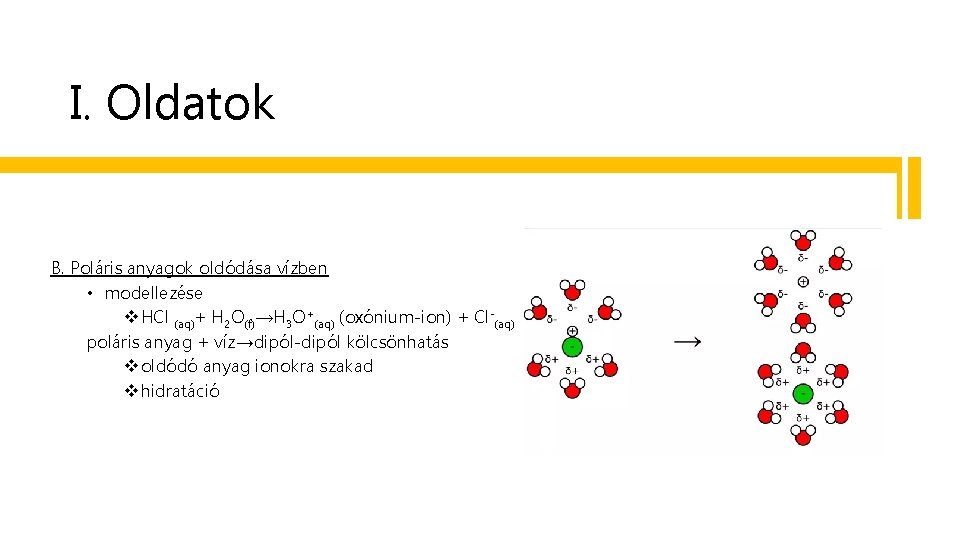
I. Oldatok B. Poláris anyagok oldódása vízben • modellezése v HCl (aq)+ H 2 O(f)→H 3 O+(aq) (oxónium-ion) + Cl-(aq) poláris anyag + víz→dipól-dipól kölcsönhatás v oldódó anyag ionokra szakad v hidratáció

I. Oldatok 3. Oldékonyság • tulajdonság-egy anyag adott oldószerben való oldhatóságát fejezi ki • az oldékonyságot befolyásoló tényezők: v oldott anyag és oldószer természete Ø apoláris oldószerben apoláris anyag ( CCl 4 -ban I 2) Ø poláris oldószerben poláris és ionos kötésű anyag ( H 2 O-ben HCl és Na. Cl) v hőmérséklet Ø szilárd anyagok és folyadékok (általában) ↑ Ø gázak↓ v nyomás Ø szilárd anyagok, folyadékokØ gázak↑

I. Oldatok 4. A koncentráció A. Tömegszázalékos koncentráció • Kifejezi, hogy 100 g oldatban hány gramm oldott anyag van. • jelölések: v mf- feloldott anyag tömege v mo- oldat tömege v mo=mf + mvíz v c%- tömegszázalékos koncentráció Számítási képlet mo (g) ……………. mf(g) 100 g ……………. c%

I. Oldatok B. A moláris koncentráció (anyagmennyiség-koncentráció) • Kifejezi az 1 liter oldatban feloldott anyag móljainak számát. • jelölések: v ν- feloldott anyag móljainak száma (mol) v Vo- az oldat térfogata (l) v CM- moláris koncentráció( mol/l , M) v m- a feloldott anyag tömege (g) v M- az anyag molekulatömege (g/mol) Számítási képlet Vo(l) ……………. ν(mol) 1 l ………………CM

Feladatok E. Tétel 3. feladat: Számítsa ki annak a 7, 3% tömegszázalékos koncentrációjú (S 2) hidrogén-klorid oldatnak a grammban kifejezett tömegét, amely ugyanolyan mennyiségű feloldott anyagot tartalmaz, mint 300 m. L; 0, 2 M-os koncentrációjú (S 1) hidrogén-klorid oldat! Megoldás: S 1 (HCl) : • V 1=300 ml=0, 3 l • CM=0, 2 M S 2 (HCl) : • C=7, 3% • m 0=? S 1: ν 1=CM • V 1=0, 2 • 0, 3=0, 06 mol MHCl=36, 5 g/mol m 1=ν 1 • M=0, 06 mol • 36, 5 g/mol=2, 19 g→mf S 2: 100 g oldat……………. . 7, 3 g feloldott anyag mo…………… 2, 19 g mo=30 g oldat
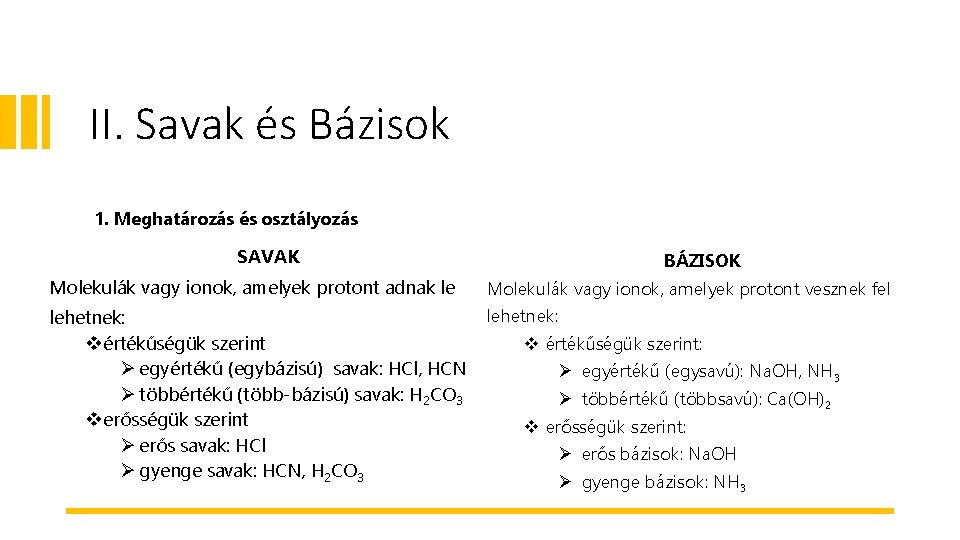
II. Savak és Bázisok 1. Meghatározás és osztályozás SAVAK BÁZISOK Molekulák vagy ionok, amelyek protont adnak le Molekulák vagy ionok, amelyek protont vesznek fel lehetnek: v értékűségük szerint Ø egyértékű (egybázisú) savak: HCl, HCN Ø többértékű (több-bázisú) savak: H 2 CO 3 v erősségük szerint Ø erős savak: HCl Ø gyenge savak: HCN, H 2 CO 3 lehetnek: v értékűségük szerint: Ø egyértékű (egysavú): Na. OH, NH 3 Ø többértékű (többsavú): Ca(OH)2 v erősségük szerint: Ø erős bázisok: Na. OH Ø gyenge bázisok: NH 3

II. Savak és Bázisok 2. Ionizáció vizes közegben A. Savak: • erős savak teljes mértékben ionizálnak v HCl (aq)+ H 2 O(f)→H 3 O+(aq) (oxónium-ion)+ Cl-(aq) • gyenge savak részben ionizálnak, a reakció reverzibilis v HCN(aq) + H 2 O(f)↔CN-(aq) + H 3 O+(aq) • többértékű savak lépcsőzetesen disszociálnak v H 2 CO 3(aq) + H 2 O(f)↔HCO 3 -(aq) + H 3 O+(aq) v HCO 3 -(aq) + H 2 O(f)↔CO 32 -(aq) + H 3 O+(aq) B. Bázisok: • erős bázisok teljes mértékben ionizálnak v Na. OH(sz)→Na+(aq) +HO-(aq) • gyenge bázisok kis mértékben, reverzibilis reakció v NH 3(aq) + H 2 O(f)↔NH 4+(aq) + HO-(aq)
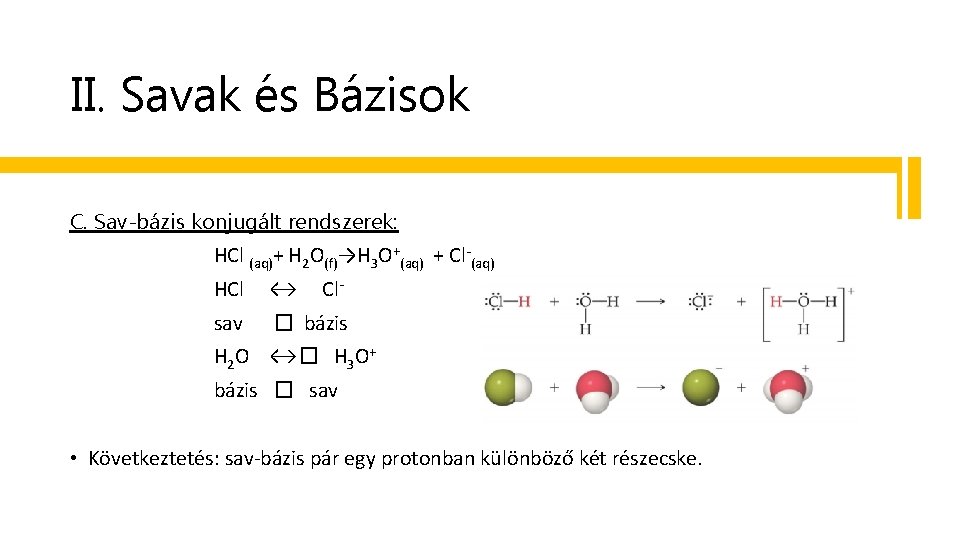
II. Savak és Bázisok C. Sav-bázis konjugált rendszerek: HCl (aq)+ H 2 O(f)→H 3 O+(aq) + Cl-(aq) HCl ↔ Cl- sav � bázis H 2 O ↔� H 3 O+ bázis � sav • Következtetés: sav-bázis pár egy protonban különböző két részecske.

II. Savak és Bázisok p. H p. OH • egy oldat kémiai jellegére utal • függ az oxónium ion koncentrációjától • matematikai alak: p. H= - lg [H 3 O+] erős savak esetében: CM= [H 3 O+] v p. H értéke < 7, az oldat savas jellegű v p. H értéke =7, az oldat semleges v p. H értéke >7, az oldat bázikus jellegű • bázisok estében alkalmazható • függ a hidroxid ion koncentrációjától • matematikai alak: p. OH= -lg [HO-] erős bázisok esetében: CM= [HO-] Összefüggés a p. H és a p. OH között [H 3 O+] • [HO-] = 10 -14 → p. H + p. OH= 14
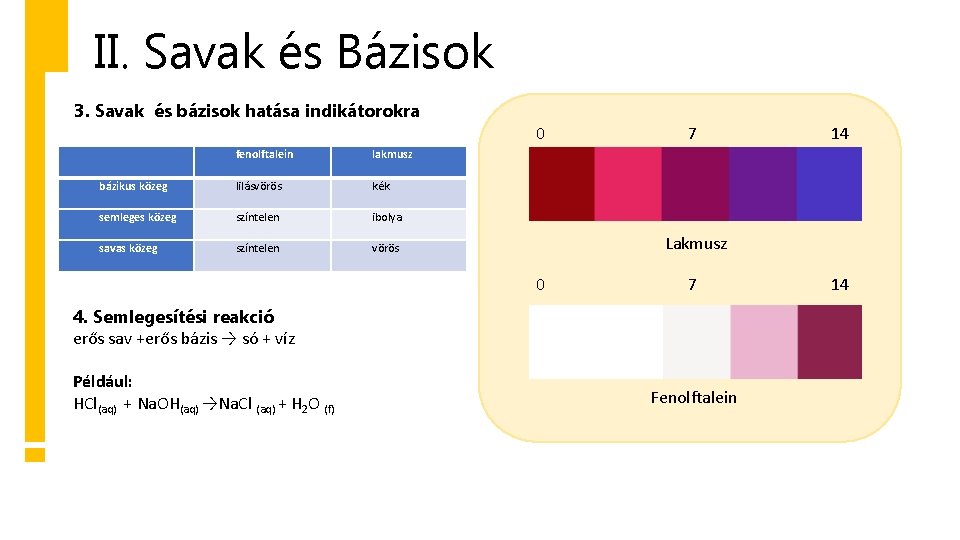
II. Savak és Bázisok 3. Savak és bázisok hatása indikátorokra 0 fenolftalein lakmusz bázikus közeg lilásvörös kék semleges közeg színtelen ibolya savas közeg színtelen vörös 7 Lakmusz 0 7 4. Semlegesítési reakció erős sav +erős bázis → só + víz Például: HCl(aq) + Na. OH(aq) →Na. Cl (aq) + H 2 O (f) 14 Fenolftalein 14

Feladatok 2018 Szimuláció E. Tétel 4. alpont 2 liter oldatban levő nátrium-hidroxid teljesen reagál 0, 2 mol hidrogén-kloriddal. a) Írja lejátszodó reakció egyenletét. b) Határozza meg a Na. OH oldat p. H értékét! Megoldás: a) Na. OH + HCl → Na. Cl + H 2 O
![Feladatok b) p. OH→p. H=14 -p. OH= -lg [HO-] = CM 1 mol Na. Feladatok b) p. OH→p. H=14 -p. OH= -lg [HO-] = CM 1 mol Na.](http://slidetodoc.com/presentation_image_h/ac73c8780c86d85f5a22932c1ff0cefd/image-16.jpg)
Feladatok b) p. OH→p. H=14 -p. OH= -lg [HO-] = CM 1 mol Na. OH………. . 1 mol HCl X mol Na. OH………. 0, 2 mol HCl → X= 0, 2 mol Na. OH reagál 1 liter Na. OH oldat…………. . CM 2 liter Na. OH oldat…………. 0, 2 mol Na. OH →CM= 0, 1 mol/l=10 -1 mol/l p. OH= -lg [HO-] =-lg[10 -1]=1 p. H=14 -p. OH p. H= 14 -1=13 Felelet: Na. OH oldat p. H értéke 13, erős bázis

# d ra ma on th jot Köszönöm a figyelmet! Madaras Ildikó-Adél
- Slides: 17