Oldatok elegyek Tbbkomponens homogn egyfzis rendszerek Elegyek komponensek

Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott anyag) képest

Fontosabb koncentráció egységek Molaritás mol oldott anyag/dm 3 oldat Molalitás mol oldott anyag/kg oldószer Tömeg koncentráció g oldott anyag/dm 3 oldat Moltört oldott anyag molszáma/összmolszám Tömegszázalék 100 g oldatban ? g oldott anyag van

Oldhatóság – telített oldat Egy anyag oldhatósága azt fejezi ki, hogy adott hőmérsékleten hány grammja oldódik 100 g oldószerben S: g/100 g oldószer
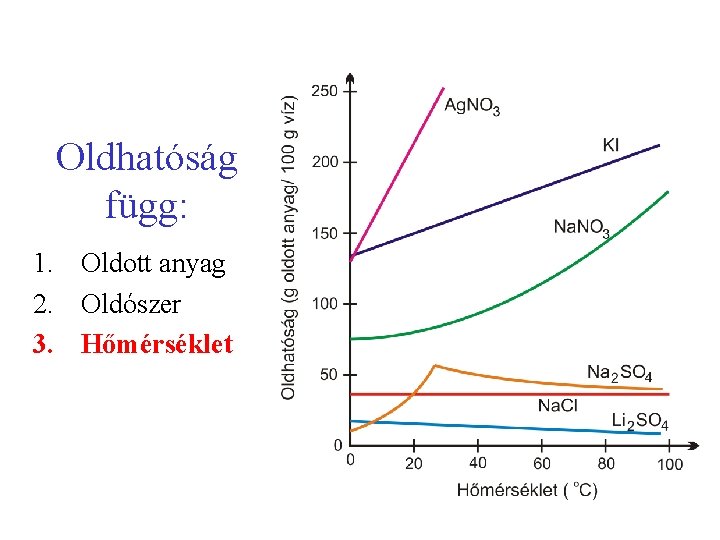
Oldhatóság függ: 1. Oldott anyag 2. Oldószer 3. Hőmérséklet

Feladat: A KNO 3 oldhatósága 60 ºC-on 111 g/100 g víz és 20 ºC-on 31 g/100 g víz. Mi történik, ha 50 g KNO 3 -ot és 100 g vizet összekeverünk 20 ºC-on ? Mi történik, ha a hőmérsékletet 60 ºC-ra emeljük ? Mi történik, ha még 50 g KNO 3 -ot dobunk az oldatba ? Mi történik, ha az oldatot 20 ºC-ra lehűtjük ?
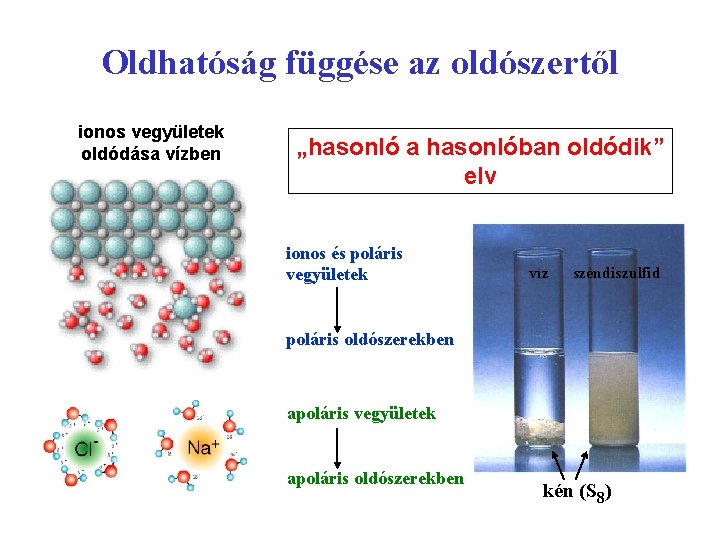
Oldhatóság függése az oldószertől ionos vegyületek oldódása vízben „hasonló a hasonlóban oldódik” elv ionos és poláris vegyületek víz széndiszulfid poláris oldószerekben apoláris vegyületek apoláris oldószerekben kén (S 8)
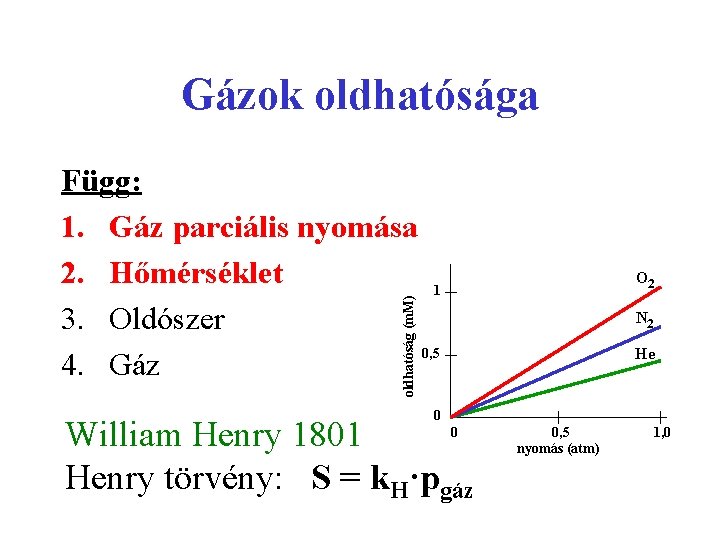
Gázok oldhatósága Függ: 1. Gáz parciális nyomása 2. Hőmérséklet 1 3. Oldószer 0, 5 4. Gáz oldhatóság (m. M) O 2 N 2 He 0 William Henry 1801 Henry törvény: S = k. H·pgáz 0 0, 5 nyomás (atm) 1, 0

Nyomás Adott hőmérsékleten a gáz oldhatósága (S) az oldattal egyensúlyban levő gáz parciális nyomásával (pgas) arányos. S = k. H pgas Henry-törvény

gáz Henry állandó (20 °C, víz) k. H (m. M/atm) -------------------------Levegő 0, 79 Szén-dioxid 23 Hélium 0, 37 Neon 0, 5 Argon 1, 5 Hidrogén 0, 85 Nitrogén 0, 7 Oxigén 1, 3
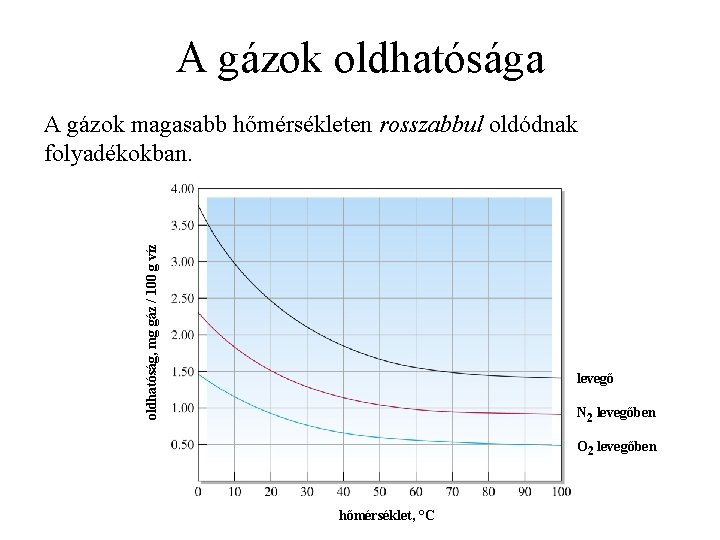
A gázok oldhatósága oldhatóság, mg gáz / 100 g víz A gázok magasabb hőmérsékleten rosszabbul oldódnak folyadékokban. levegő N 2 levegőben O 2 levegőben hőmérséklet, °C

Dekompressziós betegség

Feladat: A legkisebb O 2 koncentráció, mely szükséges a vizi élethez kb. 0, 13 m. M (4, 2 mg/l). Ha a tó 20 ºC-os, teljesül ez a feltétel ? (k. H(O 2, 20 ºC)= 1, 3 m. M/atm) Levegő 21% oxigént tartalmaz parc. Ny. 0, 21∙ 1 atm = 0, 21 atm S= k. H∙p. O 2 = 1, 3 m. M/atm ∙ 0, 21 atm = 0, 27 m. M 0. 27 m. M

Kolligatív tulajdonságok Egy kolligatív tulajdonság az a tulajdonság, amely csak az oldott anyag mennyiségétől függ és független a minőségétől. 1. 2. 3. 4. Gőznyomás csökkenés Forráspont emelkedés Fagyáspont csökkenés Ozmózisnyomás

Gőznyomás csökkenés Francois-Marie Raoult törvény: egy nem illékony oldott anyag oldatának gőznyomása az oldószer móltörtjével arányos. poldat=xoldószer·p*oldószer Tenzió csökkenés: Δp=xoldott·p*oldószer !!!!!! Csak híg oldatoknál érvényes !!!!!!
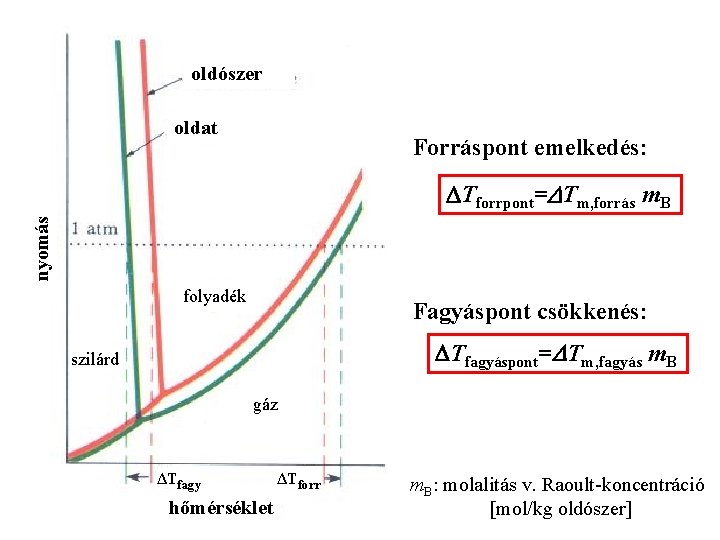
oldószer oldat Forráspont emelkedés: nyomás DTforrpont=DTm, forrás m. B folyadék Fagyáspont csökkenés: DTfagyáspont=DTm, fagyás m. B szilárd gáz ΔTfagy hőmérséklet ΔTforr m. B: molalitás v. Raoult-koncentráció [mol/kg oldószer]

Feladat Egy vizes glükóz (C 6 H 12 O 6) oldat -0. 56 ºC-on fagy meg. Hány fokon forr ez az oldat atmoszférikus nyomáson ? (ΔTM, forrp=0, 52 ºCkg/mol; ΔTM, fpcs=1, 86 ºCkg/mol 100, 16 ºC

Feladat Egy vizes glükóz (C 6 H 12 O 6) oldat -0. 56 ºC-on fagy meg. Hány fokon forr ez az oldat atmoszférikus nyomáson ? (ΔTM, forrp=0, 52 ºCkg/mol; ΔTM, fpcs=1, 86 ºCkg/mol 0, 56 1, 86 DTfagyáspont=DTm, fagyás m. B 0, 52 DTforrpont=DTm, forrás m. B 100, 16 ºC
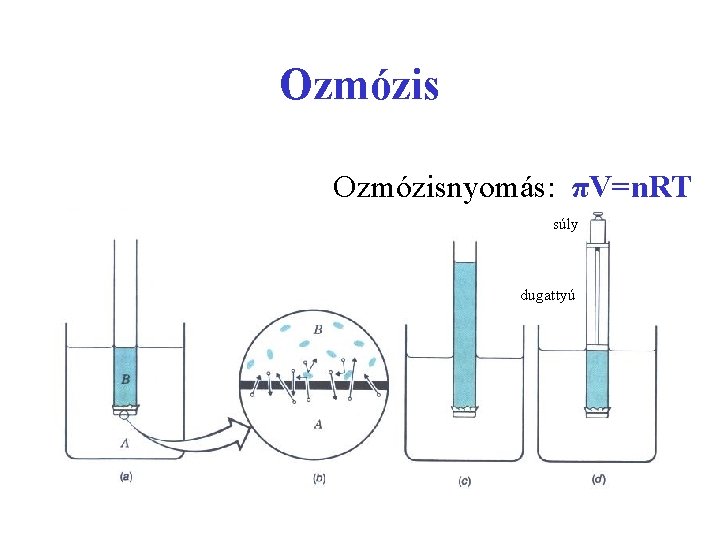
Ozmózisnyomás: πV=n. RT súly dugattyú
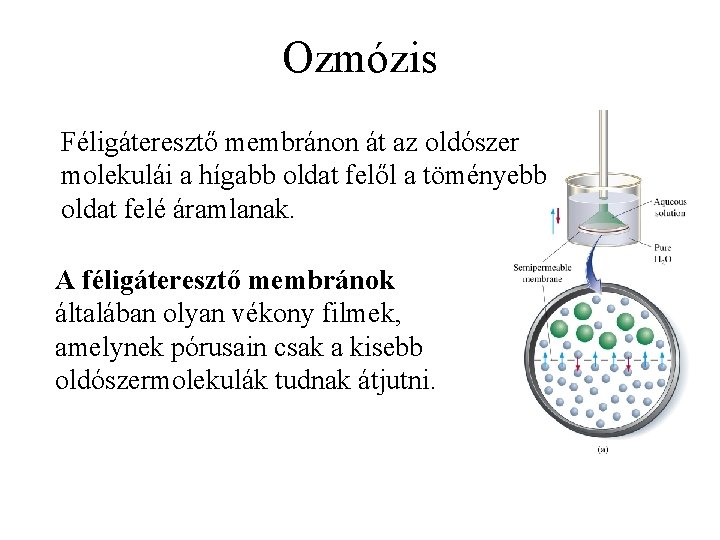
Ozmózis Féligáteresztő membránon át az oldószer molekulái a hígabb oldat felől a töményebb oldat felé áramlanak. A féligáteresztő membránok általában olyan vékony filmek, amelynek pórusain csak a kisebb oldószermolekulák tudnak átjutni.

Ozmózis A nyomás, ami az ozmotikus áramlást megállítaná az oldat ozmózisnyomása: p = (n/V)RT = c RT Az ozmózisnyomás nem függ az oldott anyag minőségétől. Ha a hidrosztatikus nyomás által okozott áramlás és az ozmotikus áramlás egyensúlyban áll, elértük az ozmózisnyomást, p. EOS

Ozmózis Víztisztítás Reverz ozmózis során az ozmózisnyomásnál nagyobb nyomással megfordítják az áramlást. Tiszta oldószer áramlik ki az oldatból a nyomás hatására. cellulóz-acetát membrán, <70 atm

Ozmózis izotóniás oldatok (izoozmotikus): azonos ozmózisnyomásuk van emberben: 0, 9%-os Na. Cl oldat (fiziológiás sóoldat)
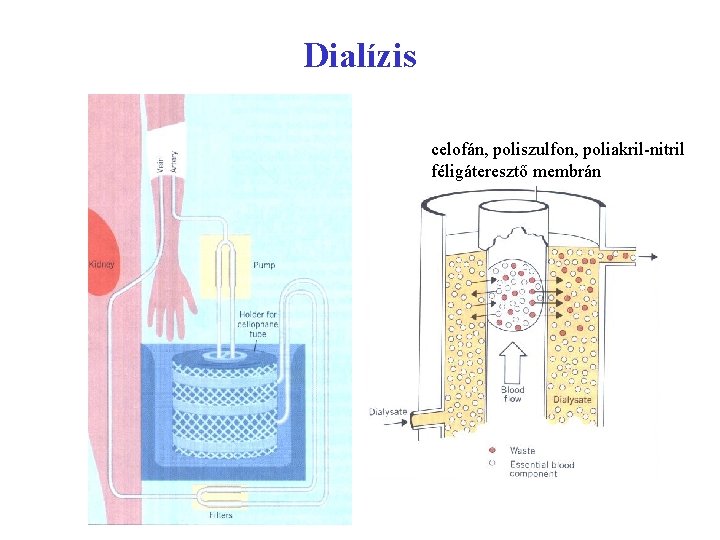
Dialízis celofán, poliszulfon, poliakril-nitril féligáteresztő membrán

Feladat: Mekkora annak a proteinnek a molekulatömege, melynek 1 gját 100 ml vízben oldva 17 ºC-on 253 Pa ozmózisnyomást észlelünk ? πV= n. RT = m. RT/M M= m. RT/(πV) = 1∙ 8, 314∙ 290, 15/(253∙ 100∙ 10– 6)= 95348, 1 g/mol 9, 5· 104 g/mol

Feladat: Három oldatot készítünk: 1. 0, 01 mol acetont oldunk 100 g vízben 2. 0, 01 mol Na. Cl-t oldunk 100 g vízben 3. 0, 01 mol Ca. Cl 2 -t oldunk 100 g vízben. Mennyi az oldatok fagyáspontja ? (ΔTM, fpcs=1, 86 ºCkg/mol) DTfagyáspont=DTm, fagyás m. B -0, 186, -0, 372, -0, 558 ºC

Híg oldatok törvényei: Kolligatív tulajdonságok 1. 2. 3. 4. Gőznyomás csökkenés Δp=xoldott·p*oldószer DTforrpont=DTm, forrás m. B Forráspont emelkedés DTfagyáspont=DTm, fagyás m. B Fagyáspont csökkenés Ozmózisnyomás πV=n. RT m. B: molalitás v. Raoult-koncentráció [mol/kg oldószer]
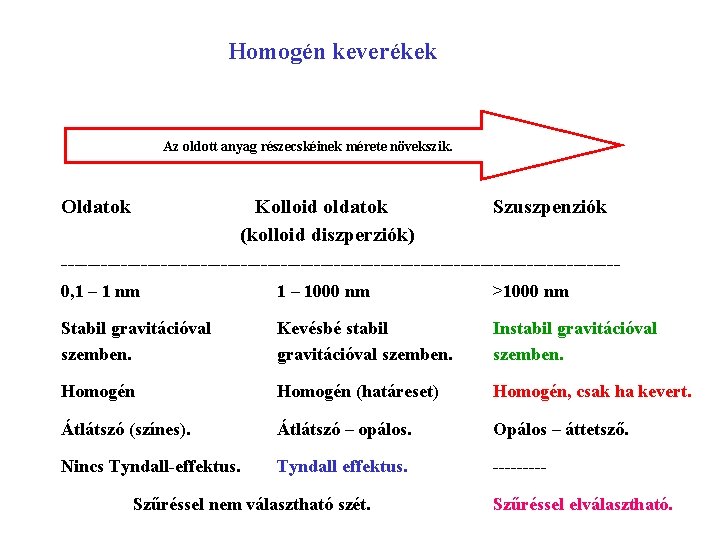
Homogén keverékek Az oldott anyag részecskéinek mérete növekszik. Oldatok Kolloid oldatok Szuszpenziók (kolloid diszperziók) ------------------------------------------0, 1 – 1 nm 1 – 1000 nm >1000 nm Stabil gravitációval szemben. Kevésbé stabil gravitációval szemben. Instabil gravitációval szemben. Homogén (határeset) Homogén, csak ha kevert. Átlátszó (színes). Átlátszó – opálos. Opálos – áttetsző. Nincs Tyndall-effektus. Tyndall effektus. ----- Szűréssel nem választható szét. Szűréssel elválasztható.

A kolloidok 1 és 1000 nm közötti méretű részecskéket tartalmaznak A Tyndall effektus során a kolloid részecskék fényszórása jelenik meg.

Koaguláció során a kolloid részek kicsapódnak Tömény elektrolit is okozhatja EOS
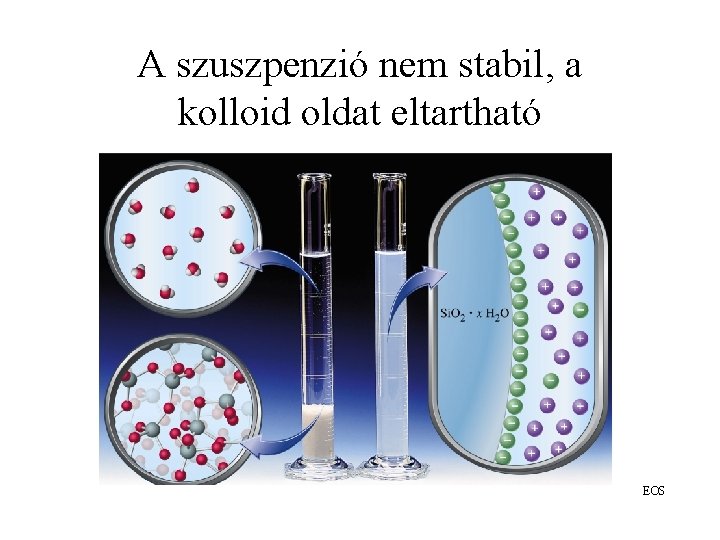
A szuszpenzió nem stabil, a kolloid oldat eltartható EOS
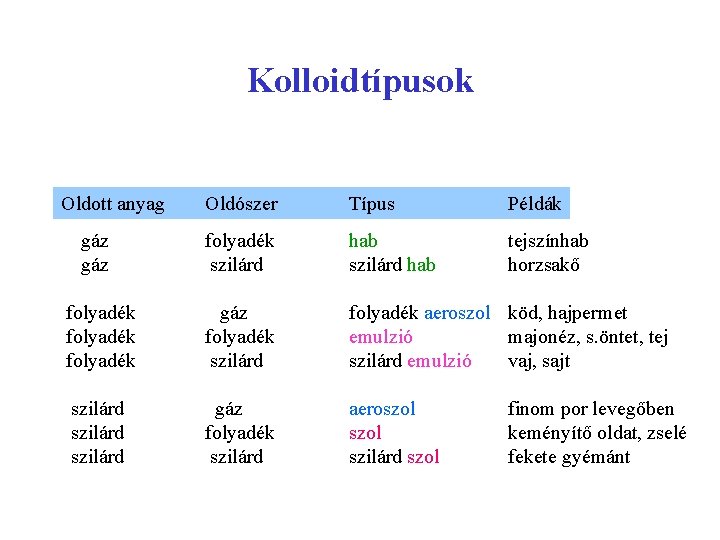
Kolloidtípusok Oldott anyag Oldószer Típus Példák folyadék szilárd hab tejszínhab horzsakő folyadék gáz folyadék szilárd folyadék aeroszol köd, hajpermet emulzió majonéz, s. öntet, tej szilárd emulzió vaj, sajt szilárd gáz folyadék szilárd aeroszol szilárd szol gáz finom por levegőben keményítő oldat, zselé fekete gyémánt

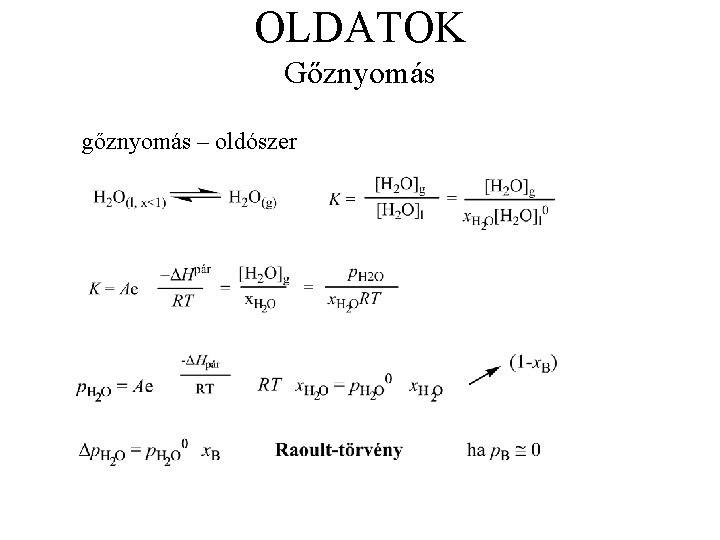
OLDATOK Gőznyomás gőznyomás – oldószer
![FORRÁSPONT-EMELKEDÉS Clausius Clapeyron egyenlet: DTf=DTm, forrás m. B: molálitás v. Raoult-koncentráció [mol/kg] oldószerre jellemző FORRÁSPONT-EMELKEDÉS Clausius Clapeyron egyenlet: DTf=DTm, forrás m. B: molálitás v. Raoult-koncentráció [mol/kg] oldószerre jellemző](http://slidetodoc.com/presentation_image_h/26c430588fe3c2f41c00441a4bf10608/image-34.jpg)
FORRÁSPONT-EMELKEDÉS Clausius Clapeyron egyenlet: DTf=DTm, forrás m. B: molálitás v. Raoult-koncentráció [mol/kg] oldószerre jellemző állandó: DTm: molális forráspontcsökkenés
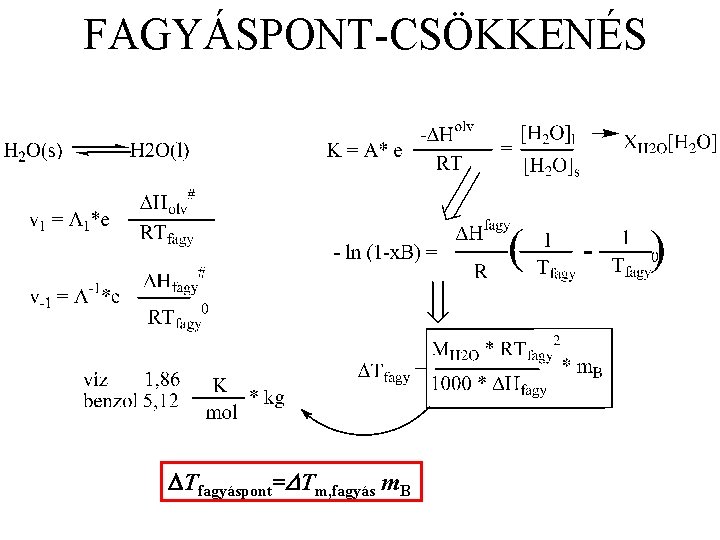
FAGYÁSPONT-CSÖKKENÉS DTfagyáspont=DTm, fagyás m. B
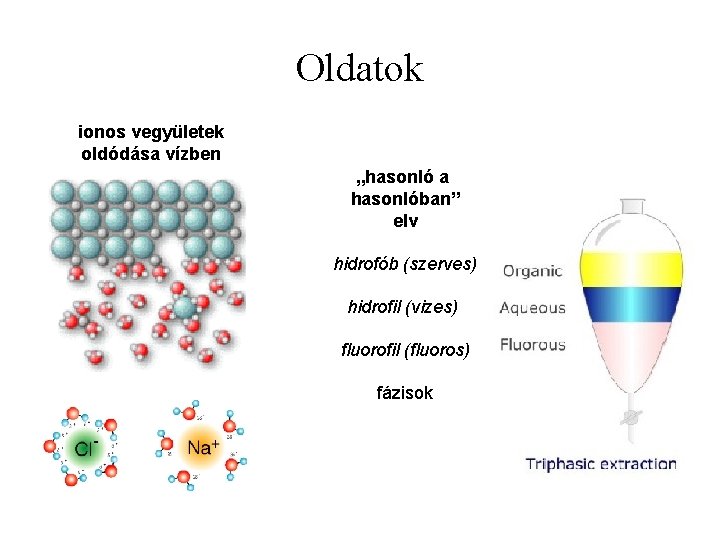
Oldatok ionos vegyületek oldódása vízben „hasonló a hasonlóban” elv hidrofób (szerves) hidrofil (vizes) fluorofil (fluoros) fázisok
- Slides: 36