ODABRANA POGLAVLJA ANALITIKE KEMIJE Milan SakBosnar Odjel za

ODABRANA POGLAVLJA ANALITIČKE KEMIJE Milan Sak-Bosnar Odjel za kemiju, Sveučilište Josipa Jurja Strossmayera
Odabrana poglavlja analitičke kemije Naziv kolegija Status kolegija Izborni Studij Dodiplomski studij kemije Okvirni sadržaj kolegija Principi i primjena različitih suvremenih analitičkih tehnika (kombinirane tehnike, kemijski senzori i biosenzori, automatizirani postupci) u geokemiji, medicini, kriminalistici, arheologiji, proizvodnji i kontroli hrane, zaštiti okoliša, i drugim područjima ljudskog djelovanja. Opća i posebna znanja koja se stječu na kolegiju (cilj) Upoznavanje s najnovijim napretcima u analitičkoj kemiji. Nastava Predavanja Seminari Vježbe (sati/tjedan) 2 1 0 (ukupno) 30 15 0 Oblici provođenja nastave i način provjere znanja Predavanja, pisanje i izlaganje seminarskih radova, kolokviji, domaće zadaće Literatura potrebna za studij i pripremanje ispita D. A. Skoog, F. J. Holler, A. Nieman, Principles of Instrumental Analysis, 5 th Edition, Saunders College Publishing, New York, 1998. Ostala raspoloživa literatura, uključivši i izvore s Interneta Dopunska literatura Journal of Chemical Education Ostali znanstveni časopisi iz analitičke kemije Bodovi (ECTS) sa obrazloženjem 3 boda od kojih se 2 dodjeljuju za potpuno izvršavanje obveza (redovito pohađanje nastave, izrada seminara) i 1 za uspješno položen završni ispit. Način polaganja ispita Pismeni i usmeni ispit, koji se polaže nakon odslušanih predavanja. Konačnu ocjenu čine: redovito pohađanje i aktivno sudjelovanje u nastavi – 10%, seminarski radovi tijekom semestra – 20%, kolokviji - 15+15%, uspjeh na završnom ispitu – 40%. Uvjeti za upis kolegija Osnovni kemijski kolegiji

ANALIZA POVRŠINSKI AKTIVNIH TVARI (Surfactant Analysis)

SADRŽAJ 1. Uvod n n Površinski aktivne tvari (tenzidi) - definicija Osobine tenzida Klasifikacija tenzida Primjena tenzida 2. Analiza anionskih tenzida n n Titracijske metode Spektrofotometrijske metode Kromatografske metode FIA/SIA metode 3. Analiza kationskih tenzida n n n Primjena Volumetrijske metode Potenciometrijske metode Spektrofotometrijske metode Ostale metode

SADRŽAJ 4. Analiza neionskih tenzida n n n Titracijske metode Spektrofotometrijske metode Ostale metode 5. Potenciometrijski senzori n n n n Kemijski i biokemijski senzori Ionsko-selektivne elektrode (ISE) Definicija i podjela Odziv ISE Granice detekcije Kemijske interferencije i selektivnost Metode određivanja selektivnosti

SADRŽAJ 6. Tenzidne ionsko-selektivne elektrode (tenzidni senzori) n n n n Definicija i klasifikacija Dizajn senzora Odziv tenzidnih senzora (elektroda) • Ionski tenzidi • Neionski tenzidi Karakterizacija tenzidnih senzora • Odziv senzora na anionske tenzide • Odziv senzora na kationske tenzide • Odziv senzora na neionske tenzide Primjena tenzidnih senzora • Detekcija završne točke pri potenciometrijskim titracijama n Titracija ionskih tenzida n Titracije neionskih tenzida Prednosti i ograničenja upotrebe tenzidno-selektivnih elektroda u odnosu na klasične metode Mogućnosti razvoja tenzidno-selektivnih elektroda • Sinteza novih tipova senzorskih materijala • Uvođenje novih nosača senzora

UVOD Površinski aktivne tvari (engleski naziv “surfactant” je izvedenica od surface active agent) ili tenzidi su bifunkcionalni organski spojevi koji se sastoje od hidrofilnog i hidrofobnog dijela. Za tenzide se kaže da imaju glavu (“head”) i rep (“tail”). Glava je hidrofilna (sklona je vodi) i obično se označava kao krug. Rep je u pravilu dugački ugljikovodični lanac (najčešće 8 -20 ugljikovih atoma) i hidrofoban je (odbija vodu, otuda sklon je ulju). Rep se označava ili kao ravna crta i valoviti rep. Hidrofilni ostaci su električki nabijeni (pozitivno ili negativno), ili su neutralne polarne skupine.

Osobine tenzida Molekulska struktura tenzida ukazuje na njihove neuobičajene osobine koje imaju najrazličitije primjene. Te osobine dijele se u dvije široke kategorije: adsorpciju (adsorption) i molekulsko samoudruživanje (self-assembly). Adsorpcija je tendencija molekula tenzida da se skupljaju na granici dvaju faza. Molekule tenzida obično se nalaze na granici uljne i vodene faze ili vodene faze i zraka. Ta molekulska osobina rezultira makroskopskim svojstvima kao što su kvašenje, pjenjenje, emulgiranje itd. Molekule tenzida adsorbiraju se na kapljici ulja. Hidrofilni dio okrenut je vodi, dok je hidrofobni dio okrenut uljnoj fazi:
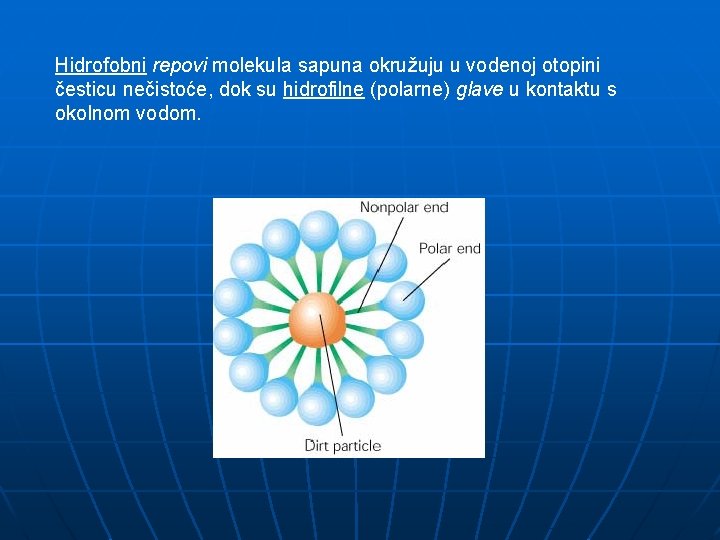
Hidrofobni repovi molekula sapuna okružuju u vodenoj otopini česticu nečistoće, dok su hidrofilne (polarne) glave u kontaktu s okolnom vodom.

Molekulsko samoudruživanje (Self-Assembly) Molekulsko samoudruživanje je tendencija molekula tenzida da se organiziraju u organizirane strukture. To uključuje formiranje micela (micelle), dvosloja (bilayer) i tekućih kristala (liquid crystal). Formiranje micela dopušta hidrofobnim repovima da budu izvan vode a hidrofilnim glavama da ostanu u vodi. U jednoj miceli obično se nalazi nekoliko desetina do nekoliko stotina molekula tenzida.

Molekule tenzida se također u vodi mogu udružiti tvoreći tenzidne dvosloje:
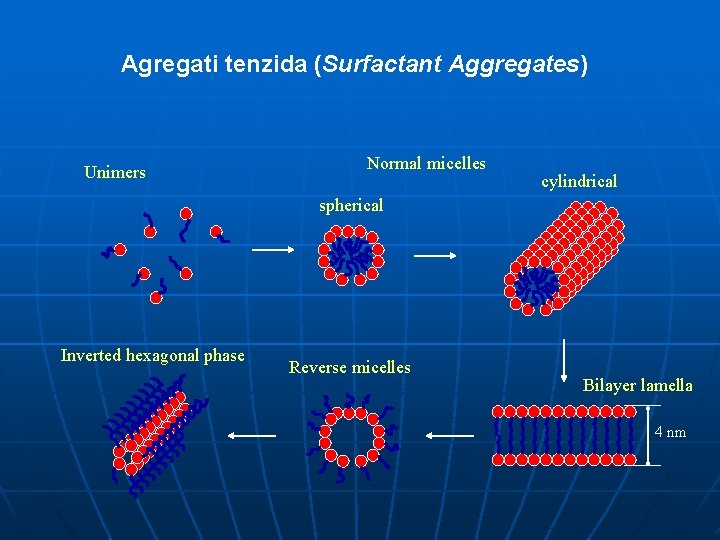
Agregati tenzida (Surfactant Aggregates) Unimers Normal micelles cylindrical spherical Inverted hexagonal phase Reverse micelles Bilayer lamella 4 nm

Kritična koncentracija za stvaranje micela (Critical Micelle Concentration, CMC) Tenzidi egzistiraju kao pojedinačne molekule (monomeri) do jedne granične koncentracije, kritične koncentracije za stvaranje micela (CMC). To je jedno od najvažnijih svojstava tenzida. Micela natrijevog dodecilsulfata: Alifatski lanci usmjereni su ka unutrašnjosti micele, dok su SO 32 - grupe (hidrofilne) usmjerene ka površini.

Kritična koncentracija za stvaranje micela (Critical Micelle Concentration, CMC) CMC 14 12 10 • 8 CMC 6 4 2 0 0 1 Surfactant concentration • Ispod CMC prisutni su samo monomeri Iznad CMC prisutne su micele u ravnoteži s monomerima
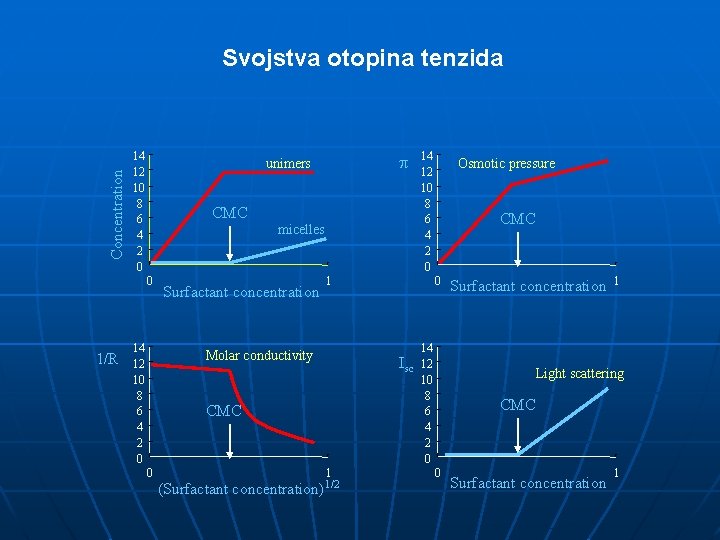
Concentration Svojstva otopina tenzida 14 12 10 8 6 4 2 0 CMC micelles 0 1/R unimers 14 12 10 8 6 4 2 0 Surfactant concentration CMC 14 Isc 12 10 8 6 4 2 0 CMC (Surfactant Osmotic pressure 0 1 Molar conductivity 0 14 12 10 8 6 4 2 0 1 concentration)1/2 Surfactant concentration 1 Light scattering CMC 0 Surfactant concentration 1
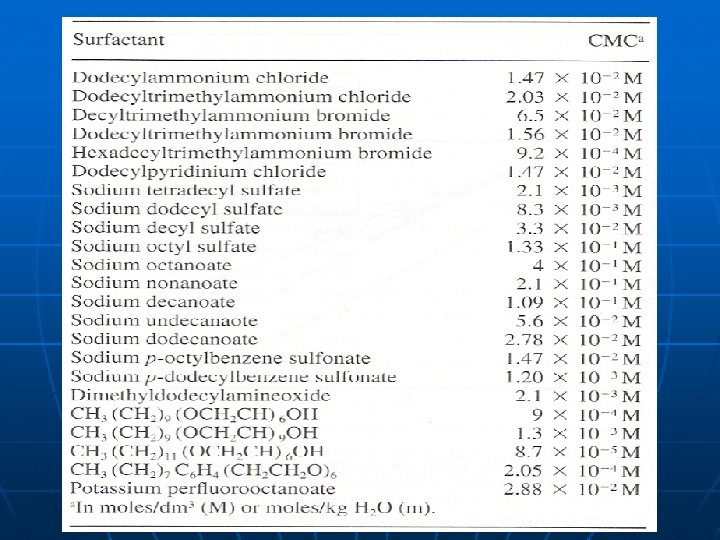

Klasifikacija površinski aktivnih tvari (tenzida) Prema hidrofilnim skupinama u strukturi molekula i njihovom elektrokemijskom ponašanju tenzidi se svrstavaju u četiri glavne kategorije (Tablica 1). Anionski tenzidi su površinski aktivne tvari s jednom ili više funkcionalnih grupa, koje u vodenim otopinama ioniziraju dajući negativno nabijene površinski aktivne organske ione. Kationski tenzidi su površinski aktivne tvari s jednom ili više funkcionalnih grupa, koje u vodenim otopinama ioniziraju dajući pozitivno nabijene površinski aktivne organske ione. Neionski tenzidi su površinski aktivne tvari koje ne disociraju u vodenoj otopini. Topljivost neionskih tenzida u vodi potječe od funkcionalnih grupa u njihovoj strukturi s jakim afinitetom prema vodi. Amfolitski tenzidi su površinski aktivne tvari s jednom ili više funkcionalnih grupa koje u zavisnosti od uvjeta sredine u kojoj se nalaze mogu disocirati u vodenoj otopini tako da spoj dobije karakteristike anionskih ili kationskih tenzida.
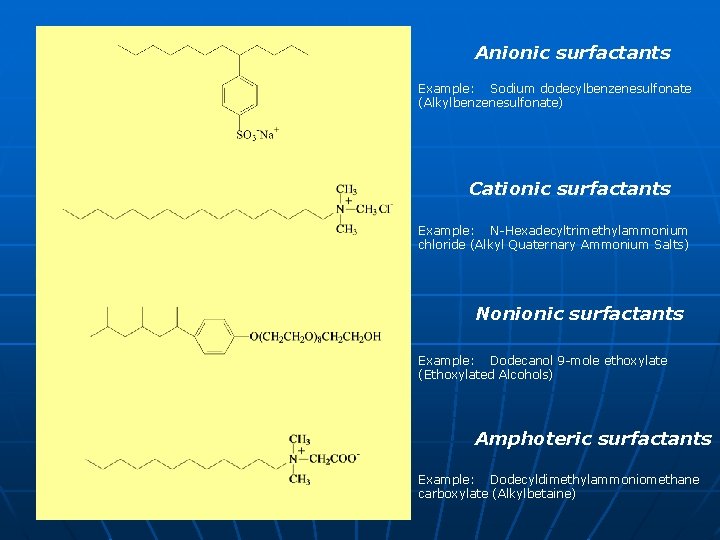
Anionic surfactants Example: Sodium dodecylbenzenesulfonate (Alkylbenzenesulfonate) Cationic surfactants Example: N-Hexadecyltrimethylammonium chloride (Alkyl Quaternary Ammonium Salts) Nonionic surfactants Example: Dodecanol 9 -mole ethoxylate (Ethoxylated Alcohols) Amphoteric surfactants Example: Dodecyldimethylammoniomethane carboxylate (Alkylbetaine)

Ukupna svjetska proizvodnja tenzida u 2003. godini iznosila je oko 18, 2 miliona tona. Vrijednost proizvodnje iznosila je 23. 2 milijarda US$ u 2007. Najveći udio imaju alkilbenzensulfonati, velika skupina anionskih tenzida široko zastupljenih u praškastim detergentima, čija se ukupna svjetska proizvodnja u 2000. godini procjenjuje na oko 3 milijuna tona. Svjetska proizvodnja tenzida (%) prema tipovima tenzida


Razvoj i primjena površinski aktivnih tvari u stalnom je porastu. Današnja opća potražnja za “zelenim proizvodima” nametnula je potrebu razvoja biorazgradljivih i ekološki prihvatljivih tenzida. Tenzidi su danas prisutni u mnoštvu proizvoda za čišćenje u domaćinstvima, sredstvima za čišćenje u industriji, kozmetičkim i farmaceutskim proizvodima, sredstvima za zaštitu bilja itd. Mogu biti u praškastom obliku (praškasti detergenti), u obliku vodenih otopina (tekući detergenti, šamponi, dezinficijensi) i emulzija (kozmetički preparati, sredstva za čišćenje podova i metalnih površina). Iako je u današnje vrijeme u proizvodima većina površinski aktivnih tvari biorazgradljiva, njihovo nakupljanje ili akumulacija produkata njihove razgradnje u prirodnim vodama u ekstremnim slučajevima može dovesti do uništavanja flore i faune. Kao zaključak se nameće činjenica da je analitika tenzida veoma značajna kako za razvoj novih tenzida i njihovu proizvodnju i primjenu u praksi s jedne strane, tako i za njihovu kontrolu u okolišu.

ANALIZA ANIONSKIH TENZIDA Anionski tenzidi su visoko-pjeneće površinski aktivne tvari. Djelotvorniji su od ostalih vrsta tenzida, posebno za uklanjanje zaprljanja s prirodnih tkanina. Lako se raspršuju i kao takvi se koriste u praškastim detergentima. Osjetljivi su na tvrdoću vode, te je iz tog razloga tvrdoj vodi potrebno dodavanje tvari koje kompleksiraju kalcij i magnezij. Izraz alkilbenzensulfonati (ABS) je uobičajeni izraz za anionske tenzide s razgranatim alkilnim lancem. Teško se razgrađuju. Njihova upotreba u razvijenim zemljama je ograničena samo na slučajeve kada njihova primjena neće izazvati zagađenja prirodnih vodotokova (npr. kao emulgatori u agrokemikalijama). Za razliku od ABS, linearni alkilbenzensulfonati (LAS) se lako i brzo razgrađuju u aerobnim uvjetima. LAS imaju najnižu cijenu od svih tenzida i koriste se u cijelom svijetu. Kao i ABS osjetljivi su na tvrdoću vode. Gruba podjela anionskih tenzida prama kemijskoj strukturi lipofilnog dijela molekule tenzida prikazana je u tablici 2. S obzirom na široku primjenu anionskih tenzida u najrazličitijim granama, značaj njihovog analitičkog određivanja u sirovinama, poluproizvodima i gotovim proizvodima kao i u otpadnim vodama, od iznimne je važnosti u kontroli kvalitete istih, ali i u analitici i monitoringu okoliša.


ANALIZA ANIONSKIH TENZIDA n Titracijske metode • Vizualne titracije • Potenciometrijske titracije • Turbidimetrijske metode n Spektrofotometrijske metode n Kromatografske metode n Analiza injektiranjem u protok (Flow injection analysis)

Titracijske metode n n n Titracijske metode su među prvima našle široku primjenu u kvantitativnoj analizi ionskih tenzida. Zasnivaju se na stvaranju ionskih asocijata anionskih tenzida s kationskim titransima, najčešće velikim molekulama nekog kationskog tenzida: Određivanje završne točke može biti vizualno - u prisusutvu indikatora, ili instrumentalno – uz odgovarajući senzor (potenciometrijski, turbidimetrijski, tenzidimetrijski, optički).

Vizualne titracije Vizualnu titraciju anionskog tenzida su prvi puta opisali Hartley i Runnicles 1938. godine u titraciji alkansulfonata s cetilpiridinijevim kloridom uz bromfenol plavo kao indikator. 1948. godine Epton je predstavio novu titrimetrijsku metodu za brzo određivanje anionskih tenzida, u kojoj je iskoristio različitu topljivost anionskog tenzida i ionskog asocijata anionskog tenzida i metilenskog plavila (indikator), u vodi i organskom otapalu (diklormetanu). Kao titrans je upotrijebio Hyamine 1622 (diizobutil-fenoksietoksi-etil-dimetilbenzil-amonijev klorid). Hyamine 1622 Metilensko plavo

Titracija po Eptonu Vodotopivi anionski tenzid (An-) titrira se kationskim tenzidom (Cat+) uz indikator metilensko plavo (MB+) Prije početka titracije: Anionski tenzid (An-) s kationskom bojom metilensko plavo (MB+) stvara 1: 1 - ionski asocijat, topiv u diklormetanu: Titracija: Kationski (Cat+) i anionski (An-) tenzid tvore 1: 1 - ionski asocijat Cat. An, topiv u diklormetanu: Završna točka: Prijelaz indikatora u vodenu fazu (nestanak boje u organskoj fazi):
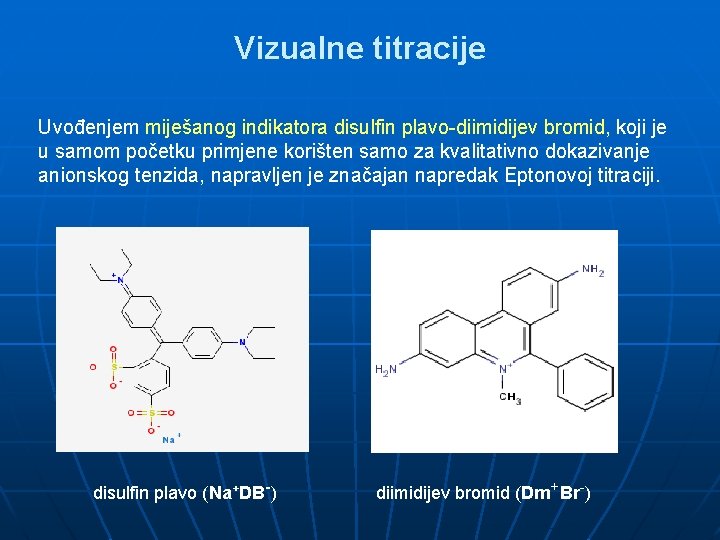
Vizualne titracije Uvođenjem miješanog indikatora disulfin plavo-diimidijev bromid, koji je u samom početku primjene korišten samo za kvalitativno dokazivanje anionskog tenzida, napravljen je značajan napredak Eptonovoj titraciji. disulfin plavo (Na+DB-) diimidijev bromid (Dm+Br-)

Vizualne titracije U usporedbi s ostalim poznatim indikatorima, ovaj daje najoštriji prijelaz u završnoj točki. Sastoji se od anionske (disulfin plavo, Na+DB-) i kationske (diimidijev bromid, Dm+Br-) boje, a sama titracija se odvija u kiseloj sredini, u nekoliko reakcija otapanja i kompleksiranja. U suvišku anionskog tenzida kloroformni sloj je obojen ružičasto: Dm+ + An- Dm. An kloroform a u suvišku kationskog tenzida se oboji plavo: Cat+ + DB- Cat. DB kloroform

Vizualne titracije Titracija u dvije faze Otopina uzorka je stavljena u titracijsku posudu (odmjerni cilindar), dodani su miješani indikator i kloroform i dvofazna smjesa je protrešena ili miješana. Ružičasti kationski indikator diimidij-bromid (Dm+Br-) reagira s anionskim tenzidom (An-), a produkt reakcije ekstrahira se kloroformom, bojeći ga u ružičasto: Dm+ + An- Dm. An kloroform Vodeni sloj je u ovoj fazi žut (disulfin plavo je također i kiselo-bazni indikator; žut je u kiselim otopinama, a plav u alkalnim). Kationski titrant (Cat+) dodaje se u malim inkrementima, uz temeljito miješanje između dodataka.

Procesi pri titraciji u dvije faze: 1) Kationski titrant (Cat+) reagira prvo s anionskim tenzidom (An-) u vodenom sloju, pri tome nastaje bezbojna sol koja se ekstrahira kloroformom: Cat+ + An- Cat. An kloroform 2) Kada je većina anionskog tenzida u vodenom sloju istitrirana, daljnji inkrementi kationskog tenzida počinju istiskivati kationski indikator iz njegove soli s anionskim tenzidom (Dm. An) u kloroformnom sloju, a ružičasta boja počinje migrirati natrag u vodeni sloj: Cat+ (voda) + Dm. An (CHCl 3) Cat. An (CHCl 3) + Dm+ (voda) 3) Kada je na taj način sav kationski indikator istisnut, kloroformni sloj je gotovo bezbojan – točnije, neutralno je sive boje. To je završna točka titracije. Vodeni sloj je narančast. 4) Daljnji inkrementi kationskog titranta reagiraju s anionskim indikatorom disulfinplavo (DB-). Sol je ekstrahirana u kloroformnom sloju i boja ga plavo. To ukazuje da je završna točka premašena: Cat+ + DB- Cat. DB kloroform Te promjene boje su obrnute kada se kationski tenzid titrira anionskim.

Titracija u dvije faze Titrant Testirajući različite kationske tenzide velikih molekula, diizobutil-fenoksietoksi-etildimetil-benzil-amonijev klorid, poznatiji kao benzetonijev klorid ili Hyamine 1622 kojeg je još Epton odabrao za titrans za određivanje anionskih tenzida, pokazao je niz prednosti u odnosu na ostale: Prednosti: Økomercijalna dostupnost u obliku čistog monohidrata Øniska cijena Ødobra topljivost u vodi Østabilnost otopine bez efekta kristalizacije.

Titracija u dvije faze Budući da u kombinaciji s miješanim indikatorom disulfin plavo-diimidijev bromid Hyamine 1622 daje dobro uočljiv prijelaz u završnoj točki, uveden je kao standardni titrans u opisanoj titraciji u dvije faze za kvantitativno određivanje anionskih tenzida u sirovinama anionskih tenzida i proizvodima koji ih sadrže. Titracija se u ovom obliku godinama primjenjuje u analitici ionskih tenzida kao standardna metoda. Unatoč nizu nedostataka ova metoda je referentna i danas. Još uvijek se koristi u mnogim laboratorijima.

Titracija u dvije faze Nedostaci: vizualna detekcija završne točke (problem kod mutnih i obojenih uzoraka) Ø točnost određivanja ovisi o iskustvu analitičara koji ju izvodi Ø primjenjivost upitna kod sve složenijih sastava detergenata (kemijske interferencije), posebice onih namijenjenih pranju modernih tkanina Ø metoda se teško može automatizirati Ø uporaba kloroforma, kancerogenog organoklornog organskog otapala Ø povećani troškovi za zbrinjavanje otpada. Ø

Titracija u dvije faze Titracija sapuna Sapuni su anionske površinski aktivne tvari, koje imaju značajnu funkciju u obaranju pjene u detergentima za strojno pranje rublja. natrijev oleat natrijev stearat Primjena sapuna kao sredstva za obaranje pjene obilježava čitavu jednu epohu u detergentskoj industriji koja je uslijedila nakon uvođenja masovne primjene perilica za pranje rublja, i u izvjesnoj mjeri traje sve do danas. U modernim sastavima ih sve češće zamjenjuju tzv. antipjeniči.

Titracija u dvije faze Titracija sapuna Iako su sapuni, kao i anionski tenzidi po svojoj prirodi površinski aktivne tvari, titracijom uz disulfin plavo-diimidijev bromid se ne titriraju. U kiselom p. H-području sapuni su prisutni kao slobodne masne kiseline: Sapuni se titriraju u alkalnom p. H-području uz 2, 7 -diklorofluorescein kao indikator i kationski tenzid (Hyamine 1622, Cat+) kao titrans:

Titracija u dvije faze Titracija sapuna U detergentima koji uz sintetske anionske tenzide (alkilbenzensulfonate , alkilsulfate i dr. ) sadrže i sapune, sadržaj sapuna se određuje iz razlike utrošaka titransa (Hyamine 1622, Cat+), u titracijama uz disulfin plavo-diimidijev bromid i 2, 7 diklorofluorescein. 1. Titracija (uz miješani kiseli indikator disulfin plavo-diimidijev bromid) titriraju se samo sintetski anionski tenzidi, An-: 2. Titracija (uz 2, 7 -diklorfluorescin kao indikator, u alkalnoj sredini), zajedno s anionskim tenzidima (An- ) titriraju se i sapuni (RCOO-): Razlika utrošaka između prve i druge titracije odgovara sadržaju sapuna.

Titracija u dvije faze Titracije ionskih tenzida su po svojoj prirodi stehiometrijske reakcije u kojima se određuje molarna koncentracija. Za preračunavanje u masenu koncentraciju potrebno je imati točne podatke o molekulskim masama analita. Ukoliko nam je analit nepoznat, podatke o molarnoj koncentraciji dobivene titiracijskim metodama je potrebno upotpuniti podacima dobivenim nekom od identifikacijskih metoda (HPLC, LC ili GC vezanim sustavima u kojima se kromatografske tehnike kombiniraju s masenom sprektroskopijom, IRspektroskopija, NMR).

Spektrofotometrijske metode su metode vrlo visoke osjetljivosti. Spektrofotometrija u ultraljubičastom i vidljivom području (UV-VIS spectroscopy) se koristi za kvantitativna određivanja anionskih tenzida. U literaturi su poznata brojna istraživanja u kojima je bio cilj pronaći kationsku boju specifičnu i osjetljivu za anionski tenzid kao analit. MBAS - metoda Kao standardna metoda za određivanje anionskih tenzida u otpadnim vodama koristi se tzv. MBAS metoda (Methylene Blue Active Substances), spektrofotometrijska metoda u kojoj se kao kationska boja koristi metilensko plavilo (MB). Ova metoda se koristi već više od pola stoljeća za određivanje niskih koncentracija anionskih tenzida.

MBAS - metoda Metoda se zasniva na stvaranju ionskog asocijata (MBAn) anionskog tenzida (An-) i metilenskog plavila (MB+), koji se zatim ekstrahira s pogodnim organskim otapalom (kloroformom), dok sama boja u njemu nije topljiva. Intenzitet obojenja proporcionalan je koncentraciji tenzida. Anionski tenzid (An-) s kationskom bojom metilensko plavo (MB+) stvara 1: 1 - ionski asocijat, topiv u kloroformu:

MBAS – metoda Princip određivanja u MBAS metodi veoma je sličan principu koji se koristi u titraciji u dvije faze. Njom se određuju samo anionski tenzidi (NE i sapuni !), budući da se određivanje izvodi u kiselom mediju. Metoda ima ograničenja u praksi jednaka kao i titracija u dvije faze, budući da još neki anionski materijali, koji nisu tenzidi, s metilenskim plavilom formiraju ionski par topljiv u organskom otapalu. Naime, metoda koja se zasniva na ekstrakciji asocijata nekog aniona i metilenskog plavila s organskim otapalom, primjenjuje se i za određivanje tetrafluoroborata, perklorata i tiocijanata, kao i cijanokompleksa prijelaznih metala. Spektrofotometrijske tehnike su pogodne za automatizaciju određivanja što je rezultiralo primjenom tehnike s injektiranjem u protok (Flow Injection Analysis, FIA) za određivanje anionskih tenzida u otpadnim vodama.

ANALIZA KATIONSKIH TENZIDA kationski tenzidi (cationic surfactants, CS) predstavljaju samo 5 -6% ukupno proizvedenih tenzida, - najčešće su kvarterni amonijevi spojevi: R 1 R 2 R 3 R 4 N+X- X=Cl-, Br R=alkilna grupa: - X dobro podnose promjene p. H, - u aerobnim uvjetima biorazgradivi, ali zadržavaju toksičnost i pri malim koncentracijama. -

ANALIZA KATIONSKIH TENZIDA Primjena imaju antimikrobna, baktericidna, antikorozijska i antistatička svojstva, te svojstva lakog stvaranja emulzija, - vrlo su često korišteni u industrijskim, dezinfekcijskim, kozmetičkim i farmaceutskim proizvodima, algicidnim sredstvima, sredstvima za suzbijanje plijesni, te sredstvima za čišćenje, - za čišćenje i dezinfekciju operacijskih dvorana i opreme, sterilizaciju boca (industrija hrane i pića), - često kombinirani s neionskim tenzidima, ali ne i s anionskim, - smjese tenzida imaju bolja svojstva od sustava samo s jednom vrstom tenzida, omogućavaju korištenje kemikalija manje čistoće niža cijena, - budući da se velike količine kationskih tenzida svakodnevno proizvode i koriste, te s obzirom na činjenicu da su zagađivači okoliša vrlo je važno moći odrediti njihove točne koncentracije. -

ANALIZA KATIONSKIH TENZIDA Volumetrijske metode koncentracija tenzida određuje se na temelju utrošenog volumena titransa poznate koncentracije. - Titracija u dvije faze: princip: stvaranje ionskog para s ionom suprotnog naboja, - referentna metoda za određivanje CS, - temelji se na ekstrakciji ionskog para CS i anionske boje u organskom otapalu (kloroform), - zatim se dodaje AS (titrans) koji prvo reagira s CS u vodenom sloju, a zatim istiskuje anionski indikator iz njegove soli s CS pri čemu boja koja sama nije topiva u organskom sloju odlazi u vodeni sloj, - kad je sav indikator istisnut, organski sloj se obezboji (E. P. ), - vizualno određivanje E. P. brojni nedostaci. -

ANALIZA KATIONSKIH TENZIDA Potenciometrijske metode - tenzidno-selektivne elektrode kao indikatori u direktnoj potenciometriji i potenciometrijskim titracijama, zasniva se na stvaranju ionskog para između suprotno nabijenih iona: CS i AS (anionic surfactant) kao titransa, - 1970. prva tenzidna ISE s tekućom membranom za CS slijedi razvoj različitih membrana (čvrste, tekuće s kompleksom CS i AS, prevučene preko Al-žice, modificirane molekulskim sitima, screenprinted elektrode, komercijalne. . . ), razne varijacije senzorskih materijala i plastifikatora kako bi se dobila elektroda sa što bržim odzivom, bez interferencija, sa što nižom granicom detekcije, širim rasponom djelovanja, . . . -

ANALIZA KATIONSKIH TENZIDA Spektrofotometrijske metode intenzitet obojenja proporcionalan je koncentraciji tenzida, - tenzid stvara kompleks s bojom suprotnog naboja i utječe na njen spektar, - temelje se na ekstrakciji ionskog asocijata CS i anionske boje u organskom otapalu pri čemu asocijat mora biti lako topiv u org. otapalu, a netopiv u vodi, a boja obrnuto, - mjerenjem apsorbancije određuje se koncentracija CS, - kako bi se pronašla optimalne metoda, ispituje se stvaranje kompleksa s različitim bojama. -

ANALIZA KATIONSKIH TENZIDA Ostale metode mikrofluidičke metode - Ružička i Hansen 1975. – analitički postupak s injektiranjem u protok (FIA), - povećanje brzine i učinkovitosti serijskom analizom uzoraka, točno, precizno, automatizirano, - najčešće uz spektrofotometrijski (UV-Vis) detektor. - kromatografske metode - visoka cijena, dugotrajnost, priprema uzoraka. - kapilarna elektroforeza - kraća analiza i priprema uzoraka, manje reagensa, - nedostatak je adsorpcija tenzida na stjenkama kapilare. -

ANALIZA NEIONSKIH TENZIDA Neionski tenzidi se razlikuje od ionskih po tome što su njihove molekule u vodenoj otopini nedisocirane. 1. Polietilenglikoleteri masnih alkohola ili etoksilati masnih alkohola (Fatty alcohol poly(ethylene glycol) ether or fatty alcohol ethoxylate, FAE) Najveći broj neionskih tenzida u svojoj strukturi imaju hidrofobnu skupinu, npr. kratak polimerni lanac, dok je hidrofilna skupina poli(etoksilirani) lanac, u vodi topljiv polimer s najčešće 6 do 100 etoksi (EO) jedinica.

ANALIZA NEIONSKIH TENZIDA Najrasprostranjeniji od svih komercijalnih neionskih tenzida su oni dobiveni od masnih alkohola i etilen oksida. Masni alkoholi mogu biti: Prirodni: dobivaju se od biljnih ulja i masti. Iako postoje mnogi postupci za dobivanje prirodnih masnih alkohola, najčešće se dobivaju redukcijom masnih kiselina ili estera masnih kiselina. Ø Ø Sintetički: alkoholi dobiveni Zieglerovom metodom imaju alkilni lanac s parnim brojem ugljikovih atoma (C 12 to C 20). S druge strane alkilni lanac alkohola dobivenim Oxo-procesom može imati neparan broj ili paran i neparan broj ugljikovih atoma.

ANALIZA NEIONSKIH TENZIDA 2. Alkilpoliglukozidi (Alkyl polyglucoside, APG) Drugu skupinu neionskih tenzida čine tenzidi koji su po svojoj kemijskoj strukturi alkilpoliglukozidi. Ova skupina je svoj komercijani značaj dobila u posljednjih dvadesetak godina i čini tzv. “novu generaciju neionskih tenzida”. U njihovim molekulama je hidrofilna skupina šećer, najčešće polisahard, ali mogu biti i disaharidi, trisaharidi i ostali šećeri. Alkyl polyglucoside (where n = 1 to 3, and R = C 9 - C 13).

ANALIZA NEIONSKIH TENZIDA n n n Alkilpoliglukozide (APG) prvi je puta opisao Emil Fisher prije više od 100 godina i od 1922 proizvode se u velikim količinama. Ovi tenzidi sastoje se od masnog alkohola kao hidrofobnog dijela i glukoze kao hidrofilnog dijela, pri čemu se hidrofilnost može varirati preko stupnja oligomerizacije. Njihova sinteza (Fisherova sinteza) koristi potpuno obnovljive proizvode. APG se koriste u praškastim proizvodima, a posebice u tekućim detergentima, tekućim sredstvima za pranje suđa i gelovima za tuširanje. Posjeduju visoku moć pjenušanja, blago djeluju na kožu i lako su biorazgradljivi. Očekuje se da će APG igrati važnu ulogu u budućnosti.

ANALIZA NEIONSKIH TENZIDA n Titracijske metode • Vizualne titracije • Potenciometrijske titracije n Spektrofotometrijske metode n Tenzametrijske metode

Titracijske metode Vizualne titracije Jedna od prvih vizualnih titracija opisana za određivanje neionskih (NS) tenzida je titracija s cinkovim sulfatom. Neionski tenzid se prvo prevede u kompleksni spoj s kalijevim ferocijanidom: a zatim se nastali kompleks titrira s cinkovim sulfatom uz difenilamin kao indikator:

Titracijske metode Vizualne titracije Kasnije je opisana reakcija taloženja polietilenglikola s natrijevim tetrafenilboratom u prisustvu barijeva(II) klorida: i titracija taloga živinim nitratom: Zaključeno je da polietilenglikol s tetrafenilboratom i barijem ne reagira stehiometrijski i ustanovljeno da je molarni odnos tetrafenilborata i barija u istaloženom kompleksu uvijek bio 1: 2. Vizualne titracije danas nemaju značajnu primjenu u analizi neionskih tenzida, ali su važne jer su prethodile razvoju potenciometrijskih titracija.

Spektrofotometrijske metode se kao i potenciometrijske titracije zasnivaju na sposobnosti polietera, u ovom slučaju etoksiliranih neionskih tenzida (EONS), da formiraju komplekse s velikim metalnim kationima kao što su Pb 2+ ili Ba 2+ : Standardna metoda za određivanje sadržaja neionskih tenzida u otpadnim vodama poznata kao Bi. AS (Bismuth Active Substances) metoda se zasniva na taloženju neionskih tenzida s modificirnim Dragendorffovim regensom (otopina kalijeva tetrajodobizmutata i barijevog klorida): U nastalom talogu se nakon otapanja u vrućoj otopini amonijevog tartarata koncentracija bizmuta određuje potenciometrijski, atomskom apsorpcijskom spektrometrijom (AAS) ili ultraljubičastom spektrofotometrijom.

Spektrofotometrijske metode Bi. AS metodom se određuju samo etoksilirani neionski tenzidi (alkohol etoksilati, alkilfenol etoksilati). Metoda se službeno primjenjuje za ispitivanja biorazgradljivosti tenzida. I ova je metoda iskorištena za automatizaciju primjenom tehnike s injektiranjem u protok (FIA)

POTENCIOMETRIJSKI SENZORI (BIO)KEMIJSKI SENZORI (Bio)kemijski senzori su uređaji za pretvorbu kemijske ili biološke veličine u električni signal. Područje primjene kemijskih senzora je raznoliko. Ciljani analiti mogu biti razni kationi ili anioni, zatim plinovi, otrovne organske pare, različiti metaboliti, proteini, mikroorganizmi itd. Veliku podgrupu kemijskih senzora čine biosenzori, senzori koji određuju neku biološku veličinu (šećere, proteine, enzime, antitijela). Najrazvijenija grupa senzora su elektrokemijski senzori. S obzirom na elektrokemijsku veličinu koju mjere, dijele se na potenciometrijske (napon), amperometrijske (struja) i konduktometrijske senzore (otpor). Zajednička karakteristika im je da koriste elektrode na kojima se odvijaju kemijske reakcije ili na njima dolazi do izmjene prijenosa naboja. Ime senzora koje se koristi u praksi često oblikuje veličina koja biva pretvorena u električni signal, i/ili princip konverzije.

Tako se npr. kemijski senzori za detekciju plinova u zraku nazivaju plinski senzori, kemijski senzor za detekciju vlage skraćeno se naziva senzor vlage, amperometrijski senzor za određivanje šećera u krvi glukozni senzor itd. Kemijski senzori omogućavaju određivanje ciljanog analita u prisutnosti interferirajućih sastojaka. Imaju sposobnost više ili manje selektivnog prepoznavanja analita. Shema kemijskog senzora Za selektivno vezanje analita na senzor odgovoran je element za prepoznavanje (recognition element) tzv. receptor. Kao posljedica interakcije analita i receptora dolazi do promjene jednog ili više fizikalno-kemijskih parametara. Pretvornik ih prevodi u mjerljiv izlazni signal, koji se može pojačati, obrađivati i prikazivati u pogodnom obliku.

Dobre osobine kemijskog senzora postižu se dobrim odabirom receptora i pretvornika. Karakteristike senzora određuje njegova selektivnost, osjetljivost, stabilnost i trajnost. Selektivnost pokazuje u kojoj mjeri senzor razlikuje analit od supstanci slične ili različite kemijske strukture, i praktično je određena elementom za prepoznavanje (receptorom). Osjetljivost senzora je određena receptorom i pretvornikom. Osjetljivot senzora moguće je povećati uvođenjem dodatnih stupnjeva pojačavanja signala, i tako povećati njegovu preciznost i sniziti granicu detekcije. Kod potenciometrijskih senzora pri interakciji analita i receptora dolazi do promjene elektrodnog potencijala receptora u funkciji koncentracije analita. Pretvornik pojačava izlazni naponski signal (pri nultoj struji), obrađuje ga i prikazuje u pogodnom obliku.

IONSKO-SELEKTIVNE ELEKTRODE Ionsko-selektivne elektrode (ion-selective electrode, ISE) su elektrokemijski senzori koji omogućavaju potenciometrijsko određivanje analita. Pokazuju selektivan odziv na neki od iona prisutnih u otopini. Potencijal takve elektrode logaritamski ovisi o aktivitetu iona na kojeg je elektroda selektivna. Mjerenje ionsko-selektivnom elektrodom se izvodi u elektrokemijskoj mjernoj ćeliji koja se sastoji od dva galvanska polučlanka: ionskoselektivne elektrode i referentne elektrode: Elektrokemijska mjerna ćelija s ionsko-selektivnom elektrodom

Za osjetljivo i selektivno prepoznavanje određene ionske vrste odgovorna je membrana. Prema sastavu membrane, ionsko-selektivne elektrode se mogu podijeliti na elektrode sa čvrstom membranom i elektrode s ionskoizmjenjivačkom membranom. Elektrode sa čvrstom membranom su elektrode čija je membrana sastavljena od jedne ili više kristaličnih tvari. Potencijal takve membrane ovisan je o koncentraciji iona prenosioca naboja uz njenu površinu. Elektrode s ionsko-izmjenjivačkom membranom su elektrode čija membrana sadrži tvar koja posjeduje sposobnost izmjene iona. Ove elektrode mogu biti izrađene od posebne vrste stakla (npr. staklena p. H-elektroda) ili od neke organske ionsko-izmjenjivačke tvari otopljene u pogodnom otapalu u plastičnom (najčešće PVC) matriksu. Potencijal membrane određen je izmjenom iona iz otopine s ionima vezanim na izmjenjivačku tvar u membrani.

Ionsko-selektivne elektrode su jeftini i jednostavni uređaji koji mogu biti minijaturizirani, pomoću njih se mogu izvoditi on-line i in situ mjerenja i dobiti čitav niz informacija koje se ne mogu dobiti drugim analitičkim tehnikama. U idealnom slučaju one ne troše nikakav analit tijekom mjerenja i obično ne zahtijevaju nikakvu posebnu pripremu uzorka. Imaju široku primjenu, posebno značajnu u kliničkim analizama kada su potrebni mjerni instrumenti za mjerenja veoma malih uzoraka ili za in-situ mjerenja.

Odziv ionsko-selektivne elektrode Ionsko-selektivne membrane potenciometrijskih ionsko-selektivnih elektroda reagiraju više ili manje selektivno na određenu ionsku vrstu označenu kao analit. U idealnom slučaju na membrani nastaje potencijal koji odgovara Nernstovoj jednadžbi: (1) Izraz se označava kao Nernstov nagib elektrode S.

Aktivitet iona u otopini je termodinamička veličina. Pojednostavljeno predstavlja produkt srednjeg koeficijenta aktiviteta f i koncentracije c: (2) U idealnim otopinama vrijednost za f iznosi 1, iz čega proizlazi da je aktivitet iona jednaka njegovoj koncentraciji. Teorijski se f za otopine više ionske jakosti izračunava iz proširene Debye. Hückelove jednadžbe: (3) r = efektivni ionski radius, A, B = konstante ovisne o temperaturi i prirodi otapala, I = ionska jakost. Ionska jakost se izračunava prema izrazu: (4)

U praksi se koeficijent aktiviteta f za otopine niže ionske jakosti (I<0, 5) izračunava pomoću Daviesove jednadžbe: (5) gdje A za vodu kao otapalo ima vrijednost 0, 512. Aktivitet primarnog iona u membrani, aa, M se u idealnom slučaju može smatrati konstantnom, pa izraz (1) nakon transformacije glasi: (6)
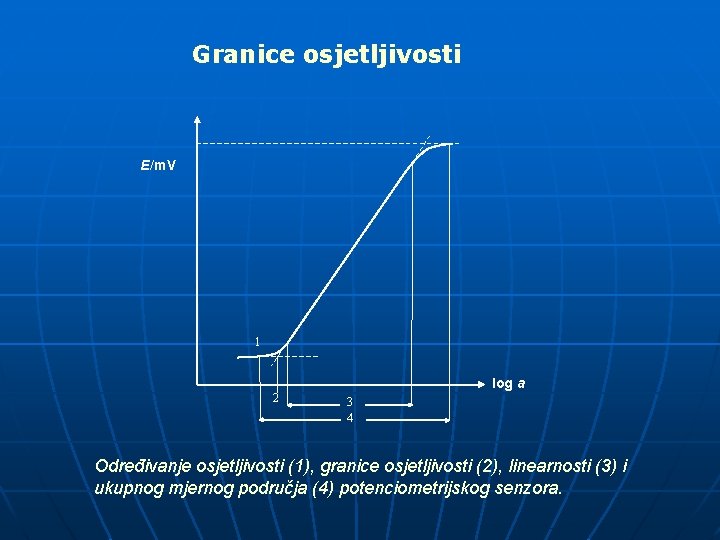
Granice osjetljivosti E/m. V 1 2 log a 3 4 Određivanje osjetljivosti (1), granice osjetljivosti (2), linearnosti (3) i ukupnog mjernog područja (4) potenciometrijskog senzora.

Kemijske interferencije / selektivnost Selektivnost ionsko-selektivne elektrode određuje njezinu osjetljivost kada otopina uz primarni ion (analit) A, sadrži i interferirajući ion B. Odziv membrane u prisustvu nekoliko vrsta iona uvjetovan je konstantama ravnoteže reakcija izmjene primarnog i interferirajućeg iona između organske i vodene faze. Rezultirajući potencijal se može točno opisati pomoću koeficijenata potenciometrijske selektivnosti, ne znajući pri tome niti jednu konstantu ravnoteže.

Utjecaj interferenta na odziv ionsko-selektivne elektrode (potenciometrijskog senzora) opisan je Nikolskii–Eisenmanovom (N-E) jednadžbom: E = elektromotorna sila galvanskog članka, E Ө = standardni elektrodni potencijal, = Nernstov nagib, = koeficijent potenciometrijske selektivnosti, = aktiviteti iona analita A i interferenta B, z. A, z. B = naboji iona analita A i interferenta B.

Metode određivanja koeficijenata potenciometrijske selektivnosti Metode za određivanje koeficijenata potenciometrijske selektivnosti pripadaju mjerenjima koja se mogu svrstati u dvije glavne grupe: metode miješanih otopina Ø metode odvojenih otopina. Ø Metode miješanih otopina su: metoda stalne interferencije, metoda stalnog primarnog iona, metoda dviju otopina i metoda usporednog potencijala. Metode odvojenih otopina su: metoda odvojenih otopina (a. A = a. B) i metoda odvojenih otopina (EA = EB).

Metode miješanih otopina Najčešće se koristi metoda stalne interferencije, koja pripada skupini metoda miješanih otopina. Od četiri metode miješanih otopina, metoda usporednog potencijala je posebna po tome što ne ovisi o Nikolskii-Eisenmanovoj jednadžbi niti bilo kojoj od njezinih izmjena. Metoda je 1995. godine preporučena od IUPAC-a kao metoda koja daje analitički relevantne koeficijente selektivnosti za slučajeve kada je potrebno ispitati interferencije iona različitih naboja ili čak molekula bez naboja.

Metoda stalne interferencije (Fixed Interference Method, FIM) Metoda stalne interferencije pripada grupi metoda miješanih otopina. Elektromotorna sila galvanskog članka koji se sastoji od ionskoselektivne elektrode i referentne elektrode, se mjeri u otopini stalnog aktiviteta interferenta a. B, i promjenjivog aktiviteta analita, a. A. Metoda stalne koncentracije interferenta daje realnije podatke nego metoda odvojenih otopina. Odziv elektrode se mjeri u seriji otopina promjenjivog aktiviteta analita a. A i stalnog aktiviteta interferenta a. B. Koeficijent selektivnosti se potom odredi grafički, što je vrlo subjektivna i neprecizna metoda.

Mnogo je pouzdanija metoda prilagođavanje Nikolskii–Eisenmanove jednadžbe (koja se koristi kao model) eksperimentalnim podacima dobivenim metodom konstantne koncentracije interferenta. Za slučaj anionske tenzidno-selektivne elektrode (z. A= -1, z. B = -1 ) N-E jednadžba glasi: Korištenjem Solvera, analitičkog alata uključenog u Microsoft Excel, izračunava se minimalna suma razlika kvadrata varirajući vrijednosti EӨ, nagib, , a. A i a. B. selectivity. xls
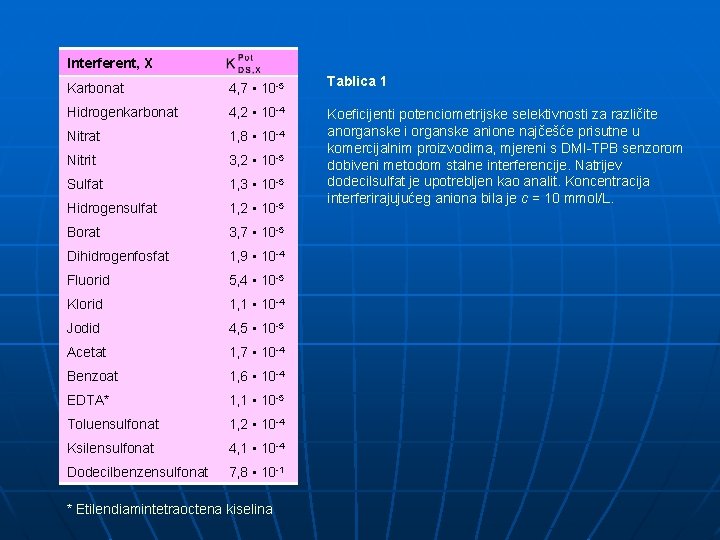
Interferent, X Karbonat 4, 7 • 10 -5 Hidrogenkarbonat 4, 2 • 10 -4 Nitrat 1, 8 • 10 -4 Nitrit 3, 2 • 10 -5 Sulfat 1, 3 • 10 -5 Hidrogensulfat 1, 2 • 10 -5 Borat 3, 7 • 10 -5 Dihidrogenfosfat 1, 9 • 10 -4 Fluorid 5, 4 • 10 -5 Klorid 1, 1 • 10 -4 Jodid 4, 5 • 10 -5 Acetat 1, 7 • 10 -4 Benzoat 1, 6 • 10 -4 EDTA* 1, 1 • 10 -5 Toluensulfonat 1, 2 • 10 -4 Ksilensulfonat 4, 1 • 10 -4 Dodecilbenzensulfonat 7, 8 • 10 -1 * Etilendiamintetraoctena kiselina Tablica 1 Koeficijenti potenciometrijske selektivnosti za različite anorganske i organske anione najčešće prisutne u komercijalnim proizvodima, mjereni s DMI-TPB senzorom dobiveni metodom stalne interferencije. Natrijev dodecilsulfat je upotrebljen kao analit. Koncentracija interferirajujućeg aniona bila je c = 10 mmol/L.

Metoda usporednog potencijala Prethodno spomenute metode određivanja koeficijenta potenciometrijske selektivnosti vrijede samo u slučaju Nernstovskog ponašanja elektrode u odnosu na analit i interferent. Potrebu za iznalažanjem metode neovisne o Nikolskii–Eisenmanovoj jednadžbi prvi su diskutirali Gadzekpo i Christian 1984. godine *. Predložili su tzv. “metodu usporednog potencijala“ [Matched potential method (MPM)], koja je potpuno neovisna o Nikolskii–Eisenmanovoj jednadžbi, i koja je trebala prevladati teškoće pri izračunavanju koeficijenata selektivnosti, kad su uključeni ioni različitog naboja, ili čak i neutralne molekule (npr. neionski tenzidi). * V. P. Gadzekpo, G. D. Christian: Anal. Chim. Acta 164 (1984) 279 -282

Ta je metoda strogo ovisna o eksperimentalnim uvjetima, prvenstveno koncentraciji, pa se umjesto pojma «koeficijent» s velikim slovom K koristi pojam «faktor» s malim slovom k, koji se inače primjenjuje u svim slučajevima ne-Nernstovskog odziva elektrode. Pri tome se faktor selektivnosti definira kao odnos aktiviteta (koncentracija) analita i interferenta koji daje jednaku promjenu potencijala u referentnoj otopini: (1) gdje su a. A i a. B aktiviteti analita i interferenta.

Faktor potenciometrijske selektivnosti se određuje tako što se prvo izmjeri promjena potencijala nakon promjene aktiviteta (koncentracije) analita (iona ili molekule). Potom se u identičnu referentnu otopinu dodaje interferent sve dok se ne dobije ista promjena potencijala, tj. EA=EInt. Primijenjujući tu metodu na etoksilirane neionske tenzide (EONS), te koristeći koncentracije umjesto aktiviteta (što je prihvatljivo, jer su sva izračunavanja provedena pri koncentracijama ispod 10 -3 mol/L), jednadžba se može napisati kao: (2) Promjena koncentracije analita dana je kao: (3) gdje je = izmjerena koncentracija EONS, a = koncentracija EONS u početnoj referentnoj otopini.

Elektrodni potencijal pri dan je relacijom: (4) te se nakon preuređenja dobije jednadžba: (5) Analogno, promjena koncentracije interferenta dana je sljedećim izrazom: (6) gdje je = izmjerena koncentracija interferenta a = koncentracija interferenta u početnoj referentnoj otopini. Elektrodni potencijal pri dan je izrazom: (7)
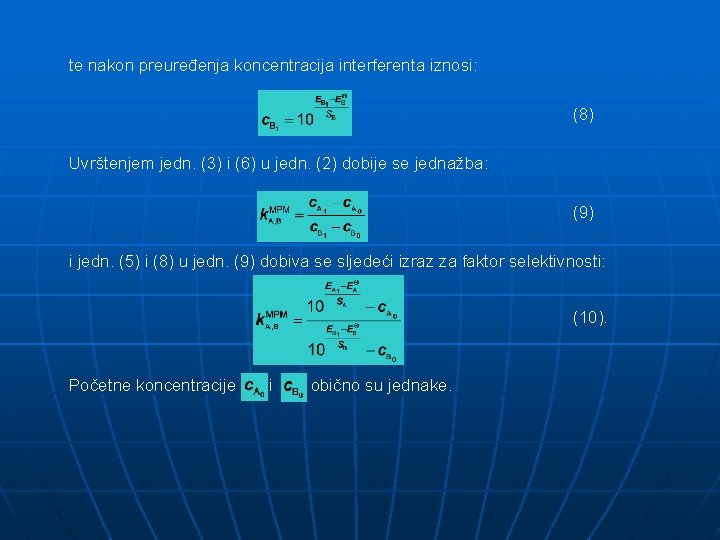
te nakon preuređenja koncentracija interferenta iznosi: (8) (9) Uvrštenjem jedn. (3) i (6) u jedn. (2) dobije se jednažba: i jedn. (5) i (8) u jedn. (9) dobiva se sljedeći izraz za faktor selektivnosti: (10). Početne koncentracije i obično su jednake.
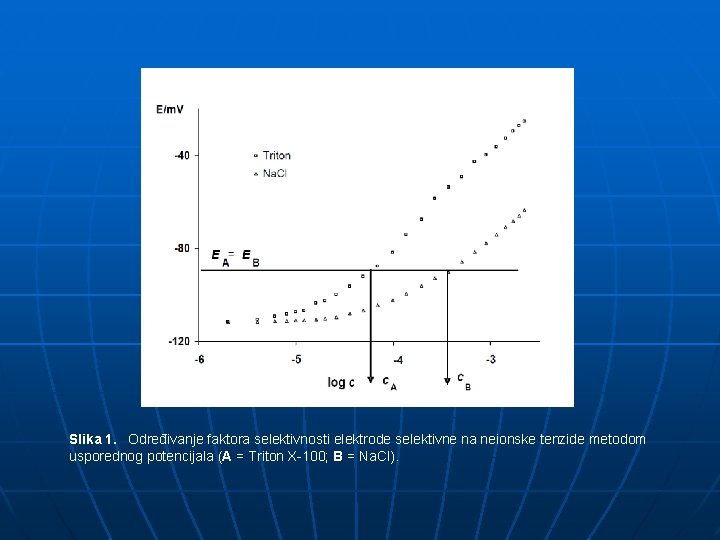
Slika 1. Određivanje faktora selektivnosti elektrode selektivne na neionske tenzide metodom usporednog potencijala (A = Triton X-100; B = Na. Cl).

Jednadžba (10) može se upotrijebiti za izračunavanje koeficijenta selektivnosti interferent, u području zajedničkih vrijednosti elektrodnih potencijala. Na taj način se mukotrpno i subjektivno grafičko određivanje faktora selektivnosti može zamijeniti točnijom i preciznijom numeričkom metodom (slika 1. ).

Selektivnost i odziv elektrode: - Pri konstantnom backgroundu matrice (Störionenhintergrund) ioni interferenta daju konstantan osnovni signal, - Interferirajući ioni (interferenti) su aditivni, mijenjaju osnovni signal ali ne i nagib (slope). Teorija vrijedi samo pri konstantnom backgroundu.

Smisao koeficijenata selektivnosti - - Podatak o koeficijentima selektivnosti omogućava procjenu grešaka i njihovu korekciju matematičkim metodama. Koje je značenje koeficijenta selektivnosti : log = -2. 7 To znači da natrij i kalij daju podjednak signal, ako je koncentracija natrija 102. 7 puta (ili 500 puta) viša od koncentracije kalija.

TENZIDNE IONSKO-SELEKTIVNE ELEKTRODE (Surfactant selective electrodes, surfactant sensors)

TENZIDNE IONSKO-SELEKTIVNE ELEKTRODE Tenzidne ionsko-selektivne elektrode (tenzidni senzori, surfactant sensors) su elektrokemijski senzori koji omogućavaju potenciometrijsko određivanje površinski aktivnih tvari (tenzida). Potencijal takve elektrode logaritamski ovisi o aktivitetu tenzidnog iona/molekule na kojeg je elektroda selektivna. Mjerenje tenzidnom ionsko-selektivnom elektrodom se izvodi u elektrokemijskoj mjernoj ćeliji koja se sastoji od dva galvanska polučlanka: tenzidne ionsko-selektivne elektrode i referentne elektrode:
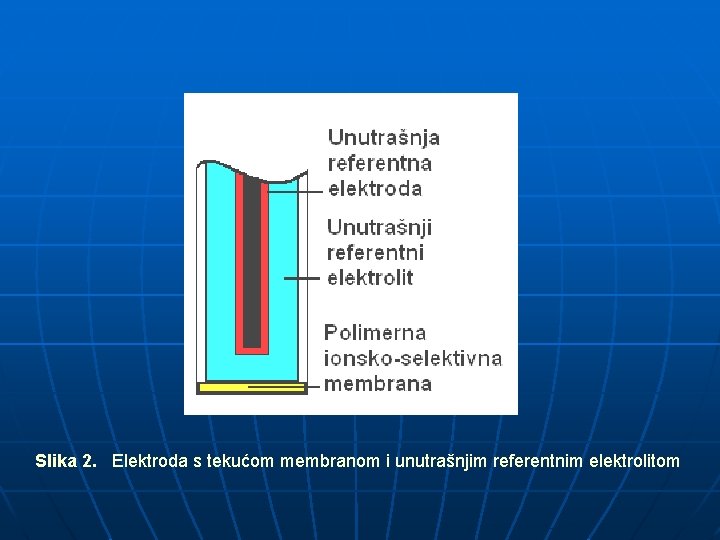
Slika 2. Elektroda s tekućom membranom i unutrašnjim referentnim elektrolitom
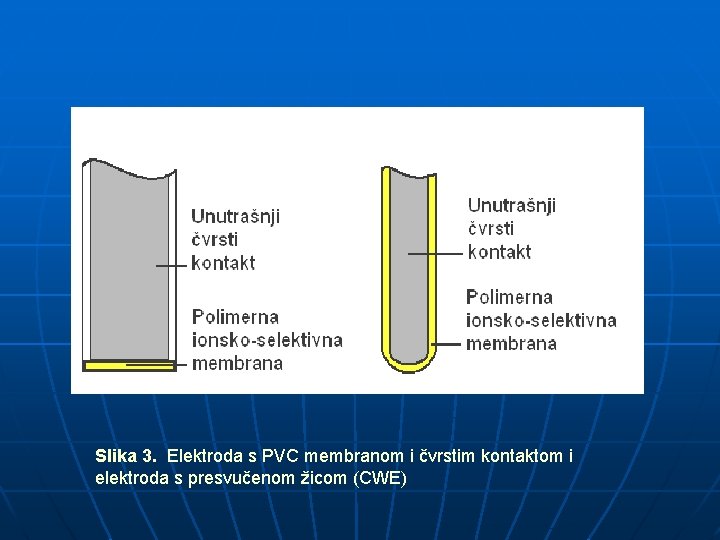
Slika 3. Elektroda s PVC membranom i čvrstim kontaktom i elektroda s presvučenom žicom (CWE)

Coated-wire electrode 1 – thin layer of surfactant-sensing material in PVC matrix, 2 – platinum wire, 3 – insulating layer.
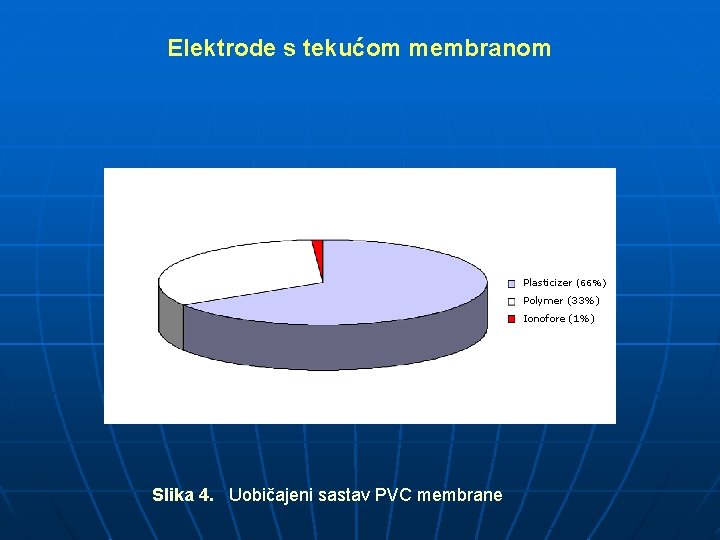
Elektrode s tekućom membranom Plasticizer (66%) Polymer (33%) Ionofore (1%) Slika 4. Uobičajeni sastav PVC membrane

Sensor design
PVC polymeric membrane electrode Membrane composition Plasticizer (66%) Polymer (33%) Ionofore (1%)

Membrane preparation

1. Ag/Ag. Cl reference electrode, 2. inner reference solution, 3. PVC tube, 4. polymeric membrane with incorporated surfactant sensing material.

Odziv tenzidnih senzora (elektroda) (surfactant sensor (electrode) response)

Ionski tenzidi (ionic surfactants) Tenzidni ioni stvaraju ionske asocijate (ionske parove, ion-pairs) s ionima suprotnog naboja: (1), gdje je Cat+ = veliki "onium" kationi (uključivši kvaterni amonijev, arsonijev, piridinijev, fosfonijev itd. ), bazne boje, veliki kompleksni kationi nastali iz metalnih iona i neutralnih liganada, veliki organski kationi, itd. (lipofilnog karaktera), An- = anioni anionskih tenzida, veliki organski i anorganski anioni, itd. (lipofilnog karaktera).

Elektromotorna sila koja se uspostavlja na membrani senzora uronjenog u otopinu anionskog tenzida (analita) definirana je Nernstovim izrazom: (2), gdje je Eo = konstanta, S = nagib senzora (elektrode), a(An-) = aktivitet tenzidnog aniona. Za ionski par Cat. An (jedn. 1) konstanta produkta topljivosti je (3) gdje su a(Cat+) i a(An ) aktiviteti odgovarajućih tenzidnih iona.

Iz jedn. (3) slijedi , te nakon uvrštenja u jedn. (2), dobiva se sljedeći izraz za odziv elektrode: (4) koji nakon preuređenja daje: (5), gdje je

Neionski tenzidi (nonionic surfactants) Etoksilirani neionski tenzidi (ethoxylated nonionic surfactants) Barijev ion tvori pseudokationske komplekse s etoksiliranim neionskim tenzidima (EONS) prema sljedećoj shemi: (6) Vrijednost “x” varira u ovisnosti o broju etoksi (EO) jedinica u molekuli tenzida. Radi jednostavnosti gornja se jednadžba može napisati kao: (7), gdje je L=EONS

Membrana senzora sadrži teško topljivi pseudokationski tetrafenilboratni ionsko-izmjenjivački kompleks kao senzorski materijal, koji se dobiva reakcijom tetrafenilboratnog iona (TPB) s pseudokationskim kompleksom: (8) Stehiometrija reakcija (6) - (8) ovisi o dužini lanca etoksiliranog (hidrofilnog) lanca ispitivanog neionskog tenzida kao i o prirodi ostatka molekule tenzida (hidrofobni dio). Senzor pokazuje odziv na TPB- i na Ba. Lx 2+ ione prema Nernstovoj jednadžbi: (9) i (10)

Karakterizacija tenzidnih senzora
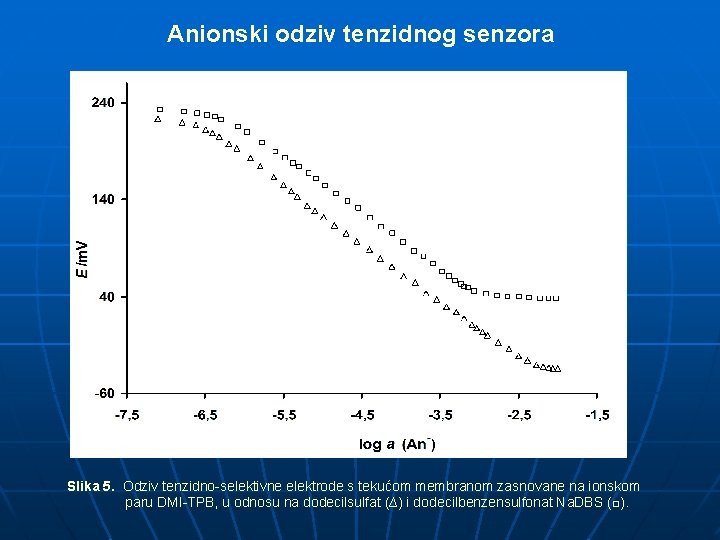
Anionski odziv tenzidnog senzora Slika 5. Odziv tenzidno-selektivne elektrode s tekućom membranom zasnovane na ionskom paru DMI-TPB, u odnosu na dodecilsulfat (∆) i dodecilbenzensulfonat Na. DBS (□).
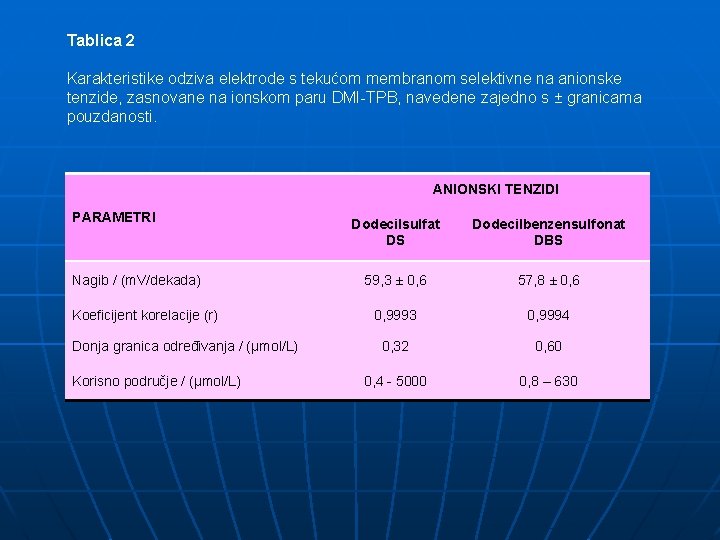
Tablica 2 Karakteristike odziva elektrode s tekućom membranom selektivne na anionske tenzide, zasnovane na ionskom paru DMI-TPB, navedene zajedno s ± granicama pouzdanosti. ANIONSKI TENZIDI PARAMETRI Nagib / (m. V/dekada) Koeficijent korelacije (r) Donja granica određivanja / (μmol/L) Korisno područje / (μmol/L) Dodecilsulfat DS Dodecilbenzensulfonat DBS 59, 3 ± 0, 6 57, 8 ± 0, 6 0, 9993 0, 9994 0, 32 0, 60 0, 4 - 5000 0, 8 – 630

Kationski odziv tenzidnog senzora Fig. 6. Response characteristics of DMI-TPB surfactant sensor toward Hyamine (■), CPC (□) and CTAB (▲).
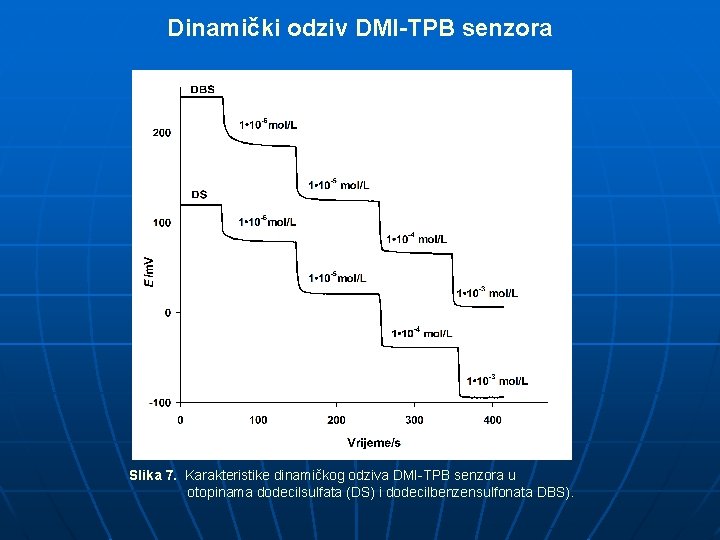
Dinamički odziv DMI-TPB senzora Slika 7. Karakteristike dinamičkog odziva DMI-TPB senzora u otopinama dodecilsulfata (DS) i dodecilbenzensulfonata DBS).

Primjena tenzidnih senzora

Detekcija završne točke pri potenciometrijskim titracijama

Potenciometrijske titracije ionskih tenzida Potenciometrijske titracije su titracijske metode u kojima se za određivanje završne točke koriste potenciometrijski senzori. Ispitivanjima mogućnosti primjene potenciometrijskih titracija za određivanje anionskih tenzida kao zamjene za vizualne titracije u velikoj mjeri su pridonijela opažanja interferencije anionskih tenzida u titracijama u kojima je kao senzor bila upotrijebljena kalcijeva ili nitratna ionsko-selektivna elektroda. Nakon toga su uslijedila istraživanja na razvoju tenzidnih ionskoselektivnih elektroda, potenciometrijskih senzora namijenjenih za primjenu u analitici tenzida. Najvažniji dio elektrode/senzora je membrana, koja se najčešće sastoji od ionskog asocijata, tzv. ionofora, te odgovarajućeg plastifikatora i PVC matrice. Ionofor je odgovoran za elektroaktivnost membrane.

Potenciometrijske titracije ionskih tenzida Primjena potenciometrijskih tenzidnih senzora je vezana za promjene potencijala u otopini analita (anionskog tenzida): a koje su posljedica kemijske reakcije titranta (kationskog tenzida) i analita (anionskog tenzida): U slučaju određivanja anionskih tenzida, veličina promjene potencijala ovisi o koncentraciji analita i produktu topljivosti soli koja je nastala u reakciji između anionskog tenzida (analita) i kationskog tenzida (titranta). Soli niskog produkta topljivosti daju stabilne ionske asocijate, zbog čega je promjena potencijala u točki ekvivalencije kod njih veća nego kod soli s višim produktom topljivosti.

Potenciometrijske titracije ionskih tenzida Budući da za veliku promjenu potencijala u području završne točke titracije ionski asocijat treba biti što je moguće manje disociran, dobar titrant je reagens s velikom afinitetom za analit. Istraživanja su pokazala da je 1, 3 -didecil-2 -metil-imidazolijev klorid (DMIC), koji je po svojoj prirodi također kationski tenzid, dobar izbor kationskog titranta za potenciometrijske titracije anionskih tenzida: Potenciometrijske titracije s tenzidnim ionsko-selektivnim elektrodama pogodne su za čiste otopine tenzida. U detergentima se primjenjuju manje ili više uspješno. U analizi detergenata, koji su po svojoj prirodi višekomponentni sustavi, potencijalni interferenti prisutni u titracijskoj otopini mogu nepovoljno utjecati na odziv elektrode i značajno narušiti preciznost određivanja.

Potenciometrijske titracije ionskih tenzida Tako npr. povećana koncentracija nekih soli može štetno utjecati na odziv elektrode što uzrokuje deformaciju titracijske krivulje, tj. njezino proširenje u području infleksije uzrokovano nastajanjem micela tenzida. Na neke interferencije moguće je utjecati ispravnim odabirom p. Hpodručja u kojem je utjecaj interferenta zanemarljiv. Primjenom potenciometrijskih senzora za određivanje završne točke u titracijama tenzida, određivanja je moguće automatizirati, čime se povećava brzina određivanja i izbjegavaju subjektivne pogreške analitičara. Sljedeći ne manje važan razlog razvoja potenciometrijskih titracija u analitici tenzida je upotreba kloroforma u titraciji u dvije faze, što predstavlja ozbiljan ekološki problem koji za sobom povlači troškove oko zbrinjavanja otpada. Primjena potenciometrijskih senzora u analitici tenzida, proizašla iz njihovog razvoja u posljednja četiri desetljeća, je danas sve značajnija.
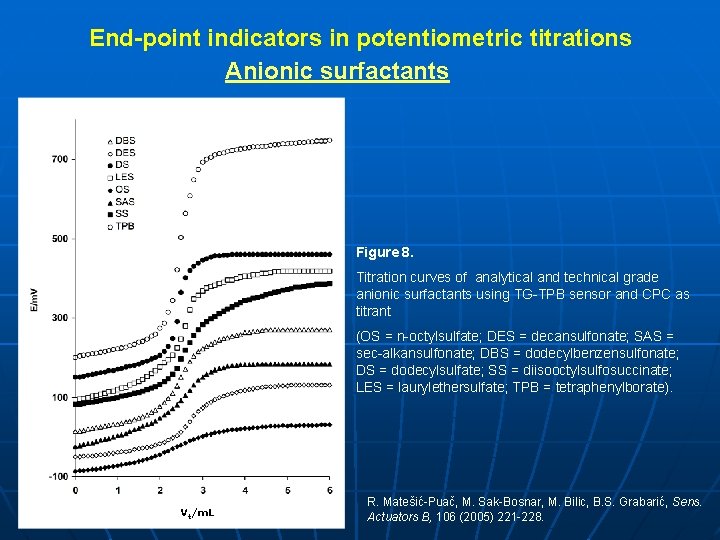
End-point indicators in potentiometric titrations Anionic surfactants Figure 8. Titration curves of analytical and technical grade anionic surfactants using TG-TPB sensor and CPC as titrant (OS = n-octylsulfate; DES = decansulfonate; SAS = sec-alkansulfonate; DBS = dodecylbenzensulfonate; DS = dodecylsulfate; SS = diisooctylsulfosuccinate; LES = laurylethersulfate; TPB = tetraphenylborate). Vt/m. L R. Matešić-Puač, M. Sak-Bosnar, M. Bilic, B. S. Grabarić, Sens. Actuators B, 106 (2005) 221 -228.
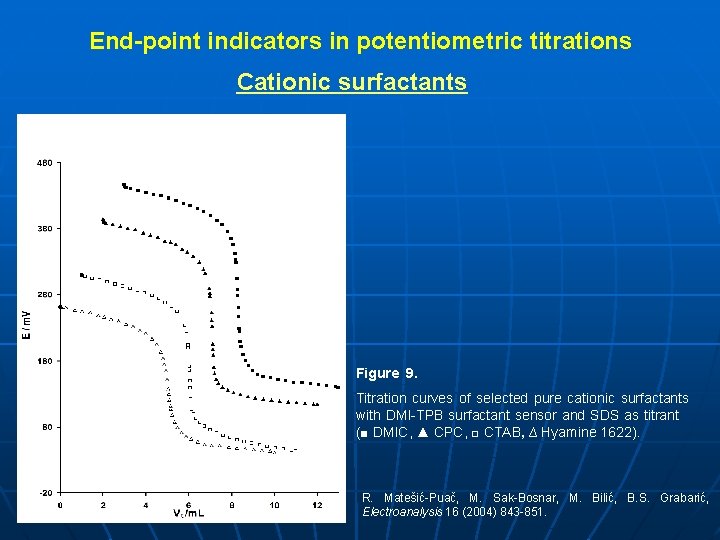
End-point indicators in potentiometric titrations Cationic surfactants Figure 9. Titration curves of selected pure cationic surfactants with DMI-TPB surfactant sensor and SDS as titrant (■ DMIC, ▲ CPC, □ CTAB, ∆ Hyamine 1622). R. Matešić-Puač, M. Sak-Bosnar, M. Bilić, B. S. Grabarić, Electroanalysis 16 (2004) 843 -851.
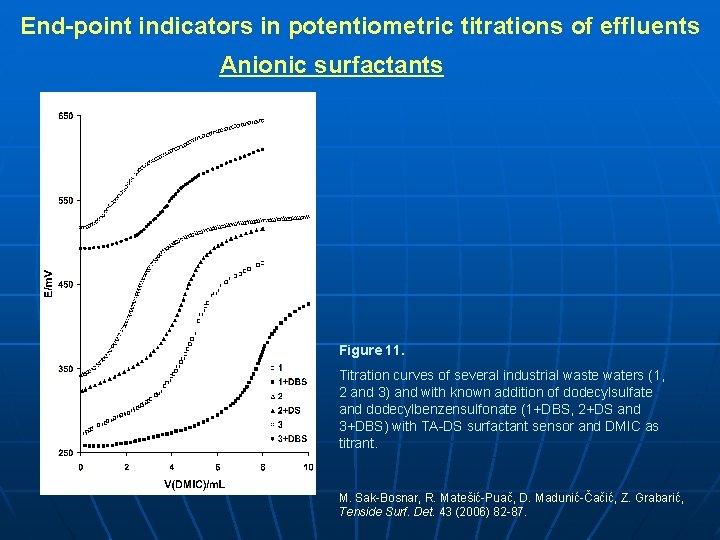
End-point indicators in potentiometric titrations of effluents Anionic surfactants Figure 11. Titration curves of several industrial waste waters (1, 2 and 3) and with known addition of dodecylsulfate and dodecylbenzensulfonate (1+DBS, 2+DS and 3+DBS) with TA-DS surfactant sensor and DMIC as titrant. M. Sak-Bosnar, R. Matešić-Puač, D. Madunić-Čačić, Z. Grabarić, Tenside Surf. Det. 43 (2006) 82 -87.

Potenciometrijske titracije etoksiliranih neionskih tenzida Potenciometrijske titracije se danas često primjenjuju kao alternativa ostalim metodama za određivanje neionskih tenzida. Zasnivaju se na sposobnosti polietera da stvaraju komplekse s velikim metalnim kationima, najčešće barijevim i olovnim, koji se zatim titriraju s natrijevim terafenilboratom. Za određivanje završne točke titracije koristi se tenzidno-selektivna elektoda za neionske tenzide. Osim za određivanje neionskih tenzida, primjena potenciometrijskih titracija je omogućila izučavanje mehanizama nastajanja kompleksa velikih metalnih kationa i etoksiliranih neionskih tenzida. Značajno područje primjene potenciometrijskih titracija u analizi neionskih tenzida predstavlja analiza otpadnih voda. Rezultati pokazuju zadovoljavajući nivo slaganja u odnosu na standardnu metodu (Bi. AS, Bismuth Active Substances). Prednosti potencimetrijskih titracija u odnosu na standardnu metodu su mnogobrojne. Određivanje je jednostavno za izvođenje, nije potrebna posebna priprema uzorka, a cijena je prihvatljiva.

Potenciometrijske titracije etoksiliranih neionskih tenzida Barijev ion tvori pseudokationske komplekse s etoksiliranim neionskim tenzidima (EONS) prema reakciji: (6) Vrijednost “x” varira u ovisnosti o broju etoksi (EO) jedinica u molekuli tenzida. Radi jednostavnosti gornja se jednadžba može napisati kao: (7), gdje je L=EONS

Potenciometrijske titracije etoksiliranih neionskih tenzida Nastali pseudokationski kompleks titrira se standardnom otopinom natrijevog tetrafenilborata (TPB): (8). Stehiometrija reakcija (6) - (8) ovisi o dužini lanca etoksiliranog (hidrofilnog) lanca ispitivanog neionskog tenzida kao i o prirodi ostatka molekule tenzida (hidrofobni dio). Senzor pokazuje odziv na TPB- prema Nernstovoj jednadžbi: (9) i koristi se za kontinuirano direktno praćenje aktiviteta TPB- tijekom titracije, a indirektno i koncentracije EONS.
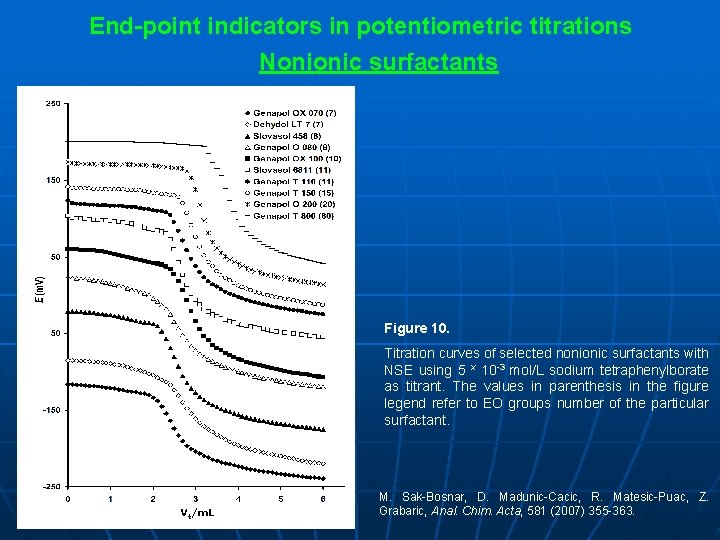
End-point indicators in potentiometric titrations Nonionic surfactants Figure 10. Titration curves of selected nonionic surfactants with NSE using 5 x 10 -3 mol/L sodium tetraphenylborate as titrant. The values in parenthesis in the figure legend refer to EO groups number of the particular surfactant. Vt/m. L M. Sak-Bosnar, D. Madunic-Cacic, R. Matesic-Puac, Z. Grabaric, Anal. Chim. Acta, 581 (2007) 355 -363.
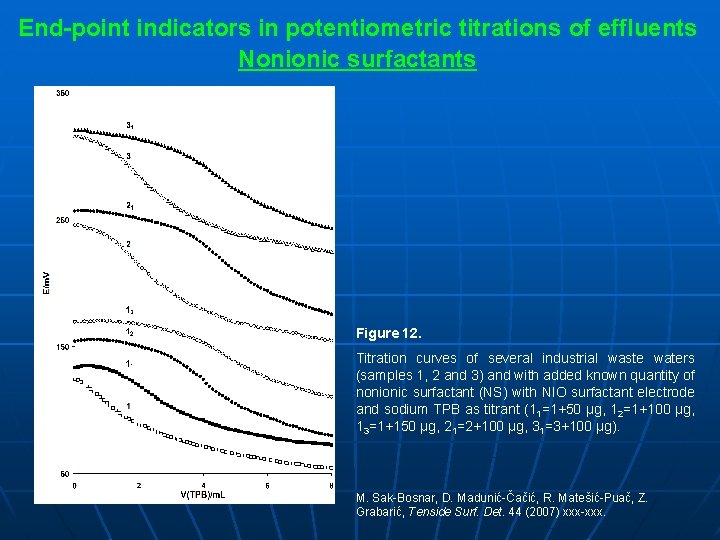
End-point indicators in potentiometric titrations of effluents Nonionic surfactants Figure 12. Titration curves of several industrial waste waters (samples 1, 2 and 3) and with added known quantity of nonionic surfactant (NS) with NIO surfactant electrode and sodium TPB as titrant (11=1+50 μg, 12=1+100 μg, 13=1+150 μg, 21=2+100 μg, 31=3+100 μg). M. Sak-Bosnar, D. Madunić-Čačić, R. Matešić-Puač, Z. Grabarić, Tenside Surf. Det. 44 (2007) xxx-xxx.

Prednosti i ograničenja upotrebe tenzidnoselektivnih elektroda u odnosu na klasične metode Primjena tenzidno-selektivnih elektroda pruža uvjete neophodne za rad u modernim visoko-automatiziranim laboratorijima. Prednosti upotrebe tenzidno-selektivnih elektroda su sljedeća: n n n n Rutinske analize mogu se automatizirati, čime se značajno skraćuje vrijeme analize. Analiza se može prilagoditi zahtjevima koji se mogu usuglasiti sa standardima dobre laboratorijske prakse (good laboratory praxis, GLP). Pri analizi se koriste manje količine reagenasa bez potrebe za primjenom toksičnih otapala. Određivanje završne točke titracije lišeno je subjektivnih procjena pa je time i znatno pouzdanije. Isključeni su problemi vezani za titraciju zamućenih ili obojenih uzoraka. Priprema uzorka obično je nepotrebna, osim ako je potrebno raditi s razrjeđenjima, kada je zbog slabijeg odziva elektrode potrebno stvoriti što bolje uvjete. Podešavanje p. H-vrijednosti otopine za titraciju obično je nepotrebno, osim u posebnim slučajevima.

Prednosti i ograničenja upotrebe tenzidnoselektivnih elektroda u odnosu na klasične metode Ograničenja upotrebe tenzidno-selektivnih elektroda su sljedeća: n n n ograničene mogućnosti primjene direktne potenciometrije, postepeni gubitak odzivnih karakteristika elektrode (skraćen vijek trajanja), ograničena selektivnost.

MOGUĆNOSTI RAZVOJA TENZIDNO-SELEKTIVNIH ELEKTRODA Nedostatci tenzidno-selektivnih elektroda su uglavnom vezani za: • svojstva tekućih membrana • izbor senzorskog materijala.

1. Sinteza novih tipova senzorskih materijala Dizajniranjem anionskog i/ili kationskog dijela ionskog para (geometrija molekule, veličina hidrofobnog dijela, polarnost itd. ) mogla bi se postići povećana selektivnost elektrode, čime bi se otvorila mogućnost diferencijalne titracije smjese tenzida. Također bi se na isti način mogla povećati osjetljivost elektrode, što bi proširilo područje linearnog odziva elektrode i snizila granica detekcije pri određivanju tenzida.

2. Uvođenje novih nosača senzora Uvođenjem novih nosača senzora, npr. sol-gel materijala mogli bi se izbjeći ili umanjiti nedostatci klasične polimerne matrice. Poboljšanja obuhvaćaju sljedeće osobine: • povećanje kemijske inertnosti • povećanje otpornosti prema bubrenju • obrada pri niskim temperaturama • prilagođena poroznost • kemijsko vezivanje elektroaktivnih mjesta na nosač senzora, čime bi se produljio vijek trajanja senzora, spriječilo ispiranje elektroaktivnih komponenata te smanjio drift signala. • Uvođenje električki-vodljivih polimera moglo bi se, pored poboljšanja gore spomenutih osobina, poboljšati i električne osobine senzora (smanjenje impedancije, šuma itd. ).
- Slides: 122