Obtencin de biomasa y exopolisacridos de Humphreya coffeata

Obtención de biomasa y exopolisacáridos de Humphreya coffeata en cultivo sumergido Investigan: Sara Gallego Giraldo Gisell García Giraldo Asesora: Luz Deisy Marín Palacio Grupo de Investigación en Procesos Ambientales y Biotecnológicos

Contenido 1. Introducción 1. 1. Antecedentes 2. Diseño Metodológico 3. Resultados y Discusiones 3. 1 Cinética de crecimiento celular 3. 2 Producción de exopolisacáridos (EPS) 3. 3 Escalamiento del proceso 4. Conclusiones 5. Recomendaciones 6. Bibliografía
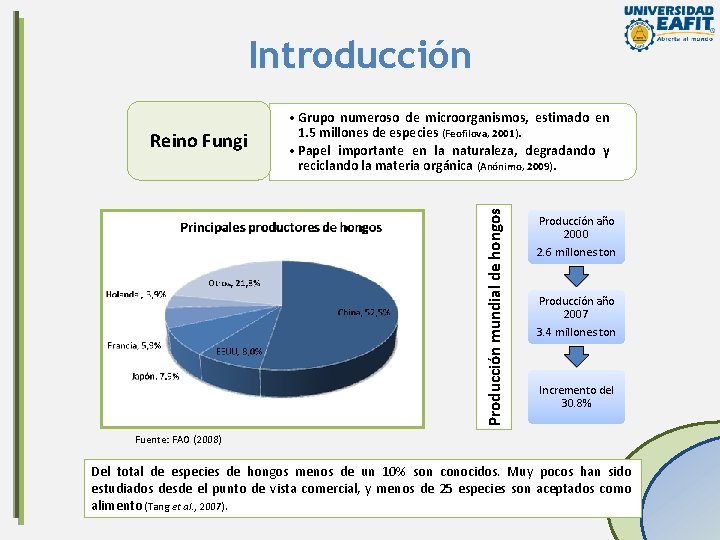
Introducción Producción mundial de hongos Reino Fungi • Grupo numeroso de microorganismos, estimado en 1. 5 millones de especies (Feofilova, 2001). • Papel importante en la naturaleza, degradando y reciclando la materia orgánica (Anónimo, 2009). Producción año 2000 2. 6 millones ton Producción año 2007 3. 4 millones ton Incremento del 30. 8% Fuente: FAO (2008) Del total de especies de hongos menos de un 10% son conocidos. Muy pocos han sido estudiados desde el punto de vista comercial, y menos de 25 especies son aceptados como alimento (Tang et al. , 2007).

Phylum Basidiomycota • Representado por más de 30. 000 especies. • Productores de una amplia gama de metabolitos biológicamente activos con actividad antitumoral e inmunológica, hasta agentes antimicrobianos, antifúngicos, antivirales, citostáticos, enzimas, reguladores de crecimiento y aromas (Brizuela et al. , 1998). Género Ganoderma • Usados en la medicina tradicional China (Zhong y Tang, 2004). • Los compuestos químicos con mayores propiedades bioactivas son los triterpenoides y polisacáridos (Berovič et al. , 2003). • Polisacáridos: pertenecen al grupo de los β-Glucanos, con enlaces β-(1, 3) en la cadena principal y puntos de ramificación β-(1, 6) (Tang et al. , 2007). Ganoderma lucidum • Crece en latitudes cálidas del planeta, más en los climas subtropicales que en los templados (Santafé y Zuluaga, 2007). • Cultivo en sustratos sólidos, medio líquido estacionario o cultivo sumergido. • Resultados promisorios para tratamiento del cáncer y otras enfermedades como hepatitis, bronquitis crónica e hipertensión (Xu et al. , 2008). www. google. com/imagenes
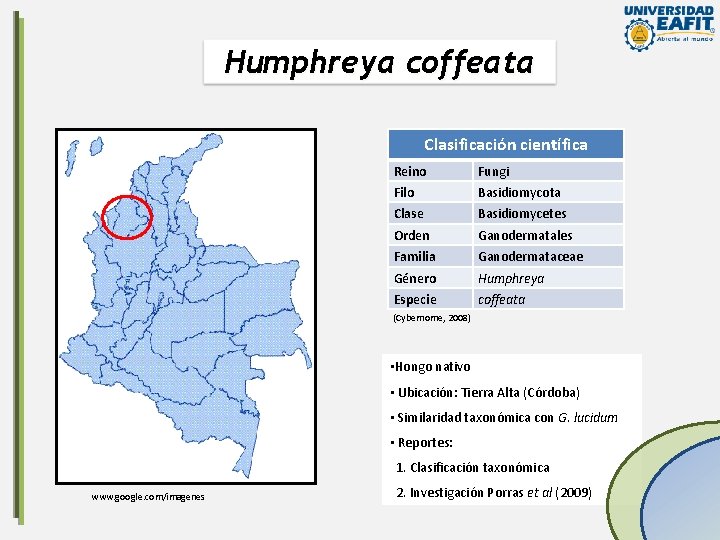
Humphreya coffeata Clasificación científica Reino Fungi Filo Basidiomycota Clase Basidiomycetes Orden Ganodermatales Familia Ganodermataceae Género Humphreya Especie coffeata (Cybernome, 2008) • Hongo nativo • Ubicación: Tierra Alta (Córdoba) • Similaridad taxonómica con G. lucidum • Reportes: 1. Clasificación taxonómica www. google. com/imagenes 2. Investigación Porras et al (2009)
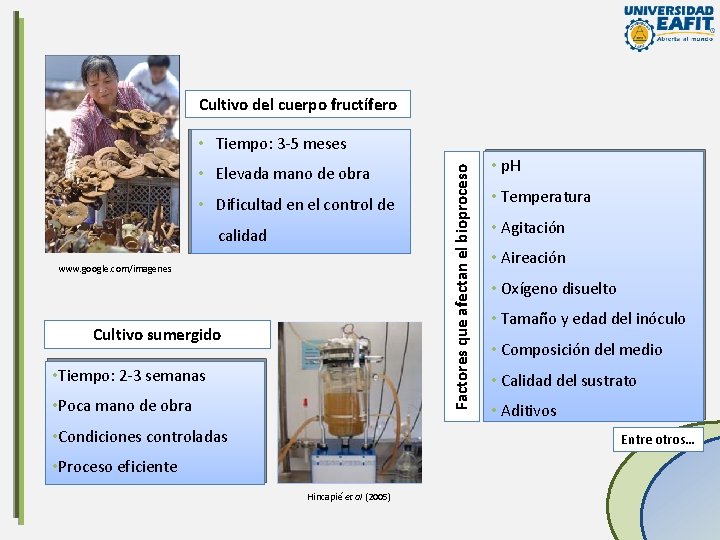
Cultivo del cuerpo fructífero • Elevada mano de obra • Dificultad en el control de calidad www. google. com/imagenes Cultivo sumergido • Tiempo: 2 -3 semanas • Poca mano de obra • Condiciones controladas Factores que afectan el bioproceso • Tiempo: 3 -5 meses • p. H • Temperatura • Agitación • Aireación • Oxígeno disuelto • Tamaño y edad del inóculo • Composición del medio • Calidad del sustrato • Aditivos Entre otros… • Proceso eficiente Hincapié et al (2005)
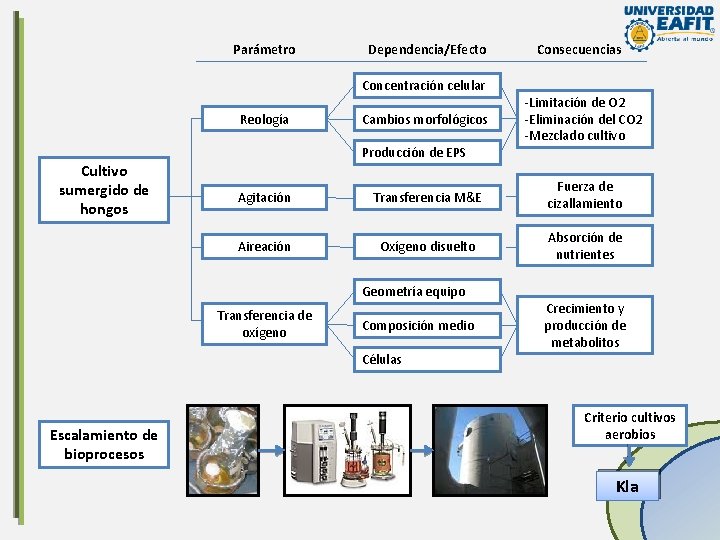
Parámetro Dependencia/Efecto Concentración celular Reología Cultivo sumergido de hongos Cambios morfológicos Producción de EPS Consecuencias -Limitación de O 2 -Eliminación del CO 2 -Mezclado cultivo Agitación Transferencia M&E Fuerza de cizallamiento Aireación Oxígeno disuelto Absorción de nutrientes Geometría equipo Transferencia de oxígeno Composición medio Crecimiento y producción de metabolitos Células Escalamiento de bioprocesos Criterio cultivos aerobios Kla
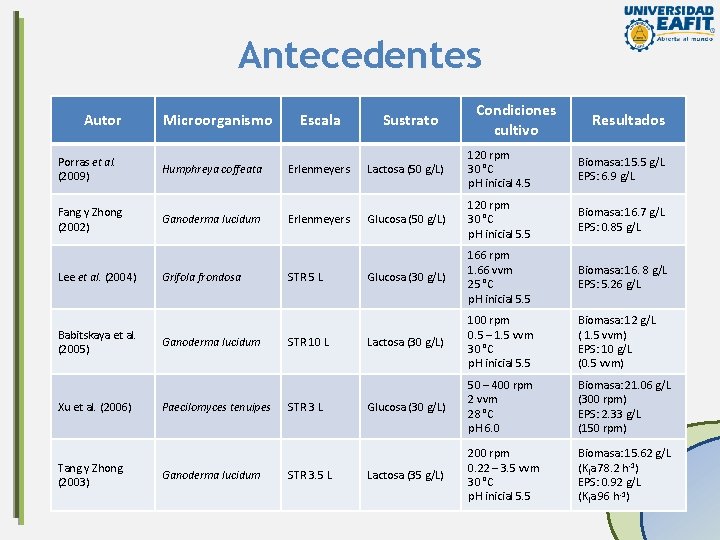
Antecedentes Autor Microorganismo Escala Porras et al. (2009) Humphreya coffeata Erlenmeyers Fang y Zhong (2002) Ganoderma lucidum Erlenmeyers Lee et al. (2004) Babitskaya et al. (2005) Xu et al. (2006) Tang y Zhong (2003) Grifola frondosa Ganoderma lucidum Paecilomyces tenuipes Ganoderma lucidum STR 5 L STR 10 L STR 3. 5 L Sustrato Condiciones cultivo Resultados Lactosa (50 g/L) 120 rpm 30 °C p. H inicial 4. 5 Biomasa: 15. 5 g/L EPS: 6. 9 g/L Glucosa (50 g/L) 120 rpm 30 °C p. H inicial 5. 5 Biomasa: 16. 7 g/L EPS: 0. 85 g/L Glucosa (30 g/L) 166 rpm 1. 66 vvm 25 °C p. H inicial 5. 5 Biomasa: 16. 8 g/L EPS: 5. 26 g/L Lactosa (30 g/L) 100 rpm 0. 5 – 1. 5 vvm 30 °C p. H inicial 5. 5 Biomasa: 12 g/L ( 1. 5 vvm) EPS: 10 g/L (0. 5 vvm) Glucosa (30 g/L) 50 – 400 rpm 2 vvm 28 °C p. H 6. 0 Biomasa: 21. 06 g/L (300 rpm) EPS: 2. 33 g/L (150 rpm) Lactosa (35 g/L) 200 rpm 0. 22 – 3. 5 vvm 30 °C p. H inicial 5. 5 Biomasa: 15. 62 g/L (Kla 78. 2 h-1) EPS: 0. 92 g/L (Kla 96 h-1)

Objetivos OBJETIVO GENERAL: Evaluar el efecto de la aireación y velocidad de agitación en Evaluar el efecto de la aireación y velocidad de agitación la producción de biomasa y exopolisacáridos de un cultivo de Humphreya coffeata en un biorreactor de 2 L, con el fin en la producción biomasa y exopolisacáridos de un de realizar de el escalamiento del bioproceso desde el nivel de laboratorio a escala piloto. cultivo de Humphreya coffeata en un biorreactor de 2 L, con el fin el de crecimiento realizar el escalamiento del coffeata bioproceso 1. de Humphreya con 1. Evaluar el crecimiento de Humphreya coffeata con variación en el flujo de aire y velocidad de agitación desde el nivel de laboratorio a escala piloto. variación en deel biomasa flujo de seco aire y velocidad de agitación mediante la medición por peso mediante la medición de biomasa por peso seco. Evaluar el efecto de la aireación y velocidad de 2. Evaluar el efecto 2. agitación de la enaireación y velocidad de la producción de exopolisacáridos determinando la concentración de carbohidratos totales. agitación en la producción de exopolisacáridos 3. Escalar el bioproceso a planta de piloto, teniendo determinando la concentración carbohidratos 3. Escalar el bioproceso a planta piloto, teniendo como criterio el coeficiente volumétrico decoeficiente transferencia de como criterio el volumétrico de totales. masa K a. transferencia de masa KLa. L
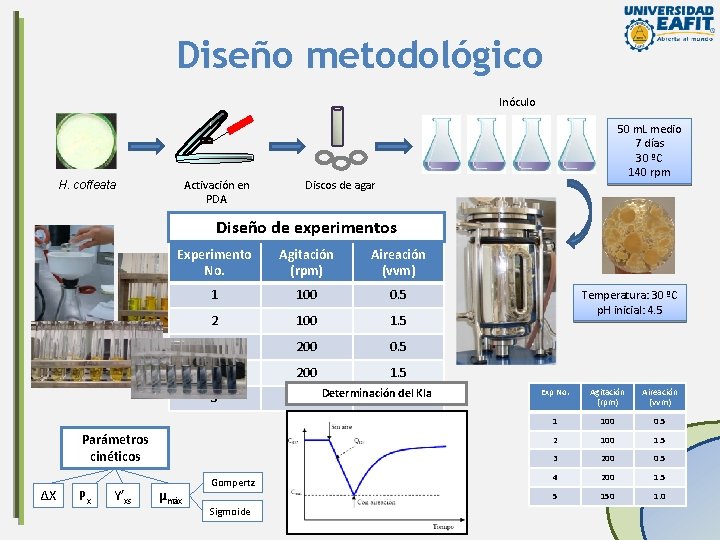
Diseño metodológico Inóculo Activación en PDA H. coffeata Discos de agar 7 días, 30 ºC Diseño Experimento No. 1 2 3 Px Y’xs µmáx de experimentos Agitación (rpm) 1. 8 L Medio Aireación (vvm) Biomasa: Peso seco 100 0. 5 100 1. 5 Azúcares reductores: DNS EPS: Fenol-ácido sulfúrico 200 Proteína total: Lowry 200 5 del Kla 150 Determinación 1. 0 Gompertz Sigmoide Temperatura: 30 ºC p. H inicial: 4. 5 0. 5 4 Parámetros cinéticos ΔX 50 m. L medio 7 días 30 ºC 140 rpm 1. 5 Exp No. Agitación (rpm) Aireación (vvm) 1 100 0. 5 2 100 1. 5 3 200 0. 5 4 200 1. 5 5 150 1. 0
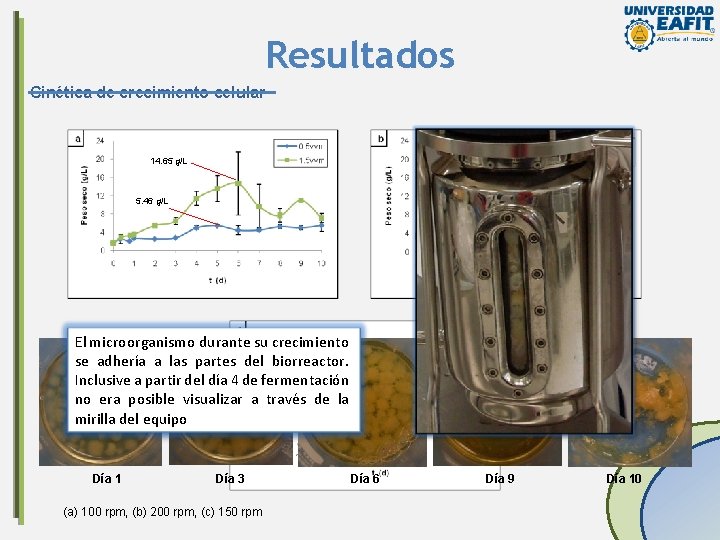
Resultados Cinética de crecimiento celular 14. 71 g/L 14. 65 g/L 7. 23 g/L 5. 46 g/L El microorganismo durante su crecimiento se adhería a las partes del biorreactor. 7. 69 g/L Inclusive a partir del día 4 de fermentación no era posible visualizar a través de la mirilla del equipo Día 1 Día 3 (a) 100 rpm, (b) 200 rpm, (c) 150 rpm Día 6 Día 9 Día 10
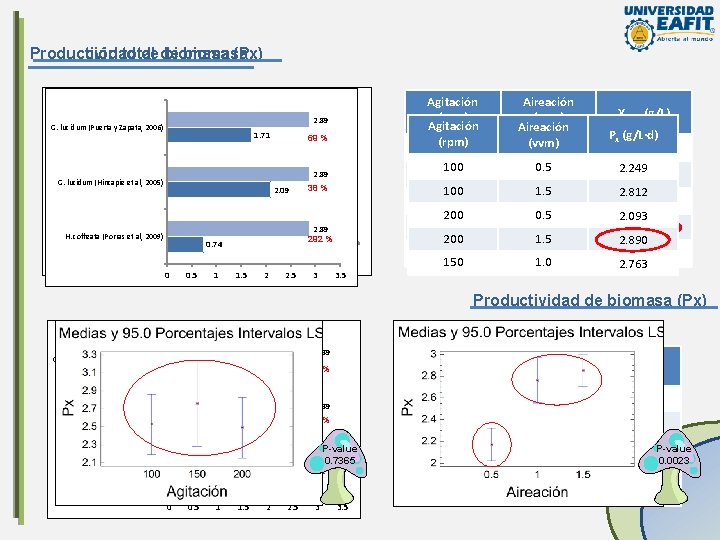
Producción total Productividad de de biomasa (Px) 30 28. 9 30 Peso seco (g/L) 15 15 28. 9 b G. lucidum (Puerta y Zapata, 2006) 25 25 20 20 28. 9 X final Xmáx cinética 86%a 1. 71 245% a 5 a 112%69 % b b 15. 5 13. 65 2. 89 G. lucidum (Hincapie et al, 2005) 10 10 2. 89 b b 2. 09 8. 37 a ab 5 2. 89 292 % H. coffeata (Porras et al, 2009) 0 38 % 0 0. 74 100 rpm 200 rpm 150 rpm- 100 rpm 200 rpm. H. coffeata (Porras et al, G. lucidum (Hincapie et G. lucidum (Puerta y 0. 5 vvm 1 vvm 1. 5 vvm Zapata, 2006) 1. 5 vv 2009) al, 2005) 0 0. 5 1 1. 5 2 2. 5 3 3. 5 Agitación (rpm) 100 Aireación (vvm) 0. 5 100 100 200 200 150 0. 5 1. 0 Xfinal (g/L) Px (g/L·d) 22. 49 ± 1. 25 2. 249 28. 12 ± 0. 45 2. 812 20. 93 ± 2. 12 2. 093 28. 90 ± 0. 42 2. 890 27. 63 ± 0. 75 2. 763 Productividad de biomasa (Px) 2. 89 G. lucidum (Puerta y Zapata, 2006) 1. 71 Agitación (rpm) Aireación (vvm) Px (g/L·d) 100 0. 5 2. 249 100 1. 5 2. 812 P-value 200 0. 5 2. 89 0. 7365 292 % 2. 093 200 1. 5 2. 890 150 1. 0 2. 763 69 % 2. 89 G. lucidum (Hincapie et al, 2005) 2. 09 H. coffeata (Porras et al, 2009) 0. 74 0 0. 5 1 1. 5 2 2. 5 38 % 3 3. 5 P-value 0. 0023
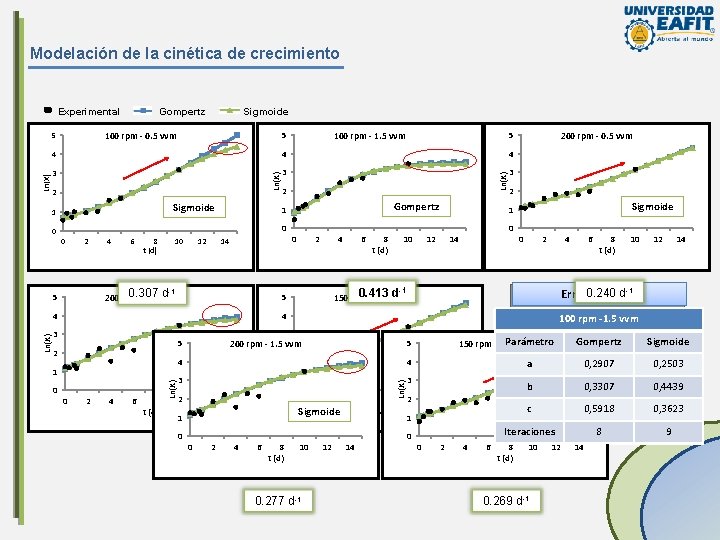
Modelación de la cinética de crecimiento Experimental Sigmoide 5 100 rpm - 0. 5 vvm 5 100 rpm - 1. 5 vvm 4 4 3 3 3 2 Sigmoide 1 0 2 4 6 8 t (d) 10 12 14 0. 307 d 200 rpm - 1. 5 vvm -1 5 0 2 4 6 8 t (d) 10 200 rpm - 0. 5 vvm 2 Sigmoide 1 12 0 14 0 2 4 Ln(X) -1 5 2 0 2 4 6 8 t (d) 3 2 10 12 2 0 14 1 0 0 2 4 Sigmoide 1 3 4 6 8 t (d) Parámetro 150 rpm - 1. 0 vvm 5 200 rpm - 1. 5 vvm 4 Sigmoide 1 8 t (d) 10 12 14 -1. 5 100 150 rpm -0. 5 200 -1. 0 vvm 0 2 4 6 Sigmoide 10 0. 277 d-1 12 14 8 t (d) Ln(X) 3 6 d-1 Error 0. 240 estándar 0. 413 d 150 rpm - 1. 0 vvm 4 Ln(X) Gompertz 5 4 0 2 1 0 0 Ln(X) 4 Ln(X) 5 Gompertz 3 2 10 12 14 1 0 Gompertz Sigmoide a 0, 2907 20, 56 21, 27 14, 73 1, 032 0, 2503 0, 6052 2, 228 5, 537 4, 623 b 0, 3307 17, 82 28, 46 19, 27 1, 481 0, 4439 11, 08 8, 648 1, 377 3, 88 c. Sigmoide 0, 5918 10, 34 18, 11 13, 26 2, 477 0, 3623 1, 182 2, 934 2, 582 1, 08 13 12 8 69 8 Iteraciones 0 2 4 6 8 t (d) 10 0. 269 d-1 12 14
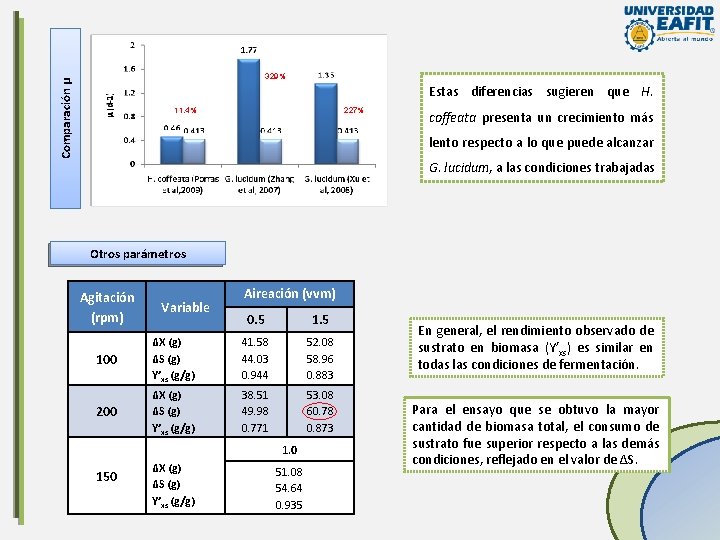
Comparación µ 329% Estas diferencias sugieren que H. 11. 4% 227% coffeata presenta un crecimiento más lento respecto a lo que puede alcanzar G. lucidum, a las condiciones trabajadas Otros parámetros Agitación (rpm) Variable Aireación (vvm) 0. 5 100 ΔX (g) ΔS (g) Y’xs (g/g) 41. 58 44. 03 0. 944 52. 08 58. 96 0. 883 200 ΔX (g) ΔS (g) Y’xs (g/g) 38. 51 49. 98 0. 771 53. 08 60. 78 0. 873 1. 0 150 ΔX (g) ΔS (g) Y’xs (g/g) 51. 08 54. 64 0. 935 En general, el rendimiento observado de sustrato en biomasa (Y’xs) es similar en todas las condiciones de fermentación. Para el ensayo que se obtuvo la mayor cantidad de biomasa total, el consumo de sustrato fue superior respecto a las demás condiciones, reflejado en el valor de ΔS.
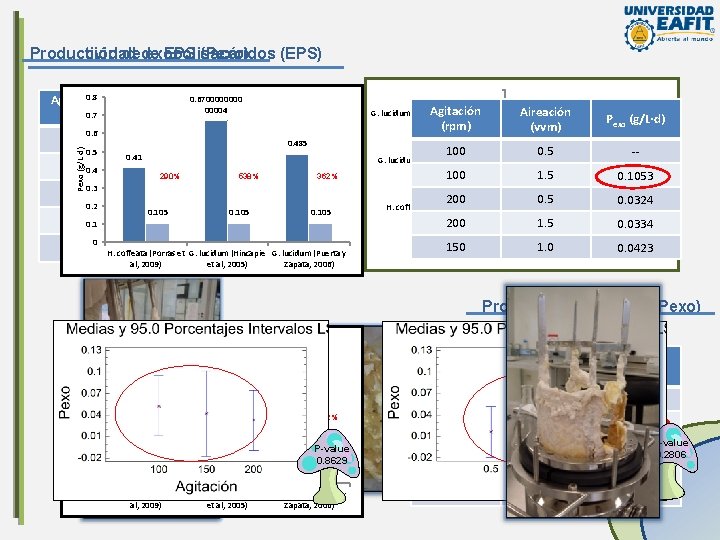
Producción dede Productividad exopolisacáridos EPS (Pexo) (EPS) 0. 8 Agitación (rpm)0. 7 Pexo (g/L d) 100 0. 6 0. 5 100 0. 4 200 0. 3 0. 2 200 0. 1 150 0 Aireación (vvm) 0. 5 (g/L) -- 0. 41 1. 5 0. 670000 EPSmáx 00004 290% 0. 5 -0. 485 1. 053 ± 0. 151 538% 0. 292 ± 0. 292 0. 105 1. 5 Tiempo (d) 0. 105 0. 234 ± 0. 192 9999 Aireación (vvm) (rpm) G. lucidum (Hincapie et al, 2005) 362% 9 100 1. 0 0. 338 ± 0. 288 G. lucidum (Puerta y 8 H. coffeata (Porras et G. lucidum (Hincapie al, 2009) et al, 2005) Zapata, 2006) Pexo (g/L·d) 407% -- 5. 34 0. 1053 555% 1. 0529999999 0. 5 9999 H. coffeata (Porras et al, 2009) 200 150 3. 88 1. 5 200 0. 105 268% 1. 0529999999 0. 5 9999 100 10 7 1. 0529999999 Agitación G. lucidum (Puerta y Zapata, 2006) 0. 0324 6. 9 1. 5 0 1 2 1. 0 0. 0334 3 4 EPS (g/L) 5 6 7 0. 0423 8 Productividad de EPS (Pexo) 0. 8 0. 6700004 0. 7 Pexo (g/L d) 0. 6 0. 5 0. 485 0. 41 290% 538% 362% 0. 3 0. 2 0. 1 0 0. 105 P-value 0. 105 0. 8629 H. coffeata (Porras et G. lucidum (Hincapie G. lucidum (Puerta y al, 2009) et al, 2005) Zapata, 2006) Agitación (rpm) Aireación (vvm) Pexo (g/L·d) 100 0. 5 -- 100 1. 5 0. 1053 200 0. 5 0. 0324 P-value 200 1. 5 0. 0334 150 1. 0 0. 0423 0. 2806
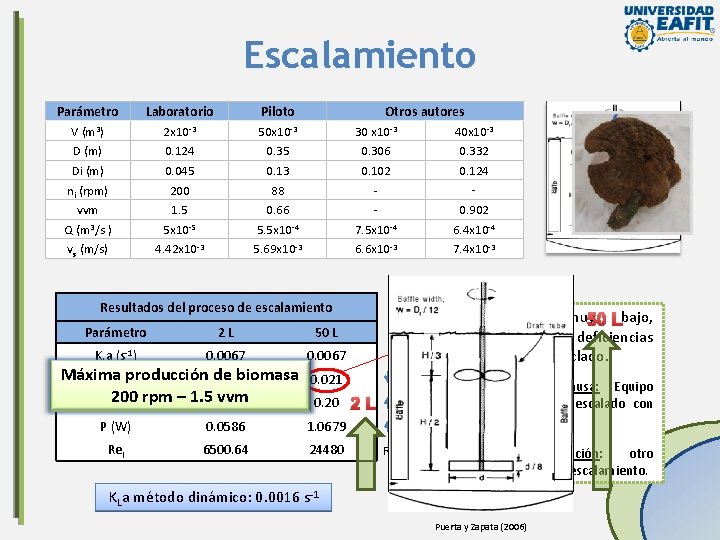
Escalamiento Parámetro Laboratorio Piloto V (m 3) 2 x 10 -3 50 x 10 -3 Otros autores 30 x 10 -3 40 x 10 -3 D (m) 0. 124 0. 35 0. 306 0. 332 Di (m) 0. 045 0. 13 0. 102 ni (rpm) 200 88 vvm 1. 5 0. 66 - 0. 124 - Q (m 3/s ) 5 x 10 -5 5. 5 x 10 -4 7. 5 x 10 -4 6. 4 x 10 -4 vs (m/s) 4. 42 x 10 -3 5. 69 x 10 -3 6. 6 x 10 -3 7. 4 x 10 -3 0. 902 Resultados del proceso de escalamiento Parámetro 2 L 50 L KLa (s-1) 0. 0067 3) Máxima producción de biomasa P/V (k. W/m 0. 029 200 rpm – 1. 50. 15 vvm Ni. Di (rpm*s) Valor muy 50 Lbajo, posibles deficiencias en el mezclado. 1. 37 veces 0. 021 0. 20 P (W) 0. 0586 1. 0679 Rei 6500. 64 24480 2 L 1. 3 veces 18 veces Régimen turbulento Posible causa: Equipo base para escalado con bajo Kla. Recomendación: otro criterio de escalamiento. KLa método dinámico: 0. 0016 s-1 Puerta y Zapata (2006)

Conclusiones La producción de biomasa a partir de una cepa de H. coffeata se favoreció por el incremento de la aireación, presentándose diferencias significativas entre los niveles trabajados. La combinación de aireación y agitación que arrojó el máximo valor de biomasa celular fue 1. 5 vvm y 200 rpm; con una producción total de 28. 90 ± 0. 42 g/L. Así mismo, la máxima productividad de biomasa se obtuvo bajo estas condiciones con un valor de 2. 89 ± 0. 042 g/L·d. La cinética de crecimiento fue ajustada satisfactoriamente al modelo cinético Sigmoide para todos los ensayos, excepto para la fermentación a 1. 5 vvm y 100 rpm, para la cual la ecuación de Gompertz obtuvo un mejor ajuste. Bajo dichas condiciones se obtuvo la máxima velocidad de crecimiento con un valor de 0. 413 d-1. La variación de la velocidad de agitación y tasa de aireación no presentó diferencias significativas para la obtención de exopolisacáridos (EPS). La producción máxima fue de 1. 053 ± 0. 151 g/L, a una velocidad de 100 rpm y aireación de 1. 5 vvm. Igualmente bajo estas condiciones se obtuvo la máxima productividad con un valor de 0. 105 g/L·d. El escalado de un volumen de 2 L a 50 L a partir de condiciones predeterminadas que favorecieron la producción de biomasa (200 rpm – 1. 5 vvm) y utilizando como criterio el KLa, arrojó que la P/V disminuiría 1. 37 veces, la P aumentaría 18 veces y la ni disminuiría 2. 3 veces. Además, por el valor arrojado para el número de Reynolds se pudo determinar que el sistema se encontraría en régimen turbulento.

Recomendaciones q Evaluar la producción de biomasa y EPS a partir de H. coffeata en un biorreactor de diferente configuración ya sea con cambios en la ubicación y forma de los bafles o combinación de impulsores para la agitación. Esto con el fin de evitar o disminuir la adhesión del microorganismo a las partes del equipo lo que dificulta la cuantificación del producto de interés. q Evaluar el efecto de la presencia de impulsores que desarrollan un flujo axial en un cultivo de H. coffeata, como es el caso de la turbina de paletas con un ángulo de 45° recomendada por diversos autores para mejorar la transferencia de oxígeno en fermentaciones miceliales viscosas. q Evaluar la producción de EPS en diferentes clases de biorreactores como son el Airlift y las columnas de burbujeo que carecen de partes mecánicas para la agitación, lo que puede evitar la adhesión del microorganismo al mismo y mejorar la expresión de los metabolitos en el medio de cultivo. q Determinar el consumo de oxígeno de H. coffeata en el biorreactor bajo las condiciones trabajadas.

Recomendaciones q Realizar controles de otras variables en el cultivo de H. coffeata tales como p. H, que influyen en la producción de los metabolitos de interés. q Diseñar un sistema para la toma de muestra que permita obtener datos representativos en la cuantificación de biomasa. q Evaluar la producción de otros metabolitos de interés tales como ácidos ganodericos (GA) e intrapolisacáridos (IPS).

Bibliografía BABITSKAYA, V. G. ; SHCHERBA, V. V. ; PUCHKOVA, T. A. ; SMIRNOV, D. A. Polysaccharides of Ganoderma lucidum: Factors Affecting Their Production. En: Applied Biochemistry and Microbiology, Vol. 41, No. 2 (2005). pp. 169– 173. BEROVIČ, M. ; HABIJANIČ, J. ; ZORE, I. ; WRABER, B. ; HODZAR, D. ; BOH, B. ; POHLEVEN, F. Submerged cultivation of Ganoderma lucidum biomass and immunostimulatory effects of fungal polysaccharides. En: Journal of Biotechnology No. 103 (2003). pp. 77– 86. BRIZUELA, M. A. ; GARCÍA, L. ; PÉREZ, L. ; MANSUR, M. Basidiomicetos: nueva fuente de metabolitos secundarios. En: Rev Iberoam Micol, No. 15 (1998). pp. 69 -74. DORAN, P. Mass Transfer. En: Bioprocess Engineering Principles. London: Academic Press Limited. 1999. pp. 202 – 205. DUBOIS, M. ; GILLES, K. ; HAMILTON, J. ; REBERS, P. ; SMITH, F. Colorimetric Method for determination of sugars and related substances. En: Division of Biochemistry, Vol. 28, No. 3 (1956). pp. 350 -356. FANG, Q. H. ; ZHONG, J. J. Submerged fermentation of higher fungus Ganoderma lucidum for production of valuable bioactive metabolites – ganoderic acid and polysaccharide. En: Biochemical Engineering Journal, No. 10 (2002 a). pp. 61– 65. FEOFILOVA, E. P. The Kingdom Fungi: Heterogeneity of Physiological and Biochemical Properties and Relationships with Plants, Animals, and Prokaryotes (Review). En: Applied Biochemistry and Microbiology, Vol. 37, No. 2 (2001). pp. 124– 137. HINCAPIÉ, A. S. ; MARTÍNEZ, L. ; TOBÓN, Y. V. Medellín, 2005. Diseño para la obtención de micelio y metabolitos de Ganoderma lucidum en un sistema de fermentación discontinuo. Trabajo de grado. Universidad EAFIT, Departamento de Ingeniería de Procesos. Área de Biotecnología. LEE, B. ; BAE, J. ; PYO, H. ; CHOE, T. ; KIM, S. ; HWANG, H. ; YUN, J. Submerged culture conditions for the production of mycelia biomass and exopolysaccharides by the edible Basidiomycete Grifola frondosa. En: Enzyme and Microbial Technology, No. 35 (2004). pp. 369– 376. LOWRY, O. H. , Protein measurement with the folin phenol reagent. En: J. Biol. Chem. No. 193 (1951). pp. 265 -275. MILLER, G. L. Use of dinitrosalicilic acid reagent for determination of reducing sugar. En: Analytical Chemistry, Vol. 31, No. 3 (1959). pp. 426 -428. PORRAS, S. M. ; VALDEZ-CRUZ, N. A. ; ROJANO, B. ; AGUILAR, C. ; ROCHA-ZAVALETA, L. ; TRUJILLO-ROLDÁN, M. Mycelial submerged culture of Humphreya coffeata for the production of valuable bioactive metabolites, cytotoxicity, genotoxicity and antioxidant activity. En: Int. J. Med. Mushrooms (2009) (In press).

Bibliografía PUERTA, J. ; ZAPATA, P. 2006. Diseño conceptual de un proceso para la elaboración de un producto funcional a partir de Ganoderma lucidum. Trabajo de grado. Universidad EAFIT, Departamento de Ingeniería de Procesos. Área de Biotecnología. SANTAFÉ, G. ; ZULUAGA, J. Búsqueda de compuestos bioactivos en hongos de la familia Ganodermataceae del departamento de Córdoba. Montería, 2007. Proyecto de investigación. Universidad de Córdoba. Departamento de química. TANG, Y. J. ; ZHONG, J. J. Role of oxygen supply in submerged fermentation of Ganoderma lucidum for production of Ganoderma polysaccharide and ganoderic acid. En: Enzyme and Microbial Technology, No. 32 (2003). pp. 478– 484. TANG, Y. J. ; ZHU, L. W. ; LI, H. M. ; LI, D. S. Submerged Culture of Mushrooms in Bioreactors – Challenges, Current State-of-the-Art, and Future Prospects. En: Food Technol. Biotechnol, No. 45 (2007). pp. 221– 229. WAGNER, R. ; MITCHELL, D. A. ; LANZI, G. ; LOPES DE ALMEIDA, A. Links between morphology and physiology of Ganoderma lucidum in submerged culture for the production of exopolysaccharide. En: Journal of Biotechnology, Vol. 114 (2004). pp. 153– 164. XU, C. ; KIM, S. ; HWANG, H. ; YUN, J. Production of exopolysaccharides by submerged culture of an enthomopathogenic fungus, Paecilomyces tenuipes C 240 in stirred-tank and airlift reactors. En: Bioresource Technology, No. 97 (2006). pp. 770– 777. XU, P. ; DING, Z. Y. ; QIAN, Z. ; ZHAO, C. X. ; ZHANG, K. C. Improved production of mycelial biomass and ganoderic acid by submerged culture of Ganoderma lucidum SB 97 using complex media. En: Enzyme and Microbial Technology, No. 42 (2008). pp. 325– 331. ZHONG, J. J. ; TANG, Y. J. Submerged Cultivation of Medicinal Mushrooms for Production of Valuable Bioactive Metabolites. En: Adv Biochem Engin/Biotechnol, No. 87 (2004). pp. 25– 59. ZWIETERING, M. H. ; JONGENBURGER, I. ; ROMBOUTS, F. M. ; VAN'T RIET, K. Modeling of the Bacterial Growth Curve. En: Applied and Environmental Microbiology, Vol. 56, No. 6 (1990). pp. 1875 -1881.

- Slides: 22