Obsazovn orbital CH1 Obecn chemie DUM 8 1


Obsazování orbitalů CH-1 Obecná chemie, DUM č. 8 1. ročník čtyřletého studia Mgr. Radovan Sloup Gymnázium Sušice Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II

Obsazování orbitalů Pravidla pro obsazování orbitalů: Platí pro atomy v zákl. stavu, kdy mají nejnižší možnou enegii! 1. Pauliho princip výlučnosti: V jednom orbitalu mohou být maximálně dva elektrony, lišící se hodnotou magnetického spinového kvantového čísla. V žádném atomu tedy není dvojice elektronů, která by měla všechna čtyři kvantová čísla stejná.

Obsazování orbitalů Pravidla pro obsazování orbitalů: Platí pro atomy v zákl. stavu, kdy mají nejnižší možnou enegii! 2. Hundovo pravidlo: V degenerovaných orbitalech vznikají elektronové páry teprve po zaplnění každého orbitalu jedním elektronem. Všechny nespárované elektrony mají stejný spin. V takovém případě má systém nejnižší energii a je proto nejstabilnější.

Obsazování orbitalů Pravidla pro obsazování orbitalů: Platí pro atomy v zákl. stavu, kdy mají nejnižší možnou enegii! 3. Pravidlo n + l: Orbitaly s energií nižší se zaplňují elektrony dříve než orbitaly s energií vyšší. Energie orbitalů se zvyšuje s rostoucí hodnotou součtu hlavního (n) a vedlejšího kvantového čísla (l). Jestliže mají dva různé orbitaly stejný součet n + l (například pro orbital 3 s a 2 p je součet n + l roven 3), potom je rozhodující hodnota hlavního kvantového čísla. Orbital, jehož hodnota n je menší, má také nižší energii a proto se dříve zaplní elektrony. Z toho vyplývá tzv. výstavbový princip: 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s 4 f 5 d 6 p. . .
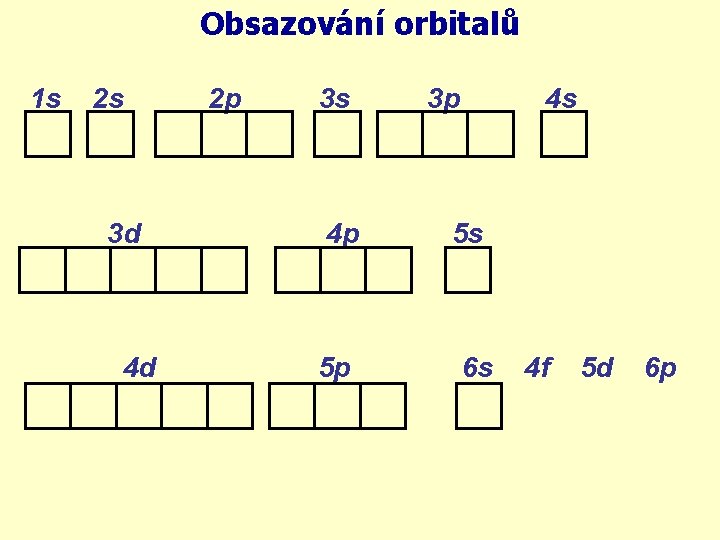
Obsazování orbitalů 1 s 2 s 3 d 4 d 2 p 3 s 4 p 5 p 3 p 4 s 5 s 6 s 4 f 5 d 6 p
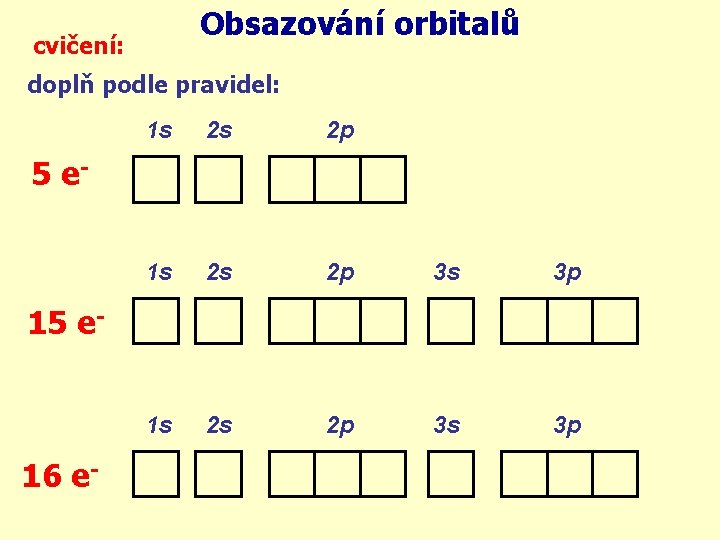
Obsazování orbitalů cvičení: doplň podle pravidel: 1 s 2 s 2 p 3 s 3 p 5 e- 16 e-
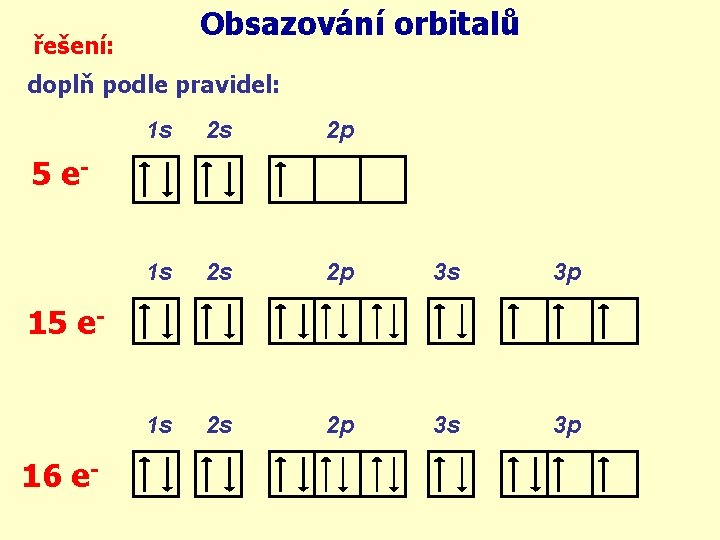
Obsazování orbitalů řešení: doplň podle pravidel: 1 s 2 s 2 p 3 s 3 p 5 e- 16 e-
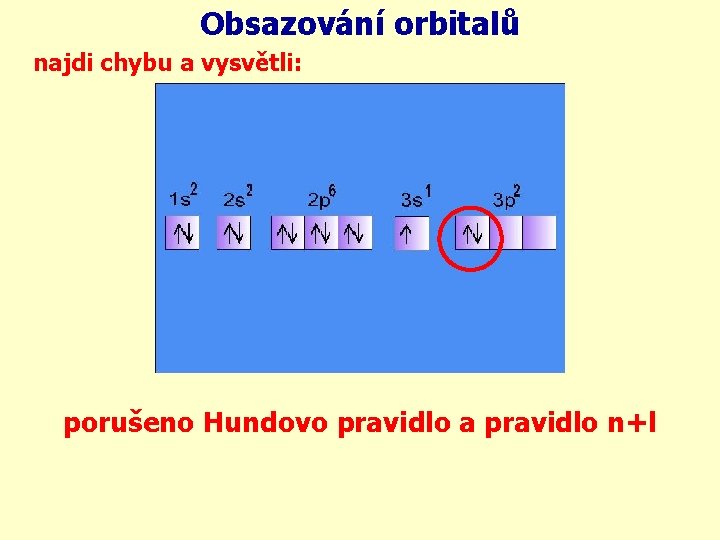
Obsazování orbitalů najdi chybu a vysvětli: porušeno Hundovo pravidlo a pravidlo n+l
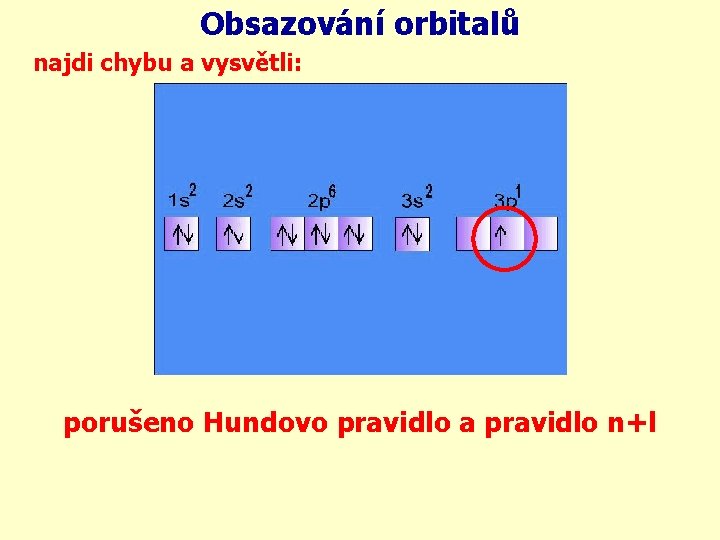
Obsazování orbitalů najdi chybu a vysvětli: porušeno Hundovo pravidlo a pravidlo n+l
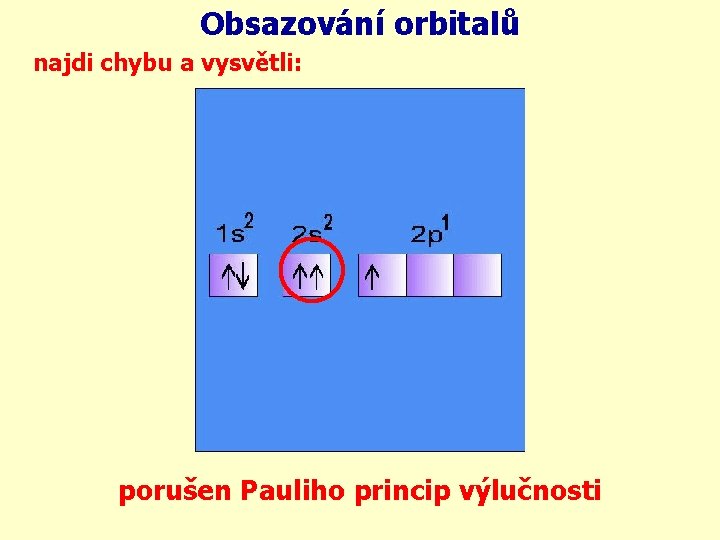
Obsazování orbitalů najdi chybu a vysvětli: porušen Pauliho princip výlučnosti
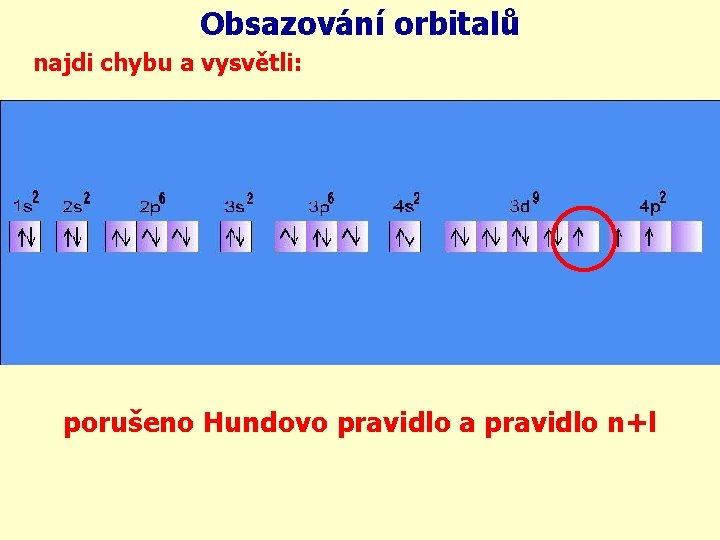
Obsazování orbitalů najdi chybu a vysvětli: porušeno Hundovo pravidlo a pravidlo n+l

OBSAZOVÁNÍ ORBITALŮ Vytvořeno v rámci projektu Gymnázium Sušice - Brána vzdělávání II Autor: Mgr. Radovan Sloup, Gymnázium Sušice Předmět: Chemie (obecná chemie) Třída: první ročník čtyřletého gymnázia Označení: VY_32_INOVACE_Ch-1_08 Anotace a metodické poznámky Po seznámení studentů s tématem kvantových čísel a obsazování orbitalů je možné použít tuto prezentaci. Po zopakování základních pravidel obsazování orbitalů je připraveno několik cvičení. Prezentaci lze použít i na interaktivní tabuli. Do připravených orbitalů mohou studenti vpisovat elektrony. Po vyplnění je na dalším slidu k dispozici řešení. Pro ukotvení správných návyků k zapisování je možné každý příklad prodiskutovat. Cvičení mohou být využita k dílčímu zkoušení. Použité materiály: Honza, J. ; Mareček, A. ; Chemie pro čtyřletá gymnázia (1. díl). Brno: Da. Ta. Print, 1995; ISBN 80 -900066 -6 -3 Vše je vytvořeno pomocí nástrojů Power Point 2003, Malování, Zoner Photo Studio 10, Word (Word. Art) 2003 Materiály jsou určeny pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízení. Jakékoliv další využití podléhá autorskému zákonu.
- Slides: 13