Objeto de Estudo SOLUES Caderno 2 Aula 02

Objeto de Estudo: SOLUÇÕES Caderno 2: Aula 02 QUÍMICA Prof. ALCEMIR MAIA
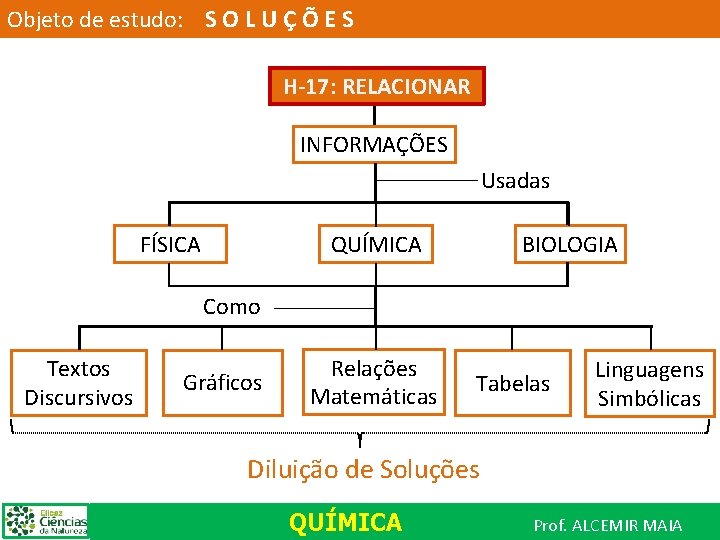
Objeto de estudo: S O L U Ç Õ E S H-17: RELACIONAR INFORMAÇÕES Usadas QUÍMICA FÍSICA BIOLOGIA Como Textos Discursivos Gráficos Relações Matemáticas Tabelas Linguagens Simbólicas Diluição de Soluções QUÍMICA Prof. ALCEMIR MAIA

Objeto de estudo: SOLUÇÕES – Diluição e concentração de Soluções Imagine que você esteja preparando uma limonada para o lanche com os amigos e acabou exagerando no limão. E agora? O que fazer? A solução é adicionar mais água. Esse tipo de procedimento – diluir ou concentrar soluções – é muito comum em nosso dia a dia. Deixamos a panela de feijão no fogo para concentrar ou “engrossar o caldo”, colocamos mais água no feijão para diluir o caldo; nas regiões do Brasil onde se toma café feito em máquina é possível escolher entre um “café curto” (mais concentrado, feito com menos água) ou um “café longo” (mais diluído, feito com mais água), entre outros exemplos. Diluir e concentrar soluções também são procedimentos muito utilizados no laboratório de Química para preparar soluções com uma concentração específica, acrescentando solvente, evaporando solvente ou misturando soluções de concentrações diferentes de modo que se obtenha a solução final com a concentração desejada. São essas operações e os conceitos relacionados a elas que veremos a seguir. QUÍMICA Prof. ALCEMIR MAIA
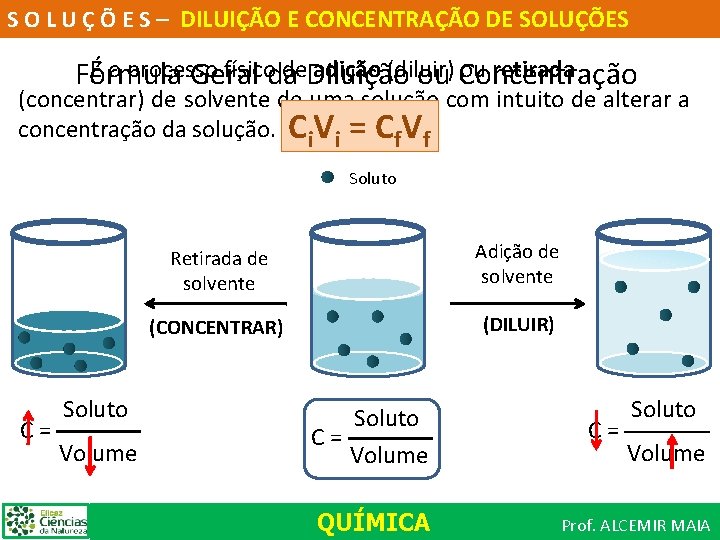
S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES É o processo físicoda de. Diluição adição (diluir) ou retirada Fórmula Geral ou Concentração (concentrar) de solvente de uma solução com intuito de alterar a concentração da solução. Ci. Vi = Cf. Vf Soluto C= Soluto Volume Retirada de solvente Adição de solvente (CONCENTRAR) (DILUIR) Soluto C= Volume QUÍMICA C= Soluto Volume Prof. ALCEMIR MAIA
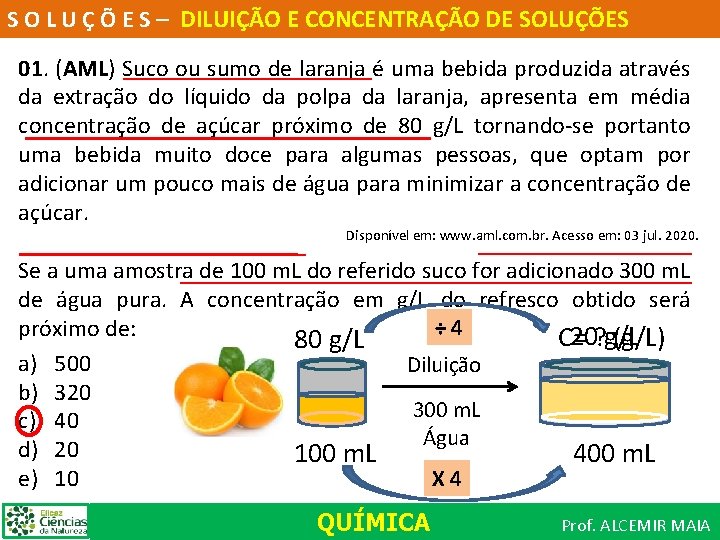
S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 01. (AML) Suco ou sumo de laranja é uma bebida produzida através da extração do líquido da polpa da laranja, apresenta em média concentração de açúcar próximo de 80 g/L tornando se portanto uma bebida muito doce para algumas pessoas, que optam por adicionar um pouco mais de água para minimizar a concentração de açúcar. Disponível em: www. aml. com. br. Acesso em: 03 jul. 2020. Se a uma amostra de 100 m. L do referido suco for adicionado 300 m. L de água pura. A concentração em g/L do refresco obtido será ÷ 4 próximo de: 20? g/L C= (g/L) a) b) c) d) e) 500 320 40 20 10 80 g/L 100 m. L Diluição 300 m. L Água QUÍMICA X 4 400 m. L Prof. ALCEMIR MAIA

S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 02. (UFRJ) Diluição é uma operação muito empregada no nosso dia a dia, quando, por exemplo, preparamos um refresco a partir de um suco concentrado. Considere 100 m. L de determinado suco em que a concentração de soluto seja 0, 4 mol x L– 1. O volume de água, em m. L, que deverá ser acrescentado para que a concentração do soluto caia para 0, 04 mol x L– 1, será de: a) b) c) d) 1000 900 500 400 X 10 100 m. L 0, 4 mol/L Diluição V H 2 O = ? (m. L) VFINAL = ? m. L = 1000 0, 04 mol/L ÷ 10 QUÍMICA Prof. ALCEMIR MAIA

S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 03. (AML) O sal é produzido através de um processo contínuo de evaporação da água do mar, onde aproximadamente ¾ de todo sal é cloreto de sódio. Para produzir uma tonelada de sal, utiliza se aproximadamente 40 m³ de água do mar que foi inicialmente bombeada. O sal é colhido mecanicamente ou manualmente, empilhado nas áreas de estocagem, onde aguardará para ser comercializado. Disponível em: https//site. google. com/professorpedrofaria. Acesso em: 03 jul. 2020 (adaptado) Admitindo velocidade de evaporação igual a 500 L/dia e que não haja cristalização no período, quantos dias serão necessários para que a concentração de cloreto de sódio seja de 37, 5 kg/m 3? a) 20 1 t sal 750 kg Na. Cl 40 m 3 água do mar b) 35 c) 30 m (kg) 1 m 3 água do mar d) 35 18, 75 kg/m 3 e) 40 QUÍMICA Prof. ALCEMIR MAIA
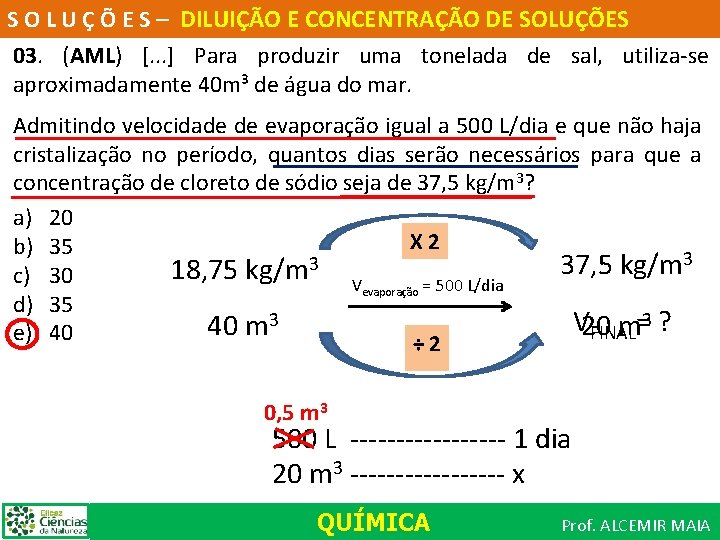
S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 03. (AML) [. . . ] Para produzir uma tonelada de sal, utiliza se aproximadamente 40 m³ de água do mar. Admitindo velocidade de evaporação igual a 500 L/dia e que não haja cristalização no período, quantos dias serão necessários para que a concentração de cloreto de sódio seja de 37, 5 kg/m 3? a) 20 X 2 b) 35 3 3 37, 5 kg/m 18, 75 kg/m c) 30 Vevaporação = 500 L/dia d) 35 3 3? V = 40 m 20 m FINAL e) 40 ÷ 2 0, 5 m 3 500 L 1 dia 20 m 3 x QUÍMICA Prof. ALCEMIR MAIA
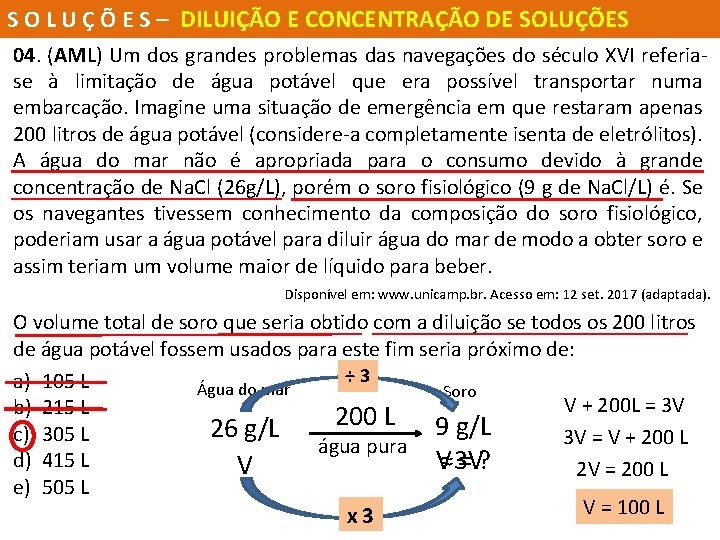
S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 04. (AML) Um dos grandes problemas das navegações do século XVI referia se à limitação de água potável que era possível transportar numa embarcação. Imagine uma situação de emergência em que restaram apenas 200 litros de água potável (considere a completamente isenta de eletrólitos). A água do mar não é apropriada para o consumo devido à grande concentração de Na. Cl (26 g/L), porém o soro fisiológico (9 g de Na. Cl/L) é. Se os navegantes tivessem conhecimento da composição do soro fisiológico, poderiam usar a água potável para diluir água do mar de modo a obter soro e assim teriam um volume maior de líquido para beber. Disponível em: www. unicamp. br. Acesso em: 12 set. 2017 (adaptada). O volume total de soro que seria obtido com a diluição se todos os 200 litros de água potável fossem usados para este fim seria próximo de: ÷ 3 a) 105 L Água do mar Soro V + 200 L = 3 V b) 215 L 200 L 9 g/L 26 g/L c) 305 L 3 V = V + 200 L água pura d) 415 L V≈3 V =? V 2 V = 200 L e) 505 L V = 100 L x 3

S O L U Ç Õ E S – DILUIÇÃO E CONCENTRAÇÃO DE SOLUÇÕES 05. (Unimar*) Você se mudou para uma casa nova com uma bonita banheira de água quente que tem a forma de um coração. Você precisa saber o volume de água da banheira, mas, devido à forma irregular desta, não é simples determinar suas dimensões e calcular o volume. Por causa disso, você procura resolver o problema criando uma solução referencia adicionando 5, 85 g de cloreto de sódio (Na. Cl) em água até perfazer o volume de 500 m. L. Então você mistura a solução de sacarose com a água da banheira fazendo uma solução diluída. Depois, retira uma amostra desta solução. E em um laboratório químico, usando um instrumento, como um espectrofotômetro, determina que a concentração de sacarose na banheira é 1, 0 × 10− 4 mol/L. Admitindo massas atômicas em mol/L: Na=23, Cl=35, 5. O volume em litros de água na banheira é próximo de: a) 50 b) 1000 c) 1500 d) 2000 e) 10500 * adaptada QUÍMICA Prof. ALCEMIR MAIA

PELA ATENÇÃO DE TODOS VCS, MUITÍSSIMO OBRIGADO
- Slides: 11