OBJETIVO Identificar las reacciones qumicas como un proceso


OBJETIVO Identificar las reacciones químicas como un proceso de reorganización atómica que genera productos y se representa mediante una ecuación química.
TIPOS DE REACCIONES QUÍMICAS • Según la reorganización de los átomos: Síntesis o combinación Descomposición Sustitución o Desplazamiento (Doble desplazamiento o intercambio)
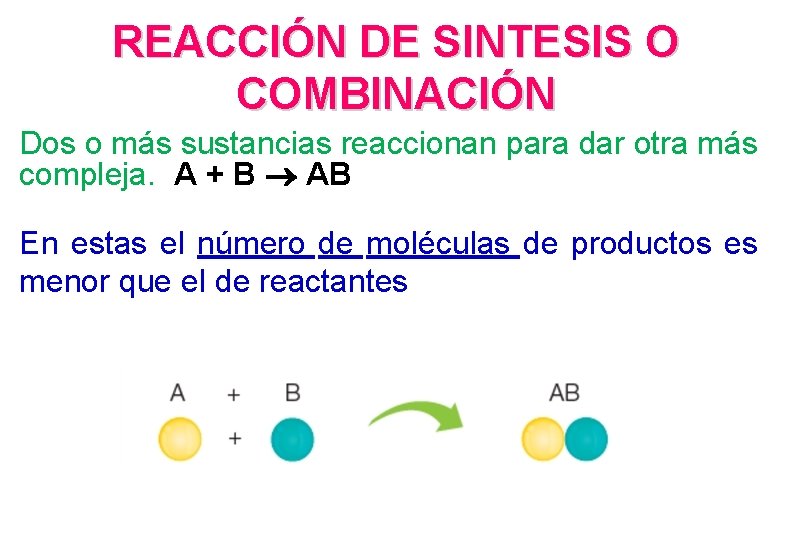
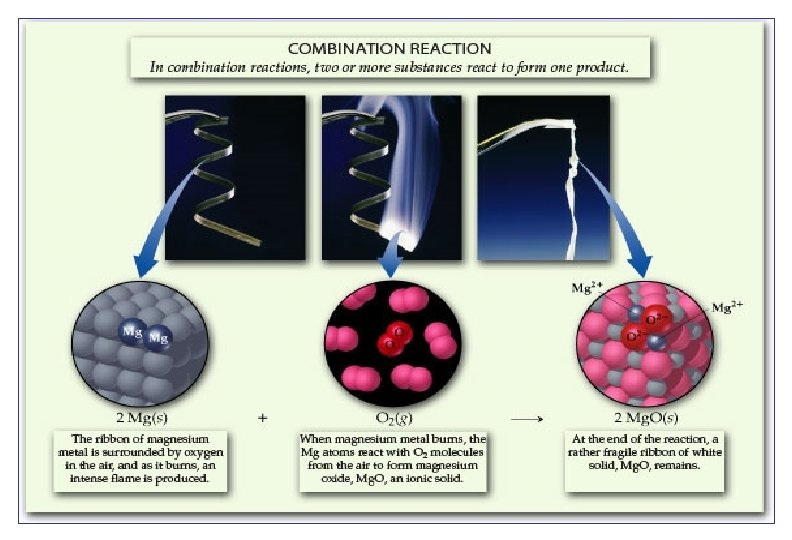
REACCIÓN DE SINTESIS O COMBINACIÓN Dos o más sustancias reaccionan para dar otra más compleja. A + B AB En estas el número de moléculas de productos es menor que el de reactantes

REACCIÓN DE SINTESIS O COMBINACIÓN Generalmente, estas reacciones son exotérmicas, es decir, se libera energía térmica al crearse el nuevo enlace químico en los productos. La formación del agua a partir de sus elementos es un ejemplo de reacción de síntesis

REACCIÓN DE SINTESIS O COMBINACIÓN § Las reacciones entre dos no metales dan compuestos covalentes: N 2 + 3 H 2 2 NH 3 § Las reacciones entre un no metal y un metal dan sales: S + Fe Fe. S § Las reacciones entre un elemento y oxígeno producen óxidos: 2 Ca + O 2 2 Ca. O S + O 2 SO 2 § Las reacciones entre un óxido y agua producen hidróxidos: Ca. O + H 2 O Ca(OH)2 § Las reacciones entre un anhídrido y agua producen ácidos: SO 2 + H 2 O H 2 SO 3 § Las reacciones entre un óxido y un anhídrido dan sales: Ca. O + SO 2 Ca. SO 3
Sintesis o Combinación • Elementos se combinan para formar un compuesto: 2 H 2 + O 2 Elemento + Elemento 2 H 2 O Compuesto 8

REACCIONES DE DESCOMPOSICIÓN Una sustancia se descompone formando dos o más simples. AB A + B Las reacciones de descomposición consisten en un proceso de división de los reactantes en sustancias con estructuras más simples. El número de moléculas de productos es mayor que el de reactantes

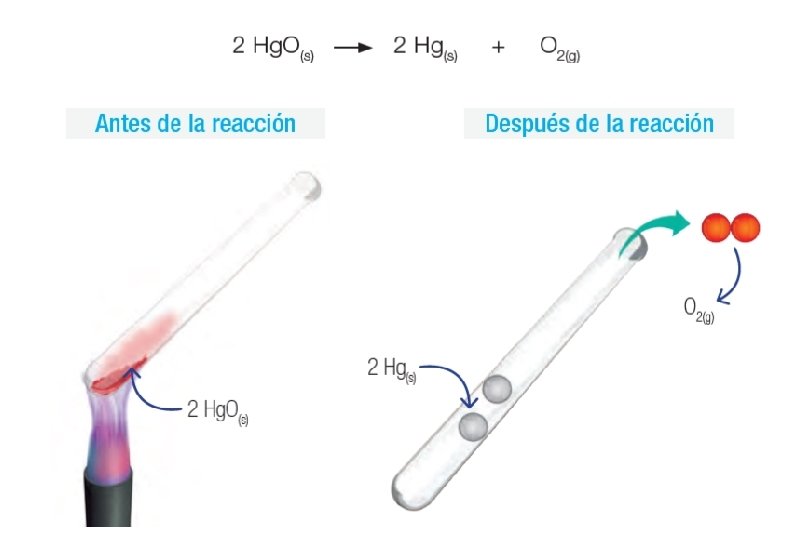
REACCIONES DE DESCOMPOSICIÓN En general, estas reacciones son endotérmicas, o sea, para romper los enlaces químicos de las sustancias reactantes es necesario absorber energía térmica. Ejemplo la descomposición del óxido de mercurio (II)
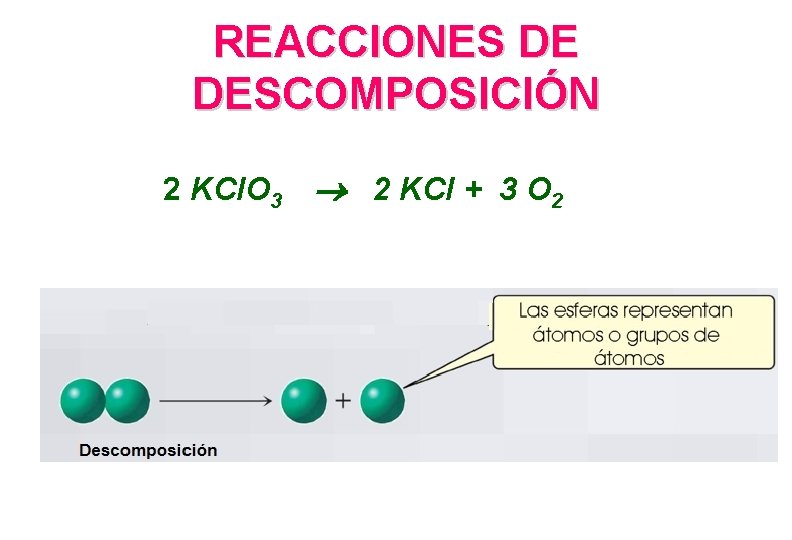
REACCIONES DE DESCOMPOSICIÓN 2 KCl. O 3 2 KCl + 3 O 2
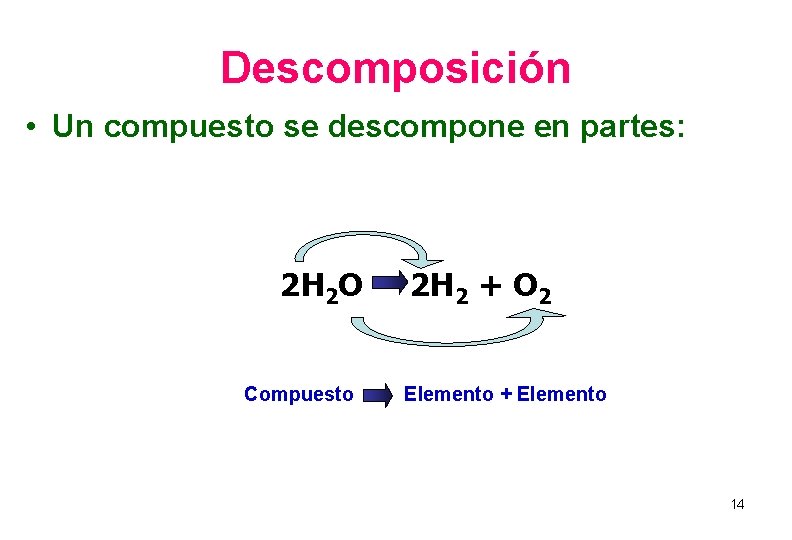
Descomposición • Un compuesto se descompone en partes: 2 H 2 O Compuesto 2 H 2 + O 2 Elemento + Elemento 14

REACCIONES DE SUSTITUCIÓN El número de moléculas de productos es igual al de reactantes, y solamente se intercambian átomos entre ellas. Hay dos tipos de sustitución: por desplazamiento simple o desplazamiento doble.
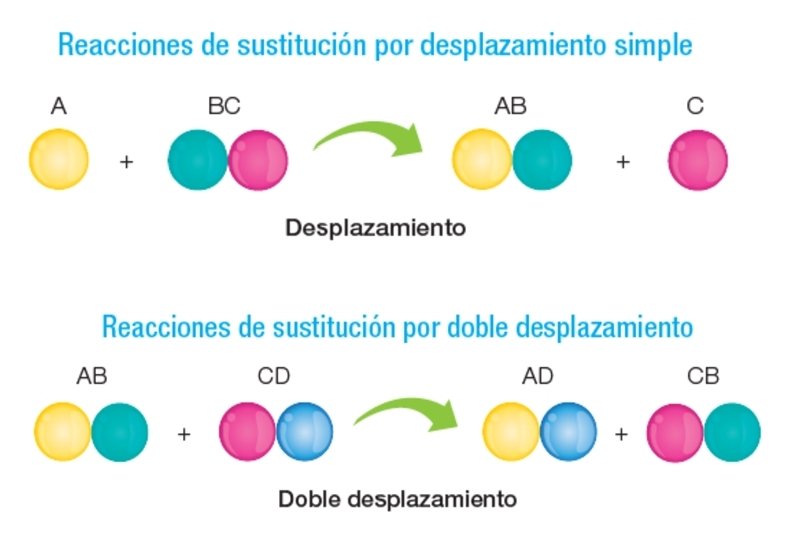

REACCIONES DE SUSTITUCIÓN o SIMPLE DESPLAZAMIENTO Uno de los elementos de un compuesto es sustituido por otro elemento. AB + X AX + B Algunos metales reaccionan con ciertos ácidos, reemplazando el hidrógeno y formando la sal correspondiente: Zn + H 2 SO 4 Zn. SO 4 + H 2 Un metal puede ser desplazado de sus sales por otro metal más activo: Zn + Cu. SO 4 Zn. SO 4 + Cu
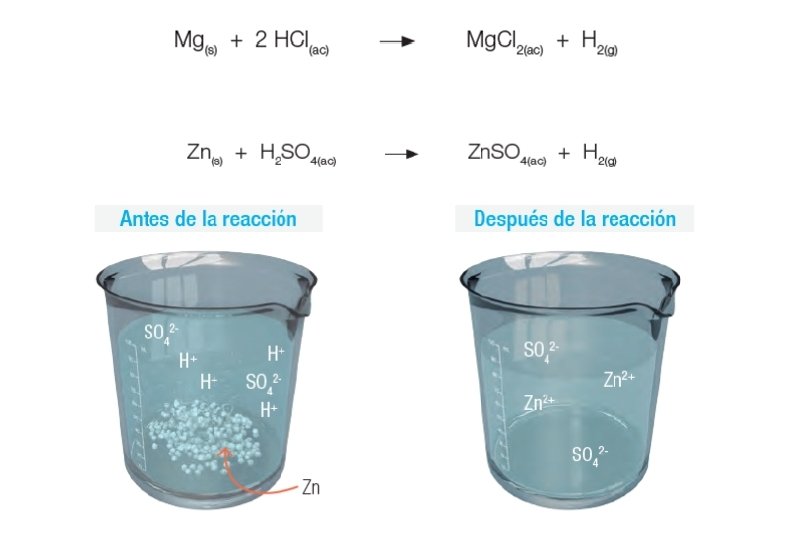

Simple Desplazamiento • Un elemento desplaza a otro elemento en un compuesto: Zn + 2 HCl Elemento + Compuesto Zn. Cl 2 + H 2 Compuesto + Elemento 19
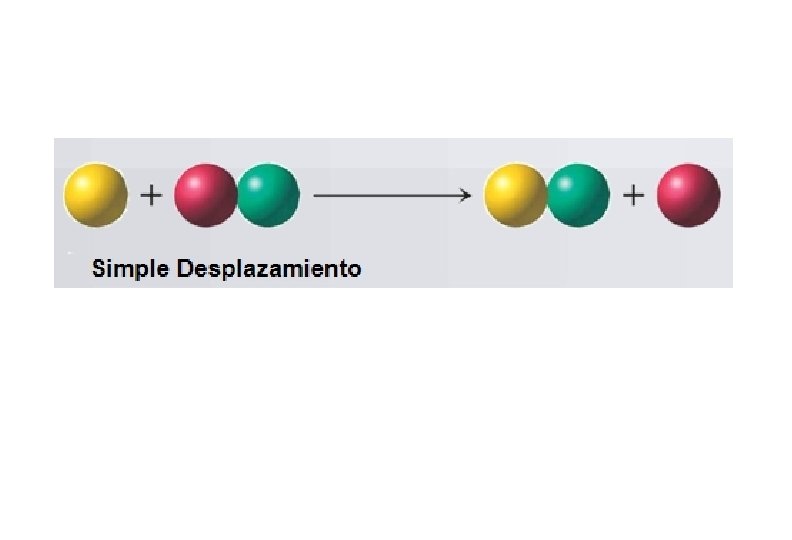
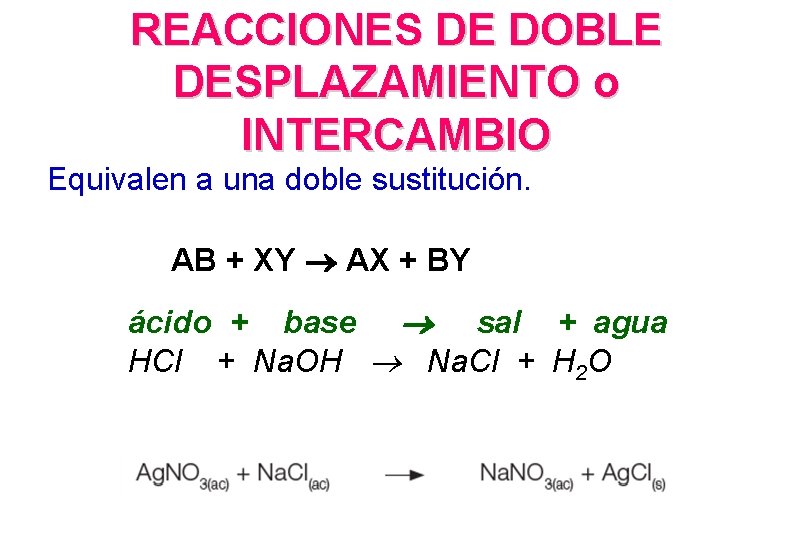
REACCIONES DE DOBLE DESPLAZAMIENTO o INTERCAMBIO Equivalen a una doble sustitución. AB + XY AX + BY ácido + base sal + agua HCl + Na. OH Na. Cl + H 2 O
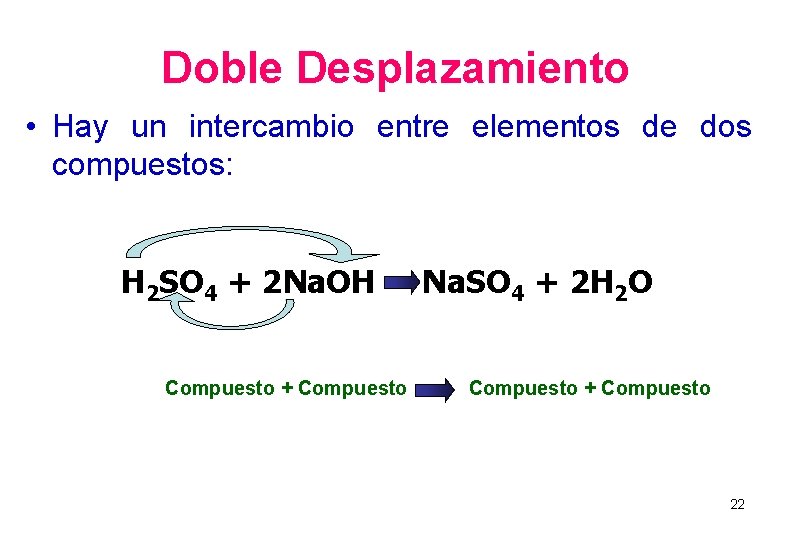
Doble Desplazamiento • Hay un intercambio entre elementos de dos compuestos: H 2 SO 4 + 2 Na. OH Compuesto + Compuesto Na. SO 4 + 2 H 2 O Compuesto + Compuesto 22

Ejercicio • Equilibre e identifique el tipo de cada una de las siguientes ecuaciones: 24

Ejercicio • Equilibre e identifique el tipo de cada una de las siguientes ecuaciones: 25

• Respuesta del ejercicio anterior: 1. 2. 3. 4. Simple Desplazamiento Combinación Neutralizaciónn Doble Desplazamiento 26
- Slides: 26