OBJETIVO Distinguir las caractersticas y propiedades de los


OBJETIVO • Distinguir las características y propiedades de los metales.

• Se caracterizan por poseer: _ Un brillo o lustre característico, llamado brillo metálico. _ Son buenos conductores del calor y de la electricidad.

_ Son maleables (se los puede trabajar formando láminas o planchas). Los elementos más maleables, en orden creciente (de – a +), son: hierro, cinc, plomo, platino, estaño, cobre, plata y oro

_ Son dúctiles (se los puede estirar generando hilos y alambres). _ A temperatura ambiente su estado físico es sólido, con excepción del mercurio, que es líquido. _ Sus temperaturas de fusión y ebullición son bastante elevadas.

_ Pierden facilmente electrones para formar cationes: Ca 2+, Fe 3+. Li +, etc. _ Forman compuestos con los no metales: Ca. O, Fe 2 S 3, Li. Br, etc. _ No forman compuestos con otros metales. _ Forman aleaciones (mezclas homogéneas)

_Algunos son duros como el cromo (Cr), hierro (Fe), manganeso (Mn). _Algunos son blandos como el oro (Au), plomo (Pb) y sodio (Na). _No reaccionan entre sí, pero reaccionan con los no metales, formando compuestos.

_Poseen elevadas densidades. _ Algunos metales tienen propiedades magnéticas, son atraidos por imanes (Fe, Co, Ni y Ga). _ Se oxidan al contacto con oxígeno formando óxidos metálicos básicos: Li 2 O, Mg. O, Ni 2 O 3, etc.

_ Los óxidos de los metales en contacto con el agua forman hidróxidos: Li. OH: Hidróxido de litio Mg(OH)2: Hidróxido de magnesio Na. OH: Hidróxido de sodio Etc.
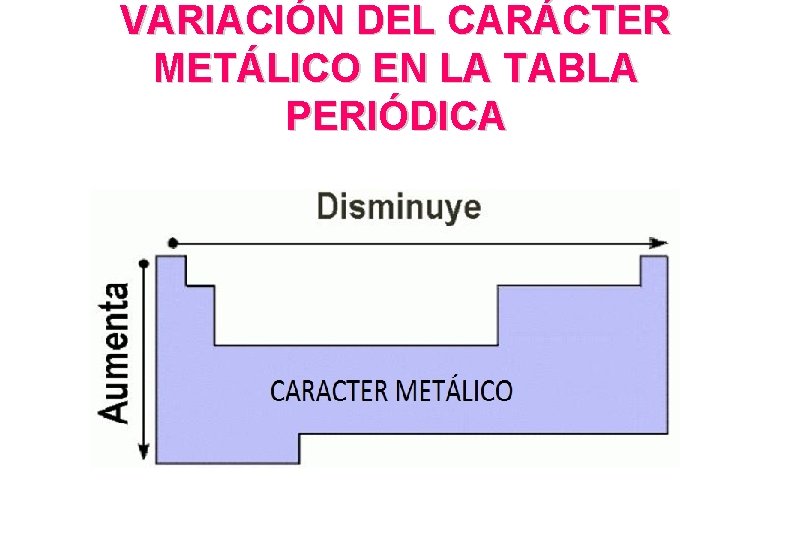
VARIACIÓN DEL CARÁCTER METÁLICO EN LA TABLA PERIÓDICA

- Slides: 12