OBJETIVO Diferenciar molculas entre tomos y TOMO Toda


OBJETIVO • Diferenciar moléculas. entre átomos y

ÁTOMO • Toda la materia esta formada por partículas diminutas llamadas átomos. • Se denomina partícula fundamental, no puede descomponerse mediante procesos químicos, ni físicos.

• Un átomo es la menor porción de un elemento que conserva las propiedades químicas del mismo

MOLÉCULA • Unión de dos o más átomos iguales o diferentes entre sí, por ejemplo: O 2, H 2 SO 4, etc. Cantidad mínima de una sustancia pura que conserva sus propiedades químicas y físicas



Están constituidas por 2 átomos O 2 O O 1 Molécula DIATÓMICA de OXÍGENO
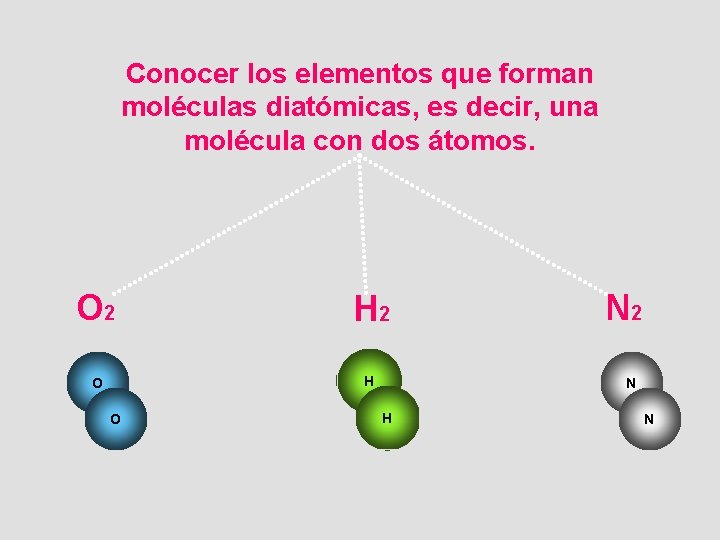
Conocer los elementos que forman moléculas diatómicas, es decir, una molécula con dos átomos. O 2 H 2 O H O N 2 N H N
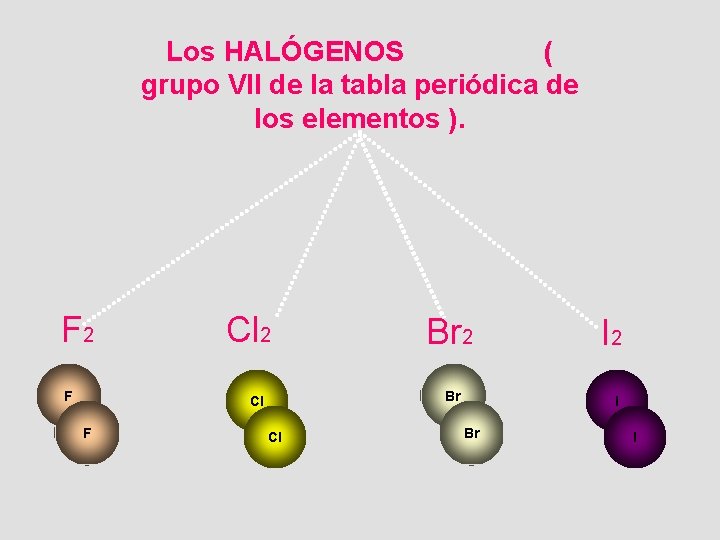
Los HALÓGENOS ( grupo VII de la tabla periódica de los elementos ). F 2 F Cl 2 Br Cl F Br 2 Cl I 2 I Br I
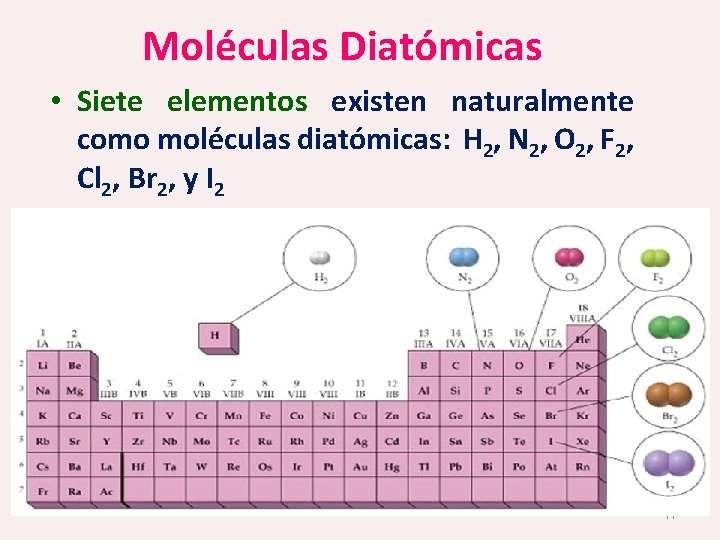
Moléculas Diatómicas • Siete elementos existen naturalmente como moléculas diatómicas: H 2, N 2, O 2, F 2, Cl 2, Br 2, y I 2 11

Están constituidas por 2 átomos, en este ejemplo son diferentes Na. Cl Na Cl Molécula de CLORURO DE SODIO 1 átomo de sodio y 1 átomo de cloro

Están constituidas por 2 átomos H 2 1 Molécula DIATÓMICA de HIDRÓGENO

Están constituidas por 2 átomos N 2 1 Molécula DIATÓMICA de NITRÓGENO
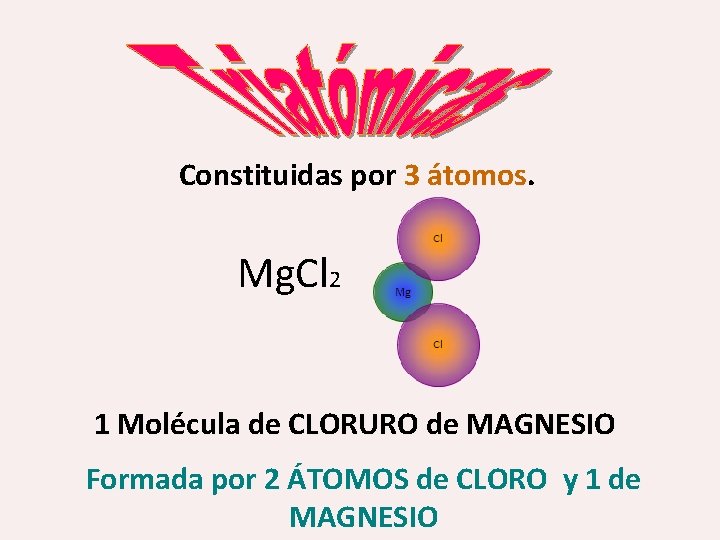
Constituidas por 3 átomos Mg. Cl 2 1 Molécula de CLORURO de MAGNESIO Formada por 2 ÁTOMOS de CLORO y 1 de MAGNESIO

Constituidas por 4 átomos NH 3 1 Molécula de AMONIACO Formada por 3 ÁTOMOS de HIDRÓGENO y 1 de NITRÓGENO

Constituidas por 5 átomos N 2 O 3 1 Molécula de TRIÓXIDO de DINITRÓGENO Formada por 3 ÁTOMOS de OXÍGENO y 2 ÁTOMOS de NITRÓGENO
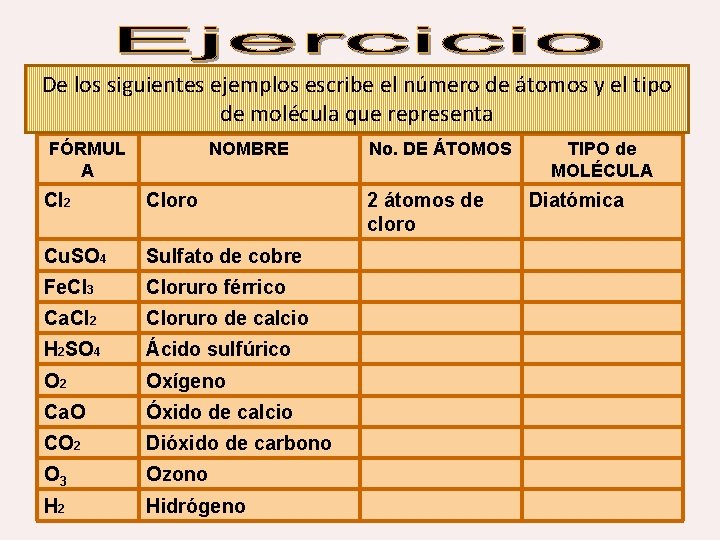
De los siguientes ejemplos escribe el número de átomos y el tipo de molécula que representa FÓRMUL A NOMBRE Cl 2 Cloro Cu. SO 4 Sulfato de cobre Fe. Cl 3 Cloruro férrico Ca. Cl 2 Cloruro de calcio H 2 SO 4 Ácido sulfúrico O 2 Oxígeno Ca. O Óxido de calcio CO 2 Dióxido de carbono O 3 Ozono H 2 Hidrógeno No. DE ÁTOMOS 2 átomos de cloro TIPO de MOLÉCULA Diatómica
- Slides: 18