OBJETIVO Conocer el origen de la tabla peridica

OBJETIVO • Conocer el origen de la tabla periódica

• Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades variaban periódicamente en relación a su masa. • De esa manera, hubo diversos intentos de agrupar los elementos, todos ellos usando la masa atómica como criterio de ordenación

DOBEREINER (1829) • La clasificación de los elementos corresponden a TRIADAS, son grupos de elementos con propiedades parecidas. • Ejemplo: (Ca, Sr, Ba) (Cl, Br, I) (S, Se, Te). • La masa del elemento intermedio es la media aritmética de la masa de los otros dos.

CHANCOURTOIS (1862) • Coloca los elementos en espiral de forma tal los que tienen propiedades parecidas queden unos encima de otros. © Ed ECIR. Química 2º Bach.

NEWLANDS (1864) Ordena los elementos por orden de masa atómica, y observa que las propiedades se repiten periódicamente cada 8 elementos. A estos grupos de 8 elementos les llamó octavas, por su parecido con la clasificación de las notas musicales. Sólo se cumplía para los primeros elementos

MENDELEIV y MEYER (1869) • El ruso Dimitri Ivanovich Mendeleiev y el alemán Lothar Meyer llegan por separado a una clasificación parecida. A partir del orden por masas atómicas, colocan en una misma columna los elementos con propiedades parecidas, estableciendo una tabla

• Mendeleiev introdujo unas mejoras importantes en la clasificación, dando prioridad a las propiedades. Por tanto: cambió el orden de algunos elementos para que se situaran en la columna que les correspondía según sus propiedades (Co. Ni) (Te- I).

MENDELEIV • La clasificación de Mendeleiev es la mas conocida y elaborada de todas las primeras clasificaciones periódicas. • Clasificó lo 63 elementos conocidos hasta entonces utilizando el criterio de masa atómica usado hasta entonces. • Hasta bastantes años después no se definió el concepto de número atómico puesto que no se habían descubierto los protones. • Dejaba espacios vacíos, que él consideró que se trataba de elementos que aún no se habían descubierto

• Predijo las propiedades de algunos elementos, tales como el germanio (Ge). • En vida de Mendeleiev se descubrió el Ge que tenía las propiedades previstas. • Un inconveniente de la tabla de Mendeleiev era que algunos elementos tenía que colocarlos en desorden de masa atómica para que coincidieran las propiedades. • Él lo atribuyó a que las masas atómicas estaban mal medidas. Así, por ejemplo, colocó el teluro (Te) antes que el yodo (I) a pesar de que la masa atómica de éste era menor que la de aquel

CLASIFICACIÓN DE MENDELEIEV

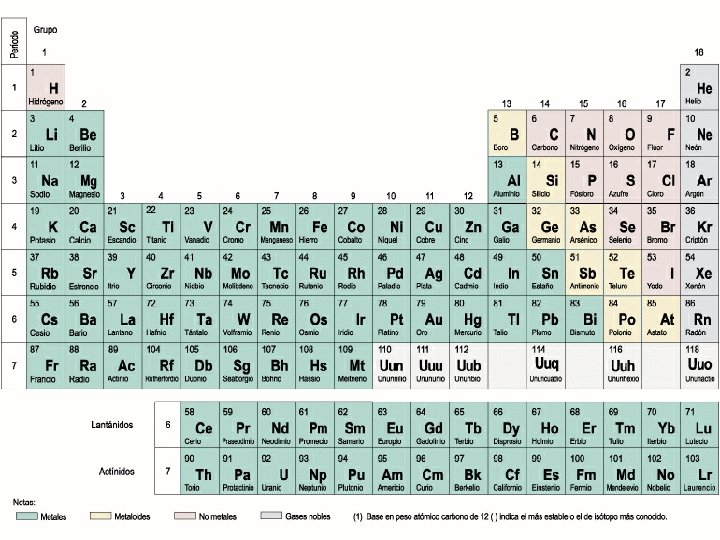
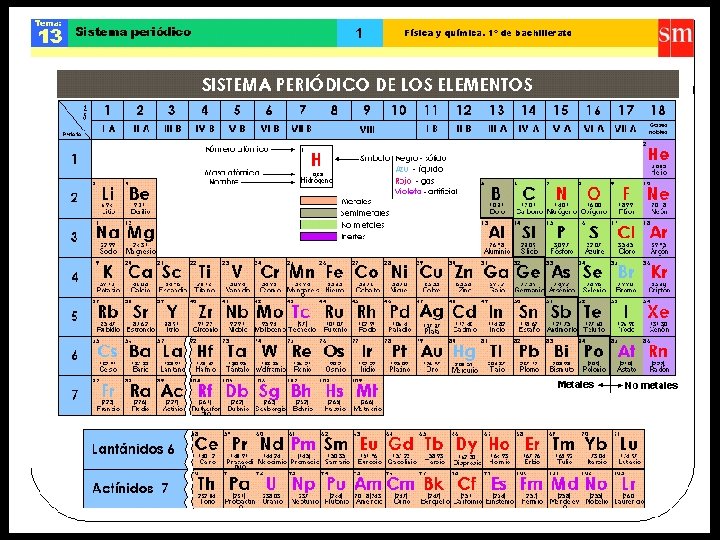
MOSELEY (1913) • Con el descubrimiento de nuevo elementos, se agregan nuevas columnas a la tabla de Mendeleiev (gases nobles, tierras raras), y con el descubrimiento por Moseley, en 1914, del número atómico, se llega a la tabla periódica actual. • Enunció la “ley periódica”: "Si los elementos se colocan según aumenta su número atómico, se observa una variación periódica de sus propiedades físicas y químicas".

• Hay una relación directa entre el último orbital ocupado por un electrón de un átomo y su posición en la tabla periódica y, por tanto, en su reactividad química, fórmula estequiométrica en los compuestos que forma.
- Slides: 16