OBECN CHEMIE STAVBA HMOTY Ing Alena Hejtmnkov CSc

OBECNÁ CHEMIE STAVBA HMOTY Ing. Alena Hejtmánková, CSc. Katedra chemie Agronomická fakulta ČZU Praha © Praha, 2003

ELEMENTÁRNÍ ČÁSTICE ATOMU atom (z řeckého tomos = nedělitelný) tvoří 3 základní elementární částice u elektron (Thompson, 1897) katodové záření u elementární náboj e- = 1, 602. 10 -19 C u hmotnost elektronu me= 9, 1091. 10 -31 kg u proton (Rutherford, 1920) u elementární náboj p+ = 1, 60210. 10 -19 C u hmotnost protonu mp= 1, 67252. 10 -27 kg (1840 krát těžší než elektron) u neutron (Chadwick, 1932) u bez náboje u hmotnost neutronu mn= 1, 67482. 10 -27 kg Obecná chemie. Stavba hmoty. 2

ELEMENTÁRNÍ ČÁSTICE ATOMU ostatní částice podle hmotnosti u lehké – leptony (elektron, pozitron, neutrino, …) u středně těžké (mezony p, K, …) u těžké – baryony (proton, neutron, hyperony, …) fotony u základní částice elektromagnetického záření u nulová klidová hmotnost Obecná chemie. Stavba hmoty. 3
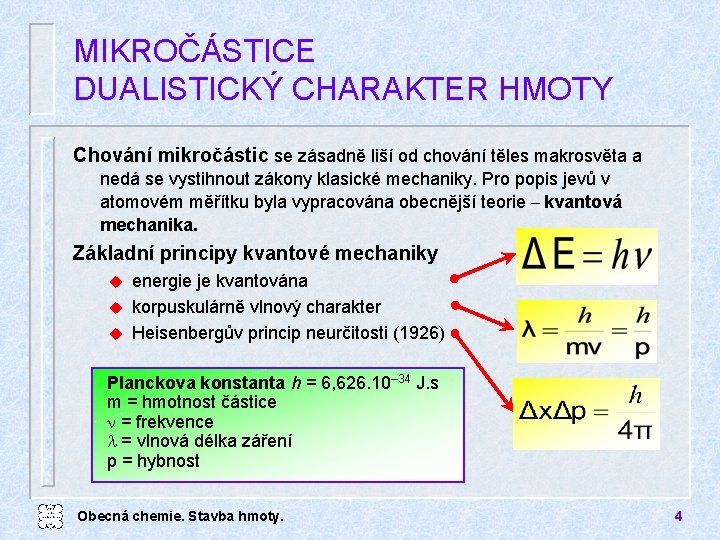
MIKROČÁSTICE DUALISTICKÝ CHARAKTER HMOTY Chování mikročástic se zásadně liší od chování těles makrosvěta a nedá se vystihnout zákony klasické mechaniky. Pro popis jevů v atomovém měřítku byla vypracována obecnější teorie – kvantová mechanika. Základní principy kvantové mechaniky energie je kvantována u korpuskulárně vlnový charakter u Heisenbergův princip neurčitosti (1926) u Planckova konstanta h = 6, 626. 10– 34 J. s m = hmotnost částice n = frekvence l = vlnová délka záření p = hybnost Obecná chemie. Stavba hmoty. 4
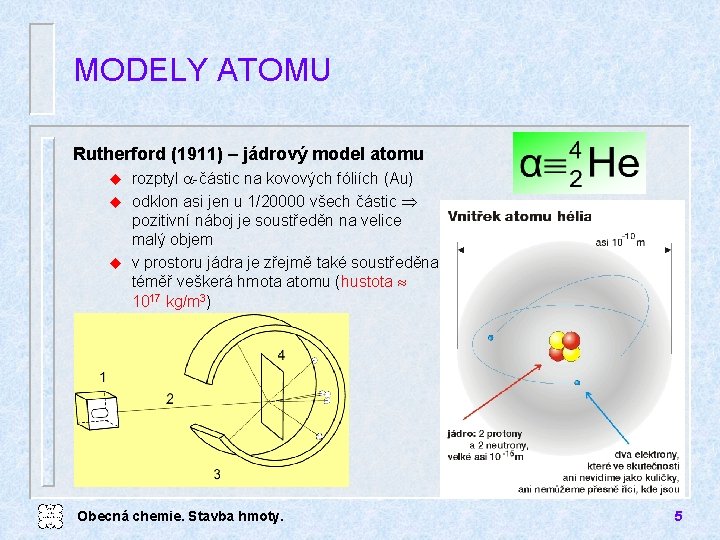
MODELY ATOMU Rutherford (1911) – jádrový model atomu rozptyl -částic na kovových fóliích (Au) u odklon asi jen u 1/20000 všech částic pozitivní náboj je soustředěn na velice malý objem u v prostoru jádra je zřejmě také soustředěna téměř veškerá hmota atomu (hustota 1017 kg/m 3) u Obecná chemie. Stavba hmoty. 5

CHARAKTERISTIKY ATOMU A, nukleonové (hmotnostní) číslo udává počet nukleonů v jádře Z, atomové (protonové) číslo udává počet protonů v jádře (také počet elektronů) Obecná chemie. Stavba hmoty. oxidační číslo elektronegativita X, chemická značka prvku N = neutronové číslo N=A–Z nukleony = protony a neutrony 6

JSOU VŠECHNY ATOMY STEJNÉ? ? Prvek u je tvořen souborem atomů, jejichž atomové číslo Z je shodné Nuklid u atomy mají shodné atomové číslo Z a neutronové číslo N x Izotop u mají shodné atomové číslo Z a různé neutronové číslo N Izobar u mají shodné nukleonové číslo A a různé atomové číslo Z Obecná chemie. Stavba hmoty. 7

JSOU VŠECHNY ATOMY STEJNÉ? ? Poměrné zastoupení izotopů téhož prvku není přesně konstantní – (vodík, lehké prvky) u využití – přírodovědné obory (koloběh vody) Atomová hmotnost u absolutní pro praxi nevhodné vyjádření u relativní MR, jednotkou je 1 u Bez izotopů celá čísla S izotopy Obecná chemie. Stavba hmoty. 8

STABILITA ATOMOVÝCH JADER Atomové jádro – u vazebná energie, úbytek hmotnosti Vazebná energie štěpení Síly – u přitažlivé jaderné u odpudivé coulombovské Obecná chemie. Stavba hmoty. 9

STABILITA ATOMOVÝCH JADER Energie chemického procesu 105 až 106 krát menší nemůže ovlivnit jádro atomu Fe U Obecná chemie. Stavba hmoty. 10

STABILITA ATOMOVÝCH JADER 56 radioaktivních nuklidů v přírodě stabilní nuklidy Obecná chemie. Stavba hmoty. 11

STABILITA ATOMOVÝCH JADER magická čísla pro celkový počet protonů nebo neutronů 2, 8, 20, 28, 50, 82, 126 velmi stabilní nuklid ! Obecná chemie. Stavba hmoty. 12

RADIOAKTIVITA H. Becquerel (1886) – expozice fotografické desky sloučeninou uranu u spontánní emise subatomových částic přeměna prvku Proč? Malá stabilita jádra u nadbytek protonů nebo neutronů u nízká vazebná energie Pierre Curie (1859 -1906) & Marie Curie-Skłodowska (1867 -1934) Obecná chemie. Stavba hmoty. 13

TYPY PŘEMĚN Přeměny a (těžká jádra Z > 83) Přeměny b– (přebytek neutronů) Důvod – změna poměru n/p Obecná chemie. Stavba hmoty. 14

TYPY PŘEMĚN Přeměny b+ (rel. přebytek protonů), uměle připravené prvky Záchyt elektronu do jádra (relativní přebytek protonů) doplnění elektronu z vyšší hladiny Záření většinou doprovází , (samostatně výjimečně) u nemění jádro u Obecná chemie. Stavba hmoty. 15

RADIOAKTIVNÍ ŘADY – POSUVOVÉ ZÁKONY Sled radioaktivních prvků – 4 řady (1 umělá řada) současně emise , – částic jednotky radioaktivity 1 curie (Ci) – počet rozpadů za sekundu v 1 g Ra 1 becquerel (Bq) – 1 rozpad za sekundu 1 Ci = 3, 7. 1010 Bq Obecná chemie. Stavba hmoty. 16

RYCHLOST RADIOAKTIVNÍHO ROZPADU T 1/2 = 6, 93 roků N – počet jader v čase t N 0 – počet jader na počátku k – rozpadová konstanta (pravděpodobnost rozpadu jádra za jednotku času) T 1/2 – poločas rozpadu 10 poločasů ~ 1/1000 N 0 prvek „vymře“ problém radioaktivního odpadu !!! Obecná chemie. Stavba hmoty. 17

ÚČINKY RADIOAKTIVNÍHO ZÁŘENÍ Obecná chemie. Stavba hmoty. 18

VÝSKYT RADIOAKTIVNÍCH PRVKŮ V PŘÍRODĚ Radioaktivní prvky – poločas rozpadu stáří Země zářiče – Radioaktivní prvky z rozpadových řad – poločas rozpadu relativně krátký Obecná chemie. Stavba hmoty. 19

UMĚLÉ RADIOAKTIVNÍ PRVKY Vznik: jadernými reakcemi tj. zasažením jádra částicí z radioaktivního zářiče (alfa záření) u z urychlovače (neutrony) u Jaderné přeměny u prosté (transmutace) u Rutherford (1919) u nové jádro se málo liší od původního u vzniklé jádro se rozpadá umělá radioaktivita Obecná chemie. Stavba hmoty. 20

UMĚLÉ RADIOAKTIVNÍ PRVKY http: //sensor. feld. cvut. cz/bavig/ Jaderné přeměny u štěpné – Fermi, Hahn, Joliot (1934 – 1939) Lavinovité štěpení exploze u princip atomové bomby (106 až 107 C v epicentru) Řízený průběh u atomové reaktory u moderátory (těžká voda D 2 O, grafit, bór, …) Obecná chemie. Stavba hmoty. 200 Me. V 21

TERMONUKLEÁRNÍ REAKCE Syntéza stálejších produktů z lehkých jader princip vodíkové bomby, Teller (1952, atol Eniwetok) u Slunce a jiné hvězdy. . . u teplota T > 106 C Obecná chemie. Stavba hmoty. 22

VYUŽITÍ RADIOIZOTOPŮ 1. Analytická chemie u NAA – Neutronová Aktivační Analýza (stopová množství) 2. Chemie a biologie u studium mechanismu reakcí (stopování) u určování distribuce prvků v biologickém materiálu radioenzymová analýza (REA) 3. Medicína u ozařování nádorů paprsky (gama) u sterilizace krve Obecná chemie. Stavba hmoty. 23

VYUŽITÍ RADIOIZOTOPŮ 4. Zemědělství u ošetření potravin (ničení choroboplodných zárodků) u prodloužení dormance brambor 5. Určení stáří u hornin u organismů Obecná chemie. Stavba hmoty. 24

NEGATIVNÍ DŮSLEDKY ZÁŘENÍ Ionizace u narušení chemických vazeb u poškození tkání u mutagenní, kancerogenní a teratogenní účinky u !!! Nejvíce nebezpečné !!! Radioaktivní izotopy s poločasem rozpadu srovnatelným se stářím živých organismů T 1/2 = 28 roků – 0, 53 Me. V Obecná chemie. Stavba hmoty. 25

Konec Obecná chemie. Stavba hmoty. 26
- Slides: 26