O tomo Modelos Atmicos Modelo de tomo que
































- Slides: 58

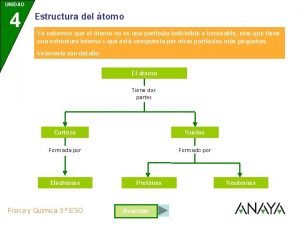
O átomo

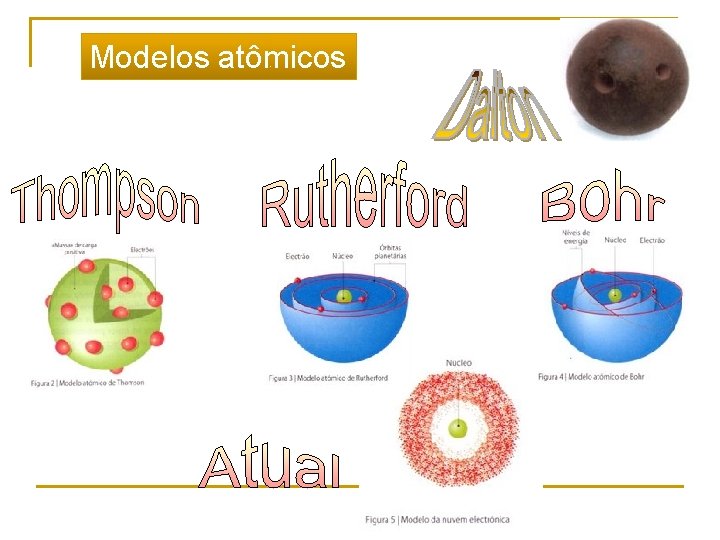
Modelos Atômicos • Modelo de átomo que pode parecer familiar a você. • Núcleo em volta do qual os elétrons orbitam em diferentes níveis de energia. Um modelo que usa ideias familiares para tentar explicar fatos não familiares observados na natureza

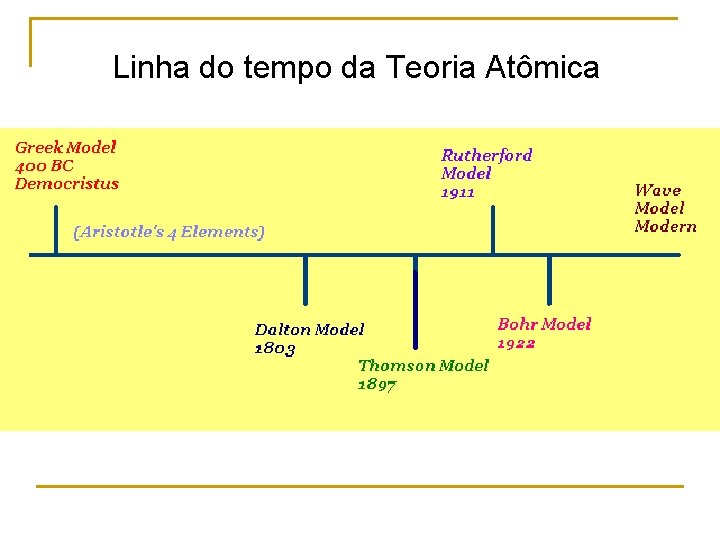
Linha do tempo da Teoria Atômica

Criador da palavra átomo


n Os filósofos importantes daquele tempo como Aristóteles e Platão não apoiaram a nova teoria. Why? Aristotle and Plato favored the earth, fire, air and water approach to the nature of matter. Their ideas held sway because of their eminence as philosophers. The atomos idea was buried for approximately 2000 years. Mais de 2000 anos se passaram.

Modelo de Dalton (1803) n No início do século XVIII, o químico inglês John Dalton realizou um número de experimentos que levaram a aceitação da ideia da existência do átomo.

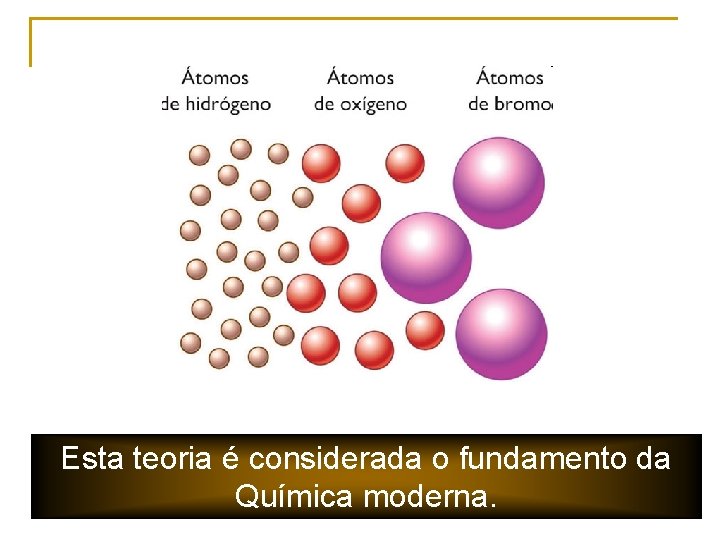
Esta teoria é considerada o fundamento da Química moderna.

A descoberta da estrutura atômica Raios catódicos e elétrons



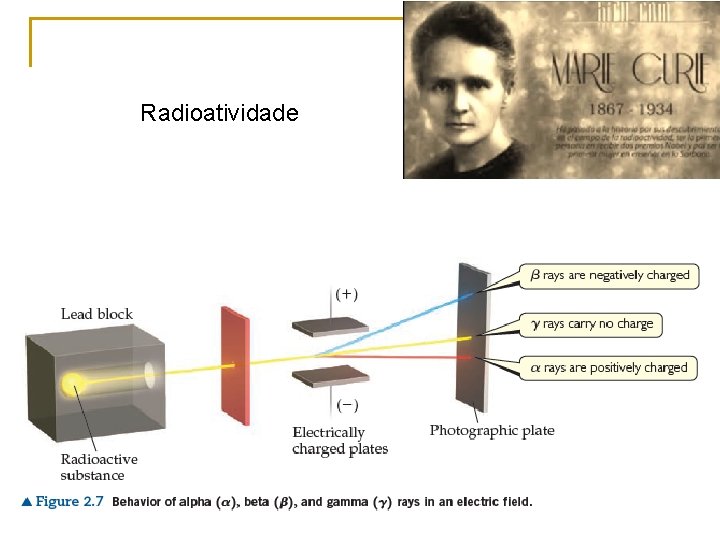
Radioatividade

Modelo de Thomson: n In 1897, the English scientist J. J. Thomson provided the first hint that an atom is made of even smaller particles. Modelo do pudim de passas

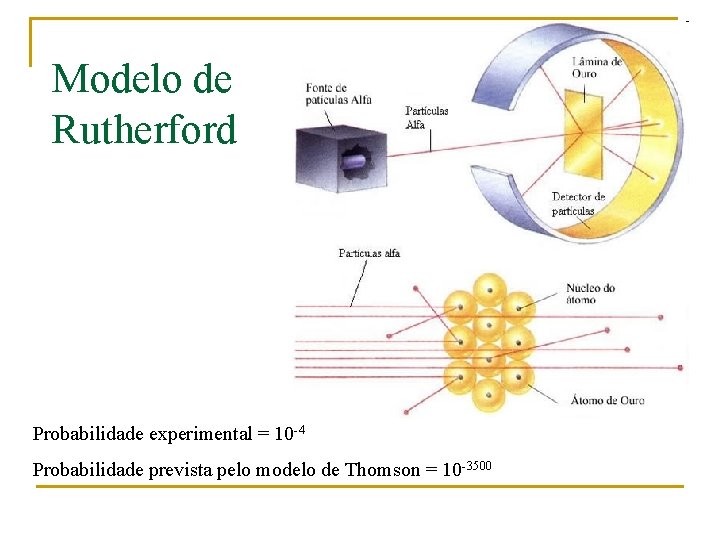
Em 1911, Ernest Rutherford propôs uma experiência na qual uma folha de ouro era bombardeada por partículas a (He 2+). a Qual era o resultado esperado?

Modelo de Rutherford Probabilidade experimental = 10 -4 Probabilidade prevista pelo modelo de Thomson = 10 -3500

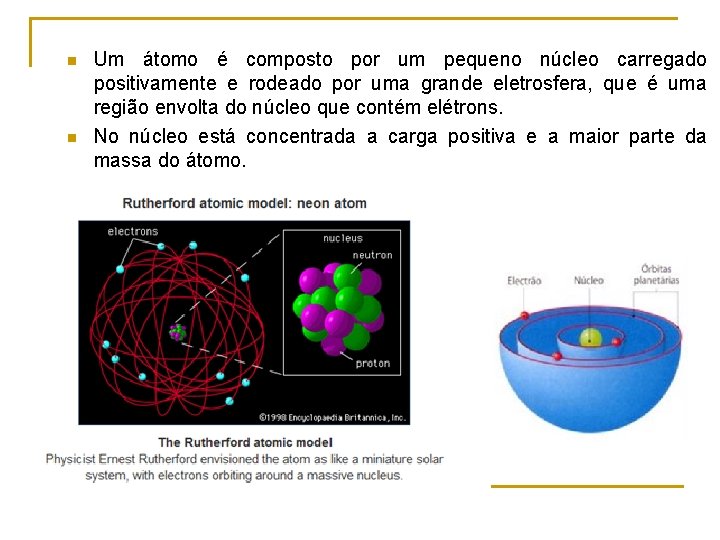
n n Um átomo é composto por um pequeno núcleo carregado positivamente e rodeado por uma grande eletrosfera, que é uma região envolta do núcleo que contém elétrons. No núcleo está concentrada a carga positiva e a maior parte da massa do átomo.

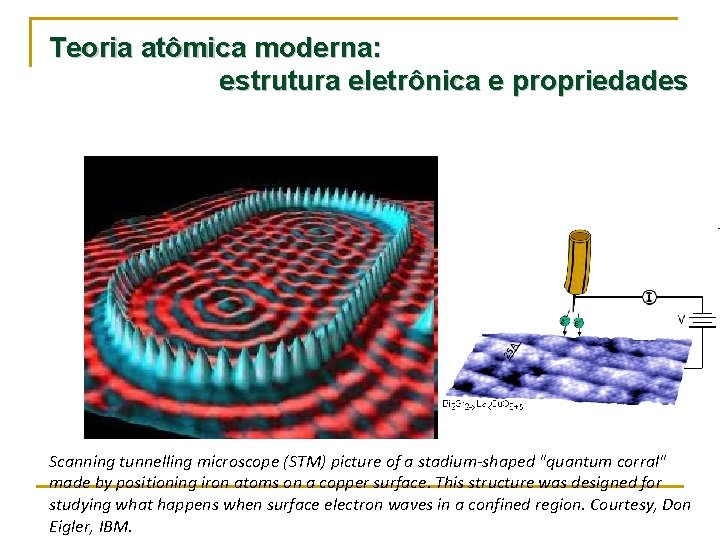
Teoria atômica moderna: estrutura eletrônica e propriedades Scanning tunnelling microscope (STM) picture of a stadium-shaped "quantum corral" made by positioning iron atoms on a copper surface. This structure was designed for studying what happens when surface electron waves in a confined region. Courtesy, Don Eigler, IBM.

O átomo segundo Bohr

Problemas encontrados por Bohr 1. Estabilidade do átomo nuclear 2. Espectros atômicos

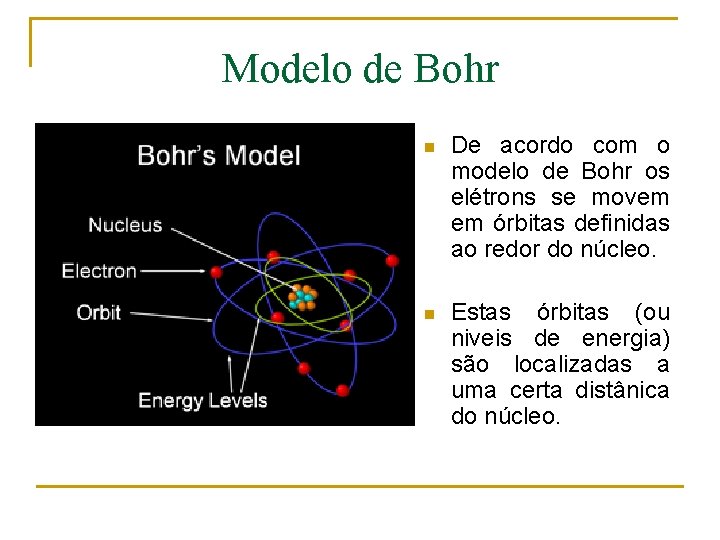
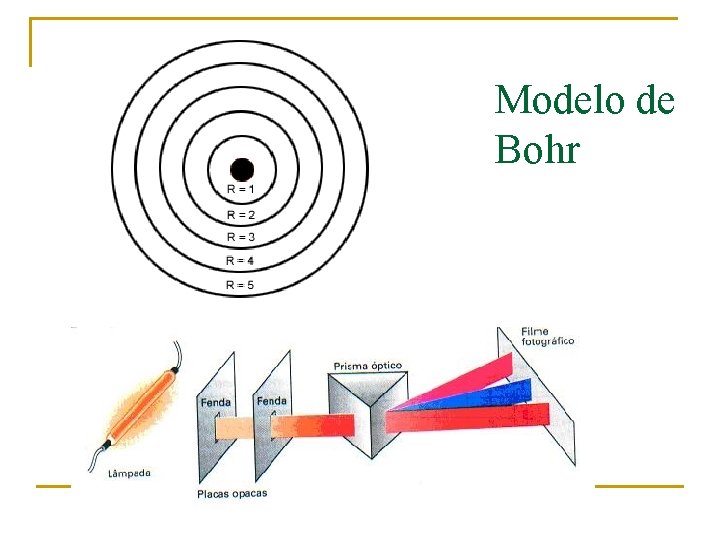
Modelo de Bohr n De acordo com o modelo de Bohr os elétrons se movem em órbitas definidas ao redor do núcleo. n Estas órbitas (ou niveis de energia) são localizadas a uma certa distânica do núcleo.

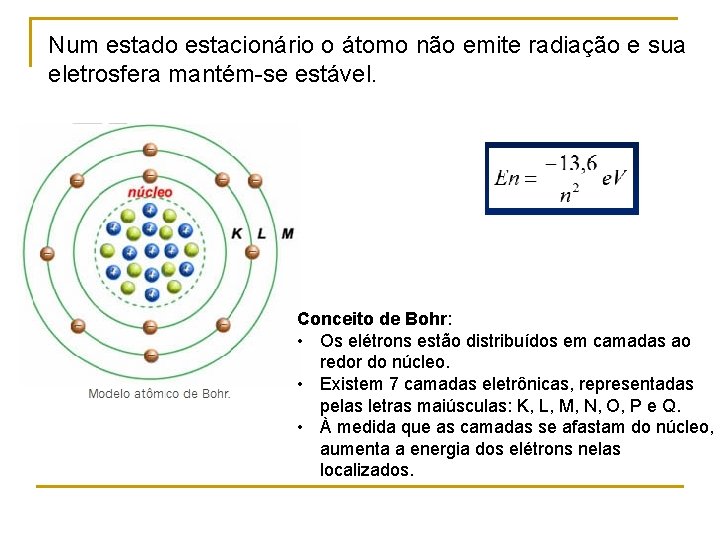
Num estado estacionário o átomo não emite radiação e sua eletrosfera mantém-se estável. Conceito de Bohr: • Os elétrons estão distribuídos em camadas ao redor do núcleo. • Existem 7 camadas eletrônicas, representadas pelas letras maiúsculas: K, L, M, N, O, P e Q. • À medida que as camadas se afastam do núcleo, aumenta a energia dos elétrons nelas localizados.

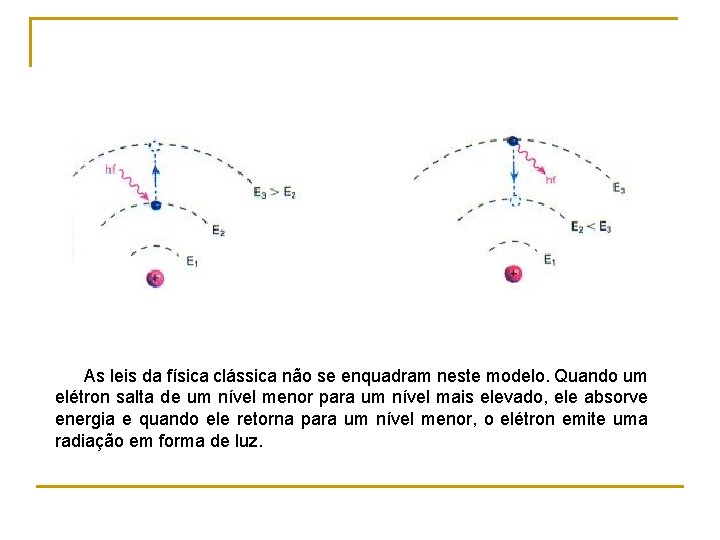
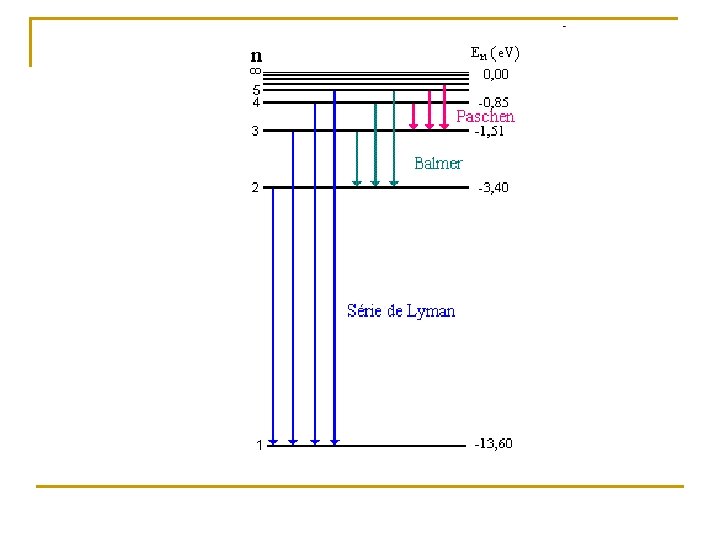
As leis da física clássica não se enquadram neste modelo. Quando um elétron salta de um nível menor para um nível mais elevado, ele absorve energia e quando ele retorna para um nível menor, o elétron emite uma radiação em forma de luz.




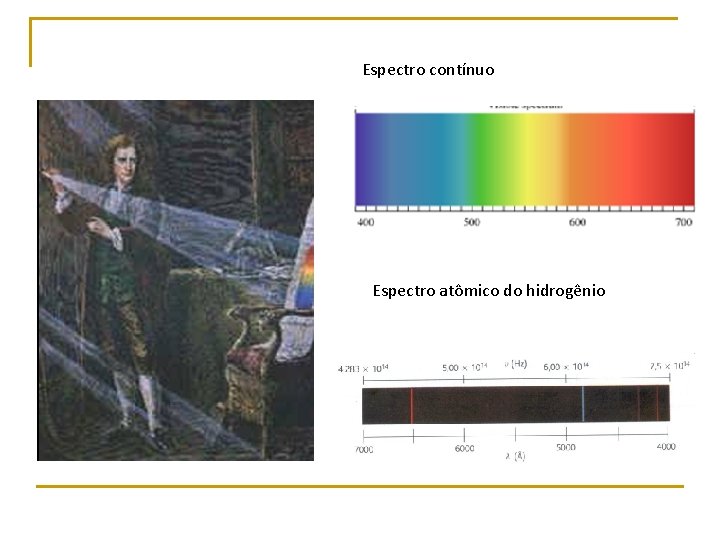
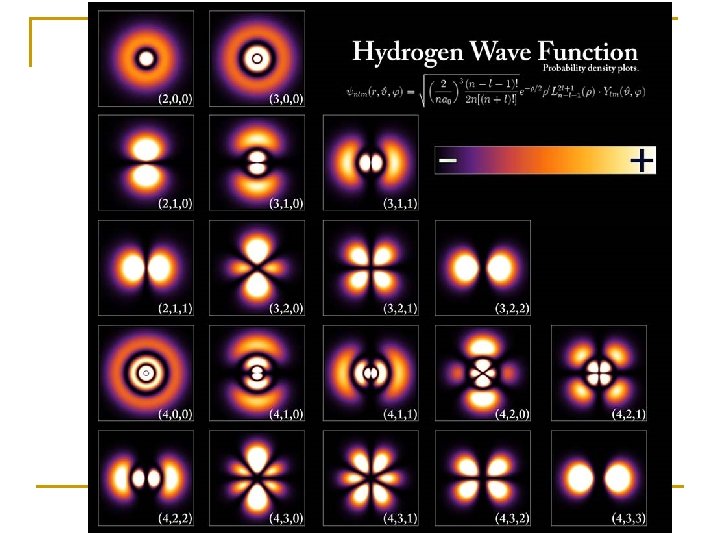
Espectro contínuo Espectro atômico do hidrogênio



Modelo de Bohr


Espectro atômico



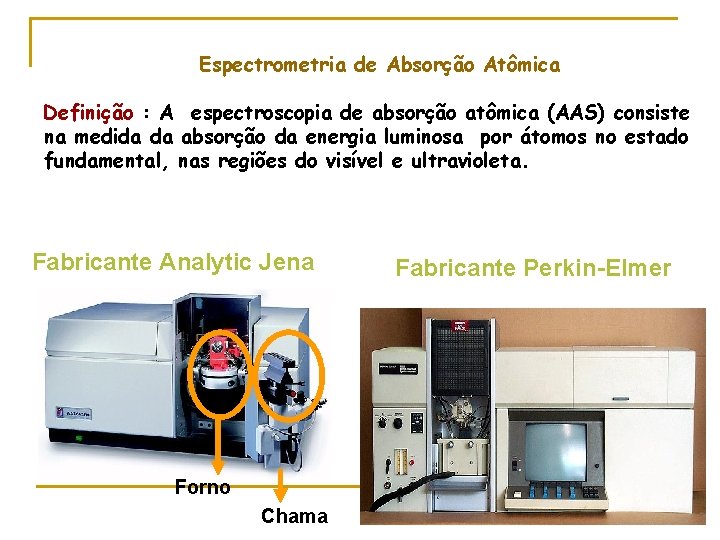
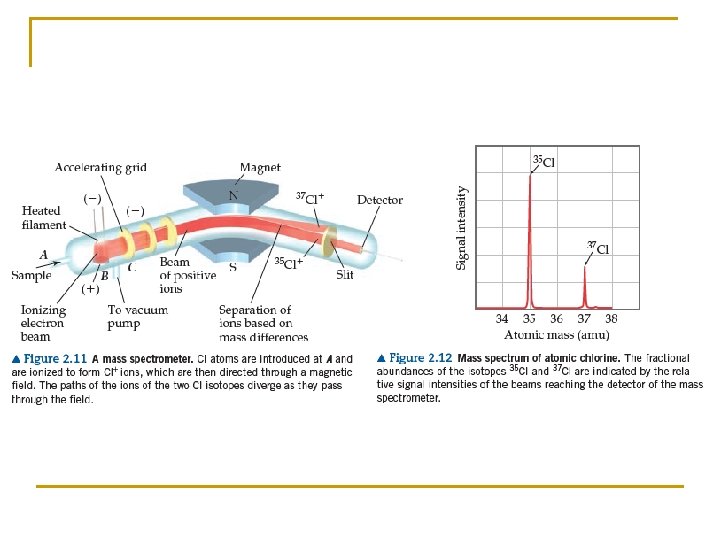
Espectrometria de Absorção Atômica Definição : A espectroscopia de absorção atômica (AAS) consiste na medida da absorção da energia luminosa por átomos no estado fundamental, nas regiões do visível e ultravioleta. Fabricante Analytic Jena Forno Chama Fabricante Perkin-Elmer

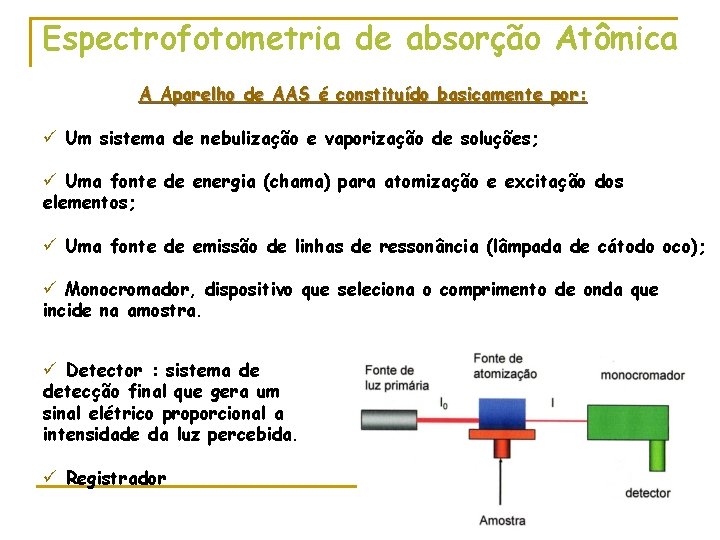
Espectrofotometria de absorção Atômica A Aparelho de AAS é constituído basicamente por: ü Um sistema de nebulização e vaporização de soluções; ü Uma fonte de energia (chama) para atomização e excitação dos elementos; ü Uma fonte de emissão de linhas de ressonância (lâmpada de cátodo oco); ü Monocromador, dispositivo que seleciona o comprimento de onda que incide na amostra. ü Detector : sistema de detecção final que gera um sinal elétrico proporcional a intensidade da luz percebida. ü Registrador



1924: Natureza do elétron é questionada. .





Estudando o espectro de emissão do átomo de hidrogênio com técnicas mais avançadas: Isso ajudou a corrigir problemas apresentados pelo modelo proposto por Niels Bohr. Arnold Sommerfeld percebeu que as linhas espectrais não eram únicas, mas formadas por conjuntos de linhas muito próximas umas das outras.

Para várias linhas espectrais, várias órbitas. . . Para cada “n”, n possíveis valores de “l”. Sommerfeld utilizou um número, chamado de “número quântico do momento angular do orbital ou azimutal” (l) para representá-las. Foi determinado que o número máximo de elétrons num subnível é dado por: 2 (2 l + 1).

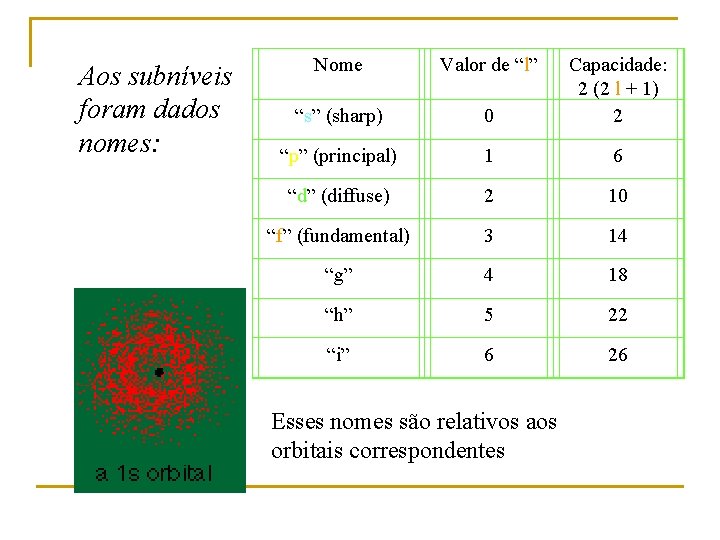
Aos subníveis foram dados nomes: Nome “s” (sharp) Valor de “l” 0 Capacidade: 2 (2 l + 1) 2 “p” (principal) 1 6 “d” (diffuse) 2 10 “f” (fundamental) 3 14 “g” 4 18 “h” 5 22 “i” 6 26 Esses nomes são relativos aos orbitais correspondentes

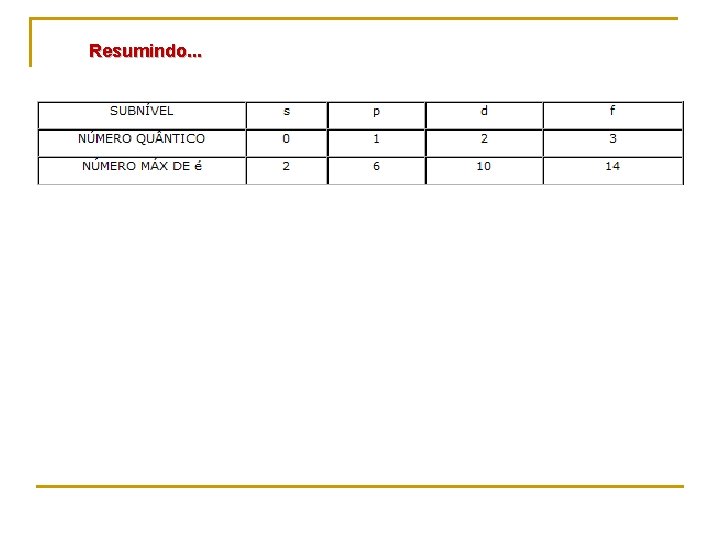
Resumindo. . .




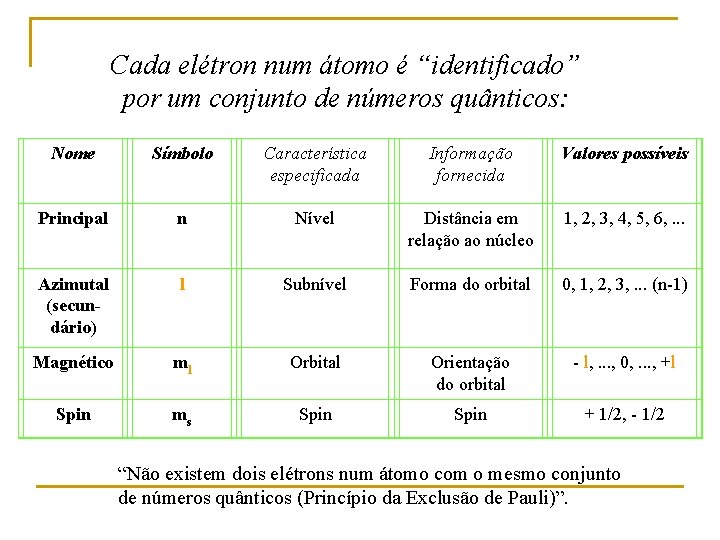
Cada elétron num átomo é “identificado” por um conjunto de números quânticos: Nome Símbolo Característica especificada Informação fornecida Valores possíveis Principal n Nível Distância em relação ao núcleo 1, 2, 3, 4, 5, 6, . . . Azimutal (secundário) l Subnível Forma do orbital 0, 1, 2, 3, . . . (n-1) Magnético ml Orbital Orientação do orbital - l, . . . , 0, . . . , +l Spin ms Spin + 1/2, - 1/2 “Não existem dois elétrons num átomo com o mesmo conjunto de números quânticos (Princípio da Exclusão de Pauli)”.

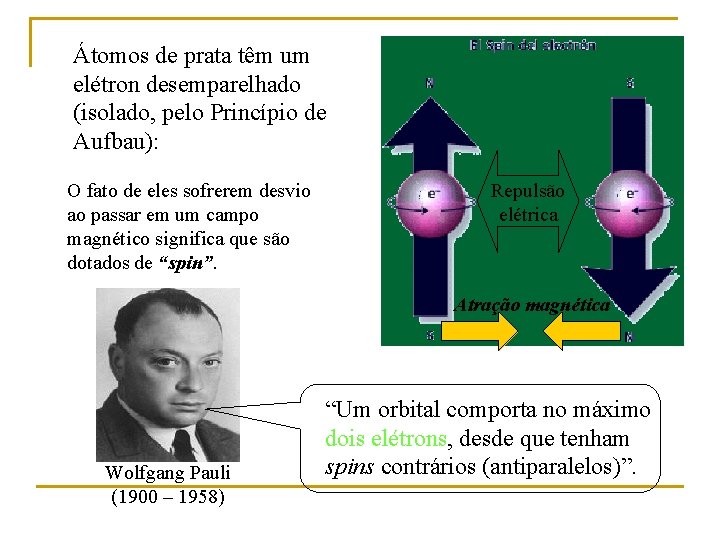
Átomos de prata têm um elétron desemparelhado (isolado, pelo Princípio de Aufbau): O fato de eles sofrerem desvio ao passar em um campo magnético significa que são dotados de “spin”. Repulsão elétrica Atração magnética Wolfgang Pauli (1900 – 1958) “Um orbital comporta no máximo dois elétrons, desde que tenham spins contrários (antiparalelos)”.



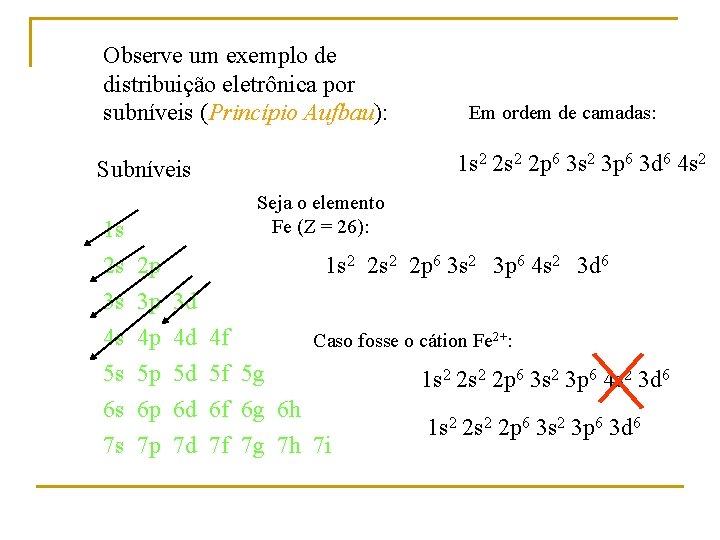
Observe um exemplo de distribuição eletrônica por subníveis (Princípio Aufbau): 1 s 2 2 p 6 3 s 2 3 p 6 3 d 6 4 s 2 Subníveis 1 s 2 s 2 p 3 s 3 p 3 d Em ordem de camadas: Seja o elemento Fe (Z = 26): 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 6 4 s 4 p 4 d 4 f Caso fosse o cátion Fe 2+: 5 s 5 p 5 d 5 f 5 g 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 6 6 s 6 p 6 d 6 f 6 g 6 h 1 s 2 2 p 6 3 s 2 3 p 6 3 d 6 7 s 7 p 7 d 7 f 7 g 7 h 7 i

Modelos atômicos

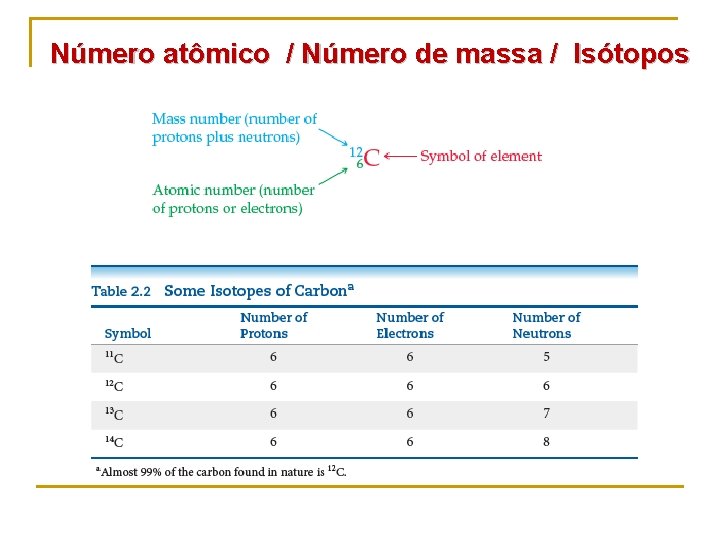
Número atômico / Número de massa / Isótopos


 Superestandar lenguaje
Superestandar lenguaje Codigo nacional de electricidad utilizacion
Codigo nacional de electricidad utilizacion Tomo fix
Tomo fix Mientras cenaban jesus tomo
Mientras cenaban jesus tomo Asumo riesgos y tomo la iniciativa
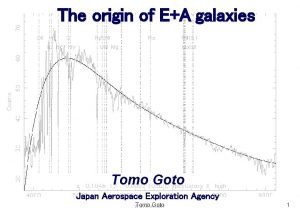
Asumo riesgos y tomo la iniciativa Tomo goto
Tomo goto Tömő utca onkológia
Tömő utca onkológia Hologic's low dose 3d mammography
Hologic's low dose 3d mammography Esde tomo único
Esde tomo único Mensajes selectos tomo 1 pdf
Mensajes selectos tomo 1 pdf Principi di chimica moderna tomo b soluzioni
Principi di chimica moderna tomo b soluzioni Tomo cerovšek
Tomo cerovšek Principi di chimica moderna - tomo a soluzioni
Principi di chimica moderna - tomo a soluzioni Tomo mano romanas veimare
Tomo mano romanas veimare Perjuangan bung tomo
Perjuangan bung tomo Stanka hrastelj
Stanka hrastelj Ajla tomo
Ajla tomo Tomo el jugo en un a. cuchillo b. vaso c. plato
Tomo el jugo en un a. cuchillo b. vaso c. plato Partes del tomo
Partes del tomo Tomo ya
Tomo ya Tomi keber
Tomi keber 1 tomo
1 tomo Ves
Ves Leo primero tomo 1 primero basico
Leo primero tomo 1 primero basico Circuitos combinacionales
Circuitos combinacionales Capas de la tierra y sus características
Capas de la tierra y sus características Experimento de la lamina de oro de ernest rutherford
Experimento de la lamina de oro de ernest rutherford Que son los modelos gerenciales para la toma de decisiones
Que son los modelos gerenciales para la toma de decisiones Modelo referencia
Modelo referencia Teoria cinetica
Teoria cinetica Preguntas sobre los textos informativos
Preguntas sobre los textos informativos Autorregistro
Autorregistro Modelos psicodinamicos
Modelos psicodinamicos Conceptos y modelos en psicopatología
Conceptos y modelos en psicopatología Que es la personalidad
Que es la personalidad Beneficios de un sistema de salud basado en aps
Beneficios de un sistema de salud basado en aps Modelo clasico de diseño de puestos
Modelo clasico de diseño de puestos Una compañia fabrica y venden dos modelos de lampara
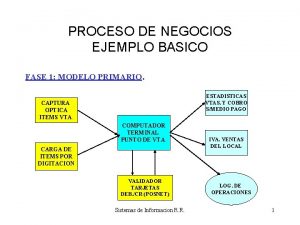
Una compañia fabrica y venden dos modelos de lampara Modelos de negocios ejemplos
Modelos de negocios ejemplos Atmico
Atmico Modelos eruditos
Modelos eruditos Modelos de registros
Modelos de registros Ejemplos de modelos mentales y formales
Ejemplos de modelos mentales y formales Modelo occidental y oriental
Modelo occidental y oriental Variables exógenas ejemplos
Variables exógenas ejemplos Modelo del diodo
Modelo del diodo Modelos matriciales
Modelos matriciales Algoritmo de euler grafos
Algoritmo de euler grafos Joyce weil y calhoun 2002 modelos de enseñanza
Joyce weil y calhoun 2002 modelos de enseñanza Modelos de desenho de cargos
Modelos de desenho de cargos Bosquejo de una lectura
Bosquejo de una lectura Modelos do
Modelos do Modelos de mintzberg
Modelos de mintzberg Enfoque tradicional características
Enfoque tradicional características Modelo social
Modelo social Modelos de negocios ejemplos
Modelos de negocios ejemplos Cronograma de atividades
Cronograma de atividades Modelos semanticos
Modelos semanticos Modelos de abordaje de la promocion de la salud
Modelos de abordaje de la promocion de la salud