o to cho iu dng BO CO PHN

Đào tạo cho Điều dưỡng BÁO CÁO PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) Người báo cáo: DS. Dương Hà Minh Khuê Tổ Dược Lâm Sàng – Khoa Dược Ngày 11/11/2016 ALLPPT. com _ Free Power. Point Templates, Diagrams and Charts

ADR là gì? Phản ứng có hại của thuốc (ADR): Một phản ứng độc hại, không mong muốn và xuất hiện ở liều thường dùng cho người để phòng bệnh, chẩn đoán hoặc chữa bệnh hoặc làm thay đổi một chức năng sinh lý.

Lợi ích của báo cáo ADR Dùng thuốc trong Thử nghiệm lâm sàng - Số lượng bệnh nhân ít - Thời gian theo dõi ngắn - Đặc điểm BN không phức tạp: suy gan, suy thận, PNCT-CCB… Thông tin hạn chế Phê duyệt Dùng thuốc trong thực tế bệnh nhân - Số lượng BN nhiều - Đặc điểm BN đa dạng Đánh giá một cách toàn diện về nguy cơ/lợi ích của thuốc khi lưu hành
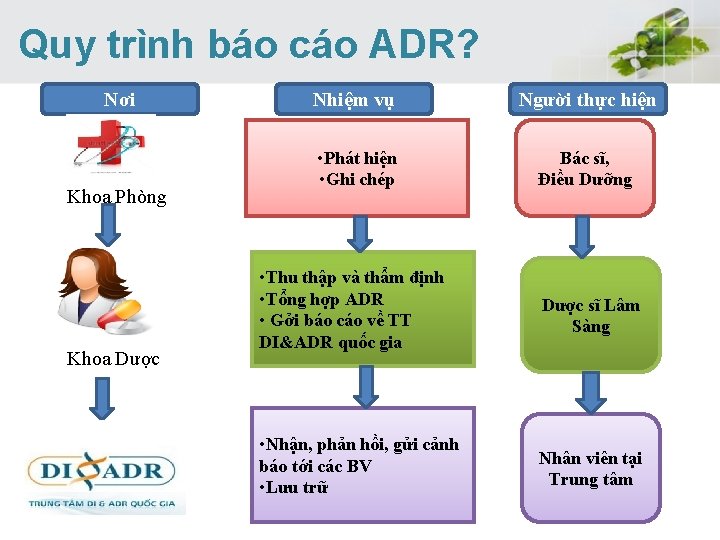
Quy trình báo cáo ADR? Nơi Khoa Phòng Khoa Dược Nhiệm vụ Người thực hiện • Phát hiện • Ghi chép Bác sĩ, Điều Dưỡng • Thu thập và thẩm định • Tổng hợp ADR • Gởi báo cáo về TT DI&ADR quốc gia Dược sĩ Lâm Sàng • Nhận, phản hồi, gửi cảnh báo tới các BV • Lưu trữ Nhân viên tại Trung tâm

Nên theo dõi ADR trên BN nào ? Mắc nhiều bệnh Tiền sử dị ứng Dùng nhiều thuốc và kéo dài Người già và trẻ em Sử dụng thuốc có nguy cơ cao

TẤT CẢ CÁC THUỐC ĐỀU CÓ KHẢ NĂNG G Y RA ADR -Kháng sinh : chiếm hơn 50% (Penicillin, Amoxicillin, Sulfonamid, …) -Thuốc giảm đau (Opiod giảm đau như morphin) -Thuốc an thần (Midazolam, …) -Thuốc điều trị đái tháo đường (Metformin) -Thuốc tác dụng trên hệ tim mạch (Lidocain, amiodaron, . . ) -Dung dịch ưu trương (Na. Cl 10%, Glucose 30%, . . ) -……

Một số thuốc có nguy cơ cao gây ADR Thuốc chủ vận adrenergic, đường tiêm tĩnh mạch (adrenalin, dobutamin, …) Thuốc mê hô hấp và tiêm tĩnh mạch (propofol, ketamin, . . ) Thuốc chống đông Thuốc cản quang (Utravist, Omipaquien, …) Thuốc kháng sinh tiêm (Fizoti, Amflox, . . ) Thuốc an thần đường tiêm (Midazolam)

Một số ca đã báo cáo tại BV • Bệnh nhân P. T. Đ. 2 t hoặc bệnh nhân Trần Thái Thịnh 12 t đều dị ứng với thuốc kháng sinh tiêm • Bệnh nhân N. M. Q. T. vào ngày 1/11/2016 được ghi nhận xuất hiện triệu chứng đỏ quanh mắt, nghẹt mũi, khó thở khi sử dụng Ultravist. Bệnh nhân có tiền sử dị ứng.

Khi nào nên báo cáo ADR ? Thuốc mới Nghiêm trọng ADR mới Xảy ra liên tục
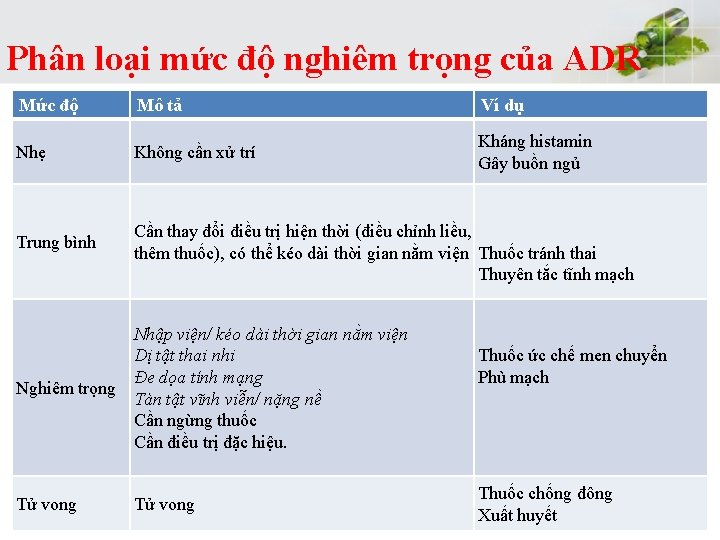
Phân loại mức độ nghiêm trọng của ADR Mức độ Mô tả Ví dụ Nhẹ Không cần xử trí Kháng histamin Gây buồn ngủ Trung bình Cần thay đổi điều trị hiện thời (điều chỉnh liều, thêm thuốc), có thể kéo dài thời gian nằm viện Thuốc tránh thai Thuyên tắc tĩnh mạch Nhập viện/ kéo dài thời gian nằm viện Dị tật thai nhi Đe dọa tính mạng Nghiêm trọng Tàn tật vĩnh viễn/ nặng nề Cần ngừng thuốc Cần điều trị đặc hiệu. Tử vong Thuốc ức chế men chuyển Phù mạch Thuốc chống đông Xuất huyết

Tình huống 1 Ngày 28/10/2016, bệnh nhân nam, 45 tuổi, sau dùng thuốc cản quang Ultravist (Iopromid) thì buồn nôn, mặt đỏ huyết áp thấp, không bắt được mạch. Đe dọa tính mạng Mức độ nghiêm trọng của ADR này: -Nhẹ -Trung bình -Nghiêm trọng -Tử vong

Tình huống 2 Ngày 17/02/2016 bệnh nhân sau khi tiêm Vancomycin thì nổi sưng đỏ quanh vị trí test thuốc với đường kính >5 mm ADR mức độ nhẹ Mức độ nghiêm trọng của ADR này: -Nhẹ -Trung bình -Nghiêm trọng -Tử vong

Báo cáo ADR vào thời điểm nào? Mức độ ADR Thời điểm báo cáo ADR nghiêm trọng Gọi ngay đến Tổ Dược Lâm sàng/Khoa Dược để thu thập thông tin và xử lý kịp thời ADR không nghiêm trọng • CBYT tại Khoa LS điền Mẫu báo cáo ADR + Ghi chép thông tin vào sổ theo dõi ADR của Khoa. • Điều dưỡng nộp báo cáo muộn nhất ngày 5 tháng tiếp theo cho DS. Khuê. Điều dưỡng ghi số ADR và ký tên vào sổ theo dõi ADR của khoa Dược

Hướng dẫn điền form báo cáo ADR

Hướng dẫn điền form báo cáo ADR

Hướng dẫn điền form báo cáo ADR

Nhiệm vụ của khoa Dược Thẩm định ADR Tổng hợp và gửi báo cáo ADR Xử lý ADR nghiêm trọng
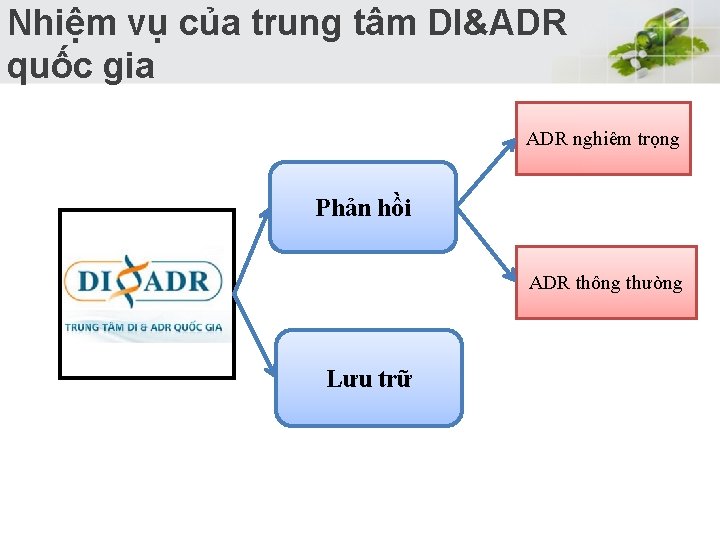
Nhiệm vụ của trung tâm DI&ADR quốc gia ADR nghiêm trọng Phản hồi ADR thông thường Lưu trữ

Tài liệu tham khảo • SOP( Quy trình thao tác chuẩn)- Khoa Dược- Bệnh viện trường Đại học Y Dược Huế • Hướng dẫn báo cáo ADR – Trung tâm thông tin thuốc và ADR quốc gia • Hướng dẫn quốc gia về cảnh giác dược - Bộ Y Tế

- Slides: 20