O Modelo Atmico de Bohr A estrutura do

O Modelo Atômico de Bohr A estrutura do átomo revelada.
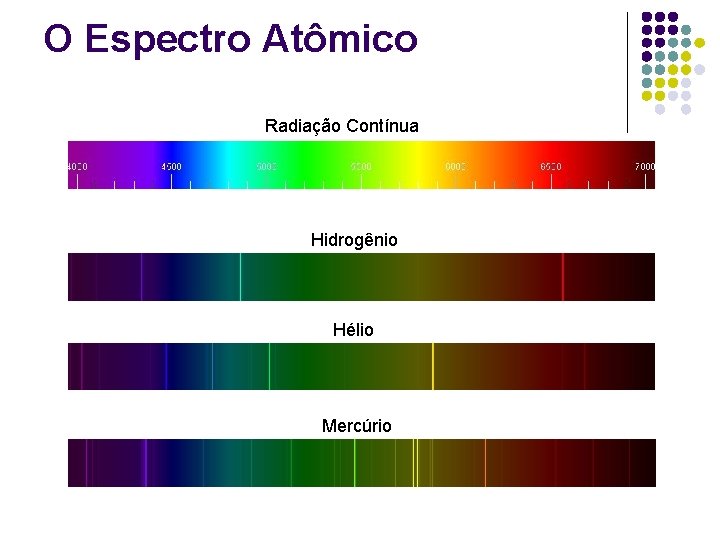
O Espectro Atômico Radiação Contínua Hidrogênio Hélio Mercúrio
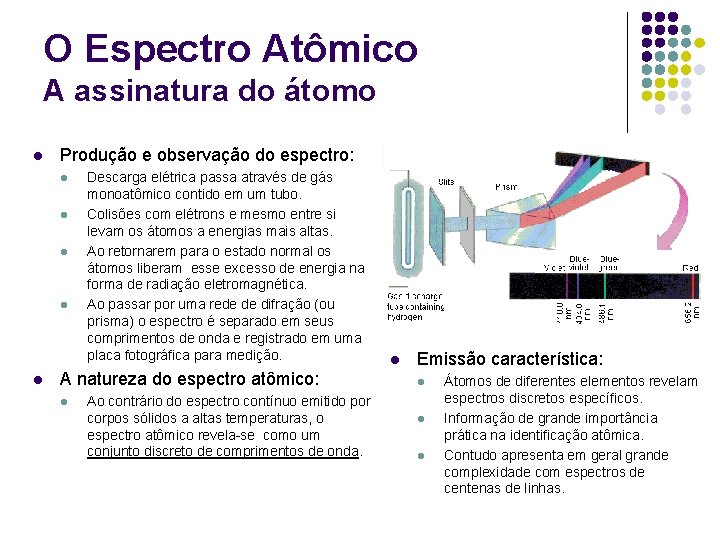
O Espectro Atômico A assinatura do átomo l Produção e observação do espectro: l l l Descarga elétrica passa através de gás monoatômico contido em um tubo. Colisões com elétrons e mesmo entre si levam os átomos a energias mais altas. Ao retornarem para o estado normal os átomos liberam esse excesso de energia na forma de radiação eletromagnética. Ao passar por uma rede de difração (ou prisma) o espectro é separado em seus comprimentos de onda e registrado em uma placa fotográfica para medição. A natureza do espectro atômico: l Ao contrário do espectro contínuo emitido por corpos sólidos a altas temperaturas, o espectro atômico revela-se como um conjunto discreto de comprimentos de onda. l Emissão característica: l l l Átomos de diferentes elementos revelam espectros discretos específicos. Informação de grande importância prática na identificação atômica. Contudo apresenta em geral grande complexidade com espectros de centenas de linhas.
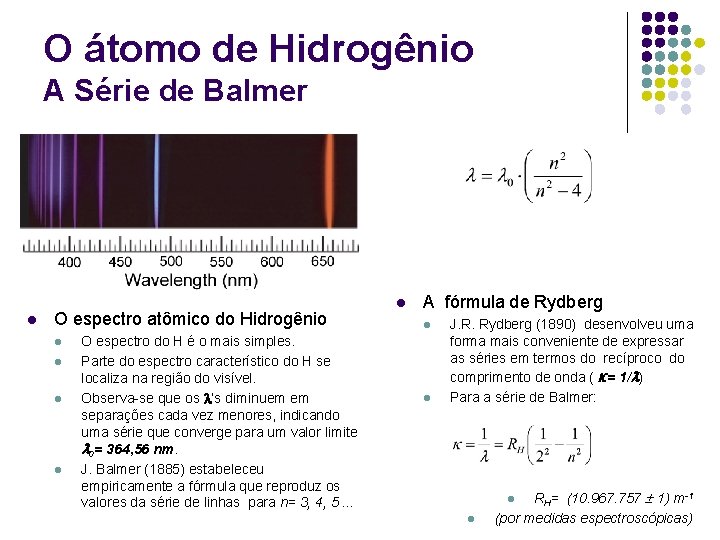
O átomo de Hidrogênio A Série de Balmer l O espectro atômico do Hidrogênio l l O espectro do H é o mais simples. Parte do espectro característico do H se localiza na região do visível. Observa-se que os ’s diminuem em separações cada vez menores, indicando uma série que converge para um valor limite 0= 364, 56 nm. J. Balmer (1885) estabeleceu empiricamente a fórmula que reproduz os valores da série de linhas para n= 3, 4, 5. . . l A fórmula de Rydberg l l J. R. Rydberg (1890) desenvolveu uma forma mais conveniente de expressar as séries em termos do recíproco do comprimento de onda ( = 1/ ) Para a série de Balmer: RH= (10. 967. 757 1) m-1 (por medidas espectroscópicas) l l

O Átomo de Bohr Modelo para o átomo de um elétron l Os postulados de Bohr (1913) 1. 2. 3. 4. O elétron orbita o núcleo em movimento circular sob a ação da força coulombiana conforme as leis da mecânica clássica. Só é possível ao elétron mover-se em órbitas para as quais o seu momento angular seja múltiplo inteiro de ћ (h/2 ). Apesar do elétron estar constantemente acelerado, ele não irradia. energia eletromagnética na órbita permitida. Radiação eletromagnética só é liberada quando o elétron “salta” de forma descontínua de uma órbita com energia Ei para outra com energia Ef, tal que a frequência da radiação emitida é dada por: = (Ei – Ef)/h. l Desenvolvimento do modelo l l l Núcleo: carga +Ze e massa M Elétron: carga –e e massa m (m << M) em órbita circular de raio r. Fc= mv 2/r = (1/4 0). Ze 2/r 2 L= mvr= cte. Quantização: L= n. ћ (n= 1, 2, 3. . . ) l Raio e velocidade das órbitas l Energia total l E= U + K
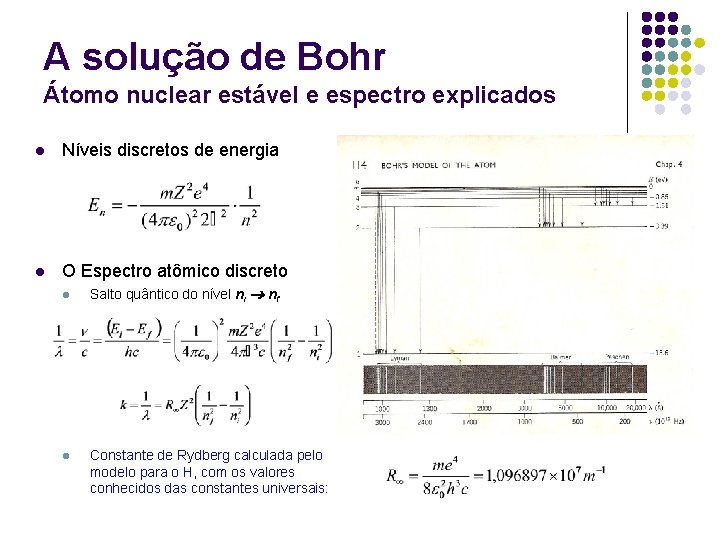
A solução de Bohr Átomo nuclear estável e espectro explicados l Níveis discretos de energia l O Espectro atômico discreto l l Salto quântico do nível ni nf Constante de Rydberg calculada pelo modelo para o H, com os valores conhecidos das constantes universais:
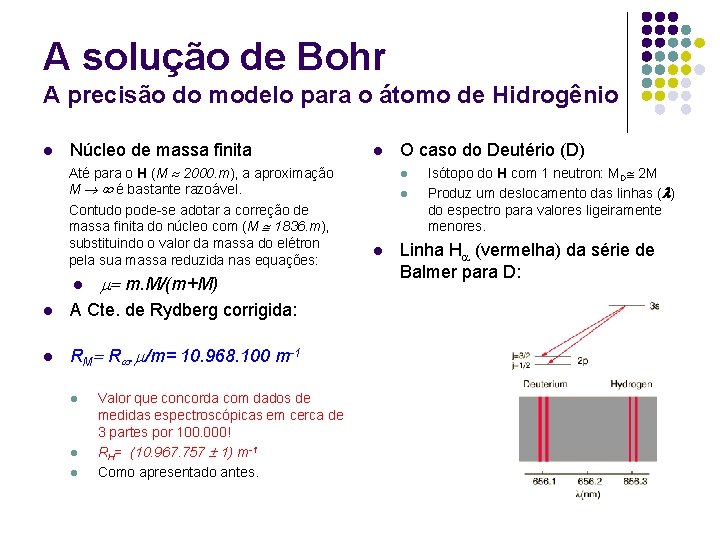
A solução de Bohr A precisão do modelo para o átomo de Hidrogênio l Núcleo de massa finita Até para o H (M 2000. m), a aproximação M é bastante razoável. Contudo pode-se adotar a correção de massa finita do núcleo com (M 1836. m), substituindo o valor da massa do elétron pela sua massa reduzida nas equações: l m. M/(m+M) l A Cte. de Rydberg corrigida: l RM R. /m= 10. 968. 100 m-1 l l l Valor que concorda com dados de medidas espectroscópicas em cerca de 3 partes por 100. 000! RH= (10. 967. 757 1) m-1 Como apresentado antes. l O caso do Deutério (D) l l l Isótopo do H com 1 neutron: MD 2 M Produz um deslocamento das linhas ( ) do espectro para valores ligeiramente menores. Linha H (vermelha) da série de Balmer para D:
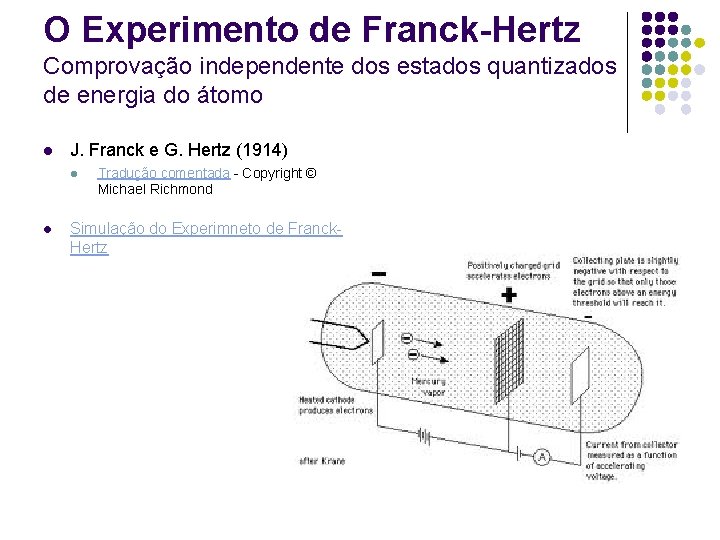
O Experimento de Franck-Hertz Comprovação independente dos estados quantizados de energia do átomo l J. Franck e G. Hertz (1914) l l Tradução comentada - Copyright © Michael Richmond Simulação do Experimneto de Franck. Hertz
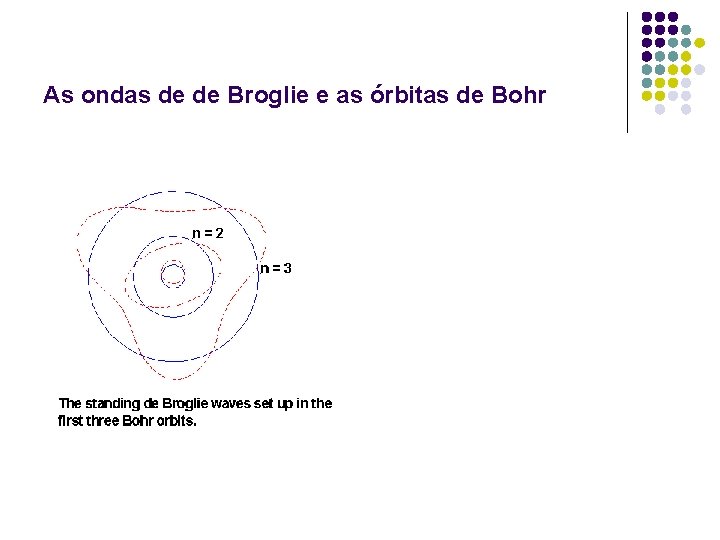
As ondas de de Broglie e as órbitas de Bohr
- Slides: 9