Nzev S Autoi SCOPT Uhersk Brod Ing Edita

Název SŠ: Autoři: SŠ-COPT Uherský Brod Ing. Edita NAĎOVÁ Název prezentace 10. Test z anorganické chemie Název sady: Obecná a anorganická chemie (pro 3. ročník oboru Mechanik seřizovač a Technik - puškař) CZ. 1. 07. /1. 5. 00/34. 0727 16. 12. 2012 Číslo projektu: Datum vzniku: Uvedení autoři, není-li uvedeno jinak, jsou autory tohoto výukového materiálu a všech jeho částí. Tento projekt je spolufinancován ESF a státním rozpočtem ČR

ANOTACE: Záměrem této sady výukových materiálů Obecná a anorganická chemie (pro 3. ročník oboru Mechanik seřizovač a Technik - puškař) je představit žákům, kteří se v této oblasti vzdělávají, obecnou a anorganickou chemii. Jednotlivé prezentace v této sadě popíší postupně tematické oblasti, které jsou probírány v běžné výuce chemie na naší SŠ. Konkrétně tato prezentace je zaměřena na test z anorganické chemie.

1. Vypočítej hmotnostní zlomek v oxidu železitém Fe 2 O 3. Kolik % železa obsahuje Fe 2 O 3? 2. 30 g Na. Cl je rozpuštěno ve 220 cm 3 H 2 O. Kolika % bude roztok?
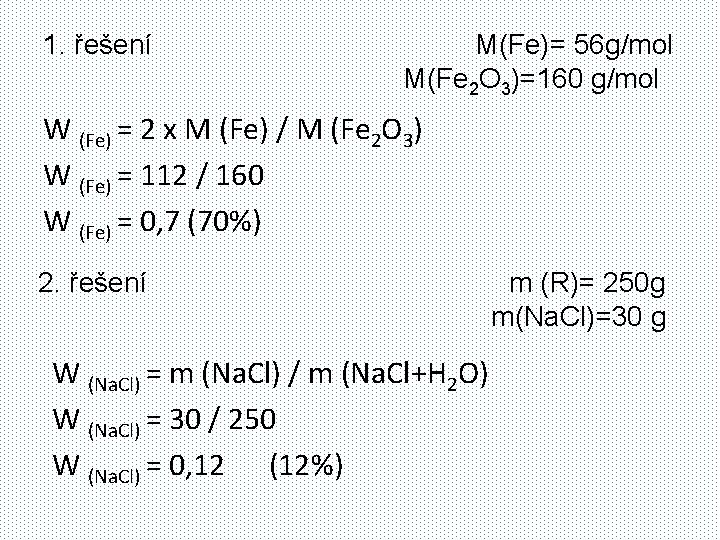
1. řešení M(Fe)= 56 g/mol M(Fe 2 O 3)=160 g/mol W (Fe) = 2 x M (Fe) / M (Fe 2 O 3) W (Fe) = 112 / 160 W (Fe) = 0, 7 (70%) 2. řešení W (Na. Cl) = m (Na. Cl) / m (Na. Cl+H 2 O) W (Na. Cl) = 30 / 250 W (Na. Cl) = 0, 12 (12%) m (R)= 250 g m(Na. Cl)=30 g

3. Vypočítejte, kolik tun vápence s 10, 7% nečistot je třeba vypálit, abychom získali 10 t páleného vápna. Napište chemickou rovnici.

3. řešení Ca. CO 3 -----> Ca. O +CO 2 ze 100 t………. 56 t z x t ……………. 10 t x/100 = 10/ 56 vápence 17, 85 t ………. 100% y t ……………… (100 -10, 7) % y/17, 85 = 100/89, 3 y = 17, 85 x 100/89, 3 x = 17, 85 t 100 % y= 19, 98 t Je třeba vypálit přibližně 20 t vápence

4. Kousek mince, který má hmotnost 0, 3 g, se rozpustí ve zředěné kyselině dusičné. K získanému roztoku sloučeniny Ag se přidá kyselina chlorovodíková. Vznikne bílá tvarohovitá sraženina, která se filtruje, promyje vodou, vysuší a zváží. Hmotnost sraženiny je 0, 199 g. Sestavte příslušné rovnice a vypočtěte, kolik % Ag obsahuje mince, jestliže znáte obsah stříbra v 1 molu sraženiny.
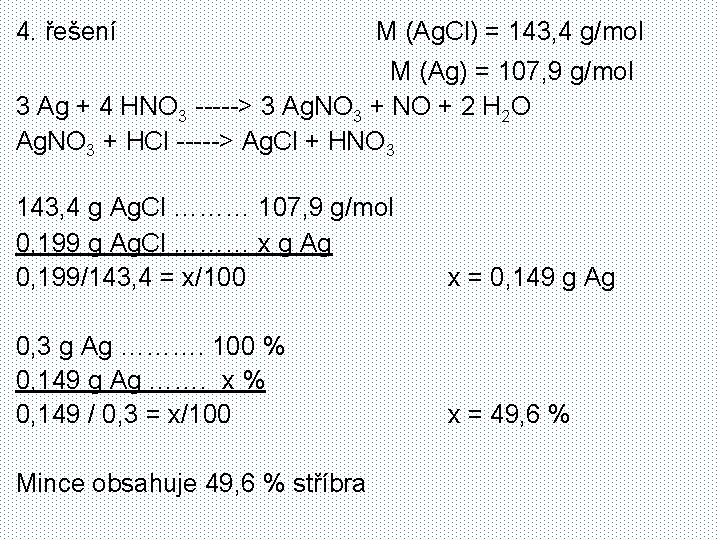
4. řešení M (Ag. Cl) = 143, 4 g/mol M (Ag) = 107, 9 g/mol 3 Ag + 4 HNO 3 -----> 3 Ag. NO 3 + NO + 2 H 2 O Ag. NO 3 + HCl -----> Ag. Cl + HNO 3 143, 4 g Ag. Cl ……… 107, 9 g/mol 0, 199 g Ag. Cl ……… x g Ag 0, 199/143, 4 = x/100 x = 0, 149 g Ag 0, 3 g Ag ………. 100 % 0, 149 g Ag ……. x % 0, 149 / 0, 3 = x/100 x = 49, 6 % Mince obsahuje 49, 6 % stříbra

Napiš, vyčísli a urči typ chemické reakce • kyselina sírová + hydroxid hlinitý -----> síran hlinitý + voda • kyselina dusitá + hydroxid vápenatý -----> dusitan vápenatý + voda • měď+ kyselina sírová -----> síran mědnatý + oxid siřičitý + voda • sulfid stříbrný + kyselina dusičná -----> dusičnan stříbrný + síra + oxid dusičitý + voda • jodid draselný + chlorid barnatý -----> chlorid draselný + jodid barnatý
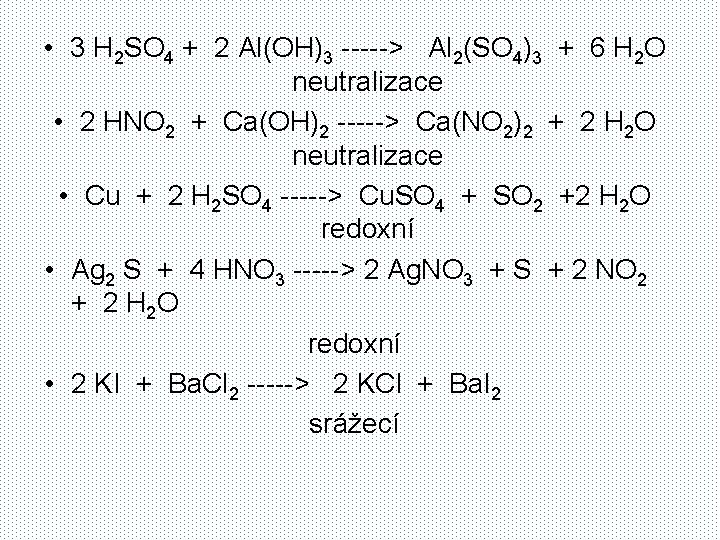
• 3 H 2 SO 4 + 2 Al(OH)3 -----> Al 2(SO 4)3 + 6 H 2 O neutralizace • 2 HNO 2 + Ca(OH)2 -----> Ca(NO 2)2 + 2 H 2 O neutralizace • Cu + 2 H 2 SO 4 -----> Cu. SO 4 + SO 2 +2 H 2 O redoxní • Ag 2 S + 4 HNO 3 -----> 2 Ag. NO 3 + S + 2 NO 2 + 2 H 2 O redoxní • 2 KI + Ba. Cl 2 -----> 2 KCl + Ba. I 2 srážecí

Vazby • 1 urči typy chemických vazeb, charakterizuj • 2 co je elektronegativita, jak ji označujeme • 3 urči typ vazby na základě rozdílu elektronegativit ve sloučenině : Na. Cl O 2 HCl

Redoxní děje • oxidace je děj, při kterém dochází: a) k zvětšování oxidačního čísla b) ke zmenšování oxidačního čísla c) k přijímání elektronů • redukce je děj, při kterém dochází: a) ke zvětšování oxidačního čísla b) ke zmenšování oxidačního čísla c) k předávání elektronů

Zdroje pro textovou část • KLIKORKA, J. , HÁJEK, B. , VOTINSKÝ, J. , Obecná a anorganická chemie, SNTL/ALFA, Praha: 1985 • KOTLÍK, B. , RŮŽIČKOVÁ, K. , Chemie I v kostce, Fragment, Havlíčkův Brod: 1996: ISBN 80 -7200056 -X • Fabini, J. , Šteplová, D. , Sokolík, R. , Anorganická chémia, SPN, Bratislava: 1969
- Slides: 13