NZEV KOLY Zkladn kola T G Masaryka Bojkovice

NÁZEV ŠKOLY: Základní škola T. G. Masaryka, Bojkovice, okres Uherské Hradiště AUTOR: Jitka Malíčková NÁZEV: Kyslíkaté kyseliny II TÉMATICKÝ CELEK: Anorganické sloučeniny ČÍSLO PROJEKTU: CZ. 1. 07/1. 4. 00/21. 0882

Kyslíkaté kyseliny II
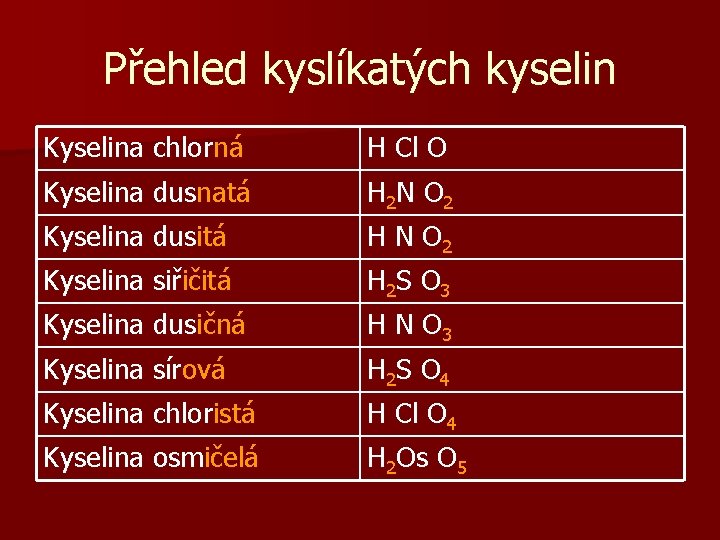
Přehled kyslíkatých kyselin Kyselina chlorná H Cl O Kyselina dusnatá H 2 N O 2 Kyselina dusitá H N O 2 Kyselina siřičitá H 2 S O 3 Kyselina dusičná H N O 3 Kyselina sírová H 2 S O 4 Kyselina chloristá H Cl O 4 Kyselina osmičelá H 2 Os O 5

Tvorba názvu ze vzorce n Kyseliny s jedním vodíkem mají lichou koncovku. n Kyseliny se dvěma vodíky mají sudou koncovku. n Součet všech oxidačních čísel je roven nule! n Je důležité dopočítat oxidační číslo určujícího prvku.

Tvorba názvu ze vzorce +I ? - II HMn. O 4 + I + VII - II HMn. O 4 n n kyselina manganistá n doplníme oxidační čísla vodíku a kyslíku dopočítáme oxidační číslo určujícího prvku +I +? +4. (-II) = 0 ? = VII kyselina má 1 vodík, koncovka je lichá –istá vytvoříme název

Tvorba názvu ze vzorce + IV - II H 2 SO 3 2. I + ? + 3. (-II) = 0 +IV kyselina siřičitá

Procvičuj H 2 Te. O 4 Kyselina telurová HBr. O 4 Kyselina bromistá H 2 Cl. O 2 Kyselina chlornatá H 2 Os. O 5 Kyselina osmičelá HCl. O 3 Kyselina chlorečná HPO 2 Kyselina fosforitá H 2 CO 3 Kyselina uhličitá HNO Kyselina dusná

Otázka Mohou mít kyseliny i vyšší počet vodíků, než jen dva?

Odpověď Např. H 3 PO 4 kyselina trihydrogenfosforečná = kyselina fosforečná

Zdroj Obrázky: http: //commons. wikimedia. org/wiki/File: Indikator-Blaukraut. JPG www. office. microsoft. com
- Slides: 10