NZEV KOLY Zkladn kola T G Masaryka Bojkovice

NÁZEV ŠKOLY: Základní škola T. G. Masaryka, Bojkovice, okres Uherské Hradiště AUTOR: Jitka Malíčková NÁZEV: Vlastnosti oxidů TÉMATICKÝ CELEK: Anorganické sloučeniny ČÍSLO PROJEKTU: CZ. 1. 07/1. 4. 00/21. 0882
Vlastnosti oxidů
Oxidy jsou dvouprvkové sloučeniny kyslíku s dalším prvkem. Podle toho, jak probíhá reakce oxidu s vodou, je rozdělujeme do tří skupin: oxidy kyselinotvorné zásadotvorné amfoterní
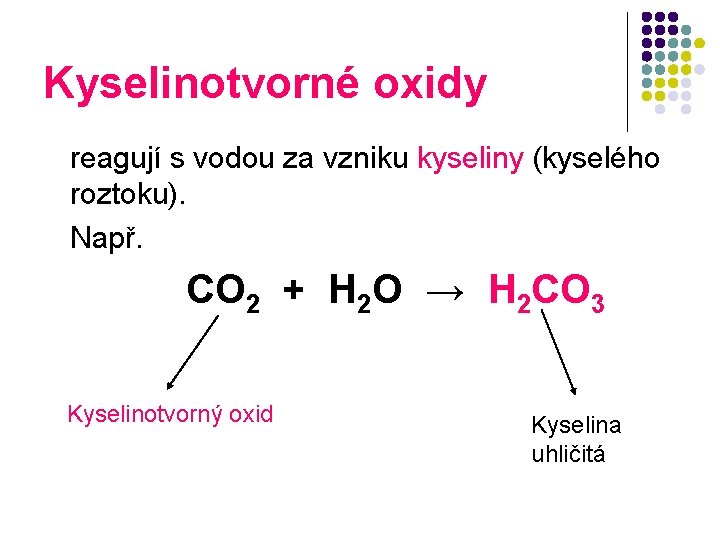
Kyselinotvorné oxidy reagují s vodou za vzniku kyseliny (kyselého roztoku). Např. CO 2 + H 2 O → H 2 CO 3 Kyselinotvorný oxid Kyselina uhličitá
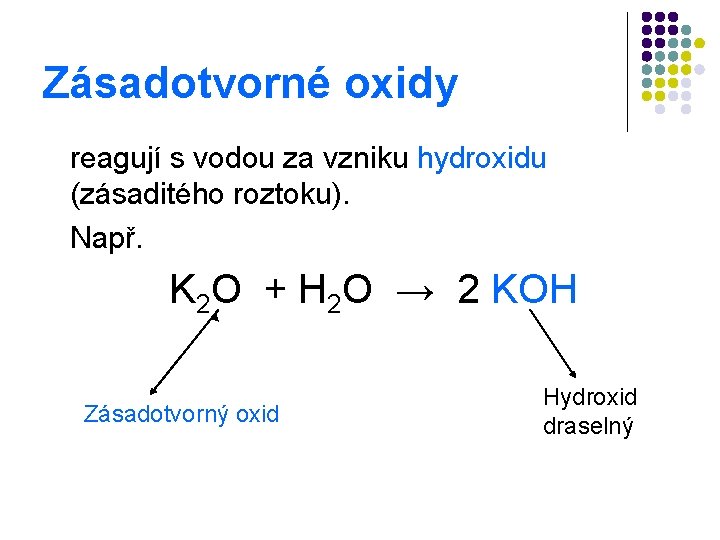
Zásadotvorné oxidy reagují s vodou za vzniku hydroxidu (zásaditého roztoku). Např. K 2 O + H 2 O → 2 KOH Zásadotvorný oxid Hydroxid draselný
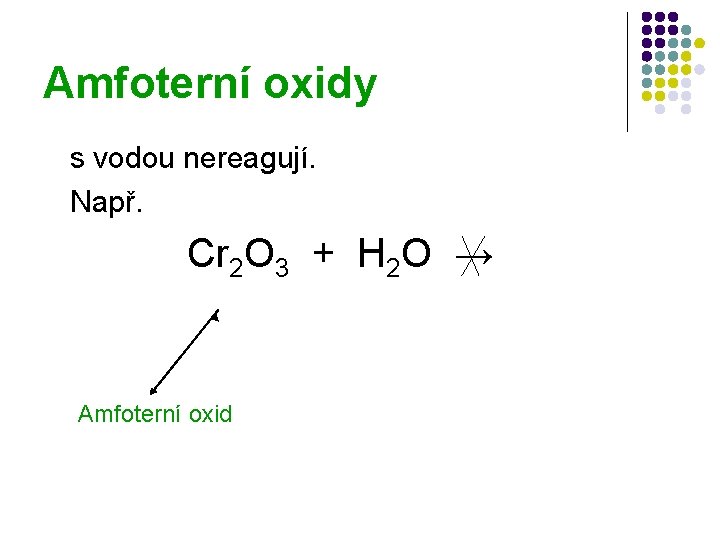
Amfoterní oxidy s vodou nereagují. Např. Cr 2 O 3 + H 2 O → Amfoterní oxid

Jak rozeznat oxidy? Určit, do které skupiny oxid náleží, lze i bez pokusu. Stačí v periodické tabulce vyhledat hodnotu relativní elektronegativity prvku, který tvoří s kyslíkem zadaný oxid. Např. CO 2 C má elektronegativitu 2, 5 E=2, 5

Jak rozeznat oxidy? Je-li E ≤ 1, je oxid zásadotvorný. K 2 O E(K)= 0, 91 Je-li 1< E ≤ 2, je oxid amfoterní. Cr 2 O 3 E(Cr)= 1, 56 Je-li E > 2, je oxid kyselinotvorný. CO 2 E(C)= 2, 5
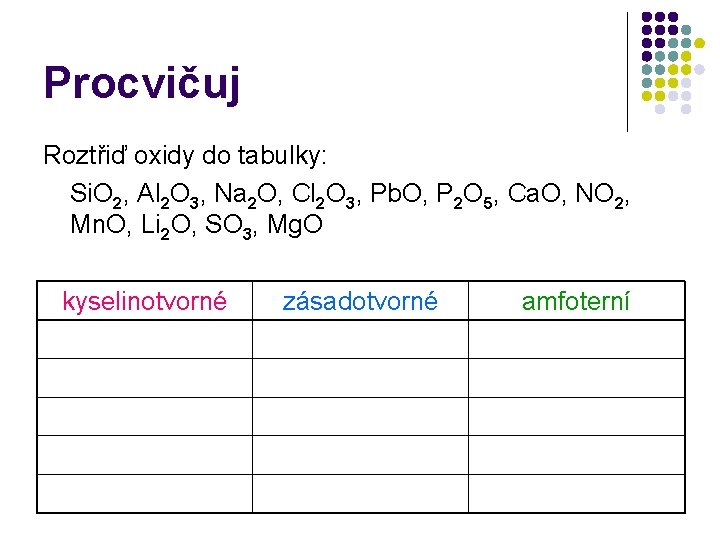
Procvičuj Roztřiď oxidy do tabulky: Si. O 2, Al 2 O 3, Na 2 O, Cl 2 O 3, Pb. O, P 2 O 5, Ca. O, NO 2, Mn. O, Li 2 O, SO 3, Mg. O kyselinotvorné zásadotvorné amfoterní
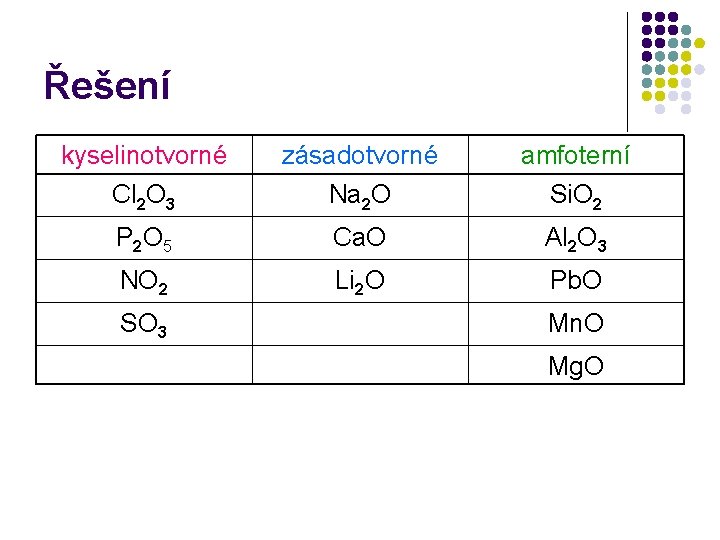
Řešení kyselinotvorné Cl 2 O 3 zásadotvorné Na 2 O amfoterní Si. O 2 P 2 O 5 Ca. O Al 2 O 3 NO 2 Li 2 O Pb. O SO 3 Mn. O Mg. O

Doplň rovnice: Vznik kyselých dešťů: SO 2 + H 2 O → Hašení páleného vápna: Ca. O + H 2 O →
Zdroj Beneš, Banýr, Pumpr: Základy chemie I www. office. microsoft. com Vypracovala: Jitka Malíčková
- Slides: 12