Nzev koly Zkladn kola Mstec Krlov Autor Ing



![Palivo Výhřevnost Vodík Methan Ethan Propan Butan [k. J/kg] 119 550 50 009 47 Palivo Výhřevnost Vodík Methan Ethan Propan Butan [k. J/kg] 119 550 50 009 47](https://slidetodoc.com/presentation_image/5301cc6902bbe3dde7487ea4307493e1/image-4.jpg)



![Zdroje Obrázky: [cit. 2012 -1 -22] dostupné pod licencí Creative Commons na: • • Zdroje Obrázky: [cit. 2012 -1 -22] dostupné pod licencí Creative Commons na: • •](https://slidetodoc.com/presentation_image/5301cc6902bbe3dde7487ea4307493e1/image-10.jpg)
- Slides: 10

Název školy: Základní škola Městec Králové Autor: Ing. Hana Zmrhalová Název: VY_32_INOVACE_06_CH 9 Číslo projektu: CZ. 1. 07/1. 4. 00/21. 2313 Téma: Anotace: PALIVA Prezentace, která slouží k vysvětlení pojmu paliva, rozdělení paliv, využití chem. reakcí jako zdroje tepla. Datum: 23. 1. 2012

Paliva • palivo je označení pro chemický prvek, chemickou látku nebo jejich směs, mající schopnost za vhodných podmínek začít a udržet chemickou reakci spalování • při spalovaní se uvolňuje energie obsažená v palivu a přeměňuje se hlavně na tepelnou energii Požadavky na paliva: – – malé náklady na těžbu, dopravu a skladování dobrá zápalnost dobrá výhřevnost malý obsah škodlivých látek CHEMIE 9. ročník ZŠ MĚSTEC KRÁLOVÉ PALIVA

Dělení paliv dle: 1) Skupenství • plynná paliva: například vodík, zemní plyn, bioplyn • kapalná paliva: například benzín, motorová nafta, petrolej, benzen, alkoholy, topný olej, mazut • pevná paliva: například uhlí, koks, brikety, dřevo 2) původu • přírodní – uhlí • vyrobená – propan-butan 3) období vzniku • fosilní – ropa, uhlí, zemní plyn • současná (recentní) - dřevo CHEMIE 9. ročník ZŠ MĚSTEC KRÁLOVÉ PALIVA
![Palivo Výhřevnost Vodík Methan Ethan Propan Butan k Jkg 119 550 50 009 47 Palivo Výhřevnost Vodík Methan Ethan Propan Butan [k. J/kg] 119 550 50 009 47](https://slidetodoc.com/presentation_image/5301cc6902bbe3dde7487ea4307493e1/image-4.jpg)
Palivo Výhřevnost Vodík Methan Ethan Propan Butan [k. J/kg] 119 550 50 009 47 794 46 357 45 752 [k. J/m³] (20°C) 10 748 (g) 33 806 (g) 61 272 (g) 88 540 (g) 114 840 (g) Ethanol 28 865 22 774 (l) Dřevo 16 000 10 000 - 17 000 21 000 - 31 000 30000 Hnědé uhlí Černé uhlí Koks CHEMIE 9. ročník ZŠ MĚSTEC KRÁLOVÉ PALIVA

TEPLO A CHEMICKÁ REAKCE Reakce, při kterých se uvolňuje teplo, Q < 0 m nazýváme exotermické reakce. Reakce, při kterých se teplo spotřebovává, nazýváme endotermické reakce. Q > 0 m Molární teplo reakce = teplo, které se uvolní (nebo spotřebuje) při reakci takových látkových množství výchozích látek, která udávají stechiometrické koeficienty v chemické rovnici. značka: Qm jednotka: k. J/mol CHEMIE 9. ročník ZŠ MĚSTEC KRÁLOVÉ PALIVA

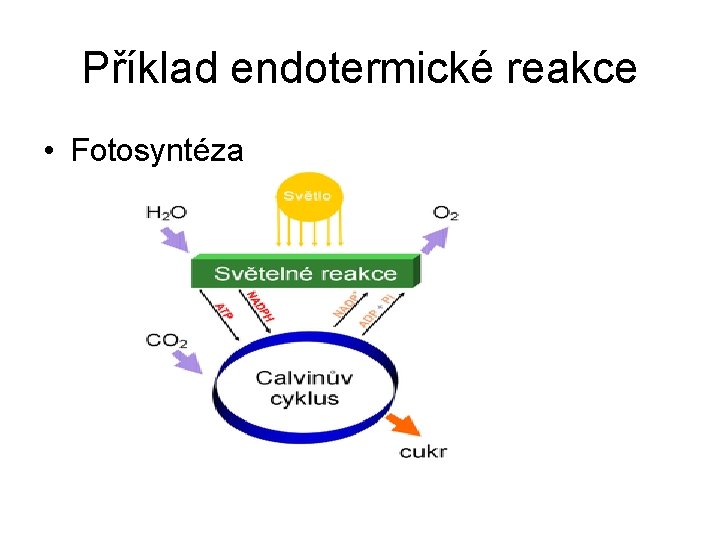
Příklad endotermické reakce • Fotosyntéza

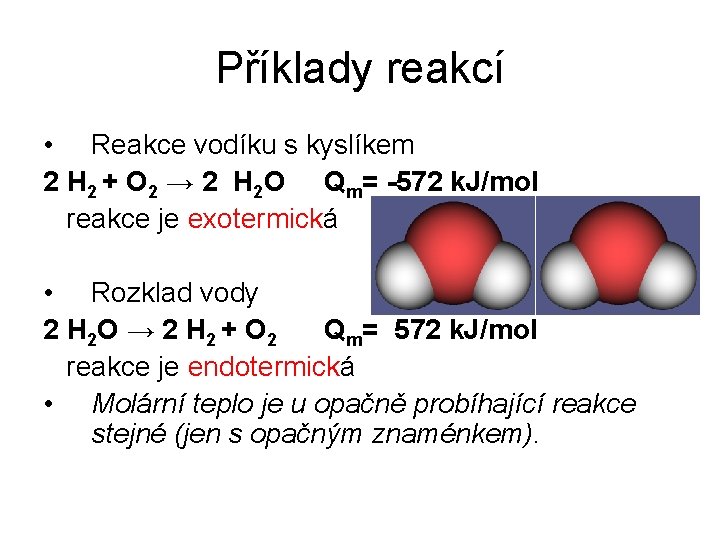
Příklady reakcí • Reakce vodíku s kyslíkem 2 H 2 + O 2 → 2 H 2 O Qm= -572 k. J/mol reakce je exotermická • Rozklad vody 2 H 2 O → 2 H 2 + O 2 Qm= 572 k. J/mol reakce je endotermická • Molární teplo je u opačně probíhající reakce stejné (jen s opačným znaménkem).

Procvičování • Která paliva lze zařadit mezi ekologická, jaké jsou produkty jejich spalování, jaké jsou jejich nevýhody? • Která paliva nadměrně znečišťují životní prostředí? • Jak se nazývají reakce, při kterých je třeba dodávat energii? • Jak se nazývají reakce, při kterých se reakce uvolňuje?

Řešení • 1) Ekologická paliva: • Vodík: 2 H 2 + O 2 → 2 H 2 O nevýhody: vysoká cena, výbušnost • Methan, propan, butan Produkty spalování: CO 2 + H 2 O nevýhody: výbušnost • 2) Uhlí, benzín, motorová nafta, topné oleje • Otázka 3 a 4 odpověď
![Zdroje Obrázky cit 2012 1 22 dostupné pod licencí Creative Commons na Zdroje Obrázky: [cit. 2012 -1 -22] dostupné pod licencí Creative Commons na: • •](https://slidetodoc.com/presentation_image/5301cc6902bbe3dde7487ea4307493e1/image-10.jpg)
Zdroje Obrázky: [cit. 2012 -1 -22] dostupné pod licencí Creative Commons na: • • http: //en. wikipedia. org/wiki/File: Fire. JPG http: //cs. wikipedia. org/wiki/V%C 3%BDh%C 5%99 evnost http: //cs. wikipedia. org/wiki/Soubor: Simple_photosynthesis_overview_cs. png http: //cs. wikipedia. org/wiki/Soubor: H 2 O_(water_molecule). jpg