NZEV KOLY Z J E Purkyn Libochovice AUTOR

NÁZEV ŠKOLY: ZŠ J. E. Purkyně Libochovice AUTOR: RNDr. Adéla Lipšová NÁZEV: VY_52_INOVACE_11_REDOXNÍ REAKCE TÉMA: REDOXNÍ REAKCE ČÍSLO PROJEKTU: CZ. 1. 07/1. 4. 00/21. 2803

Anotace Jedná se o výukové materiály určené pro podporu vzdělávání v oblasti přírodních věd – konkrétně chemie. Obsahem je prezentace pro podporu výkladu učiva na dané téma, doplněné řadou zajímavých experimentů, které je nutno provádět pod dohledem vyučujícího. Na začátku je uveden souhrn opakování látky předchozí a na konci souhrn látky probrané. Text je určen pro žáky 9. tříd základních škol.

Chemické reakce a děje 7. část Redoxní děje (oxidačně-redukční reakce)

Opakování – rychlost chem. reakce Rychlost chemické reakce lze zvýšit: - zvýšením koncentrace reaktantů zvýšením teploty reakční směsi zvýšením plošného obsahu povrchu reaktantů přítomnost katalyzátoru mícháním
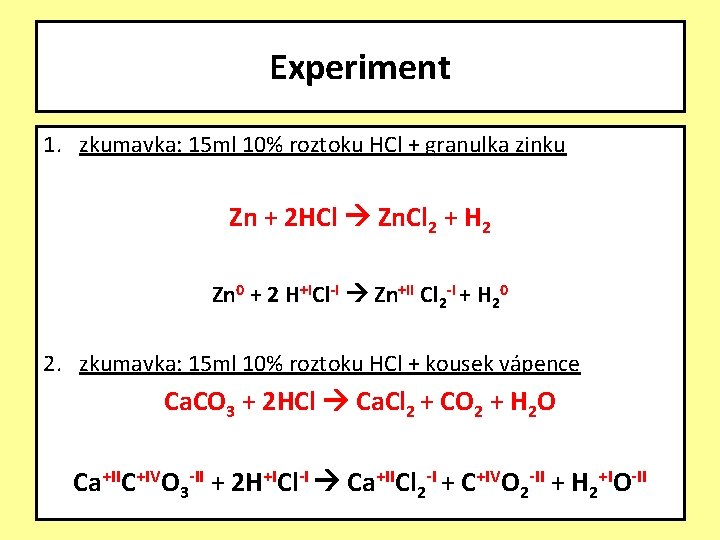
Experiment 1. zkumavka: 15 ml 10% roztoku HCl + granulka zinku Zn + 2 HCl Zn. Cl 2 + H 2 Zn 0 + 2 H+ICl-I Zn+II Cl 2 -I + H 20 2. zkumavka: 15 ml 10% roztoku HCl + kousek vápence Ca. CO 3 + 2 HCl Ca. Cl 2 + CO 2 + H 2 O Ca+IIC+IVO 3 -II + 2 H+ICl-I Ca+IICl 2 -I + C+IVO 2 -II + H 2+IO-II

Oxidační číslo Co je to oxidační číslo prvku? - hodnota náboje prvku ve sloučenině (součet kladných a záporných nábojů) - uvádí se u značky prvku vpravo nahoře římskou číslicí - má hodnotu kladnou (Na+), zápornou (Cl-) a nebo rovnou nule (Zn 0)

Redoxní (oxidačně-redukční) reakce - chemické reakce, při kt. dochází ke změně oxidačních čísel atomů, - změna oxidačních čísel atomů některých prvků je doprovázena např. změnou barvy

Experiment Změna barvy v souvislosti se změnou oxidačního čísla prvku Postup: Zkumavka: 20 ml 10% roztoku dichromanu draselného + 10 ml 20% roztoku HCl + malá lžička granulek zinku Jak se změnila barva?

Experiment - výsledek

Experiment Reakce železa s modrou skalicí Postup: Zkumavka: - 15 ml 5% roztoku Cu. SO 4 - poté do roztoku vložíme čistý železný hřebík (šroub) Co se stalo? - po čase lze pozorovat, že se na povrchu železného hřebíku vytváří vrstvička mědi a původně modrý roztok modré skalice se postupně odbarvuje

Experiment - výsledek

Redoxní (oxidačně-redukční) reakce U redoxních děju probíhá oxidace a redukce současně: 1. děj, při kterém dochází ke snižování oxidačního čísla atomu prvku, nazýváme redukce, elektrony se přijímají 2. děj, při kterém dochází ke zvyšování oxidačního čísla atomu prvku, nazýváme oxidace, elektrony se odevzdávají

Redoxní (oxidačně-redukční) reakce - mezi redoxní děje patří celá řada chemických reakcí, např. hoření (Fe + O 2 2 Fe. O) - dalším důležitým redoxním dějem jsou např. fotosyntéza a dýchání (změna oxidačních čísel prvků, přenos elektronů)

Souhrn - redoxní děje – probíhá u nich oxidace a redukce současně - dochází ke změně oxidačních čísel atomů prvků - oxidace: zvyšování oxidačního čísla, elektrony se odevzdávají Fe 0 Fe+II - redukce: snižování oxidačního čísla, elektrony se přijímají Cu+II Cu 0

Použité zdroje Použity obrázky vlastní tvorby.
- Slides: 15