NZEV KOLY Z J E Purkyn Libochovice AUTOR

NÁZEV ŠKOLY: ZŠ J. E. Purkyně Libochovice AUTOR: RNDr. Adéla Lipšová NÁZEV: VY_52_INOVACE_02_OPAKOVÁNÍ ZNALOSTÍ 8. TŘÍDY (2. ČÁST) TÉMA: OPAKOVÁNÍ ZNALOSTÍ 8. TŘÍDY (2. ČÁST) ČÍSLO PROJEKTU: CZ. 1. 07/1. 4. 00/21. 2803

Anotace Jedná se o výukové materiály určené pro podporu vzdělávání v oblasti přírodních věd – konkrétně chemie. Obsahem jsou otázky, pro zopakování znalostí z 8. třídy základní školy. Každá otázka má vypracovanou odpověď. Text je určen pro žáky 9. tříd základních škol.

Chemie pro 9. třídu ZŠ

Opakování znalostí 8. třídy – 2. část 16. Co víte o nekovech? - jsou prvky plynného, kapalného i pevného skupenství - jsou křehké, nevedou teplo ani el. proud - přechod mezi nimi tvoří polokovy, kt. vzhledem připomínají kovy, ale vlastnostmi se spíše podobají nekovům Patří sem např. C, N 2, P, O 2, S, halogeny a vzácné plyny a samozřejmě i H 2.

17. Co to jsou halogenidy? - jsou to sloučeniny halogenů s jinými prvky, nejčastěji s kovy jsou dvouprvkové oxidační číslo mají –I patří sem fluorid, chlorid, bromid a jodid

18. Co to jsou sulfidy? - dvouprvkové sloučeniny, kt. obsahují síru - oxidační číslo mají –II Pb. S – galenit Zn. S – sfalerit Fe. S -pyrit

19. Co to jsou oxidy? - Opět dvouprvkové sloučeniny - Oxidační číslo mají –II - Jsou to nejčetnější sloučeniny – CO, CO 2, Fe 2 O 3, Al 2 O 3

20. Co to jsou bezkyslíkaté kyseliny? - Dvouprvkové sloučeniny, kt. neobsahují kyslík - Obsahují pouze vodík a halový prvek (tedy chlor, fluor, brom a jod) - HCl - sůl je chlorid Cl. HBr – bromid Br. HI – jodid IHF – fluorid F-

21. Co to jsou kyslíkaté kyseliny? - Jsou tříprvkové sloučeniny - Obsahují vodík, kyslík a kyselinotvorný prvek, kt. je vždy uprostřed vzorce - Dle kyselinotvorného prvku určujeme danou kyselinu - Jsou to l. , kt. ve vodě odštěpují kation vodíku a anion zbytku kyseliny - Jsou to žíraviny a leptají pokožku - Kys. sírová, sůl je síran a oxidační stupeň –II (SO 4 -II) Kyselina siřičitá Kys. křemičitá Kys. uhličitá Kys. dusičná

22. Co to jsou hydroxidy - tříprvkové sloučeniny - ve své molekule obsahují hydroxidový anion (OH-) - váže se na kation kovu - jsou to žíraviny - oxidační číslo hydroxylové skupiny je –I Příklady: - Na. OH - KOH - Ca(OH)2

23. Voda (chemický vzorec, teplota varu, skupenství) - H 2 O - Teplota varu je 100°C (při normálním tlaku okolí) - Voda se vyskytuje ve všech tří skupenství: kapalné – voda pevné – led plynné - pára

24. Co je to neutralizace? Uveď příklad této reakce. - reakce mezi kyselinou a zásadou (hydroxidem) - vzniká při ní voda a sůl Na. OH + H 2 SO 4 Na 2 SO 4 + H 2 O Neutralizace se využívá při bezpečnosti práce: - při polití kyselinou postižené místo opláchneme proudem studené vody a poté nalijeme zředěnou zásadu (nebo mýdlo) - při polití zásadou postižené místo opláchneme proudem studené vody a poté použijeme zředěnou kyselinu (např. ocet) - při zasažení oči pouze vypláchneme proudem vody a ihned vyhledáme lékaře!

25. Pojmenuj Fe. S - sulfid železnatý Na 2 S - sulfid sodný Pb. S - sulfid olovnatý Si. Cl 4 - chlorid křemičitý Ca. O - oxid vápenatý PCl 5 - chlorid fosforečný

26. Pojmenuj Al. Cl 3 - chlorid hlinitý NO 2 - oxid dusičitý Cl 2 O - oxid chlorný I 2 O 5 - oxid jodičný Au 2 O 3 - oxid zlatitý Os. O 4 - oxid osmičelý

27. Pojmenuj prvky Fe - železo N 2 - dusík Ag - stříbro Li - lithium S - síra I 2 - jod

28. Pojmenuj Br 2 - brom P - fosfor C - uhlík Ca - vápník Os - osmium Hg - rtuť
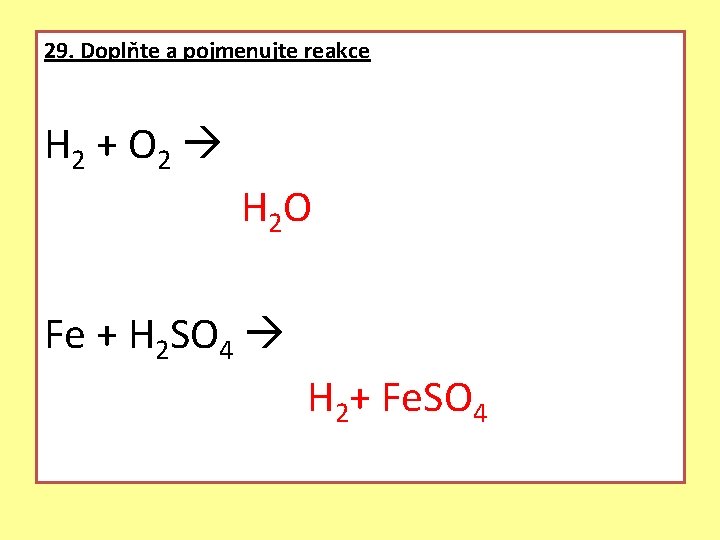
29. Doplňte a pojmenujte reakce H 2 + O 2 H 2 O Fe + H 2 SO 4 H 2+ Fe. SO 4
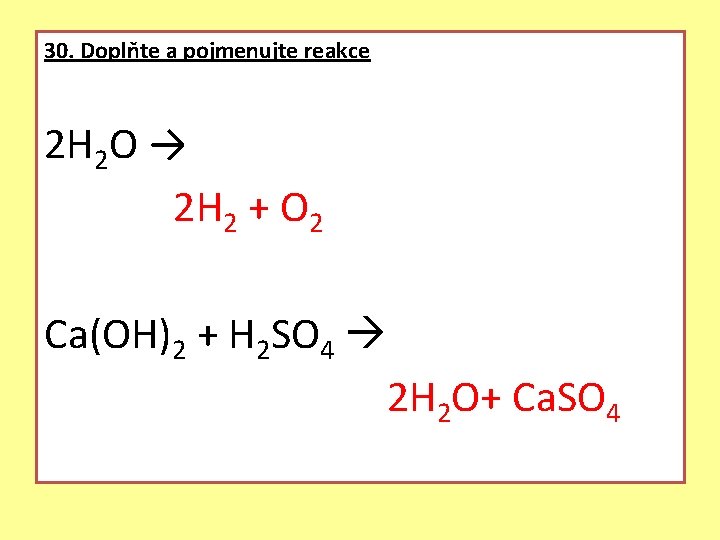
30. Doplňte a pojmenujte reakce 2 H 2 O → 2 H 2 + O 2 Ca(OH)2 + H 2 SO 4 2 H 2 O+ Ca. SO 4

Použité zdroje Použity obrázky vlastní tvorby.
- Slides: 19