Nzev ablony Inovace v prodopisu 52CH 1310 2

Název šablony: Inovace v přírodopisu 52/CH 13/10. 2. 2013, Vrtišková Vzdělávací oblast: Člověk a příroda Název výukového materiálu: KYSELINY A ZÁSADY Autor: Mgr. Eva Vrtišková Předmět: Chemie Třída: VIII. Tematický okruh: Kyseliny Téma: Kyslíkaté kyseliny Druh výukového materiálu: prezentace Použití ICT: interaktivní tabule, prezentace v. ppt, interaktivita Didaktické, metodické poznámky (popis použití výukového materiálu ve výuce): výklad Použité zdroje: - Chemie, učebnice pro devátý ročník ZŠ a primu víceletých gymnázií. FRAUS 2003, Plzeň. - Poznámky k učebnicím chemie - Vlastní zdroje

KYSELINY Kyslíkaté kyseliny

Rozdělení kyselin • Bez kyslíku • Vodík a kyselinotvorný prvek • Kyseliny odvozené od halogenovodíků • HF k. fluorovodíková • HCl k. chlorovodíková • HI k. jodovodíková • H 2 S k. sulfanová • HCN k. kyanovodíková • Kyslíkaté • Vodík, kyselinotvorný prvek, kyslík • HCl. O k. chlorná • HNO 3 k. dusičná • H 2 SO 4 k. sírová • H 2 CO 3 k. uhličitá • H 2 SO 3 k. siřičitá • H 3 PO 4 k. fosforečná

Co už víme • Kyseliny jsou látky, které ve vodném prostředí odštěpují vodíkový kation • Ionizace : HCl H+ +Cl • Přesněji H 3 O+ • Reakcí kovu a kyseliny vzniká vodík a příslušná sůl • Podle počtu vodíků rozdělujeme kyseliny na: jednosytné, dvojsytné, . . . • Silné kyseliny mají všechny molekuly rozštěpeny na ionty • Jejich koncentrované roztoky jsou žíraviny
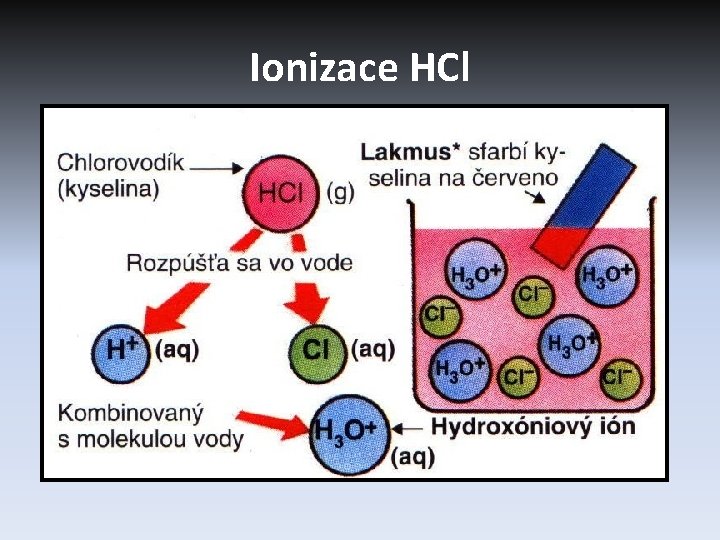
Ionizace HCl
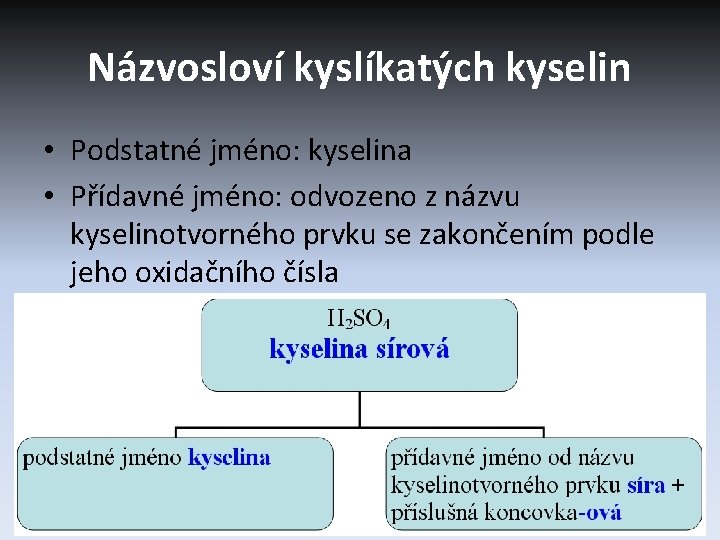
Názvosloví kyslíkatých kyselin • Podstatné jméno: kyselina • Přídavné jméno: odvozeno z názvu kyselinotvorného prvku se zakončením podle jeho oxidačního čísla

Vzorce kyslíkatých kyselin • Ve vzorci píšeme vlevo značku vodíku, uprostřed značku nekovu (kyselinotvorného prvku) a vpravo značku kyslíku Kyselina dusičná má tedy vzorec HNO 3 Kyselina sírová má tedy vzorec H 2 SO 4.

Vlastnosti a význam Expedují se jako koncentrované vodné roztoky Např. kyselina sírová, dusičná, fosforečná Pevné skupenství má kyselina boritá Pouze ve zředěném vodném roztoku existují slabé kyseliny : uhličitá, siřičitá , křemičitá • Vodné roztoky jsou kyselé p. H<7 • Ve vodném roztoku ionizují • Např. HNO 3 H+ + NO 3 - • •

Nejdůležitější a nejznámější kyseliny Kyselina sírová H 2 SO 4 Koncentrovaná 96 -98% Hustá bezbarvá kapalina Hygroskopická = odebírá látkám vodu organické látky jejím působením uhelnatí • Zředěná reaguje téměř se všemi kovy( kromě Pb, Au, Pt) • ředění kyselin!!!! Uvolňuje se velké množství tepla • •

Dehydratace cukru kyselinou sírovou

Kyselina sírová • Ve vodě ionizuje na 2 kationty vodíku a síranový anion • H 2 SO 4 2 H+ +SO 42 • • Kyselina sírová má rozsáhlé použití: Umělá hnojiva 62% Jiné chem. látky 19% Výbušniny, guma, baterie 7% Nátěrové hmoty a barviva 6% Umělé hedvábí 3% Výroba nafty 2% Výroba železa a oceli 1% 30% kyselina
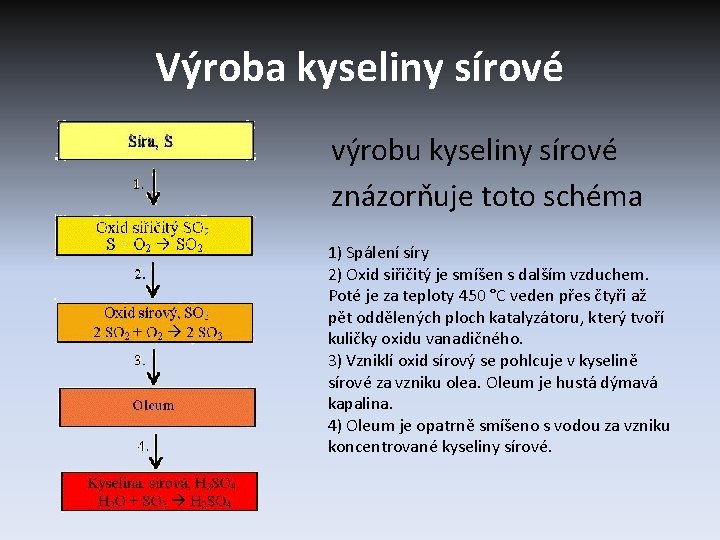
Výroba kyseliny sírové výrobu kyseliny sírové znázorňuje toto schéma 1) Spálení síry 2) Oxid siřičitý je smíšen s dalším vzduchem. Poté je za teploty 450 °C veden přes čtyři až pět oddělených ploch katalyzátoru, který tvoří kuličky oxidu vanadičného. 3) Vzniklí oxid sírový se pohlcuje v kyselině sírové za vzniku olea. Oleum je hustá dýmavá kapalina. 4) Oleum je opatrně smíšeno s vodou za vzniku koncentrované kyseliny sírové.

Kyselina dusičná HNO 3 • Koncentrovaná 67% • Bezbarvá, nestálá kapalina, účinkem světla se rozkládá na oxid dusičitý ( uchovávat v tmavých lahvích) • Velmi reaktivní ( s kovy nevzniká vodík, ale oxidy) • Silná žíravina, její zředěné roztoky mají oxidační účinky • Směs HCl s HNO 3 v poměru 3: 1 –lučavka královská

Výroba a použití Průmyslová výroba kyseliny dusičné Velká část amoniaku z Haberova procesu vstupuje do výroby kyseliny dusičné. Surovinami pro výrobu jsou amoniak, vzduch a voda. 1) Amoniak se smísí se vzduchem poté se vede při tlaku 1 MPa a teplotě 800 °C přes katalyzátor. Katalyzátor tvoří jemné pletivo z platiny a rhodia. 2) Vzniklý oxid dusný se ochladí a přidá se více vzduchu. 3) Ke vzniklému oxidu dusičitému se přidá vzduch a vše se smíchá z vodou Většina kyseliny dusičné se používá k výrobě hnojiv Část je použita na výrobu výbušnin, jako trinitrotoluen (TNT) Část se použije na výrobu nylonu a terylenu. Část se používá k výrobě léků.

Obrázky • http: //kekule. science. upjs. sk/chemia/kaz/rozpust anie%20 kyselin. jpg • http: //www. chemierol. wz. cz/nazvoslovi%20 kysel iny. jpg • http: //upload. wikimedia. org/wikipedia/common s/thumb/a/af/Papier_p. H. jpg/220 px. Papier_p. H. jpg • http: //dragonadam. wz. cz/obrazky/disociace_h 2 s o 4. jpg • http: //projektalfa. ic. cz/v_sirova_k. htm • http: //projektalfa. ic. cz/v_dusicna_k. htm
- Slides: 15