Nzev ablony Inovace v prodopisu 52CH 083 11

Název šablony: Inovace v přírodopisu 52/CH 08/3. 11. 2012, Vrtišková Vzdělávací oblast: Člověk a příroda Název výukového materiálu: ČÁSTICOVÉ SLOŽENÍ LÁTEK Autor: Mgr. Eva Vrtišková Předmět: Chemie Třída: 8. Tematický okruh: Chemické látky Téma: Molekuly, chemické sloučeniny Druh výukového materiálu: prezentace Použití ICT: interaktivní tabule, prezentace v. ppt, interaktivita Didaktické, metodické poznámky (popis použití výukového materiálu ve výuce): výklad Použité zdroje: - Chemie, učebnice pro ZŠ a víceletá gymnázia. FRAUS, 2005. - Wikipedia, otevřená encyklopedie. Dostupná online na: www. wikipedia. org - Učebnice chemie pro 8. ročník. Dostupná online na: www. zschemie. euweb. cz

MOLEKULY CHEMICKÉ SLOUČENINY Mgr. Eva Vrtišková

Od atomu k molekule • Při běžném tlaku a teplotě jsou atomy většiny prvků spojeny do složitějších celků = molekul • Výjimka: Prvky VIII. A skupiny netvoří molekuly • Nejjednodušší molekuly má vodík – vznikají spojením dvou atomů vodíku, které tak mají dva společné elektrony – Atomy v molekulách mají společné některé elektrony z vnější vrstvy 3
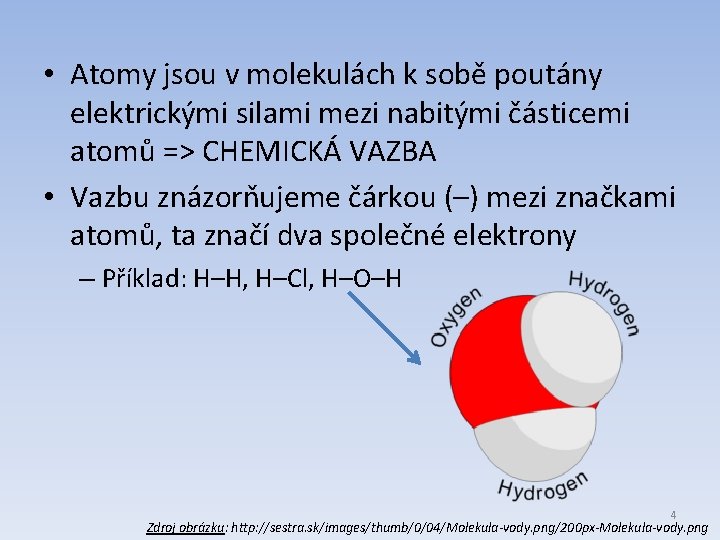
• Atomy jsou v molekulách k sobě poutány elektrickými silami mezi nabitými částicemi atomů => CHEMICKÁ VAZBA • Vazbu znázorňujeme čárkou (–) mezi značkami atomů, ta značí dva společné elektrony – Příklad: H–H, H–Cl, H–O–H 4 Zdroj obrázku: http: //sestra. sk/images/thumb/0/04/Molekula-vody. png/200 px-Molekula-vody. png

Molekuly a vzorce • Složení molekul vyjadřují vzorce • Používáme v nich značku prvků • Počet atomů se znázorňuje indexem za značkou prvku – Příklad: H 2, N 2, O 2, S 8, P 4, … Index za značkou prvku udává počet atomů tohoto prvku v molekule – Molekuly mohou být tvořeny z atomů stejného prvku nebo atomů různých prvků 5

Chemické sloučeniny • Všechny chemické látky, které jsou složené z atomů dvou a více prvků se nazývají chemické sloučeniny! • Jsou zapisovány pomocí chemických vzorců • Nejběžnější chemická sloučenina = VODA – Vzorec H 2 O – Skládá se z vodíku a kyslíku v poměru 2: 1 Molekula vody se skládá ze dvou atomů vodíku a jednoho atomu kyslíku => ch. vzorec H 2 O 6
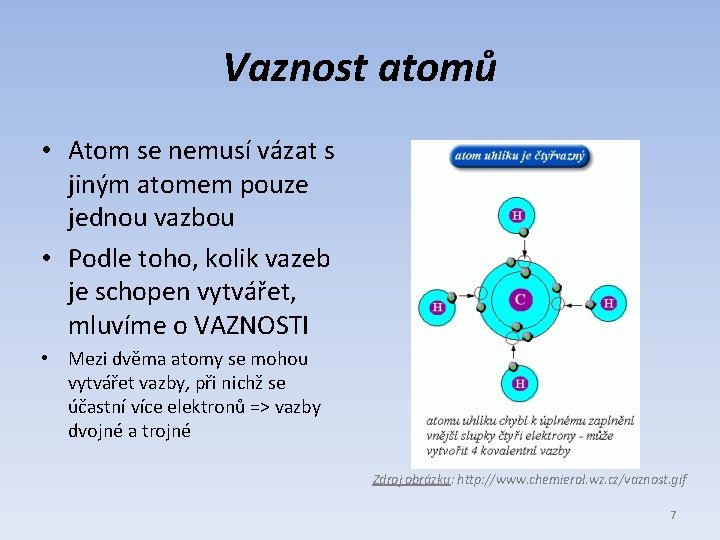
Vaznost atomů • Atom se nemusí vázat s jiným atomem pouze jednou vazbou • Podle toho, kolik vazeb je schopen vytvářet, mluvíme o VAZNOSTI • Mezi dvěma atomy se mohou vytvářet vazby, při nichž se účastní více elektronů => vazby dvojné a trojné Zdroj obrázku: http: //www. chemierol. wz. cz/vaznost. gif 7

Chemické vazby • Vznikají a zanikají při chemických reakcích – při spojování a oddělování atomů • Vazba mezi atomy založená na společném sdílení elektronů se nazývá kovalentní • Jsou-li kovalentní vazbou spojeny dva stejné atomy – vazba nepolární • Jsou-li kovalentní vazbou spojeny dva různé atomy – vazba polární 8

Chemické vazby IONTOVÁ VAZBA ELEKTRONEGATIVITA • Založena na elektrických silách mezi ionty • Velký rozdíl v ELN atomů • Existuje mnoho typů • Udává typ chemické vazby • Vyjadřuje schopnost atomu přitahovat elektrony chemické vazby • Čím větší hodnota – tím více atom přitahuje vazebné elektrony • Viz tabulka – Prvky s nejnižší/nejvyšší ELN? 9

Doplň text Prvky _____ skupiny PSP NETVOŘÍ molekuly Nejjednodušší molekuly má prvek _____ Vazby znázorňujeme _____ mezi zn. atomů Počet atomů znázorňuje _____ za značkou prvku Vazba mezi atomy založená na společném sdílení elektronů se nazývá _____ • Iontová vazba je založena na _____ vazbách mezi ionty • Typ chemické vazby udává _____ • • • 10

Zdroje • http: //sestra. sk/images/thumb/0/04/Molekul a-vody. png/200 px-Molekula-vody. png • http: //www. chemierol. wz. cz/vaznost. gif 11
- Slides: 11