Nzev ablony Inovace v chemii 52CH 293 4

Název šablony: Inovace v chemii 52/CH 29/3. 4. 2013, Vrtišková Vzdělávací oblast: Člověk a příroda Název výukového materiálu: Chemické reakce a děje Autor: Mgr. Eva Vrtišková Předmět: Chemie Třída: IX. Tematický okruh: Chemické reakce a děje Téma: Oxidace a redukce Druh výukového materiálu: prezentace Použití ICT: interaktivní tabule, prezentace v. ppt, interaktivita Didaktické, metodické poznámky (popis použití výukového materiálu ve výuce): výklad doplňuje učivo o chemických dějích a reakcích a zjednodušeně vysvětluje podstatu oxidace , redukce, elektrolýzy a řadu kovů i princip dějů v olověném akumulátoru. Použité zdroje: -Chemie, učebnice pro devátý ročník ZŠ a víceletá gymnázia. FRAUS 2007, Plzeň. - Poznámky k učebnicím chemie.

Oxidace a redukce
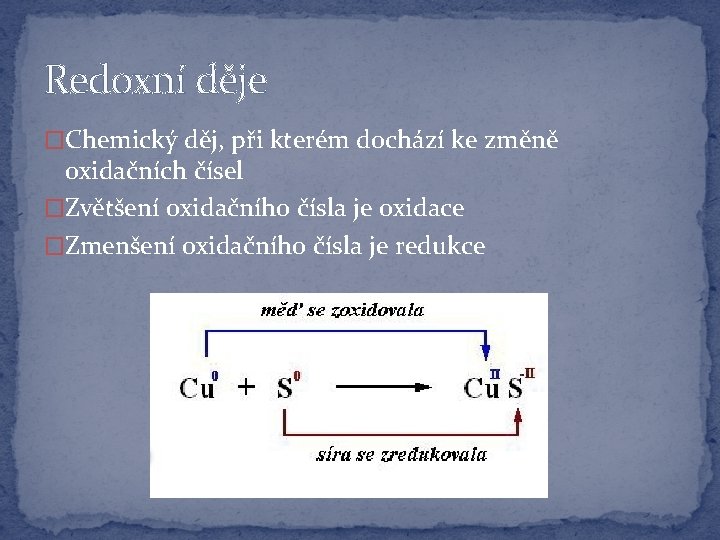
Redoxní děje �Chemický děj, při kterém dochází ke změně oxidačních čísel �Zvětšení oxidačního čísla je oxidace �Zmenšení oxidačního čísla je redukce

Oxidace a redukce �Změny oxidačního čísla jsou důsledkem změn rozdělení nebo přenosu elektronů mezi atomy a ionty v průběhu reakce �Měď se oxiduje a síra zároveň se redukuje �Elektrony se při tom nemohou ztratit, neboť každá oxidace určitých částic je doprovázena redukcí jiných �Oxidace probíhá zároveň s redukcí

Oxidační a redukční činidlo �Oxidační činidlo je látka, která elektrony přijímá (redukuje se) �Nejběžnější oxidační činidlo je kyslík, oxidační číslo jeho atomů se mění z nuly na –II �Redukční činidlo je látka, která elektrony odevzdává (oxiduje se) Jako redukční činidlo se uplatňuje oxid uhelnatý nebo uhlík

Oxidace a redukce �Označ oxidaci a redukci

Řada reaktivity kovů �Na porovnání oxidačně redukčních vlastností je založeno uspořádání kovových prvků do řady reaktivity �Pořadí bylo stanoveno na základě mnoha ověřených pokusů (nejběžnější kovy) �Ruský fyzikální chemik N. N. Beketov �Řadil kovy podle oxidačně-redukčního � potenciálu =Schopnost kovových prvků se oxidovat

Beketovova řada kovů �Neúplný seznam

Řada reaktivity kovů �Vlevo jsou velmi reaktivní kovy, které snadno tvoří kationty ( K, Ca, Na – reagují s vodou, Mg –reaguje s horkou vodou) �Vpravo jsou kovy nejméně reaktivní-méně snadno tvoří kationty (Cu, Hg, Au – ušlechtilé kovy) �Do řady reaktivity se zařazuje také vodík( není kov) �K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Au

Řada reaktivity kovů �Některé kovy nalevo od vodíku reagují se zředěnými kyselinami a uvolňuje se vodík �Kovy napravo od vodíku reagují pouze s kyselinami, které mají oxidační účinky a vodík nevzniká �Řada kovů je sestavena za předpokladu čistého povrchu kovu �Čím více je kov nalevo, tím snáze se oxiduje a je lepší redukční činidlo �Schopnost redukovat se klesá zleva doprava �Každý kov v Beketovově řadě je schopen vyredukovat všechny kovy napravo od něj (sám se oxiduje)

Řada kovů �K Na Ca Mg Al Zn Fe Pb H Cu Ag Pt Au �Zn + Cu. SO 4 �Cu + Zn. SO 4 – probíhá neprobíhá �Rozdílné oxidačně-redukční schopnosti kovů se využívá při elektrolytickém pokovování �Např. pochromování, pozlacení, �Předmět tvoří zápornou elektrodu - katodu

Elektrolýza �Chemická reakce vyvolaná průchodem stejnosměrného elektrického proudu �Na katodě = záporná elektroda- se převádějí elektrony do roztoku a dochází k redukci kationtů �Na anodě = kladná elektroda – odvádějí se elektrony a dochází k oxidaci na anionty �Obě části reakce probíhají současně, ale na různých místech �Produkty těchto reakcí mohou reagovat se složkami elektrolytu = elektrolyzovaný roztok nebo tavenina

elektrolýza Připojením elektrického zdroje k elektrodám vyvoláme elektrický proud. Elektrické pole vyvolá usměrněný pohyb kationtů a aniontů. Vzniká elektrolýza. Elektrolýza je jev, kdy při průchodu proudu elektrolytem nastávají na elektrodách látkové změny. Ionty , když dorazí k elektrodě odevzdají jí svůj náboj, mění se na atomy nebo molekuly, které se mohou vyloučit na povrchu elektrody nebo chemicky reagovat s materiálem elektrody.

Význam elektrolýzy �K výrobě hydroxidu sodného � Hliníku � Vodíku � Kyslíku �K čištění kovů �Galvanické pokovování
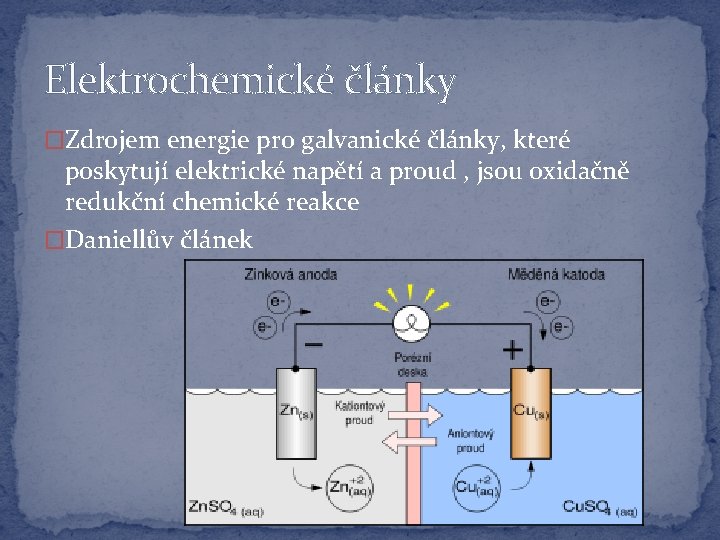
Elektrochemické články �Zdrojem energie pro galvanické články, které poskytují elektrické napětí a proud , jsou oxidačně redukční chemické reakce �Daniellův článek

Elektrochemické články � Napětí článku cca 1, 1 v (záleží na koncentraci elektrolytu) � Jednou elektrodou je zinkový plíšek v roztoku síranu zinečnatého � Druhou elektrodu tvoří měděný plíšek v roztoku síranu měďnatého � Prostory jsou odděleny porézní přepážkou- umožňuje vodivé spojení, ale brání smíchání roztoků � Je-li odebírán proud dochází k oxidaci zinku na zinečnaté kationty a redukci měďnatých iontů na atomy mědi � Zinek je záporným a měď kladným pólem článku

Elektrochemické články �Podle definice je katodou elektroda, na které probíhá redukce. U Daniellova článku je to kladná elektrodaměď �Zinek tvoří zápornou elektrodu – probíhá na ní oxidace – je anoda �U elektrolýzy je to opačně anoda = kladná �Katoda = záporná elektroda �Galvanické články poskytují stejnosměrný elektrický proud �Nevýhoda = vyčerpají se a přestanou dodávat el. proud
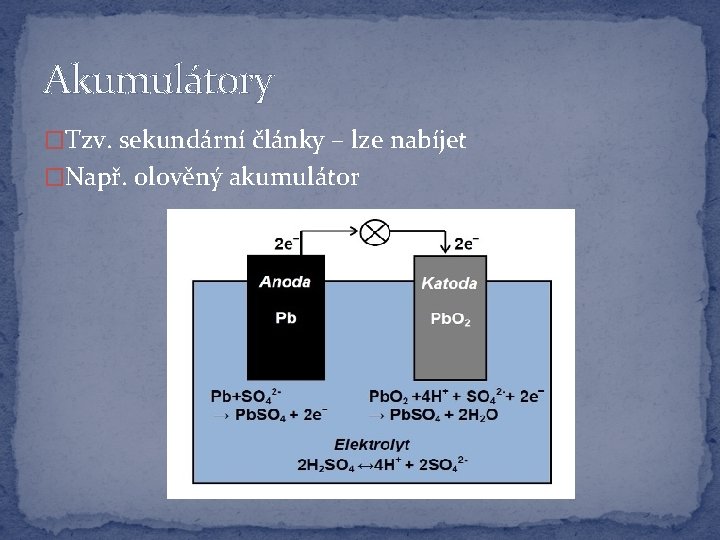
Akumulátory �Tzv. sekundární články – lze nabíjet �Např. olověný akumulátor
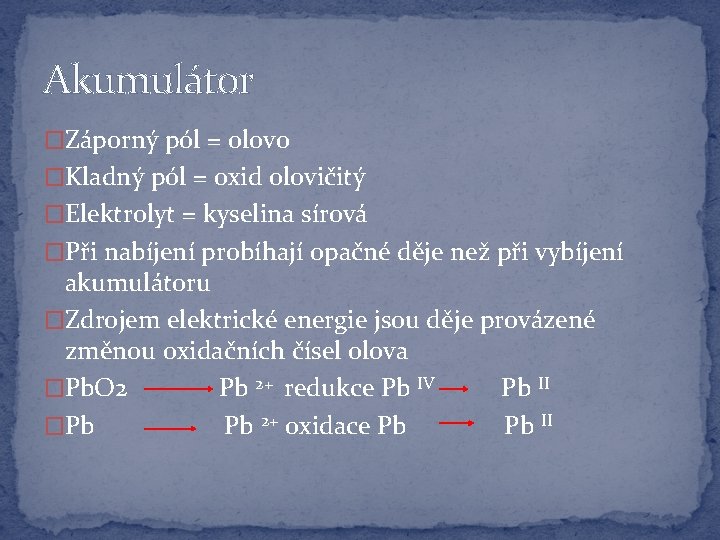
Akumulátor �Záporný pól = olovo �Kladný pól = oxid olovičitý �Elektrolyt = kyselina sírová �Při nabíjení probíhají opačné děje než při vybíjení akumulátoru �Zdrojem elektrické energie jsou děje provázené změnou oxidačních čísel olova �Pb. O 2 Pb 2+ redukce Pb IV Pb II �Pb Pb 2+ oxidace Pb Pb II

Akumulátor - výhody �Má delší životnost než galvanický článek �Redoxní děje probíhají oběma směry �Po připojení na zdroj stejnosměrného proudu lze dobít �Nabíjení a dobíjení lze opakovat �(cca 1000 x)
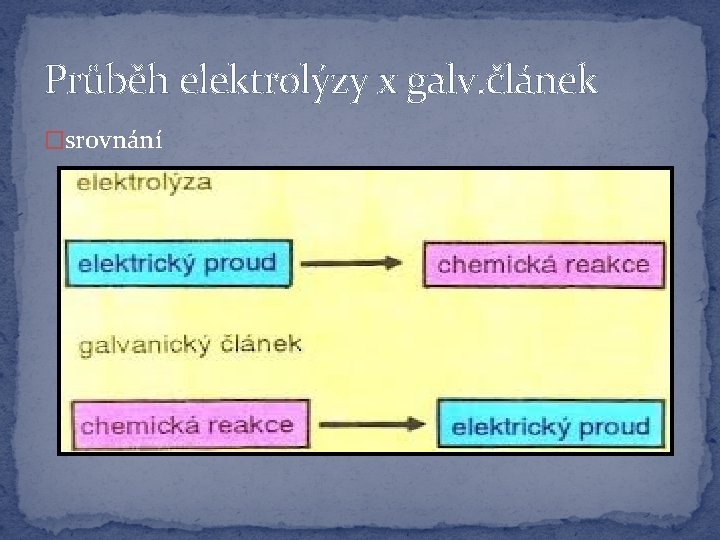
Průběh elektrolýzy x galv. článek �srovnání

Tajenka � Sekundární článek � Kladná elektroda � Částice se záporným �- - - - - �---- nábojem � Zvyšování oxidačního čísla � Elektrochemické…. �- - - �------ � Rozklad el. proudem � Látka odštěpující OH� Látka odštěpující H+ � Zmenšení oxidačního čísla � Autor řady reaktivity kovů �- - - - - - - �- - - -

Tajenka - řešení � Sekundární článek � Kladná elektroda � Částice se záporným nábojem � Zvyšování oxidačního čísla � Elektrochemické… � Rozklad el. proudem � Látka odštěpující OH� Látka odštěpující H+ � Zmenšení oxidačního čísla � Autor řady reaktivity kovů � - - - - -akumulátor � - - -anoda � - - - -elektron � - - - -oxidace � - - - články � - - -elektrolýza � - - -zásada � - - - -kyselina � - - - -redukce � - - - -Beketov
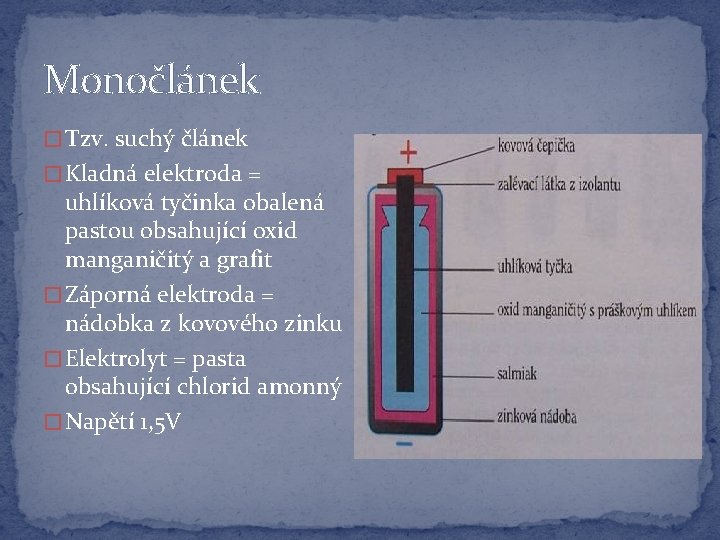
Monočlánek � Tzv. suchý článek � Kladná elektroda = uhlíková tyčinka obalená pastou obsahující oxid manganičitý a grafit � Záporná elektroda = nádobka z kovového zinku � Elektrolyt = pasta obsahující chlorid amonný � Napětí 1, 5 V

Použité zdroje http: //www. vyukovematerialy. cz/chemie/rocnik 9/foto/rada%20 re aktivity%20 kovu_. jpg http: //upload. wikimedia. org/wikipedia/commons/thumb/f/f 0/Be ketov 01. jpg/220 px-Beketov 01. jpg http: //www. oskole. sk/userfiles/image/fyzika/el_prud_v_kvapalina ch_a_plynoch/image 001. jpg http: //upload. wikimedia. org/wikipedia/commons/thumb/d/d 1/Ga lvanick%C 3%BD_%C 4%8 Dl%C 3%A 1 nek. svg/300 px. Galvanick%C 3%BD_%C 4%8 Dl%C 3%A 1 nek. svg. png http: //www. proelektrotechniky. cz/vzdelavani/obrazky/17 Akumulator. jpg http: //skoda. panda. cz/obrazky/018_2. jpg http: //cihakova-fyzika. webz. cz/obrazky/suchy. jpg http: //www. chemierol. wz. cz/pokovovani. gif
- Slides: 25