Nzev ablony Inovace v chemii 52CH 1915 2

Název šablony: Inovace v chemii 52/CH 19/15. 2. 2013 Vrtišková Vzdělávací oblast: Člověk a příroda Název výukového materiálu: Chemické děje a chemické rovnice Autor: Mgr. Eva Vrtišková Předmět: Chemie Třída: IX. Tematický okruh: Termochemie Téma: Exotermické a exotermické děje Druh výukového materiálu: prezentace Použití ICT: interaktivní tabule, prezentace v. ppt, interaktivita Didaktické, metodické poznámky (popis použití výukového materiálu ve výuce): výklad, doplňuje učivo chem. dějů. Na příkladu fotosyntézy a dýchání vysvětluje exo a endotermické děje Použité zdroje: - Chemie, učebnice pro devátý ročník ZŠ a primu víceletých gymnázií. FRAUS 2007, Plzeň. - Poznámky k učebnicím chemie. (vlastní zdroje)

Chemické reakce

Co je chemická reakce • Děj, při kterém vznikají z výchozích látek (reaktantů) látky jiné (produkty) • Jednotlivé látky je možné rozpoznat popř. oddělit • Ch. r. se mohou odehrávat nenápadně i bouřlivě • Vždy při nich některé vazby zanikají a tvoří se jiné • Atomová jádra se při reakcích nemění, celkové množství atomů nebo iontů prvků zůstává konstantní

Zákony • • Zákon zachování hmotnosti Platí pro všechny reakce Platí pro uzavřené soustavy Součet hmotností výchozích látek a produktů reakce je stále stejný Zákon zachování energie Je třeba také respektovat při ch. r. Energie při ch. r. nevzniká ani nezaniká Změny vazeb a uspořádání částic mohou být doprovázeny uvolňováním nebo pohlcováním různých druhů energie (teplo, světlo. . )
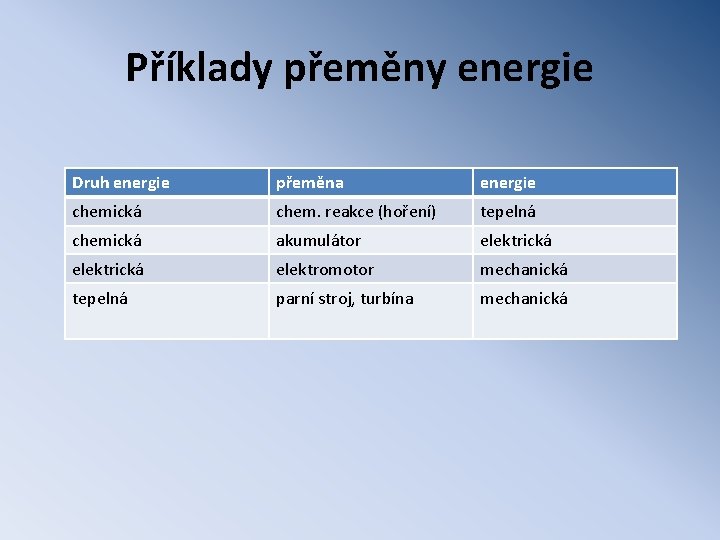
Příklady přeměny energie Druh energie přeměna energie chemická chem. reakce (hoření) tepelná chemická akumulátor elektrická elektromotor mechanická tepelná parní stroj, turbína mechanická

Termochemie • • • Zabývá se tepelnými změnami při chem. reakci Exotermické reakce. Teplo se uvolňuje Nejznámější exotermická reakce = hoření látek Množství tepla, které se uvolňuje = reakční teplo Energie potřebná na přerušení vazeb vých. látek je menší než uvolněná reakční teplo má záporné znaménko Množství tepla záleží na látkovém množství Označení Qm 2 H 2(g)+O 2(g) 2 H 2 O(l) Qm = -457 k. J/mol takto zapsaná ch. r. = termochemická rovnice

Termochemie • • • Endotermické rovnice Teplo se spotřebovává ( dodává) Např. tepelné rozklady látek Reakční teplo má kladné znaménko H 2(g) + I 2(s) 2 HI(g) Qm = 52 k. J/mol Hodnota molárního tepla závisí i na skupenství, proto je nutné jej napsat zkratkou s (solidus)-pevné l (liquidus)-kapalné g(gasus) – plynné aq (aquaeus) vodný roztok

Srovnání • dýchání • fotosyntéza Vzpomeňte na základní fakta Při fotosyntéze je potřeba dodat energii = reakce endotermická Při dýchání energie vzniká = reakce exotermická Množství energie uložené v 1 molu glukózy je 2 830 k. J Množství energie uvolněné při dýchání je až na znaménko stejné. Platí tzv. 1. termochemický zákon : molární reakční teplo reakce přímé a reakce zpětné je až na znaménko stejné. Qm (exotermická – dýchání) = -2 830 k. J/mol Qm (endotermická-fotosyntéza) = 2 830 k. J/mol

Spoj co k sobě patří • Endotermická reakce • Exotermická reakce • • • Fotosyntéza Dýchání Příjem energie Výdej energie Kladná hodnota Qm Záporná hodnota Qm Hoření Tepelný rozklad látek Hašení vápna
- Slides: 9