Nukleofiln substituce a eliminace typick pro alkylhalogenidy kter
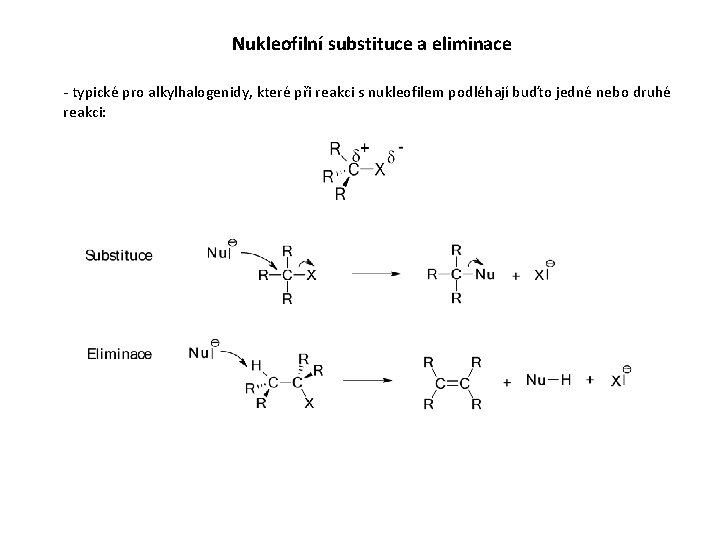
Nukleofilní substituce a eliminace - typické pro alkylhalogenidy, které při reakci s nukleofilem podléhají buďto jedné nebo druhé reakci:
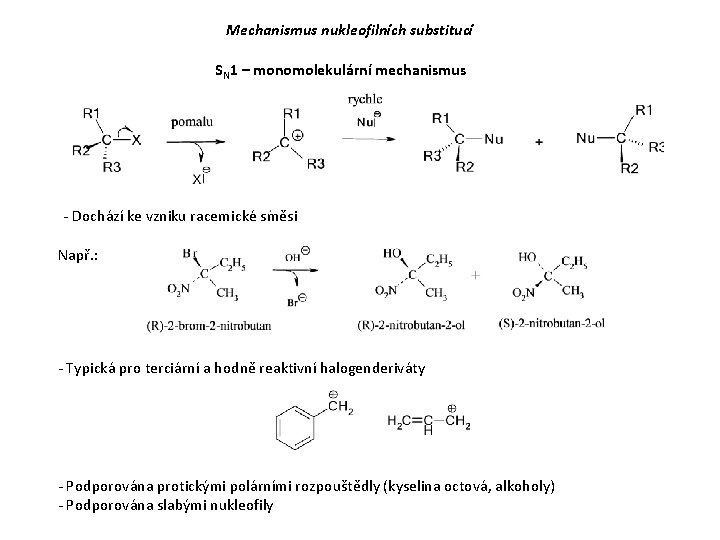
Mechanismus nukleofilních substitucí SN 1 – monomolekulární mechanismus - Dochází ke vzniku racemické směsi Např. : - Typická pro terciární a hodně reaktivní halogenderiváty - Podporována protickými polárními rozpouštědly (kyselina octová, alkoholy) - Podporována slabými nukleofily
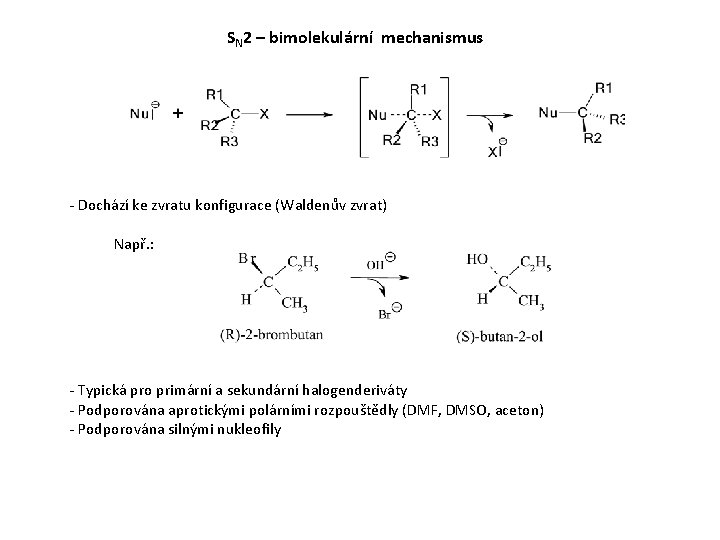
SN 2 – bimolekulární mechanismus - Dochází ke zvratu konfigurace (Waldenův zvrat) Např. : - Typická pro primární a sekundární halogenderiváty - Podporována aprotickými polárními rozpouštědly (DMF, DMSO, aceton) - Podporována silnými nukleofily
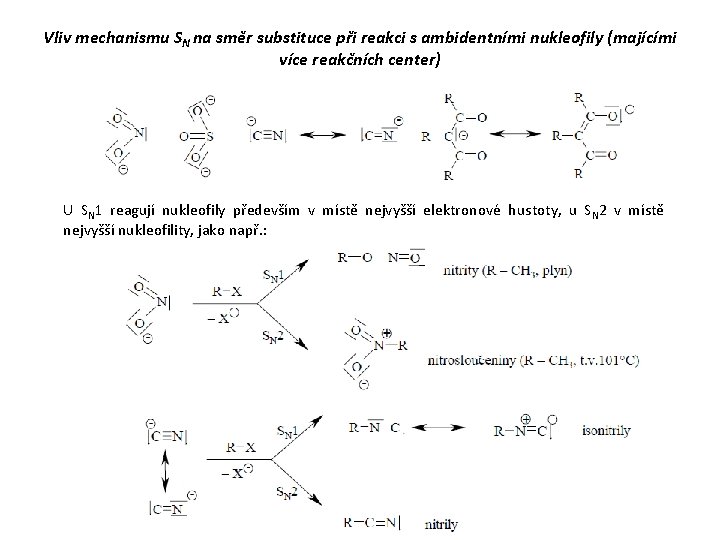
Vliv mechanismu SN na směr substituce při reakci s ambidentními nukleofily (majícími více reakčních center) U SN 1 reagují nukleofily především v místě nejvyšší elektronové hustoty, u SN 2 v místě nejvyšší nukleofility, jako např. :
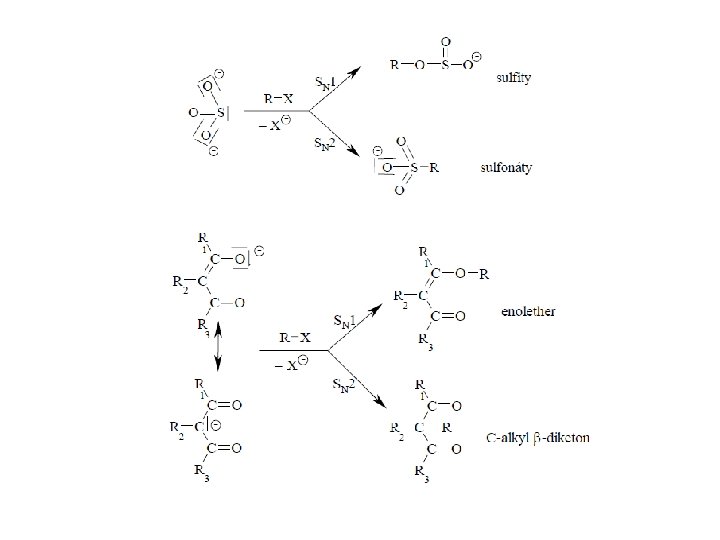
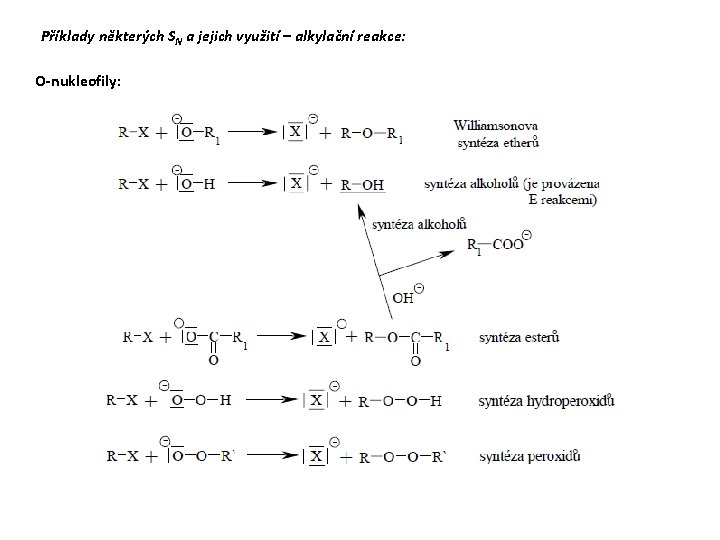
Příklady některých SN a jejich využití – alkylační reakce: O-nukleofily:
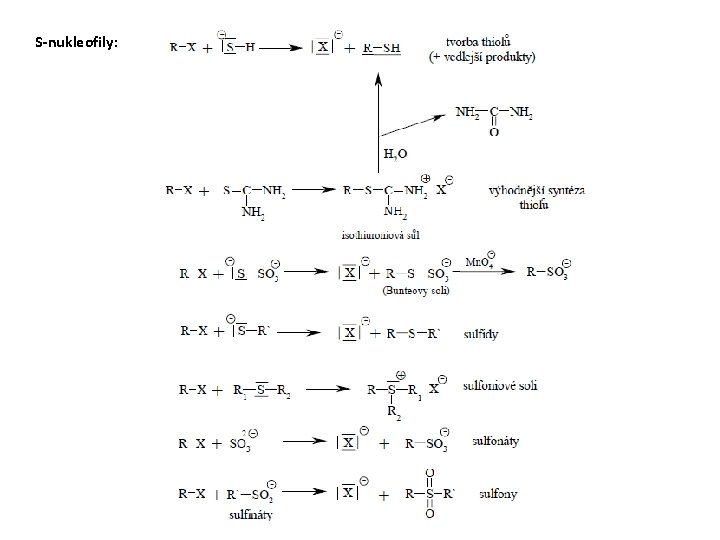
S-nukleofily:
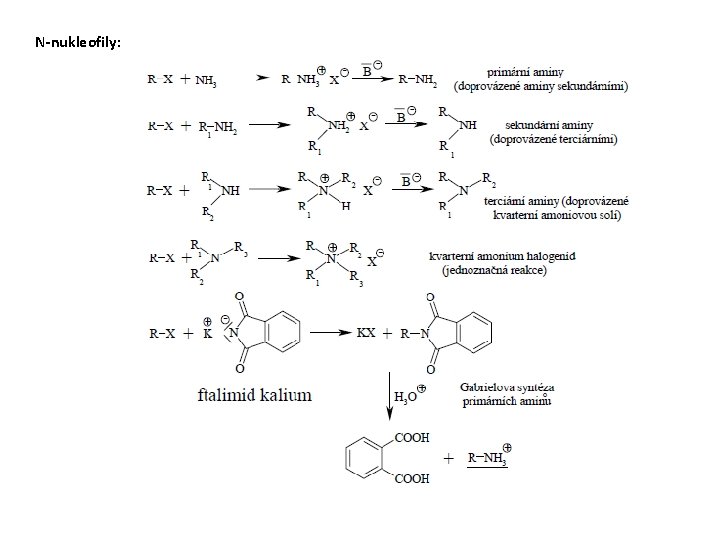
N-nukleofily:
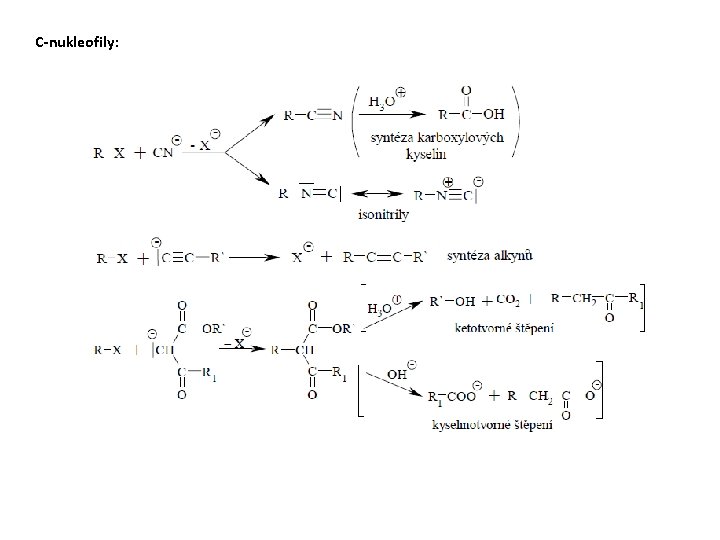
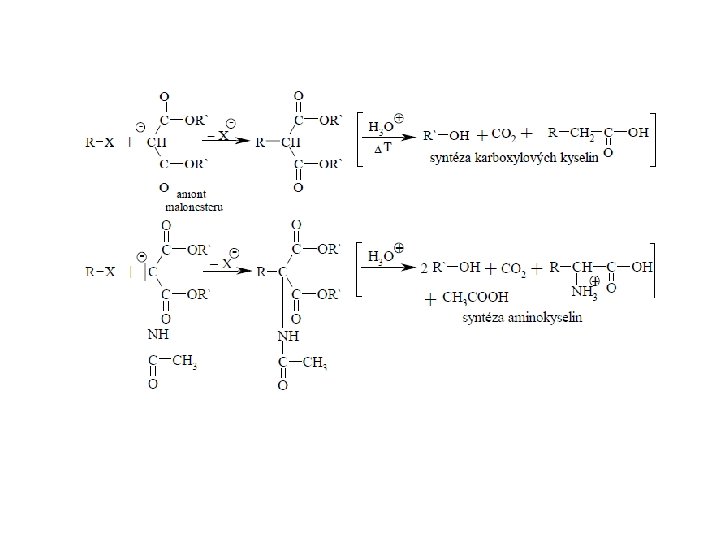
C-nukleofily:
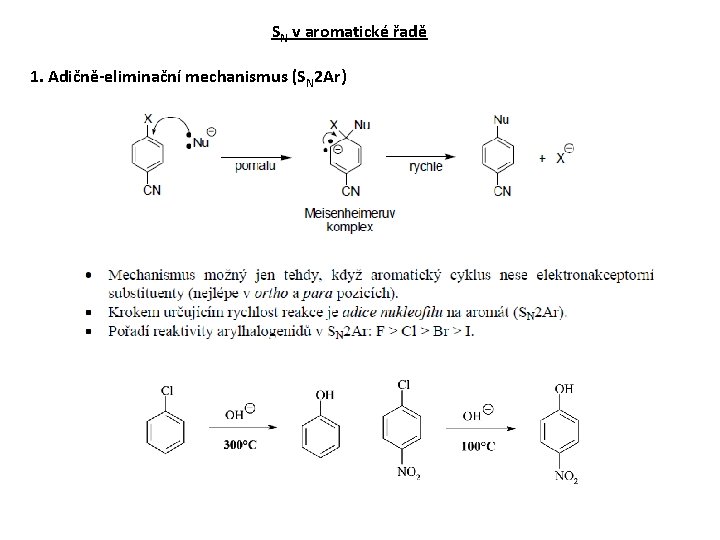
SN v aromatické řadě 1. Adičně-eliminační mechanismus (SN 2 Ar)
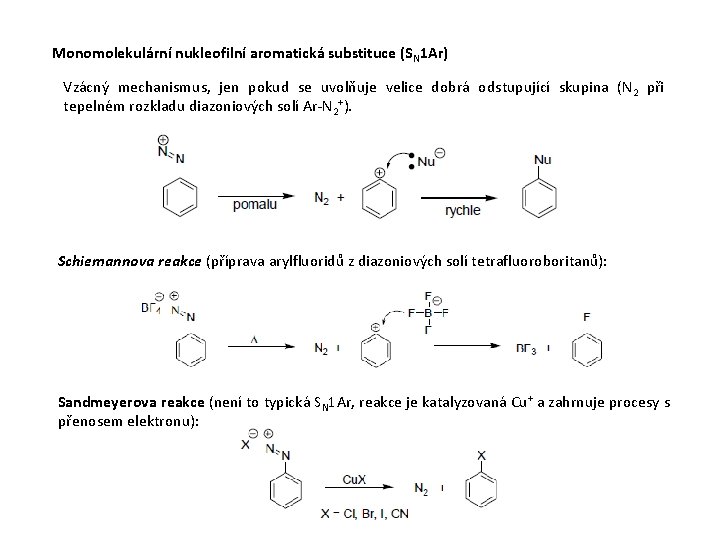
Monomolekulární nukleofilní aromatická substituce (SN 1 Ar) Vzácný mechanismus, jen pokud se uvolňuje velice dobrá odstupující skupina (N 2 při tepelném rozkladu diazoniových solí Ar-N 2+). Schiemannova reakce (příprava arylfluoridů z diazoniových solí tetrafluoroboritanů): Sandmeyerova reakce (není to typická SN 1 Ar, reakce je katalyzovaná Cu+ a zahrnuje procesy s přenosem elektronu):
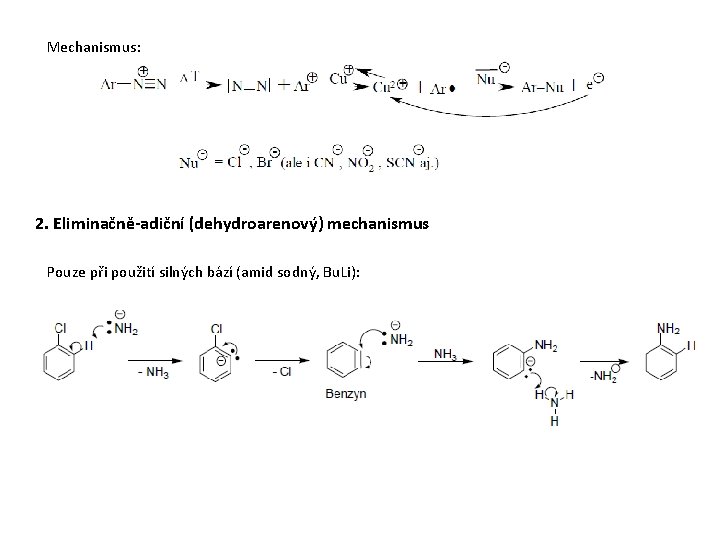
Mechanismus: 2. Eliminačně-adiční (dehydroarenový) mechanismus Pouze při použití silných bází (amid sodný, Bu. Li):
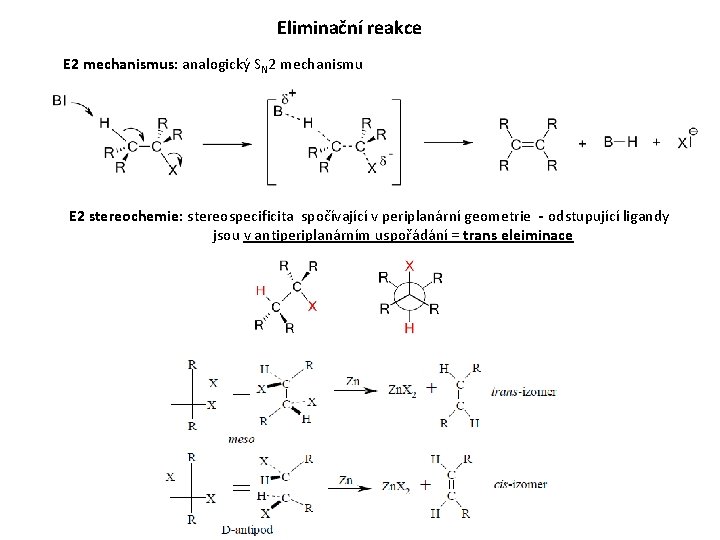
Eliminační reakce E 2 mechanismus: analogický SN 2 mechanismu E 2 stereochemie: stereospecificita spočívající v periplanární geometrie - odstupující ligandy jsou v antiperiplanárním uspořádání = trans eleiminace
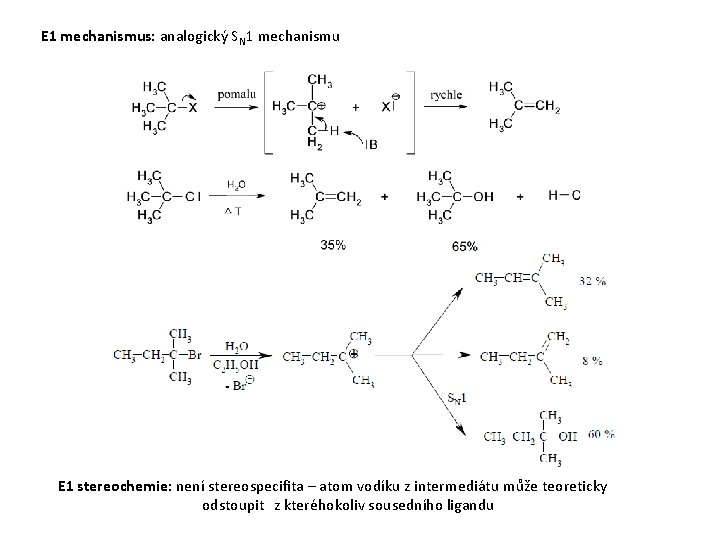
E 1 mechanismus: analogický SN 1 mechanismu E 1 stereochemie: není stereospecifita – atom vodíku z intermediátu může teoreticky odstoupit z kteréhokoliv sousedního ligandu
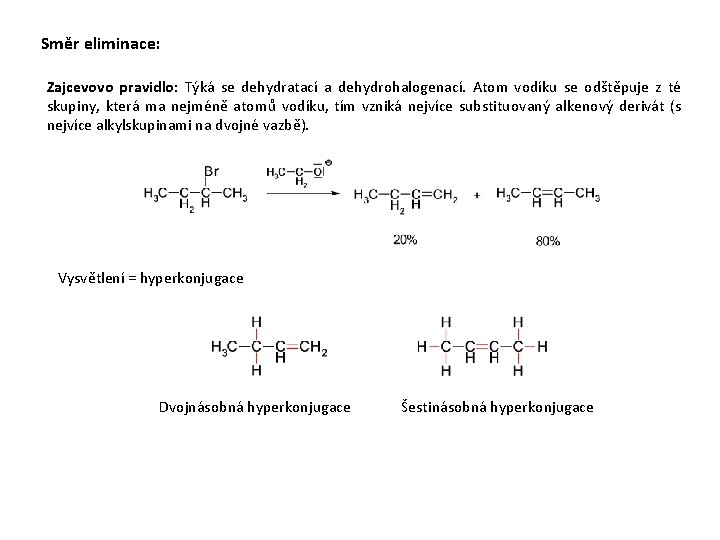
Směr eliminace: Zajcevovo pravidlo: Týká se dehydratací a dehydrohalogenací. Atom vodíku se odštěpuje z té skupiny, která ma nejméně atomů vodíku, tím vzniká nejvíce substituovaný alkenový derivát (s nejvíce alkylskupinami na dvojné vazbě). Vysvětlení = hyperkonjugace Dvojnásobná hyperkonjugace Šestinásobná hyperkonjugace
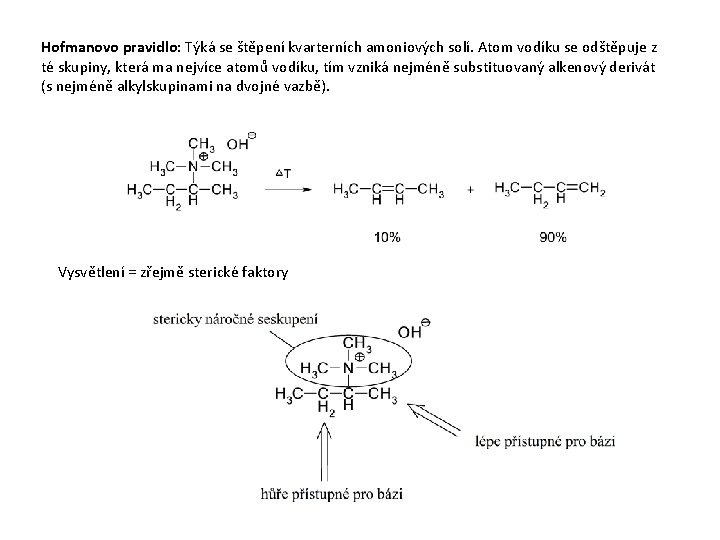
Hofmanovo pravidlo: Týká se štěpení kvarterních amoniových solí. Atom vodíku se odštěpuje z té skupiny, která ma nejvíce atomů vodíku, tím vzniká nejméně substituovaný alkenový derivát (s nejméně alkylskupinami na dvojné vazbě). Vysvětlení = zřejmě sterické faktory
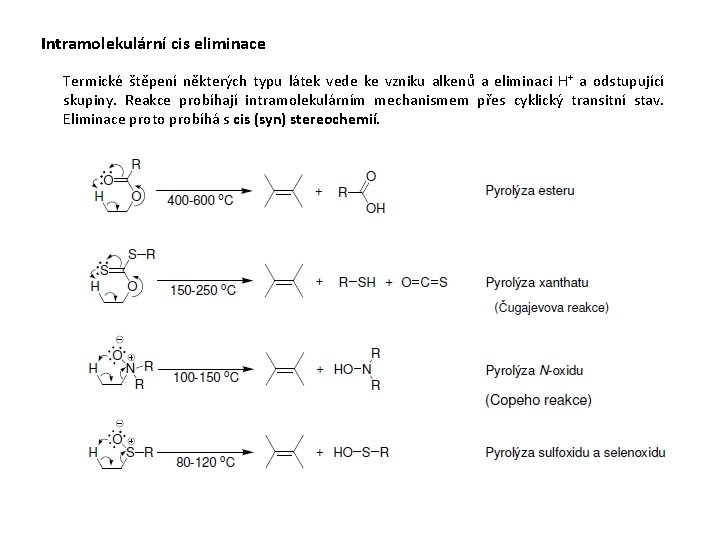
Intramolekulární cis eliminace Termické štěpení některých typu látek vede ke vzniku alkenů a eliminaci H+ a odstupující skupiny. Reakce probíhají intramolekulárním mechanismem přes cyklický transitní stav. Eliminace proto probíhá s cis (syn) stereochemií.
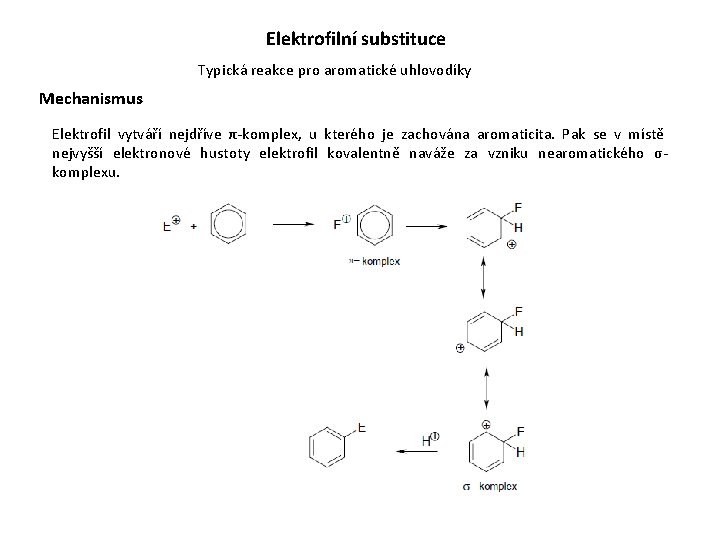
Elektrofilní substituce Typická reakce pro aromatické uhlovodíky Mechanismus Elektrofil vytváří nejdříve π-komplex, u kterého je zachována aromaticita. Pak se v místě nejvyšší elektronové hustoty elektrofil kovalentně naváže za vzniku nearomatického σkomplexu.

Typy elektrofilních činidel

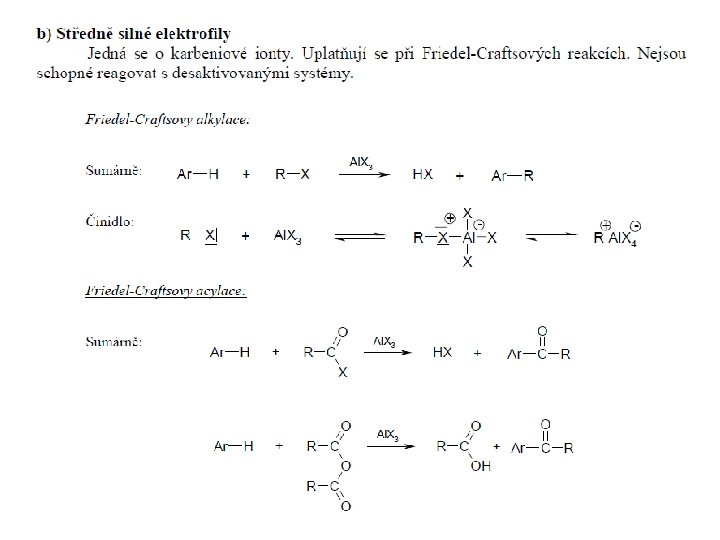

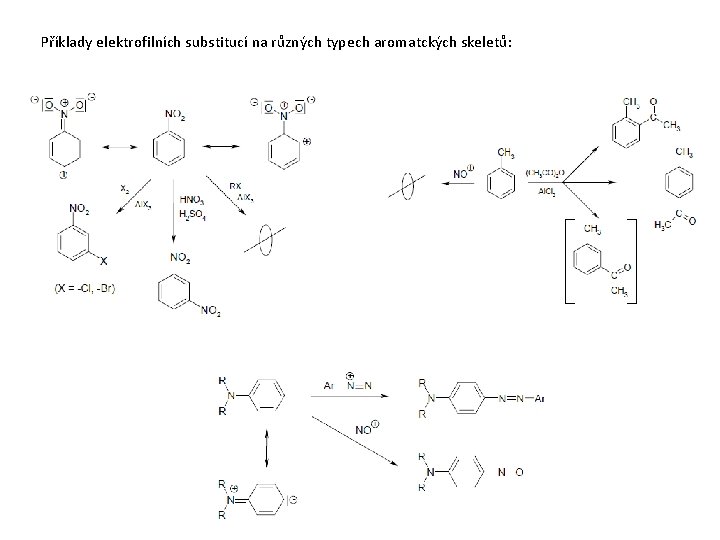
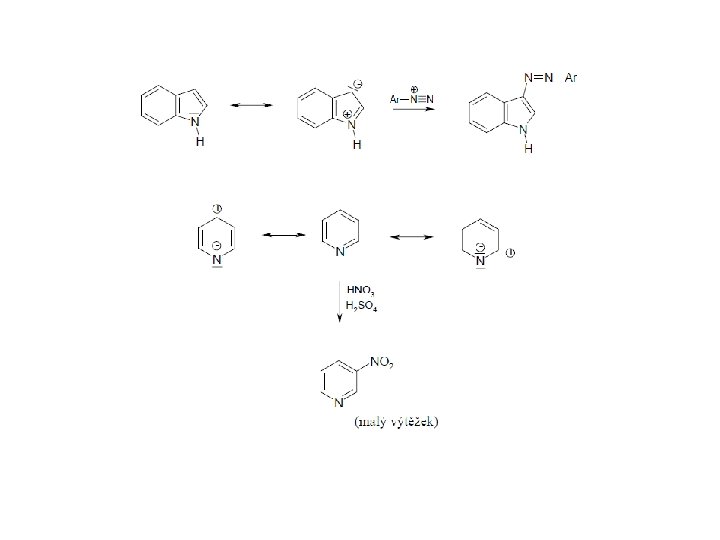
Příklady elektrofilních substitucí na různých typech aromatckých skeletů:
- Slides: 25