NTE MADDENN YAPISI VE ZELLKLER KONU ELEMENTLER SINIFLANDIRALIM













- Slides: 19

ÜNİTE: MADDENİN YAPISI VE ÖZELLİKLERİ KONU: ELEMENTLERİ SINIFLANDIRALIM KONU KAZANIMI: Elementleri metal, ametal ve soygaz olarak sınıflandırarak özelliklerini karşılaştırır. KONU KAVRAMLARI: Metal, Ametal , Soygaz

• Elementler kendi özelliklerine göre üç grupta incelenir. ELEMENTLER METALLER AMETALLER SOYGAZLAR

METALLERİN GENEL ÖZELLİKLERİ Periyodik sistemin sol tarafında yer alırlar. Parlak renge sahiptir ve ışığı yansıtır. Isıyı ve elektriği iyi iletirler. Elektron vermeye yatkındırlar. Bileşik oluşturduklarında sadece + yüklü iyon (katyon) oluştururlar. Tel, levha ve toz haline getirilebilirler. Birbirleri ile bileşik oluşturmazlar. Son katmanlarında 1 - 3 elektron bulunur. Büyük çoğunluğunun erime ve kaynama noktası ametallere göre çok yüksektir. Sert veya yumuşak olabilirler. Sert olan metal yumuşak olan metali çizebilir. Esnektir ve eğilip bükülebilir. Normal koşullarda katı haldedir. Yalnız cıva metali sıvıdır.

NOT : YARI METALLERİN GENEL ÖZELLİKLERİ Bazı fiziksel özellikleri ve görünüşleri bakımından metallere, kimyasal özellikleri bakımından daha çok ametallere benzeyen elementlerdir. Parlak ya da mat olabilirler. Metallere göre az, ametallere göre ise daha iyi elektrik akımı ve ısıyı iletebilirler. (Yarı iletken özelliktedirler) Yarı metaller özellikle elektronik devre parçalarının ve optik malzemelerin yapımında kullanılırlar. Örneğin bu elementler kamera ve mikroskop mercekleri ile projektörlerde yarı iletkenlik özelliğinden dolayı tercih edilir. Kırılgan değildir ve dövülerek işlenebilir.

AMETALLERİN GENEL ÖZELLİKLERİ Periyodik sistemin sağ tarafında yer alırlar. Mat renklidirler ve ışığı iyi yansıtmazlar. Çoğu yalıtkandır. Isı ve elektriği iyi iletmezler. (Bazıları çok az da olsa iletir. ) Oda şartlarında katı sıvı ya da gaz halinde olanları bulunur. Örneğin hidrojen, azot, helyum, klor gibi elementler oda sıcaklığında gaz halinde bulunur. Brom elementi sıvı bir ametaldir. Karbon, fosfor, kükürt ve iyot ise oda sıcaklığında katı halde bulunur. Elektron almaya yatkınlardır. Tel ve levha haline getirilemezler. Katı olanları kırılgan yapıdadır, dövülemezler ve esnek değildirler. Birbirleri ile bileşik oluşturabilirler. Genellikle son katmanlarında 4 - 8 elektron bulunur. Erime ve kaynama noktaları (karbon hariç) metallere göre oldukça düşüktür. Bileşik olduklarında çoğunlukla (-) yüklü iyonları (anyon) oluştururlar. Bununla beraber bazı ametaller (+) yüklü iyonlar da oluşturabilirler.

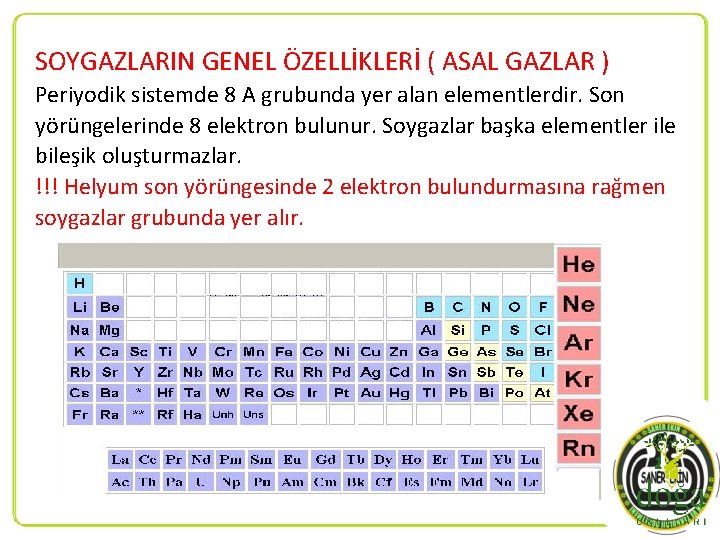
SOYGAZLARIN GENEL ÖZELLİKLERİ ( ASAL GAZLAR ) Periyodik sistemde 8 A grubunda yer alan elementlerdir. Son yörüngelerinde 8 elektron bulunur. Soygazlar başka elementler ile bileşik oluşturmazlar. !!! Helyum son yörüngesinde 2 elektron bulundurmasına rağmen soygazlar grubunda yer alır.

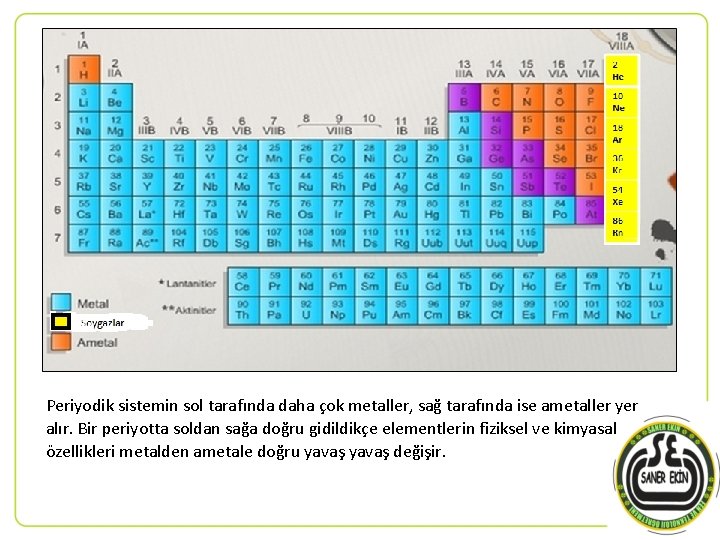
Periyodik sistemin sol tarafında daha çok metaller, sağ tarafında ise ametaller yer alır. Bir periyotta soldan sağa doğru gidildikçe elementlerin fiziksel ve kimyasal özellikleri metalden ametale doğru yavaş değişir.

Bazı elementler gösterdikleri özelliklerden dolayı özel isim almıştır. Bunlar metal sınıfında yer alan 1. ve 2. grup elementleri ile ametal sınıfında yer alan 7. grup elementleridir. ALKALİ METALLER Periyodik sistemde 1 A grubunda yer alan elementlerdir. Son yörüngelerinde 1 elektron bulundurur. Alkali metaller bileşiklerinde + 1 yüklü iyonlar ( katyonlar ) oluşturur. !!! Hidrojen elementi 1 A grubunda yer almasına rağmen alkali metal değildir.

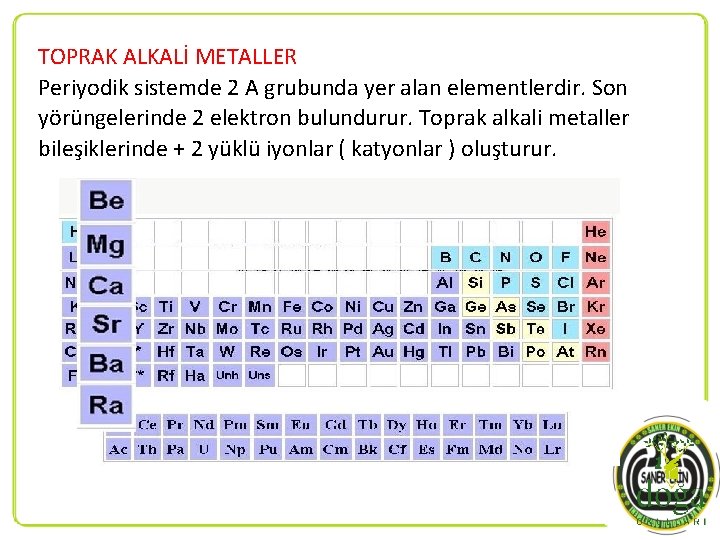
TOPRAK ALKALİ METALLER Periyodik sistemde 2 A grubunda yer alan elementlerdir. Son yörüngelerinde 2 elektron bulundurur. Toprak alkali metaller bileşiklerinde + 2 yüklü iyonlar ( katyonlar ) oluşturur.

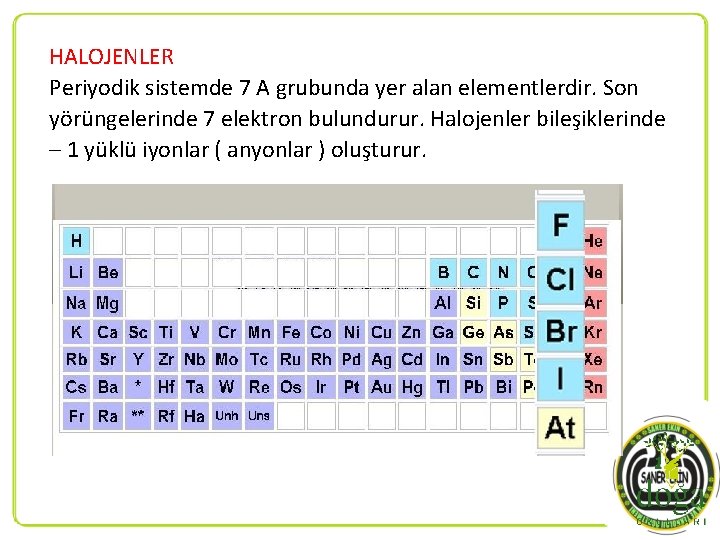
HALOJENLER Periyodik sistemde 7 A grubunda yer alan elementlerdir. Son yörüngelerinde 7 elektron bulundurur. Halojenler bileşiklerinde – 1 yüklü iyonlar ( anyonlar ) oluşturur.

PERİYODİK SİSTEMDE DEĞİŞEN ÖZELLİKLER Periyodik sistemde yukarıdan aşağıya doğru inildikçe ; • Atom numarası ve kütle numarası büyür. • Metalik özellik artar. • Ametalik özellik azalır. • Atom hacmi büyür. • Elektron ilgisi azalır. • Periyot numarası artar. • Grup numarası ( değerlik elektron sayısı ) değişmez.

Periyodik sistemde soldan sağa doğru gidildikçe ; • Atom numarası artar ve kütle numarası büyür. • Metalik özellik azalır. • Ametalik özellik artar. • Atom hacmi küçülür. • Elektron ilgisi artar. • Periyot numarası değişmez. • Grup numarası ( değerlik elektron sayısı ) artar.

PERİYODİK SİSTEMDE BULUNAN İLK 20 ELEMENTİN KULLANIM ALANLARI 1. HİDROJEN: Suyun canlıların ve petrol gibi birçok maddenin yapısında bulunur. Ayrıca roket yakıtı olarak kullanılır. 2. HELYUM: Zeplin ve balon gibi hava taşıtlarını şişirmede , roket yakıtlarını sıkıştırmada kullanılır. 3. LİTYUM: İlaçlarda , pil üretiminde seramik ve cam yapımında kullanılır. 4. BERİLYUM: Uçak ve uzay araçlarının yapımında elektrik ve ısı iletkeni olarak kullanılır. 5. BOR: Isıya dayanıklı renkli cam imalatında , seramiklerde ve roket yakıtında kullanılır.

6. KARBON: Canlı yaşamı için çok önemlidir. Canlıların yapısında , yeryüzünde kömür , petrol ve doğal gazın yapısında bulunur. 7. AZOT: Canlılar için gerekli temel elementlerden biridir. Sıvı azot soğutmada ve bazı azot bileşikleri tarımda gübre olarak kullanılır. 8. OKSİJEN: Canlılar için önemli elementtir. Dağlıçlarda ve astronotlarda solunum için oksijen tüplerinde bulundurulur. 9. FLOR: Diş macunu ve deodorant yapısında , buzdolabı ve klimalarda kullanılır. 10. NEON: Renkli reklam panolarının aydınlatılmasında, TV tüplerinde kullanılır. 11. SODYUM: Doğada sofra tuzunda , kağıt , gıda , tekstil , kimya ve sabun endüstrisinde kullanılır.

12. MAGNEZYUM: Hava taşıtlarının yapısında kullanılır, kurutulmuş meyvelerde bulunur. 13. ALÜMİNYUM: Mutfak eşyaları, elektrikli araçların yapısında ve içecek kutularında kullanılır. 14. SİLİSYUM: Kumda, kilde, camın yapısında ve yapı malzemelerinde bulunur. 15. FOSFOR: Canlılarda , sinir ve kemiklerin yapısında, suni gübre yapısında bulunur. 16. KÜKÜRT: Barut , sülfürik asit yapısında, kuru meyvelerde mikrop öldürücü olarak kullanılır. 17. KLOR: Sofra tuzunda , içme sularında mikrop öldürücü olarak kullanılır.

18. ARGON: Ampullerde ve floresan tüplerinde kullanılır. 19. POTASYUM: Sıvı deterjan, gübre, barut, cam ve lens yapımında kullanılır. 20. KALSİYUM: Çimento, alçı, kireç ile dişlerimizin ve kemiklerin yapısında bulunur.

SORU : ÇI 30 Nisan 2015 Teog

SORU: 15 Mayıs 2016 Teog Mazeret

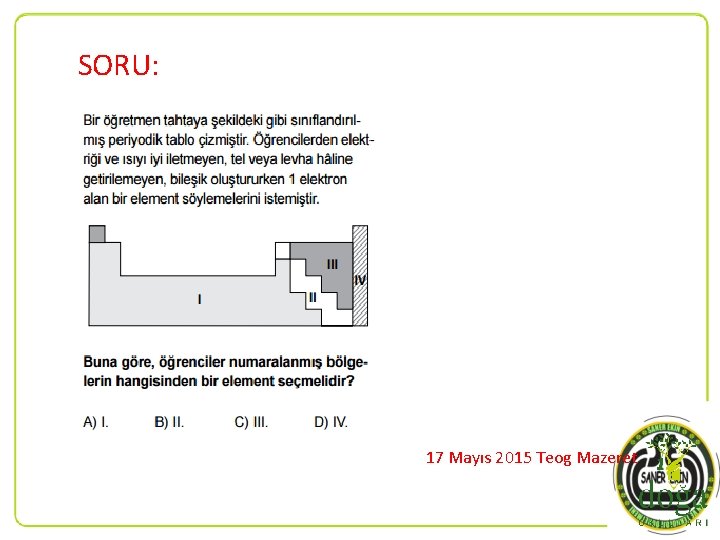
SORU: 17 Mayıs 2015 Teog Mazeret