Nomm et crire la formule des composs binaires

Nommé et écrire la formule des composés binaires ioniques

Composés ioniques binaires o o Un composé ionique est un cation (métaux) et un anion (non-métaux). Un composé binaire est composé de seulement deux éléments différents Ex: Na. Cl, Mg. Cl 2. Na. OH n’est pas binaire.

Écrire la formule d’un composé ionique binaire o o Quand on écrit la formule il faut que les charges des cations et des anions soit balancées. Une façon de s’assurer que les charges sont balancées est d’utiliser le “chassé-croisé”.

Méthode “chasé-croisé”: o o Au lieux d’utiliser des diagrammes de Lewis pour trouver la formule des composés ionique, on peut utiliser la méthode “chassé-croisé” Méthode “chasé-croisé”: n n Détermine la charge du cation Détermine la charge de l’anion Croisé les charges (ignore +/-) Réduit le ratio si nécessaire
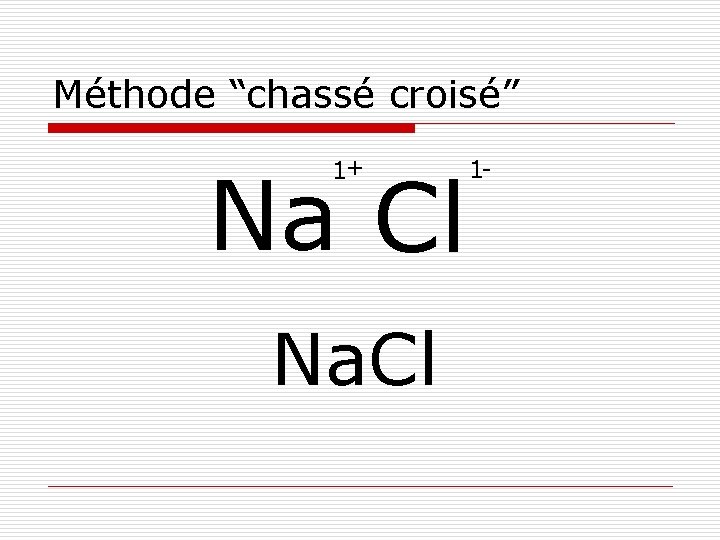
Méthode “chassé croisé” 1+ Na Cl Na. Cl 1 -

La méthode “chassé-croisé” o Attention, tu dois toujours avoir le ratio le plus simple. Exemple: Ca 2+ O 2 Ca 2 O 2 = Ca. O o On n’écrit pas les 1 dans les formules!

Méthode “chassé croisé” 2+ Be S Be 2 S 2 Be. S 2 -
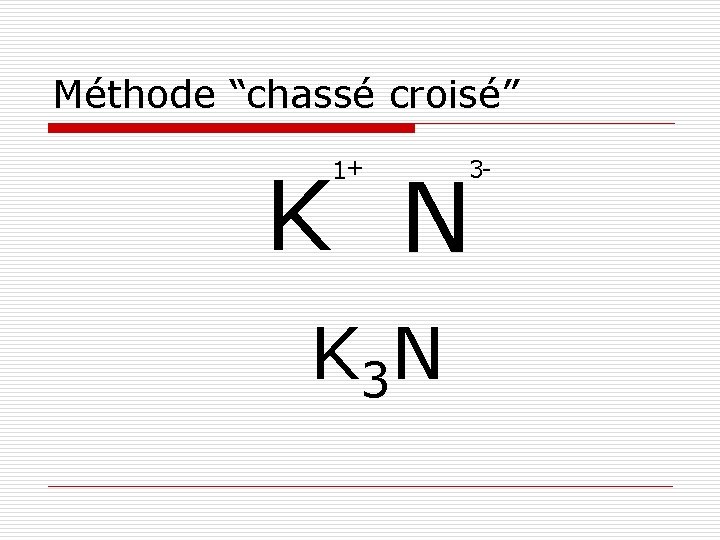
Méthode “chassé croisé” 1+ K N K 3 N 3 -

Nommer les composés ioniques binaires nom de l’anion + -ure de nom du cation (non-métaux) o Ex: Chlore Chlor + -ure = chlorure n Sauf: l’oxygène oxyde o l’azote nitrure o Le soufre sulfure Li 2 S sulfure de lithium Ba. Cl 2 chlorure de barium o o o (métaux)

Nommer les composés ioniques binaires o Souviens-toi n n o L’ion négatif est nommé en premier. Les noms sont écrits en lettres minuscule. Exemples n n n Ag. Cl o chlorure d’argent Mg. Br 2 o bromure de magnésium K 2 O o oxyde de potassium

Pratiquer o Utilise le méthode de “chasé croissé” pour déterminer la formule des composés ionique suivantes: n n n Bromure de calcium L’oxyde de lithium Silisure d’aluminum

Ions polyatomiques o o Plusieurs composés ioniques ne son pas binaire parce que un des ions contiennent plus d’un élément. Ces ions polyatomiques sont souvent des composés covalente qui ont besoin d’électron(s) extra pour remplir un couche de valence. ex: sulphate [SO 4]2 -
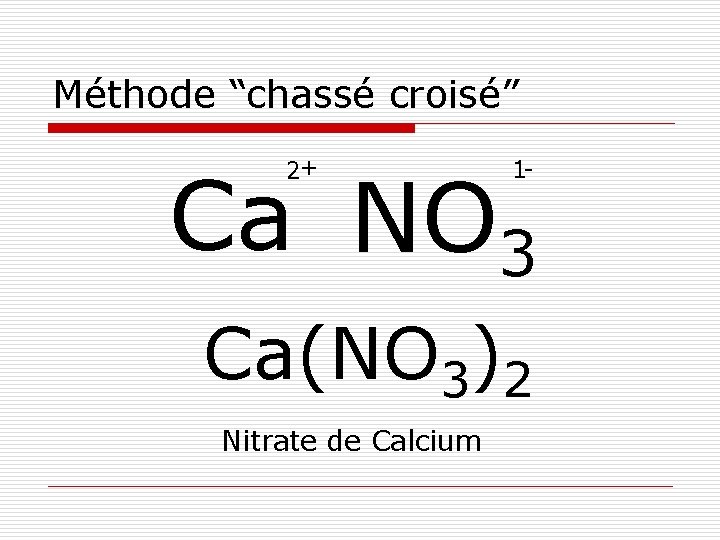
Méthode “chassé croisé” 2+ Ca NO 3 1 - Ca(NO 3)2 Nitrate de Calcium

Ions polyatomiques o o o Ba. SO 4 Mg(OH)2 (NH 4)2 S Hydroxyde de sodium Carbonate de potassium Sulphate de calcium

Note: Métaux de transition Si un métaux de transition est utilisé et il a plus qu’un charge possible, la charge est indiqué en numéros romain: n o o o Fer(II) Fe 2+ Cuivre(I) Cu 1+ Vanadium(V) V 5+ Vanadium(IV) V 4+ Ex: Chlorure de fer(III) n Fe. Cl 3 o Sulphure de cobalt(II) n o Chlorure de cuivre(II) n o Co. S Cu. Cl 2 Oxyde de cuivre(I) n Cu 2 O

Nommer composés avec métaux de transition o o o Quand on est donné un composé ionique ou le métal a plus qu’une charge possible, il faut déterminer la charge Utilisé chassé croisé à l’envers! Ex: Fe 2 O 3 L’oxyde de fer(III)

Essaye! n Fe. SO 4 n Rapelle: n n Ion polyatomique Métaux de transition
- Slides: 17