Nomenclature Composs ioniques binaires Composs ioniques forms dions
Nomenclature Composés ioniques binaires Composés ioniques formés d’ions polyatomiques Composés covalents Acides
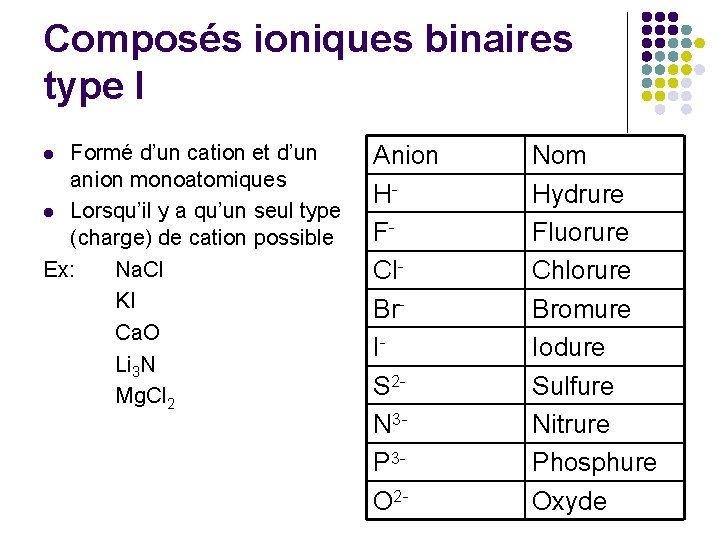
Composés ioniques binaires type I Formé d’un cation et d’un anion monoatomiques l Lorsqu’il y a qu’un seul type (charge) de cation possible Ex: Na. Cl KI Ca. O Li 3 N Mg. Cl 2 l Anion HFCl. Br. IS 2 N 3 P 3 O 2 - Nom Hydrure Fluorure Chlorure Bromure Iodure Sulfure Nitrure Phosphure Oxyde

Nommez l l l Al. Br 3 KF Ca. S l l l Bromure d’aluminium Fluorure de potassium Sulfure de calcium

Composés ioniques binaires type II Formé d’un cation et d’un anion monoatomiques l Lorsqu’il y a plusieurs types (charge) de cations possible Ex: Cu. Cl Fe 2 O 3 Mn. O 2 Pb. I 2 l

Nommez l l l Ni. O Ni 2 O 3 Cs. F Ti. O 2 Ag 2 S Sr 3 P 2 l l l Oxyde de nickel (II) Oxyde de nickel (III) Fluorure de césium Oxyde de titane (IV) Sulfure d’argent Phosphure de strontium
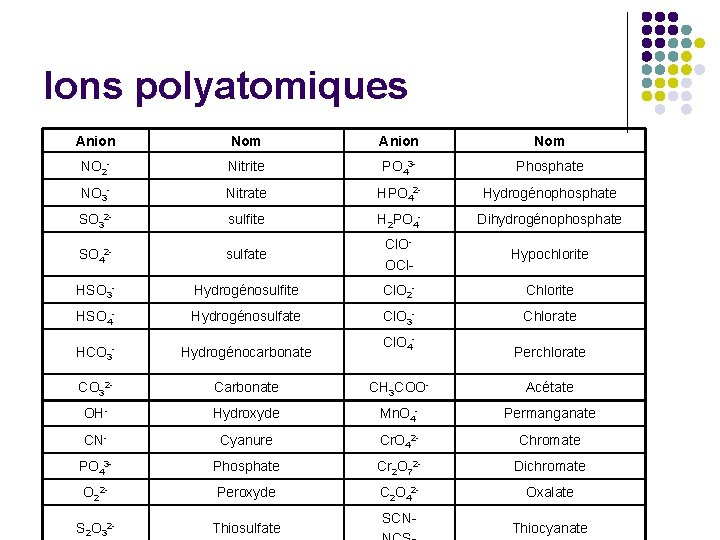
Ions polyatomiques Anion Nom NO 2 - Nitrite PO 43 - Phosphate NO 3 - Nitrate HPO 42 - Hydrogénophosphate SO 32 - sulfite H 2 PO 4 - Dihydrogénophosphate SO 42 - sulfate Cl. OOCl- Hypochlorite HSO 3 - Hydrogénosulfite Cl. O 2 - Chlorite HSO 4 - Hydrogénosulfate Cl. O 3 - Chlorate Cl. O 4 - HCO 3 - Hydrogénocarbonate CO 32 - Carbonate CH 3 COO- Acétate OH- Hydroxyde Mn. O 4 - Permanganate CN- Cyanure Cr. O 42 - Chromate PO 43 - Phosphate Cr 2 O 72 - Dichromate O 22 - Peroxyde C 2 O 42 - Oxalate S 2 O 32 - Thiosulfate SCN- Perchlorate Thiocyanate

exemples l l l Na 2 SO 4 Fe(NO 3)3 Mn(OH)2 Na. OCl Na. HCO 3 Cr. SO 3 l l l Sulfate de sodium Nitrate de fer (III) Hydroxyde de manganèse (II) Hypochlorite de sodium Hydrogénocarbonate de sodium Sulfite de chrome (II)

Composés covalents (2 non-métaux) l l Utilisez les préfixes pour les quantités d’ions Exemples: l PCl 5 PCl 3 SF 6 SO 3 SO 2 CO 2 P 4 O 6 l l l Pentachlorure de phosphore Trichlorure de phosphore Hexafluorure de soufre Trioxyde de soufre Dioxyde de carbone Hexoxyde de tétraphosphore

Acides l l l l Acides sans oxygène (hydrique) HF acide fluorhydrique HI acide iodhydrique HCl HBr HCN H 2 S l l l l l Acides avec oxygène Ions ate rique Ions ite reux HNO 3 HNO 2 H 2 SO 4 H 2 SO 3 H 3 PO 4 CH 3 COOH
- Slides: 9