NOMENCLATURA INORGNICA PARTE 2 COMPUESTOS BINARIOS HIDROGENADOS Colegio

NOMENCLATURA INORGÁNICA PARTE 2: “COMPUESTOS BINARIOS HIDROGENADOS”. Colegio Agustiniano El Bosque Un proyecto educativo único y propio Ciencias Naturales Química / I medio
Objetivos y contenidos a tratar Contenidos v Nomenclatura de Compuestos Binarios Hidrogenados. ü Hidruros metálicos ü Hidruros no metálicos ü Hidrácidos o haluros de hidrógeno Objetivos v Conocer, comprender y aplicar de manera correcta la nomenclatura de compuestos BINARIOS HIDROGENADOS.

ORIENTACIONES PARA EL ESTUDIO DE ESTE TEMA… Pon atención a los siguientes puntos para poder ayudar a poder desarrollar de mejor manera esta presentación: Ø Te recomiendo contar con un lugar para poder estudiar, no debe ser una sala de estudio, puede ser el comedor de tu casa, lo importante es que lo ordenes y acomodes para ti y tus artículos de estudio. Ø Por unos minutos desconéctate del celular, has de cuenta que estas en la sala de clases y deja el móvil en silencio. Ø Organiza tu tiempo y mantén una continuidad de principio a fin de esta presentación, lo que te permitirá no perder el hilo de el o los temas a estudiar. Ø Lee con atención y calma la información que recibirás así como las instrucciones para los desafíos o ejercitación que se encuentra al final de esta presentación. Ø Visita cada link sugerido ya sea durante la presentación o al final de ella, dado que tienen como objetivo poder explicar o reforzar de una manera distinta el contenido abordado. Ø Cuando apliques lo aprendido, trata en primera instancia de resolverlo por ti mismo, cuando ya no logres hacerlo pasa a apoyarte de las diapositivas anteriores o del texto escolar, luego al finalizar, podrás siempre encontrar el solucionario de la actividad en esta presentación. Ø No es necesario imprimir estas diapositivas, para realizar la actividad será suficiente con que la registres en tu cuaderno de asignatura, sino lo posees podrás realizarlo en una hoja anexa que luego podrás pegar en tu cuaderno. Ø Para todos los temas que se traten, en esta y en todas las presentaciones que trabajemos, podrás apoyarte del texto escolar. De no poseerlo, se adjuntará en cada ppt el link para verlo en línea. Ø Lo más importante es que confíes en tus capacidades, eres capaz de lograr lo que te propongas.

PARA NO OLVIDAR… Lo primero que debemos saber al comenzar este nuevo tema, es cual es el significado de la palabra “NOMENCLATURA” Se define como “nomenclatura química” es un conjunto de reglas o fórmulas que se utilizan para nombrar los compuestos químicos. La IUPAC (Unión Internacional de Química Pura y Aplicada; en inglés International Union of Pure and Applied Chemistry) es la máxima autoridad en esta materia, y se encarga de establecer las reglas correspondientes, para poder nombrar estos compuestos.
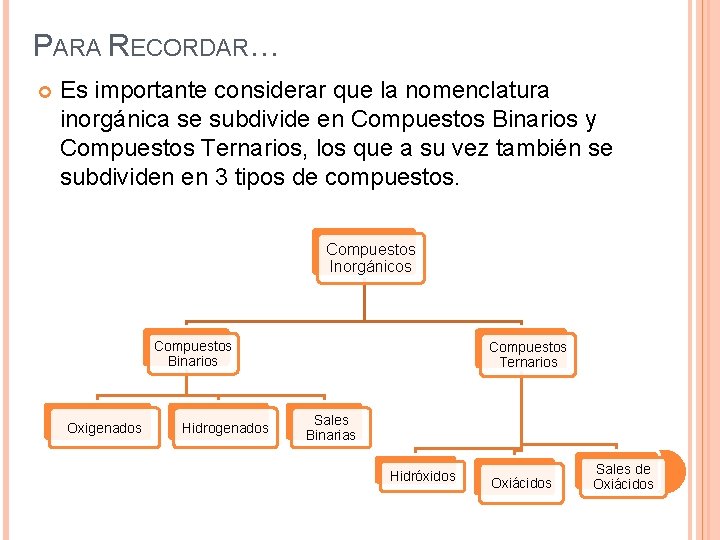
PARA RECORDAR… Es importante considerar que la nomenclatura inorgánica se subdivide en Compuestos Binarios y Compuestos Ternarios, los que a su vez también se subdividen en 3 tipos de compuestos. Compuestos Inorgánicos Compuestos Binarios Oxigenados Hidrogenados Compuestos Ternarios Sales Binarias Hidróxidos Oxiácidos Sales de Oxiácidos
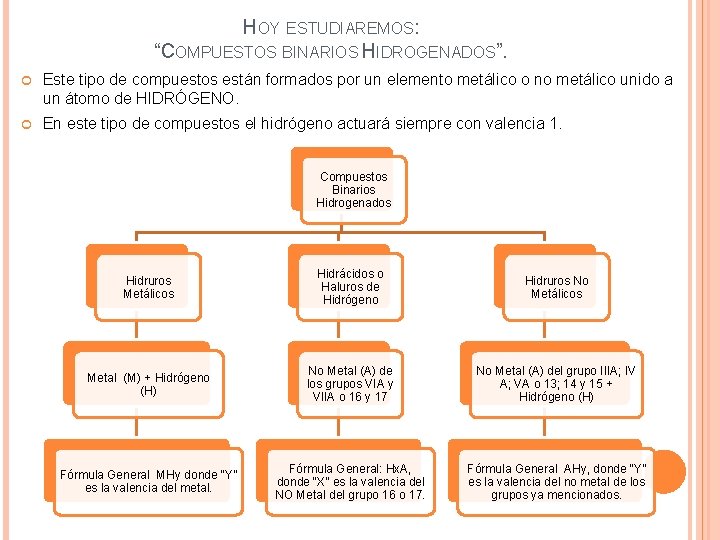
HOY ESTUDIAREMOS: “COMPUESTOS BINARIOS HIDROGENADOS”. Este tipo de compuestos están formados por un elemento metálico o no metálico unido a un átomo de HIDRÓGENO. En este tipo de compuestos el hidrógeno actuará siempre con valencia 1. Compuestos Binarios Hidrogenados Hidruros Metálicos Hidrácidos o Haluros de Hidrógeno Hidruros No Metálicos Metal (M) + Hidrógeno (H) No Metal (A) de los grupos VIA y VIIA o 16 y 17 No Metal (A) del grupo IIIA; IV A; VA o 13; 14 y 15 + Hidrógeno (H) Fórmula General MHy donde “Y” es la valencia del metal. Fórmula General: Hx. A, donde “X” es la valencia del NO Metal del grupo 16 o 17. Fórmula General AHy, donde “Y” es la valencia del no metal de los grupos ya mencionados.
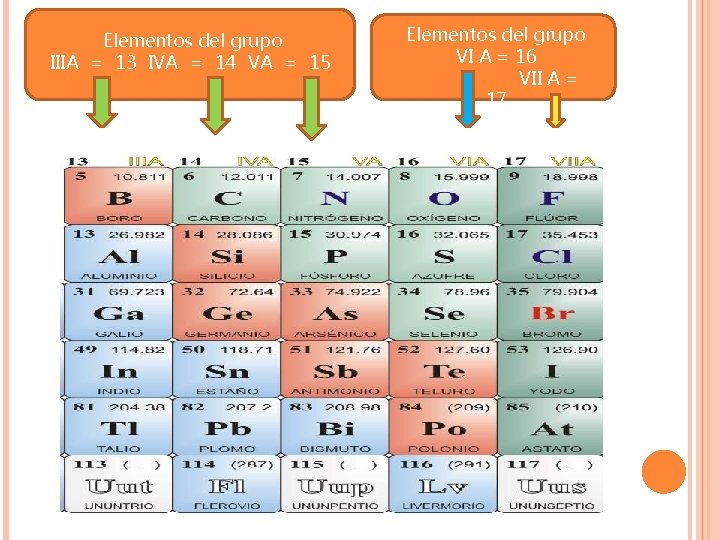
Elementos del grupo IIIA = 13 IVA = 14 VA = 15 Elementos del grupo VI A = 16 VII A = 17

1. - HIDRUROS METÁLICOS METAL (M) + HIDRÓGENO (H) Para poder formular compuestos hidruros metálicos, debemos saber que: Ø Primero recordar que la valencia del Hidrógeno (H), será siempre 1. Ø Para escribir la fórmula química de un hidruro metálico, primero escribiremos el símbolo del metal y luego el del Hidrógeno, esto se debe a que a la derecha siempre irá el elemento más electronegativo y al comparar los metales con el hidrógeno éste será siempre mayor. Ej. : Mg 1 H 2 Ø Es importante recordar que no debes saber de memoria las valencias, solo debes utilizar la tabla periódica, el texto escolar o ayuda de la web. Ø La valencia del metal ira después del símbolo del Hidrógeno y la valencia del Hidrógeno irá siempre bajo el metal, en pocas palabras se intercambian o cruzan sus valencias, pero recuerda que el 1 no se escribe, por lo que bajo del Metal nunca habrá un número, lo que no quiere decir que no haya valencia, es solo que no la escribiremos sabiendo que es “ 1”. Ej. : Mg su valencia es 2 // Hidrógeno su valencia es 1 Por lo tanto sería Mg. H 2 (el 1 en química no se escribe)
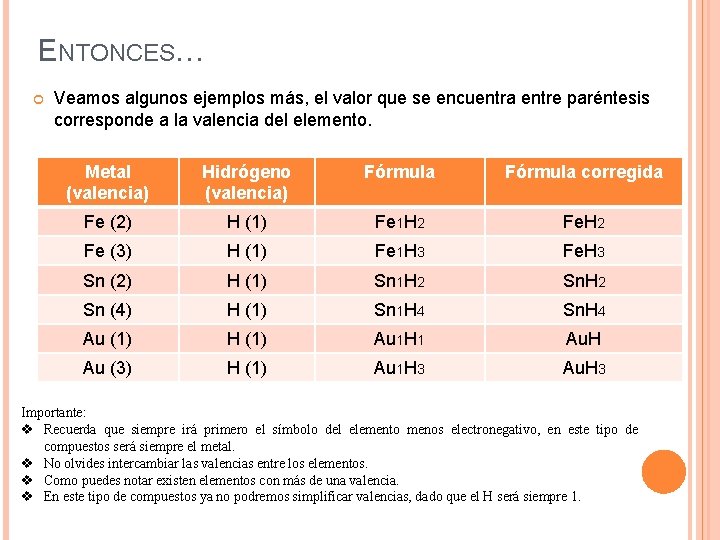
ENTONCES… Veamos algunos ejemplos más, el valor que se encuentra entre paréntesis corresponde a la valencia del elemento. Metal (valencia) Hidrógeno (valencia) Fórmula corregida Fe (2) H (1) Fe 1 H 2 Fe (3) H (1) Fe 1 H 3 Fe. H 3 Sn (2) H (1) Sn 1 H 2 Sn (4) H (1) Sn 1 H 4 Sn. H 4 Au (1) H (1) Au 1 H 1 Au. H Au (3) H (1) Au 1 H 3 Au. H 3 Importante: v Recuerda que siempre irá primero el símbolo del elemento menos electronegativo, en este tipo de compuestos será siempre el metal. v No olvides intercambiar las valencias entre los elementos. v Como puedes notar existen elementos con más de una valencia. v En este tipo de compuestos ya no podremos simplificar valencias, dado que el H será siempre 1.

¿Y CÓMO SE NOMBRAN? Según IUPAC existen 2 formas de nombrar los compuestos llamadas “SISTEMÁTICA” y “STOCK”. Existía una tercera forma llamada “Tradicional”, pero desde el 2005 fue eliminada por la IUPAC. Ejemplo: Fórmula Fe. H 3 Pasos Sistemática (antes de comenzar con esta nomenclatura, observa la siguiente dispositiva) Stock Paso 1 Escribe el prefijo correspondiente al número de átomos de Hidrógeno, seguido de la palabra HIDRURO Escribir la palabra hidruro de… Paso 2 Escribir la preposición “de” Escribir el nombre del metal Paso 3 Como H será siempre 1, bajo el metal jamás habrá un número por lo que no habrá prefijos para el metal, escribiendo directamente su nombre. Escribir en números romanos la VALENCIA DEL METAL, ojo no es la valencia del Hidrógeno, solo la del metal. En este caso NO se trabaja con las valencias simplificadas, dado que no se puede simplificar. Si el metal solo posee una valencia NO será necesario escribirla en números romanos. Trihidruro de hierro Hidruro de Hierro (III) Nombre
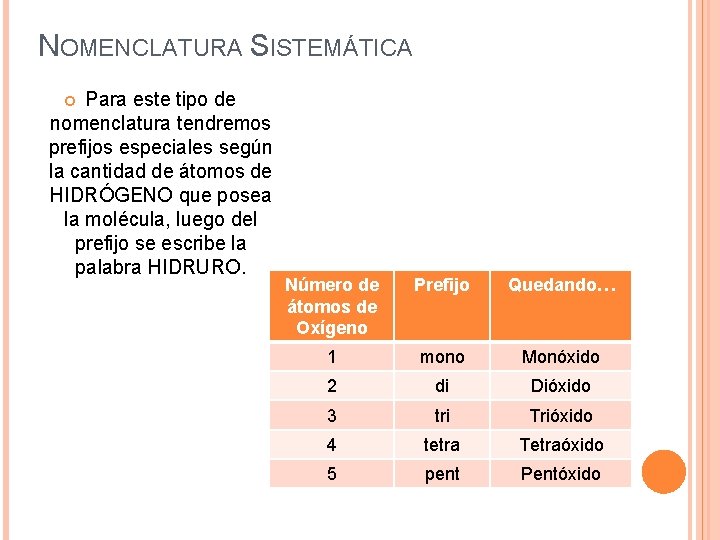
NOMENCLATURA SISTEMÁTICA Para este tipo de nomenclatura tendremos prefijos especiales según la cantidad de átomos de HIDRÓGENO que posea la molécula, luego del prefijo se escribe la palabra HIDRURO. Número de átomos de Oxígeno Prefijo Quedando… 1 mono Monóxido 2 di Dióxido 3 tri Trióxido 4 tetra Tetraóxido 5 pent Pentóxido

2. - HIDRUROS NO METÁLICOS NO METAL (A) + HIDRÓGENO (H) Para poder formular compuestos hidruros NO metálicos, debemos saber que: Ø Primero recordar que la valencia del Hidrógeno (H), será siempre 1. Ø Para escribir la fórmula química de un hidruro no metálico, primero escribiremos el símbolo del no metal y luego el del hidrógeno, esto se debe a que a la derecha siempre irá el elemento más electronegativo y al comparar los no metales en general con el hidrógeno éste será siempre mayor. Ej. : P 1 H 3 Ø Es importante recordar que no debes saber de memoria las valencias, solo debes utilizar la tabla periódica, el texto escolar o ayuda de la web. Ø La valencia del no metal ira después del símbolo del Hidrógeno y la valencia del hidrógeno irá siempre bajo el no metal, en pocas palabras se intercambian o cruzan sus valencias, como en este caso la valencia del hidrógeno será siempre 1, por lo que no se escribe. Ej. : P su valencia es 3 // Hidrógeno su valencia es 1 Ø Al cruzar sus valencias como se nos indica sería P 1 H 3, no podemos simplificar, pero tampoco podemos escribir el 1, por lo queda: PH 3.
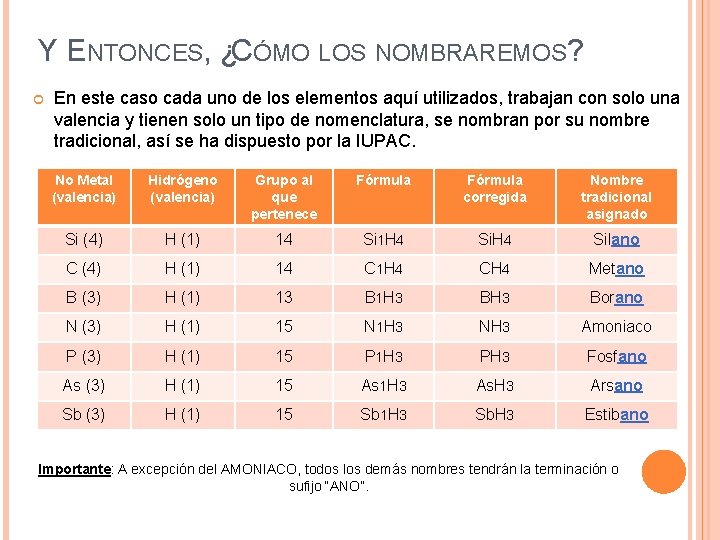
Y ENTONCES, ¿CÓMO LOS NOMBRAREMOS? En este caso cada uno de los elementos aquí utilizados, trabajan con solo una valencia y tienen solo un tipo de nomenclatura, se nombran por su nombre tradicional, así se ha dispuesto por la IUPAC. No Metal (valencia) Hidrógeno (valencia) Grupo al que pertenece Fórmula corregida Nombre tradicional asignado Si (4) H (1) 14 Si 1 H 4 Silano C (4) H (1) 14 C 1 H 4 CH 4 Metano B (3) H (1) 13 B 1 H 3 Borano N (3) H (1) 15 N 1 H 3 NH 3 Amoniaco P (3) H (1) 15 P 1 H 3 PH 3 Fosfano As (3) H (1) 15 As 1 H 3 As. H 3 Arsano Sb (3) H (1) 15 Sb 1 H 3 Sb. H 3 Estibano Importante: A excepción del AMONIACO, todos los demás nombres tendrán la terminación o sufijo “ANO”.

3. - HIDRÁCIDOS O HALUROS DE HIDRÓGENO (H) + NO METAL (A) Para poder formular compuestos hidrácidos, debemos saber que: Ø Primero recordar que la valencia del Hidrógeno (H), será siempre 1. Ø Para escribir la fórmula química de un hidrácido, primero escribiremos el símbolo del Hidrógeno y luego el del NO METAL. Ej. : H 1 Cl 1 Ø Es importante recordar que no debes saber de memoria las valencias, solo debes utilizar la tabla periódica, el texto escolar o ayuda de la web. Ø La valencia del no metal ira después del símbolo del Hidrógeno y la valencia del hidrógeno irá siempre bajo el no metal, en pocas palabras se intercambian o cruzan sus valencias, como en este caso la valencia del hidrógeno será siempre 1, entonces no se escribe. Ej. : Cl su valencia es 1 // Hidrógeno su valencia es 1 Ø Al cruzar sus valencias como se nos indica sería H 1 Cl 1, no podemos simplificar, pero tampoco podemos escribir el 1, por lo queda: HCl. Ø IMPORTANTE: v Los elementos NO Metálicos del grupo 16, actuarán siempre con valencia 2. v Los elementos No Metálicos del grupo 17, actuarán siempre con valencia 1.
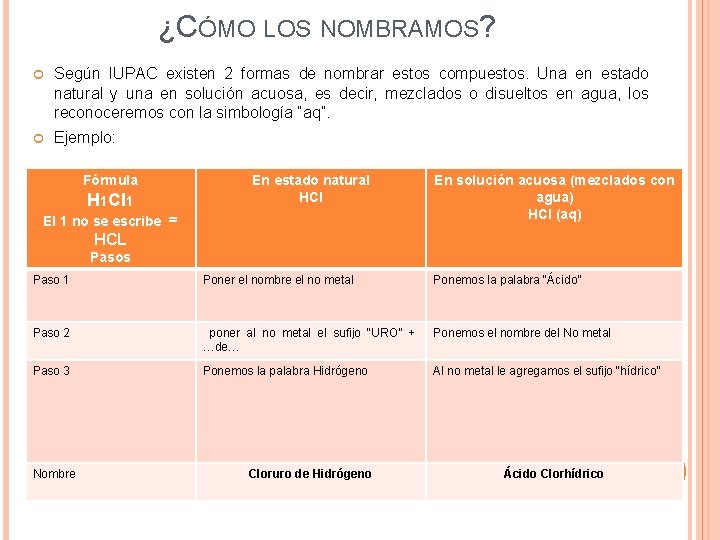
¿CÓMO LOS NOMBRAMOS? Según IUPAC existen 2 formas de nombrar estos compuestos. Una en estado natural y una en solución acuosa, es decir, mezclados o disueltos en agua, los reconoceremos con la simbología “aq”. Ejemplo: Fórmula H 1 Cl 1 El 1 no se escribe = En estado natural HCl En solución acuosa (mezclados con agua) HCl (aq) HCL Pasos Paso 1 Poner el nombre el no metal Ponemos la palabra “Ácido” Paso 2 poner al no metal el sufijo “URO” + …de… Ponemos el nombre del No metal Paso 3 Ponemos la palabra Hidrógeno Al no metal le agregamos el sufijo “hídrico” Nombre Cloruro de Hidrógeno Ácido Clorhídrico
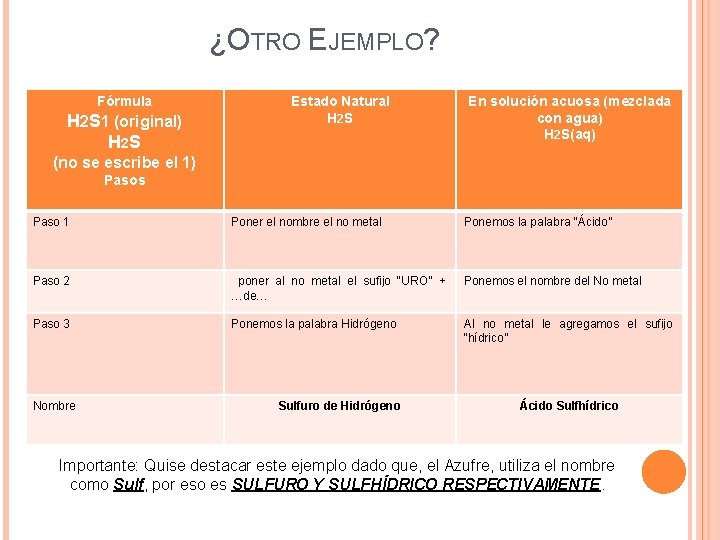
¿OTRO EJEMPLO? Fórmula H 2 S 1 (original) H 2 S Estado Natural H 2 S En solución acuosa (mezclada con agua) H 2 S(aq) (no se escribe el 1) Pasos Paso 1 Poner el nombre el no metal Ponemos la palabra “Ácido” Paso 2 poner al no metal el sufijo “URO” + …de… Ponemos el nombre del No metal Paso 3 Ponemos la palabra Hidrógeno Al no metal le agregamos el sufijo “hídrico” Nombre Sulfuro de Hidrógeno Ácido Sulfhídrico Importante: Quise destacar este ejemplo dado que, el Azufre, utiliza el nombre como Sulf, por eso es SULFURO Y SULFHÍDRICO RESPECTIVAMENTE.

PARA COMPLEMENTAR… Te invito a visitar el siguiente link para poder resumir lo visto durante esta presentación. https: //www. youtube. com/watch? v=wkqo. Qjpx. AUk

¿Y ? A R O AH
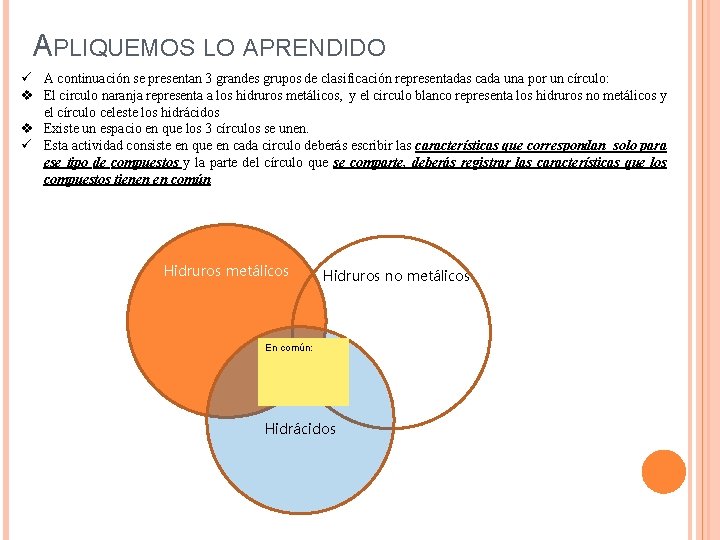
APLIQUEMOS LO APRENDIDO ü A continuación se presentan 3 grandes grupos de clasificación representadas cada una por un círculo: v El circulo naranja representa a los hidruros metálicos, y el circulo blanco representa los hidruros no metálicos y el círculo celeste los hidrácidos v Existe un espacio en que los 3 círculos se unen. ü Esta actividad consiste en que en cada circulo deberás escribir las características que correspondan solo para ese tipo de compuestos y la parte del círculo que se comparte, deberás registrar las características que los compuestos tienen en común Hidruros metálicos Hidruros no metálicos En común: Hidrácidos

Antes de seguir con el ppt realiza tu propio trabajo, luego continúa para comparar los resultados.
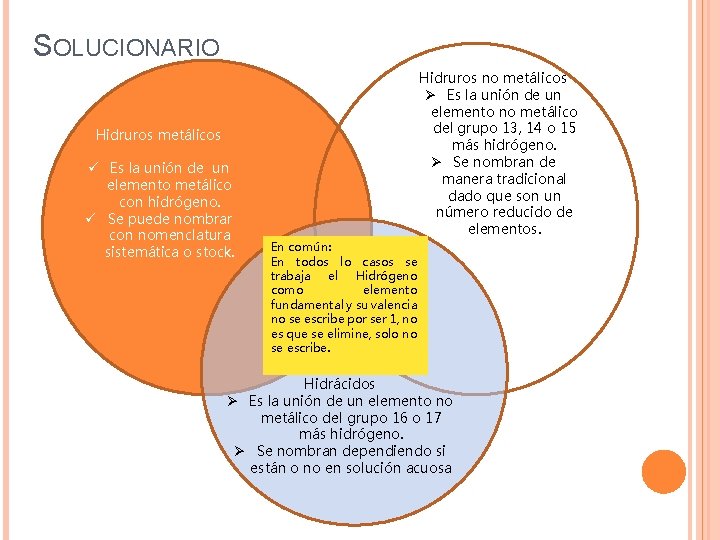
SOLUCIONARIO Hidruros no metálicos Ø Es la unión de un elemento no metálico del grupo 13, 14 o 15 más hidrógeno. Ø Se nombran de manera tradicional dado que son un número reducido de elementos. Hidruros metálicos ü Es la unión de un elemento metálico con hidrógeno. ü Se puede nombrar con nomenclatura sistemática o stock. En común: En todos lo casos se trabaja el Hidrógeno como elemento fundamental y su valencia no se escribe por ser 1, no es que se elimine, solo no se escribe. Hidrácidos Ø Es la unión de un elemento no metálico del grupo 16 o 17 más hidrógeno. Ø Se nombran dependiendo si están o no en solución acuosa

Además puedes utilizar el texto escolar, si no tienes tu texto escolar puedes utilizarlo vía web desde la página: https: //www. curriculumnacional. cl/614/w 3 -article 140104. html

MUCHAS GRACIAS POR SU ATENCIÓN.
- Slides: 23