Nomenclatura Definicin del valor tpico T de los










































- Slides: 61

Nomenclatura Definición del valor típico (T) de los no metales (n. M) Proceso inductivo deductivo para conocer las valencias de los elementos representativos y su nombre relativo fórmulas generales para ácidos y sales Autor: IQ Luis Fernando Montoya Valencia. luismontoy@une. net. co Profesor titular Centro de Ciencia Básica Escuela de ingenierías Universidad Pontificia Bolivariana A un “Clic” del conocimiento http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es

En este trabajo encontramos. Una fundamentación teórica, relacionada desde lo cotidiano resumida en un algoritmo Varios ejemplos orientados desde el algoritmo El reto es “IMAGINAR” (respaldado en el algoritmo), que va a aparecer con el siguiente “clic”, si estamos de acuerdo continuar, y si no regresar para al final poder afirmar: ! lo hicimos ¡ Para desarrollar competencias que permitan: Dominar los no metales, su valor típico, sus valencias y nombres relativos Identificar las fórmulas generales de las funciones químicas Saber nombrar una formula química Saber formular un nombre Hacer las diferentes combinaciones de un elemento con H, con O con H & O A un “Clic” del conocimiento http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es

LA NOMENCLATURA NO ES MEMORIA PERO TAMPOCO IGNORANCIA 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

CONSIDERACIONES GENERALES Los elementos existentes en la naturaleza pueden clasificarse como metales (M) y como no metales (n. M). Los n. M poseen alta electronegatividad y tienden a ganar electrones para adquirir CARGA NEGATIVA. Los M poseen baja electronegatividad y tienden a perder electrones para adquirir CARGA POSITIVA. El oxígeno (O) es el segundo elemento más electronegativo de la tabla periódica, sólo superado por el flúor. El hidrógeno (H) tiene una electronegatividad intermedia y adquiere carga positiva o negativa dependiendo si se combina con un n. M o con un M Todos los elementos, M y n. M, pueden combinarse con H, con O o con H y O para formar compuestos clasificados en grupos funcionales. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

VALENCIA Es la capacidad de enlace que posee un elemento. Al hacer la fórmula del compuestos se tiene que lograr neutralidad eléctrica y esto se obtiene haciendo el intercambio de valencias. La fórmula del compuesto formado por los elementos X de valencia x y Z de valencia z, siendo Z más electronegativo que X es: Z X X z Zx z x Esto es el intercambio de valencias Z adquiere carga – z por ser más electronegativo X adquiere carga + x por ser menos electronegativo Para establecer el orden en una fórmula, primero va la parte positiva y luego la parte negativa La carga real (en compuestos iónicos) o la carga aparente (en compuestos covalentes ) de un elemento en un compuesto se llama: “número de oxidación” 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

VALORES DE VALENCIA Para los elementos representativos, (los que están en los grupos de la tabla periódica) las valencias se obtienen a partir del número del grupo con restas sucesivas de dos en dos, ya que se obtienen con el número de electrones desapareados en la distribución electrónica normal o en la distribución electrónica excitada. Grupo VII, las valencias son: 7, 5, 3, 1 Grupo VI, las valencias son: 6, 4, 2 Grupo las valencias son: 5, 3, 1 V, Grupo IV, las valencias son: 4, 2 Grupo III, las valencias son: 3, 1 Grupo II, la valencia es: 2 Grupo I, la valencia es: 1 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

NOMBRE DE UN ELEMENTO SEGÚN EL VALOR RELATIVO DE SU VALENCIA Si el elemento posee dos valores de valencia usamos los sufijos comparativos ico (indica mayor) y oso (indica menor). Si posee tres valores de valencia la “menos menor” exige el prefijo superlativo hipo y el sufijo comparativo oso. Si el elemento posee cuatro valores de valencia además de hipo-oso de la valencia “menos menor” también se requiere para la valencia “más mayor” el prefijo superlativo per y el sufijo ico. Si solo posee un valor valencia se indica con el sufijo ico (si en una familia sólo hay un hijo, se dice que es “hijo único”) Para el n. M en las sales oxisales el sufijo ico cambia por ato y el sufijo oso cambia por ito. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

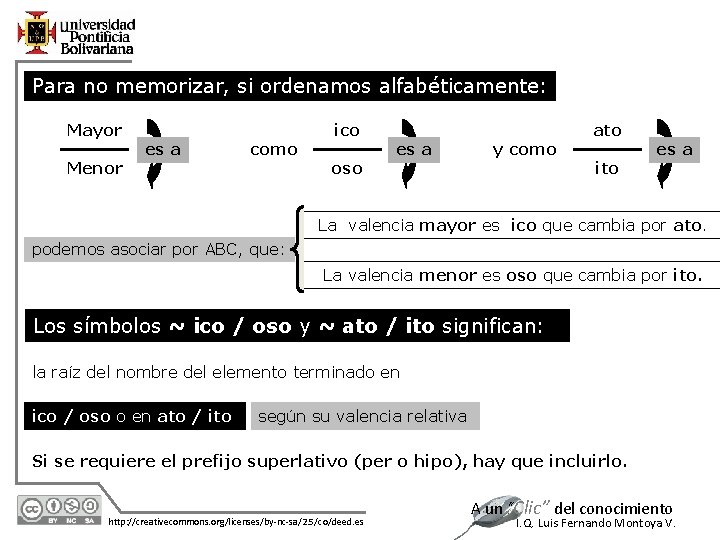
Para no memorizar, si ordenamos alfabéticamente: Mayor Menor ico es a como oso ato es a y como ito es a La valencia mayor es ico que cambia por ato. podemos asociar por ABC, que: La valencia menor es oso que cambia por ito. Los símbolos ~ ico / oso y ~ ato / ito significan: la raíz del nombre del elemento terminado en ico / oso o en ato / ito según su valencia relativa Si se requiere el prefijo superlativo (per o hipo), hay que incluirlo. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

DEFINICIÓN DEL VALOR TÍPICO (T) Para los n. M el valor típico T es la “deficiencia de la norma del octeto”. T es útil como subíndice del H en los ácidos normales. Un ácido es una fórmula que inicia por H. Los valores de T, según el grupo, son: Grupo VII, T=1 Grupo VI, T=2 Grupo V, T=3 excepto el Nitrógeno que es especial cuya T = 1 El nitrógeno (N) es tan especial que origina la química de aminoácidos. Grupo IV, T=4 excepto el Carbono que es especial cuya T = 2 El carbono (C) es tan especial que origina la química orgánica. Grupo III, T=3 Es mas fácil para el Boro (Z = 5) perder tres electrones (isoelectrónico con el Helio, Z = 2) que ganar cinco (isoelectrónico con el Neon, Z = 10) 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Existen dos casos “raros” de metales que actúan como no metal sus parámetros como no Metal (n. M) son: Cromo (Cr) y manganeso (Mn) con T = 2 y V = 6, con ésta valencia el sufijo es ico por similitud con el grupo VI (crómico y mangánico) y en oxisales cromato y manganato. Manganeso (Mn) con T = 1 y V = 7, con ésta valencia se usa el prefijo per y el sufijo ico (permangánico) por similitud con el grupo VII, y en oxisales permanganato. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

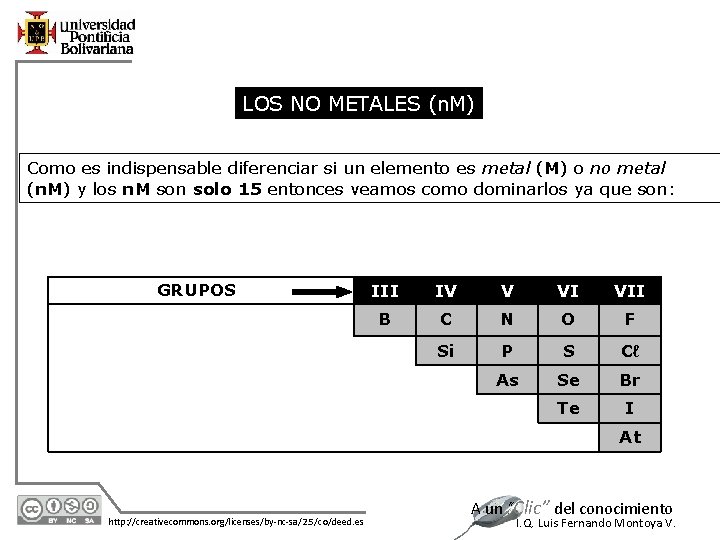
LOS NO METALES (n. M) Como es indispensable diferenciar si un elemento es metal (M) o no metal (n. M) y los n. M son solo 15 entonces veamos como dominarlos ya que son: GRUPOS III IV V VI VII B C N O F Si P S Cℓ As Se Br Te I At 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

ACRÒSTICO SUGERIDO PARA DOMINAR LOS NO METALES Grupo VII: Como siete es el número perfecto y el mas común en la Biblia, lo llamaremos el grupo de Cristo porque Cristo “Fue Cℓavado Para asociar: Flúor, Cℓoro, Brutalmente I Bromo, Atado” Iodo (o mejor Yodo) y Astato. Grupo VI : Como este grupo está antes del VII (el de Cristo), entonces sería el “Anticristo” y según nuestras abuelas el diablo huele a Azufre (Sulfur), por eso el S está en este grupo, diríamos: “Ojala Satán Para asociar Oxigeno, azufre (S), 12/7/2020 Se Selenio y http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Tenga” Telurio, A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Grupo V: Como no hay quinto malo, este es el grupo de las relaciones Colombo. Argentinas en fútbol (¿será por el 5 -0? ). En las eliminatorias para el mundial del 1998: Dicho marcador no creo que se repita porque ya “No Puede Asprilla” Para asociar con Nitrógeno, Fósforo (Phosfor) y Arsénico (As) (no es Ar porque Ar es el símbolo del Argón) Grupo IV : Como ya sabemos 12 de los 15 n. M podemos afirmar que “Si - C” para asociar: Silicio y Carbono Grupo III : Solo nos falta exclamar “Bueno ya acabamos” para asociarlo con el Boro. Del listado de los n. M vamos a excluir el Oxígeno por ser formador de funciones y el Flúor por ser el único elemento más electronegativo que el oxígeno 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

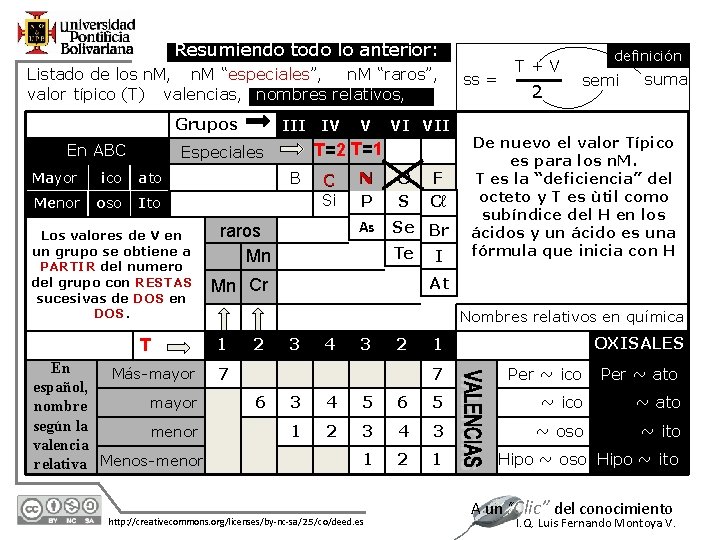
Resumiendo todo lo anterior: n. M “raros”, Listado de los n. M, n. M “especiales”, valor típico (T) valencias, nombres relativos, Grupos En ABC ico ato Menor oso Ito Los valores de V en un grupo se obtiene a PARTIR del numero del grupo con RESTAS sucesivas de DOS en DOS. T V VI VII T=2 T=1 Especiales Mayor B C Si raros Mn N P O S As Se Br Te I F Cℓ 2 definición semi suma De nuevo el valor Típico es para los n. M. T es la “deficiencia” del octeto y T es ùtil como subíndice del H en los ácidos y un ácido es una fórmula que inicia con H At Mn Cr Nombres relativos en química 1 En Más-mayor 7 español, mayor nombre según la menor valencia relativa Menos-menor 12/7/2020 III IV ss = T+V 2 6 3 4 3 2 OXISALES 1 7 Per ~ ico Per ~ ato 3 4 5 6 5 ~ ico ~ ato 1 2 3 4 3 ~ oso ~ ito 1 2 1 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Hipo ~ oso Hipo ~ ito A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

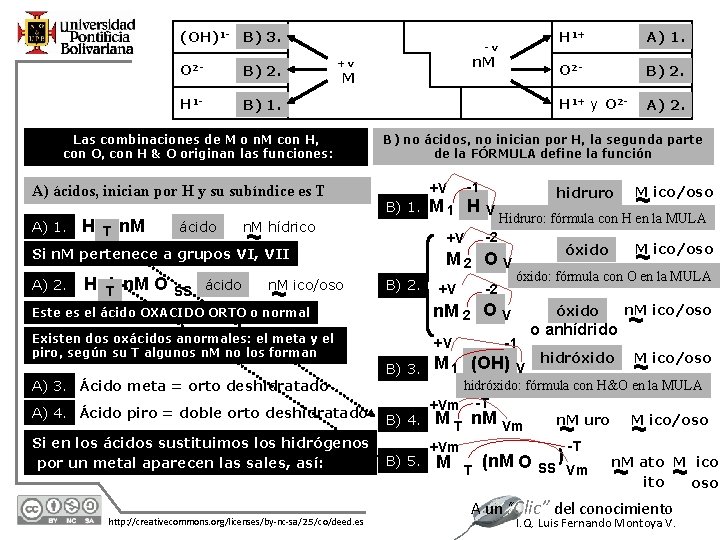
(OH)1 - B) 3. O 2 - B) 2. H 1 - B) 1. -v M Las combinaciones de M o n. M con H, con O, con H & O originan las funciones: A) ácidos, inician por H y su subíndice es T A) 1. H n. M ácido n. M +v A) 2. H n. M O SS ácido n. M ico/oso Existen dos oxácidos anormales: el meta y el piro, según su T algunos n. M no los forman B) 1. A) 4. Ácido piro = doble orto deshidratado Si en los ácidos sustituimos los hidrógenos por un metal aparecen las sales, así: 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es H M 1 O 2 - B) 2. H 1+ y O 2 - A) 2. M ico/oso ~ V Hidruro: fórmula con H en la MULA hidruro -2 +V M 2 O V B) 2. -2 +V M ico/oso ~ óxido: fórmula con O en la MULA óxido n. M 2 O V n. M ico/oso óxido -1 +V o anhídrido ~ hidróxido M ico/oso V hidróxido: fórmula con H&O en la MULA +Vm -T B) 4. M T n. M Vm n. M uro M ico/oso B) 3. A) 3. Ácido meta = orto deshidratado -1 +V n. M hídrico ~ Este es el ácido OXACIDO ORTO o normal T A) 1. B) no ácidos, no inician por H, la segunda parte de la FÓRMULA define la función ~ Si n. M pertenece a grupos VI, VII T H 1+ B) 5. ~ M 1 (OH) ~-T +Vm M T (n. M O SS ) Vm ~ n. M ato M ico ito oso ~ ~ A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

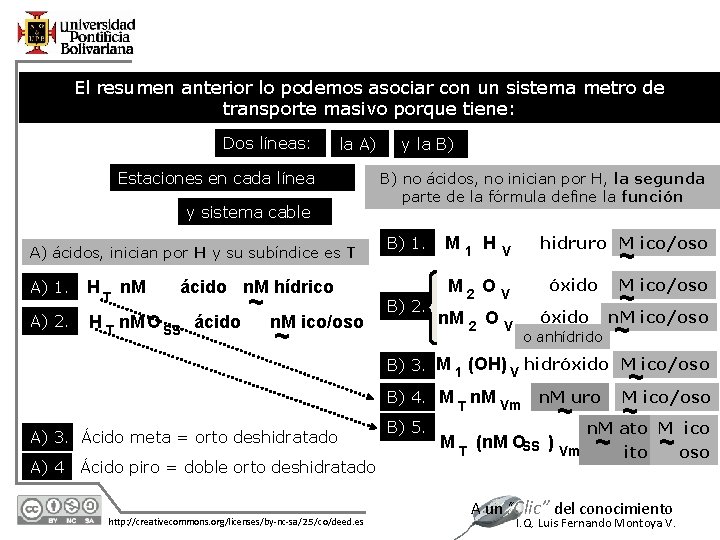
El resumen anterior lo podemos asociar con un sistema metro de transporte masivo porque tiene: Dos líneas: la A) Estaciones en cada línea y sistema cable A) ácidos, inician por H y su subíndice es T A) 1. A) 2. H T n. M ácido n. M hídrico H T n. M O SS ácido ~ n. M ico/oso y la B) B) no ácidos, no inician por H, la segunda parte de la fórmula define la función B) 1. B) 2. ~ M 1 H V M 2 OV n. M 2 O V hidruro M ico/oso ~ óxido o anhídrido M ico/oso ~ ~ n. M ico/oso B) 3. M 1 (OH) V hidróxido M ico/oso B) 4. A) 3. Ácido meta = orto deshidratado A) 4 Ácido piro = doble orto deshidratado 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es B) 5. ~ M T n. M Vm n. M uro M ico/oso ~ n. M ato ~ M ico M T (n. M OSS ) Vm ~ ito ~ oso A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Nota: Existen dos ácidos oxácidos anormales porque algunos n. M no los poseen y son: el meta y el piro Ácido meta = orto deshidratado, Ácido meta = HT - 2 n. MOSS -1 es decir orto A) 3. menos H 2 O 1 Ácido meta n. M ico/oso ~ solo existe si T > 2 por lo tanto es solo para: B, P, As y Si. Si T = 1 (Cℓ, Br, I, At y N), y si T = 2 (S, Se, Te y C) no existe el ácido meta para estos elementos. Ácido piro = doble orto deshidratado, Ácido piro = H 2 T - 2 n. M 2 OSS x 2 -1 es decir orto x 2 menos H 2 O 1 A) 4. Ácido piro n. M ico/oso ~ éste ácido solo existe si T > 1. Si T = 1 (Cℓ, Br, I, At y N), no existe el ácido piro para estos elementos. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

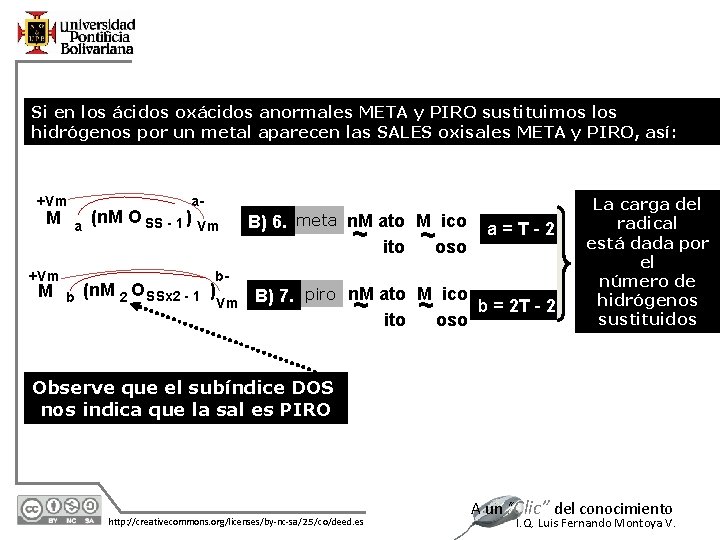
Si en los ácidos oxácidos anormales META y PIRO sustituimos los hidrógenos por un metal aparecen las SALES oxisales META y PIRO, así: a- +Vm M a b- +Vm M (n. M O SS - 1 ) Vm b (n. M 2 O SSx 2 - 1 ) Vm B) 6. meta n. M ato M ico ~ ito ~oso a=T-2 B) 7. piro n. M ato M ico ~ ito ~ oso b = 2 T - 2 La carga del radical está dada por el número de hidrógenos sustituidos Observe que el subíndice DOS nos indica que la sal es PIRO 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

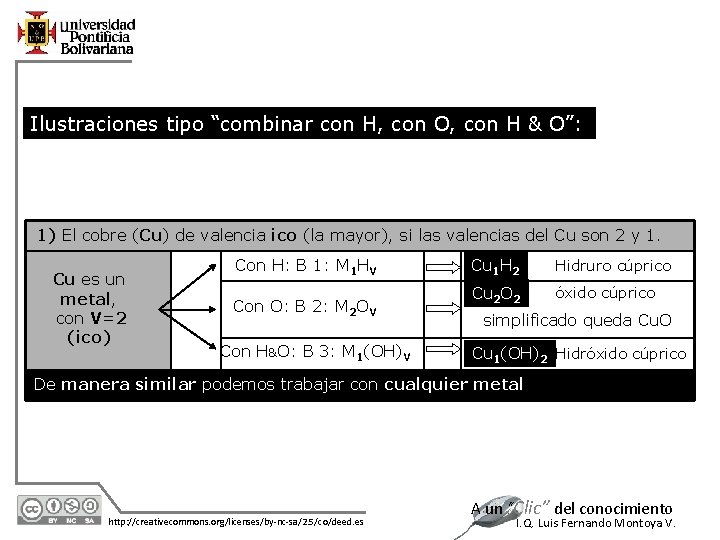
Ilustraciones tipo “combinar con H, con O, con H & O”: 1) El cobre (Cu) de valencia ico (la mayor), si las valencias del Cu son 2 y 1. Cu es un metal, con V=2 (ico) Con H: B 1: M 1 HV Con O: B 2: M 2 OV Con H&O: B 3: M 1(OH)V Cu 1 H 2 Hidruro cúprico Cu 2 O 2 óxido cúprico simplificado queda Cu. O Cu 1(OH)2 Hidróxido cúprico De manera similar podemos trabajar con cualquier metal 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

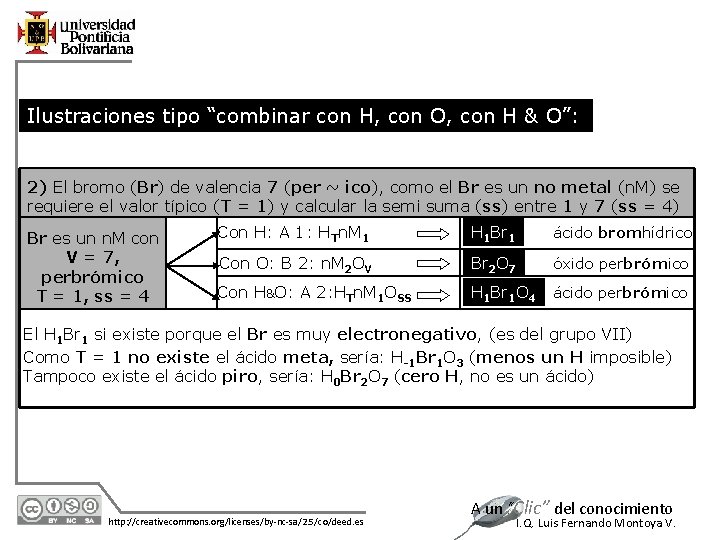
Ilustraciones tipo “combinar con H, con O, con H & O”: 2) El bromo (Br) de valencia 7 (per ~ ico), como el Br es un no metal (n. M) se requiere el valor típico (T = 1) y calcular la semi suma (ss) entre 1 y 7 (ss = 4) Br es un n. M con V = 7, perbrómico T = 1, ss = 4 Con H: A 1: HTn. M 1 H 1 Br 1 ácido bromhídrico Con O: B 2: n. M 2 OV Br 2 O 7 óxido perbrómico Con H&O: A 2: HTn. M 1 OSS H 1 Br 1 O 4 ácido perbrómico El H 1 Br 1 si existe porque el Br es muy electronegativo, (es del grupo VII) Como T = 1 no existe el ácido meta, sería: H-1 Br 1 O 3 (menos un H imposible) Tampoco existe el ácido piro, sería: H 0 Br 2 O 7 (cero H, no es un ácido) 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “combinar con H, con O, con H & O”: 3) El selenio (Se) de valencia 6 (~ ico), como el Se es un no metal (n. M) se requiere el valor del típico (T = 2) y calcular la semi suma (ss) entre 2 y 6 (ss = 4) Con H: A 1: HTn. M 1 Se es un n. M con v = 6, selénico T = 2, ss = 4 Con O: B 2: n. M 2 OV H 2 Se 1 ácido selenhídrico Se 2 O 6 óxido selénico Simplificado queda Se 1 O 3 H 2 Se 1 O 4 Con H&O: A 2: HTn. M 1 OSS ácido selénico El H 2 Se 1 si existe porque el Se es muy electronegativo, (es del grupo VI) Como T = 2 no existe el ácido meta, sería: El ácido meta con A 3: HT - 2 n. M OSS - 1 H 0 Se 1 O 3 Como T = 2 si existe el ácido piro, sería: El ácido piro con 12/7/2020 A 4: H 2 T - 2 n. M 2 OSSx 2 - 1 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es H 2 Se 2 O 7 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “combinar con H, con O, con H & O”: 4) El fósforo (P) de valencia 1 (hipo ~ oso), como el P es un no metal (n. M) se requiere el valor del típico (T = 3) y calcular la semi suma (ss) entre 3 y 1 (SS = 2) P es un n. M con V = 1, hipofosforoso T = 3, ss = 2 no existe como ácido Se “voltea” a PH 3 fosfina Con H: A 1: HTn. M 1 H 3 P 1 Con O: B 2: n. M 2 OV P 2 O 1 óxido hipofosforoso Con H&O: A 2: HTn. M 1 OSS H 3 P 1 O 2 ácido hipofosforoso Como T = 3 si existen los ácidos meta y piro, y sus formulas son: El ácido meta hipofosforoso es: A 3: HT - 2 n. M 1 OSS - 1 El ácido piro hipofosforoso es: A 4: H 2 T - 2 n. M 2 OSSx 2 - 1 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es H 1 P 1 O 1 H 4 P 2 O 3 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “cual es la formula de” Nombre Respuesta 1) Hidruro ferroso No inicia por H Función B 1: M 1 HV 2) Ácido perclórico Inicia por H Función A 2: HTn. M 1 OSS 3) Hidróxido cálcico No inicia por H Función B 3: M 1(OH)V 12/7/2020 Consideraciones: Las valencias (V) del M Fe son: 3 (mayor- ico) y 2 (menor oso) Fe 1 H 2 Consideraciones: La valencia per ~ ico del Cℓ es V= 7, por ser un n. M su T = 1 y la semisuma entre 1 y 7 es: SS =4 H 1 Cℓ 1 O 4 Consideraciones: Como el Ca es un M del grupo II su única valencia (v) es 2 (mayor ico), Ca 1(OH)2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

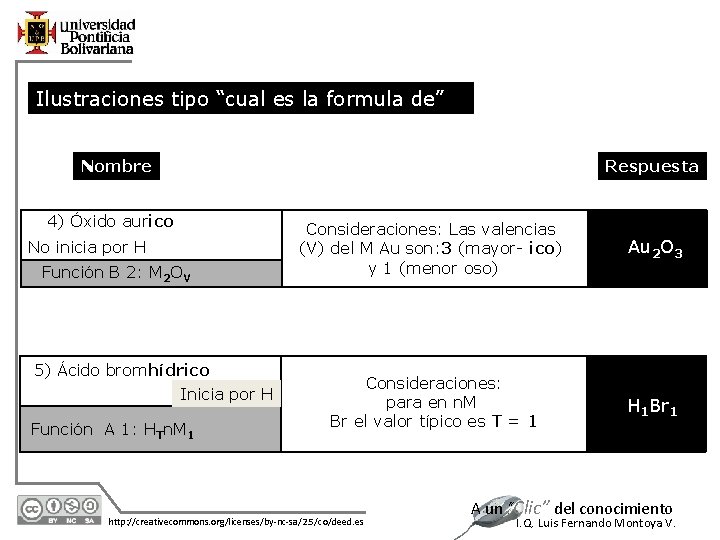
Ilustraciones tipo “cual es la formula de” Nombre 4) Óxido aurico No inicia por H Función B 2: M 2 OV 5) Ácido bromhídrico Inicia por H Función A 1: HTn. M 1 12/7/2020 Respuesta Consideraciones: Las valencias (V) del M Au son: 3 (mayor- ico) y 1 (menor oso) Au 2 O 3 Consideraciones: para en n. M Br el valor típico es T = 1 H 1 Br 1 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

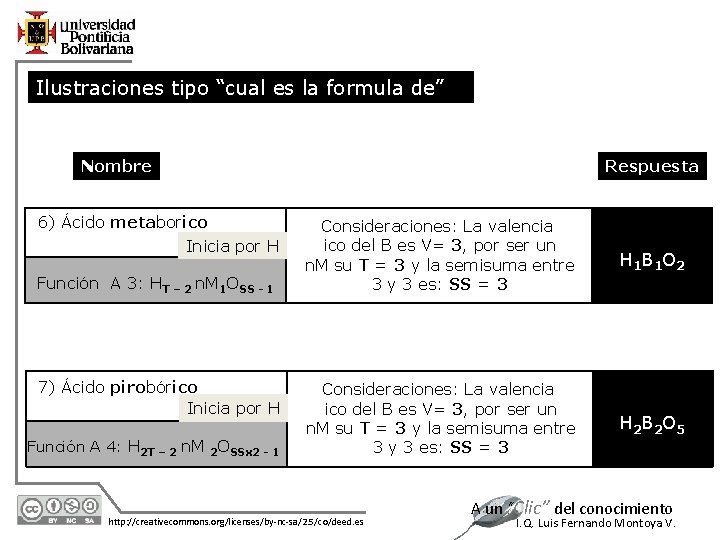
Ilustraciones tipo “cual es la formula de” Nombre 6) Ácido metaborico Inicia por H Función A 3: HT – 2 n. M 1 OSS - 1 7) Ácido pirobórico Inicia por H Función A 4: H 2 T – 2 n. M 2 OSSx 2 - 1 12/7/2020 Respuesta Consideraciones: La valencia ico del B es V= 3, por ser un n. M su T = 3 y la semisuma entre 3 y 3 es: SS = 3 H 1 B 1 O 2 Consideraciones: La valencia ico del B es V= 3, por ser un n. M su T = 3 y la semisuma entre 3 y 3 es: SS = 3 H 2 B 2 O 5 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

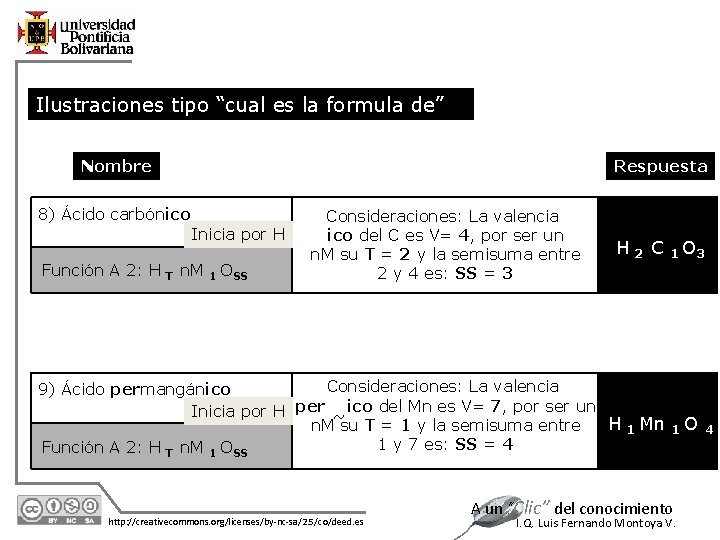
Ilustraciones tipo “cual es la formula de” Nombre Respuesta 8) Ácido carbónico Inicia por H Función A 2: H T n. M 1 OSS Consideraciones: La valencia ico del C es V= 4, por ser un n. M su T = 2 y la semisuma entre 2 y 4 es: SS = 3 H 2 C Consideraciones: La valencia 9) Ácido permangánico Inicia por H per ~ ico del Mn es V= 7, por ser un H 1 Mn n. M su T = 1 y la semisuma entre 1 y 7 es: SS = 4 Función A 2: H T n. M 1 OSS 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es 1 O 3 1 O A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V. 4

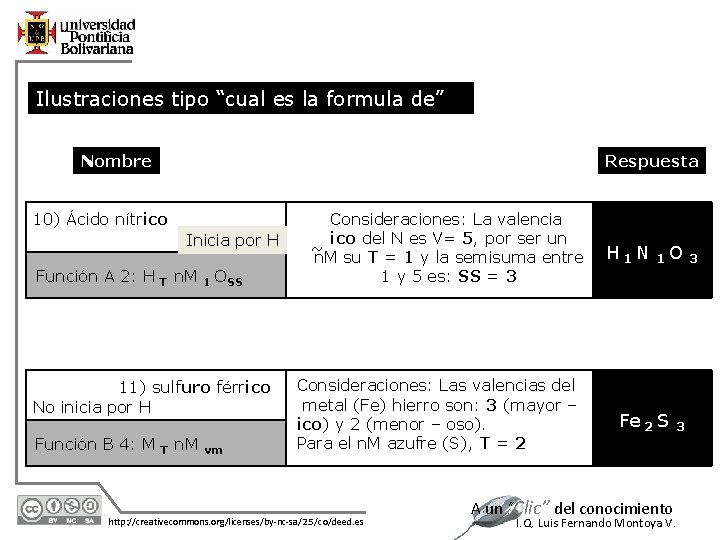
Ilustraciones tipo “cual es la formula de” Nombre Respuesta 10) Ácido nítrico Inicia por H Función A 2: H T n. M 1 OSS 11) sulfuro férrico No inicia por H Función B 4: M T n. M 12/7/2020 vm Consideraciones: La valencia ico del N es V= 5, por ser un ~ n. M su T = 1 y la semisuma entre 1 y 5 es: SS = 3 Consideraciones: Las valencias del metal (Fe) hierro son: 3 (mayor – ico) y 2 (menor – oso). Para el n. M azufre (S), T = 2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es H 1 N 1 O Fe 2 S A un “Clic” del conocimiento 3 I. Q. Luis Fernando Montoya V. 3

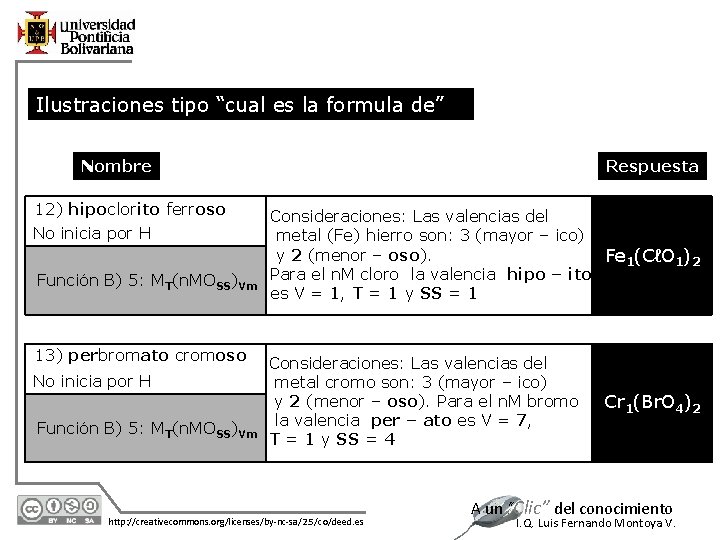
Ilustraciones tipo “cual es la formula de” Nombre 12) hipoclorito ferroso No inicia por H Función B) 5: MT(n. MOSS)Vm 13) perbromato cromoso No inicia por H Función B) 5: MT(n. MOSS)Vm 12/7/2020 Respuesta Consideraciones: Las valencias del metal (Fe) hierro son: 3 (mayor – ico) y 2 (menor – oso). Fe 1(CℓO 1)2 Para el n. M cloro la valencia hipo – ito es V = 1, T = 1 y SS = 1 Consideraciones: Las valencias del metal cromo son: 3 (mayor – ico) y 2 (menor – oso). Para el n. M bromo la valencia per – ato es V = 7, T = 1 y SS = 4 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Cr 1(Br. O 4)2 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “cual es la formula de” Nombre 14) nitrato cobaltoso No inicia por H Función B) 5: MT(n. MOSS)Vm 15) fosfito aurico No inicia por H Función B) 5: MT(n. MOSS)Vm 12/7/2020 Respuesta Consideraciones: Las valencias del metal cobalto son: 3 (mayor – ico) y 2 (menor – oso). Para el n. M nitrógeno la valencia ato es V = 5, T = 1 y SS = 3 Consideraciones: Las valencias del metal oro son: 3 (mayor – ico) y 1 (menor – oso). Para el n. M fósforo la valencia ito es V = 3, T = 3 y SS = 3 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Co 1(NO 3)2 Au 3(PO 3)3 Simplificando queda Au 1(PO 3)1 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “cual es la formula de” Nombre Respuesta 16) carbonato cuproso No inicia por H Función B) 5: MT(n. MOSS)Vm 11) cloruro sódico No inicia por H Función B 4: M T n. M 12/7/2020 vm Consideraciones: Las valencias del metal cobre son: 2 (mayor – ico) y 1 (menor – oso). Para el n. M carbono la valencia ato es V = 4, T = 2 y SS = 3 Consideraciones: La valencias del metal (Na) sodio es: 1 (metal alcalino). Para el n. M azufre (Cℓ), T = 1 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Cu 2(CO 3)1 Na 1 Cℓ A un “Clic” del conocimiento 1 I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar una fórmula dada” La fórmula nos indica la función, hay que determinar la valencia de cada elemento para conocer su nombre relativo. Como toda fórmula es eléctricamente neutra se cumple que: Suma de números de oxidación = 0 En los grupos funcionales simples, la valencia de un elemento coincide con el valor absoluto de su número de oxidación Los metales alcalinos (Li, Na, K, Rb, Cs, Fr) son Los alcalino térreos (Be, Mg, Ca, Sr, Ba, Ra) son +1 +2 En una sal haloidea el número de oxidación del no metal es -T X ya que su fórmula general es: MT n. M V. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es -T A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

En una oxisal orto de metal polivalente (número de oxidación “X”), el número de oxidación del no metal es “y”. Como tenemos “dos incógnitas” se requieren “dos ecuaciones”: Con la “semisuma” (el número de oxígenos) calculamos “y” X y T + “y” SS = 2 ya que la fórmula general de una sal oxisal es: MT(n. MOSS)Vm. Con “suma de números de oxidación = 0”, calculamos “X” Si el valor de “X” no coincide con una valencia del metal, nos indica que la sal es meta, en este caso: 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

En una oxisal meta de metal polivalente (número de oxidación “X”), el número de oxidación del no metal es “y”. Como tenemos “dos incógnitas” se requieren “dos ecuaciones”: Con la semisuma menos uno (el número de oxígenos) calculamos “y” Ma(n. MOSS- 1)Vm. ya que la fórmula general de una sal oxisal META es: Con “suma de números de oxidación = 0”, calculamos “X” En una oxisal piro (se identifica porque el n. M posee un subíndice 2) de metal polivalente (número de oxidación “X”), el número de oxidación del no metal es “y”. Como tenemos “dos incógnitas” se requieren dos ecuaciones: Con la “semi suma x 2 menos uno” (el número de oxígenos) calculamos “y” ya que la fórmula general de una sal oxisal PIRO es: Mb(n. M 2 OSSx 2 - 1)Vm. Con “suma de números de oxidación = 0”, calculamos “X” 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X Y -2 1) nombrar: Pb (S O 3)2 Función B 5: M T (n. MO SS ) Vm n. M ato M ico ~ ~ ito oso Asignamos números de oxidación para conocer la valencia de M (Pb) y de n. M (S), (T = 2) No podemos “imaginar” que X = 2, la fórmula puede estar simplificada Con el número de oxígenos (3) = SS, calculamos “Y”: 3 = 2+Y 2 Y=4 sulfito con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 2(4) + 6(-2) = 0 X = 4 Las valencias del Pb son: 4(ico), 2(oso) plúmbico Respuesta: 12/7/2020 el nombre de Pb (S O 3)2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: Sulfito plúmbico es orto A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” 2) nombrar: X -2 Sn S 2 Función B 4: M T n. M V n. M uro M ico ~ ~ oso Asignamos números de oxidación para conocer la valencia de M (Sn), n. M (S), (T = 2) con “suma de números de oxidación = 0”, calculamos “X” No “imaginar” que X = 2 1(X) + 2(-2) = 0 Respuesta: 12/7/2020 X = 4 Las valencias del Sn son: 4(ico), 2(oso) estánnico el nombre de Sn S 2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: Sulfuro estánnico A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X 3) nombrar: Y -2 Fe (P O 4) Función B 5: M T (n. MO SS ) V n. M ato M ico ~ ito ~oso Asignamos números de oxidación para conocer la valencia de M (Fe) y de n. M (P), (T = 3) Con el número de oxígenos (4) = SS, calculamos “Y”: 4 = 3+Y 2 Y=5 fosfato con “suma de números de oxidación = 0”, calculamos “X” No “imaginar” que X = 1 1(X) + 1(5) + 4(-2) = 0 X = 3 Las valencias del Fe son: 3(ico), 2(oso) férrico Respuesta: 12/7/2020 el nombre de Fe (PO 4) http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es fosfato férrico es orto A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X 4) nombrar: -2 Fe 2 Se 3 Función B 4: M T n. M uro M ico ~oso ~ V Asignamos números de oxidación para conocer la valencia de M (Fe), n. M (Se), (T = 2) con “suma de números de oxidación = 0”, calculamos “X” 2(X) + 3(-2) = 0 X = 3 Las valencias del Fe son: 3(ico), 2(oso) Respuesta: 12/7/2020 el nombre de Fe 2 Se 3 es: Seleniuro http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es férrico A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X Y -2 5) nombrar: Fe (Br O 4)2 Función B 5: M T (n. MO SS ) V n. M ato M ico ~ ito ~oso Asignamos números de oxidación para conocer la valencia de M (Fe) y de n. M (Br), (T = 1) Con el número de oxígenos (4) = SS, calculamos “Y”: 4= 1+Y 2 Y=7 perbromato con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 2(7) + 8(-2) = 0 Respuesta: 12/7/2020 X = 2 Las valencias del Fe son: 3(ico), 2(oso) el nombre de Fe (Br. O 4)2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: perbromato ferroso (es orto) A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” 2 Y -2 6) nombrar: Ca (C O 3) Función B 5: M T (n. MO SS ) Vm n. M ato M ico ~ ito ~oso Asignamos números de oxidación para conocer la valencia de n. M (C), (T = 2) El Ca es metal alcalino térreo su valencia es 2 (ico) cálcico con “suma de números de oxidación = 0”, calculamos “Y” 1(2) + 1(Y) + 3(-2) = 0 Respuesta: 12/7/2020 Y=4 el nombre de carbonato Ca (C O 3) es: carbonato cálcico http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X -2 +1 7) nombrar: Cu (O H)2 Función B 3: M (OH ) V Hidróxido M ico ~ oso Asignamos números de oxidación para conocer la valencia de M (Cu) con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 2(-2) + 2(1) = 0 X = 2 Respuesta: 12/7/2020 el nombre de Las valencias del Cu son: 2(ico), 1(oso) cúprico Cu (O H)2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: hidróxido cúprico A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

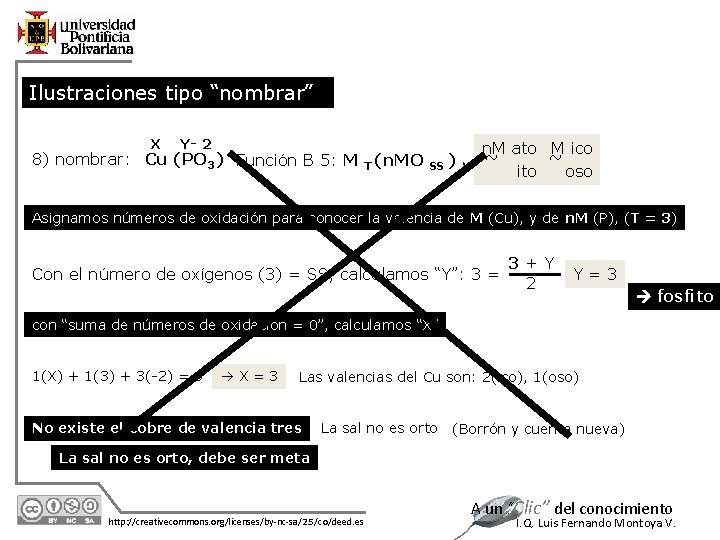
Ilustraciones tipo “nombrar” X Y- 2 8) nombrar: Cu (PO 3) Función B 5: M T (n. MO SS ) V n. M ato M ico ~ ~ ito oso Asignamos números de oxidación para conocer la valencia de M (Cu), y de n. M (P), (T = 3) Con el número de oxígenos (3) = SS, calculamos “Y”: 3 = 3+Y 2 Y=3 fosfito con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 1(3) + 3(-2) = 0 X=3 Las valencias del Cu son: 2(ico), 1(oso) No existe el cobre de valencia tres La sal no es orto (Borrón y cuenta nueva) La sal no es orto, debe ser meta 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X Y -2 Cu (P O 3) Función B 6: M a (n. M O SS-1 ) Meta n. M ato M ico ~ ~ ito oso V Asignamos números de oxidación para conocer la valencia de M (Cu), y de n. M (P), (T = 3) Con el número de oxígenos (3) = SS - 1, calculamos “Y”: 3= Y=5 3+Y -1 2 meta fosfato con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 1(5) + 3(-2) = 0 Respuesta: 12/7/2020 X = 1 Las valencias del Cu son: 2(ico), 1(oso) el nombre de Cu (PO 3) http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: Meta fosfato cuproso A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X Y -2 9) nombrar: Pb (S 2 O 7)2 Función B 7: M b (n. M 2 O SSx 2 - 1 ) El subíndice DOS del n. M nos indica que es PIRO V Piro n. M ato M ico ~ ~ ito oso Asignamos números de oxidación para conocer la valencia de M (Pb), y de n. M (S), (T = 2) Con el número de oxígenos (7) = SSx 2 - 1, calculamos “Y”: 2+Y Y = 6 piro sulfato 7= x 2 - 1 2 con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 4(6) + 14(-2) = 0 Respuesta: 12/7/2020 X=4 Las valencias del Pb son: 4(ico), 2(oso) el nombre de Pb (S 2 O 7)2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: piro sulfato plúmbico A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” 10) nombrar: X-1 Co H 2 Función B 1: M H V Hidruro M ico ~ oso Asignamos números de oxidación para conocer la valencia de M (Co) con “suma de números de oxidación = 0”, calculamos “X” 1(X) + 2(-1) = 0 X = 2 Las valencias del Co son: 3(ico), 2(oso) cobaltoso Respuesta: 12/7/2020 el nombre de Co H 2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: hidruro cobaltoso A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones tipo “nombrar” X -2 11) nombrar: Pb O 2 Función B 2: M 2 O V M ico Óxido ~ oso Asignamos números de oxidación para conocer la valencia de M (Pb) 1(X) + 2(-2) = 0 X=4 Las valencias del Pb son: 4(ico), 2(oso) Respuesta: 12/7/2020 el nombre de Pb O 2 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es es: plumbico óxido plúmbico A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Reacción de neutralización Un ácido se neutraliza con una base o hidróxido para producir una sal más agua Los reactivos (entran) son el ácido y la base 12/7/2020 Los reactivos y los productos se separan por una flecha ( ) que se lee “produce” http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Los productos (salen) son la sal y el agua A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Balanceo por tanteo de la reacción de neutralización Esta reacciones se balancean por tanteo, asignando como coeficiente estequimétrico (ce) igual a uno a la sal (la sustancia más “rara”) Al ácido, a la base y al agua le asignamos como coeficiente el signo “? ” que se lee “no se”, y por tanteo se puede conocer el valor de cada “? ” del metal (M), del no metal (n. M) y del oxigeno (O) Con los hidrógenos hacemos el chequeo del balanceo, se tiene que cumplir que # de H que entran = # de H que salen Luego de balanceada la reacción, calculamos el mínimo común múltiplo (MCM) de los coeficientes estequiométricos 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

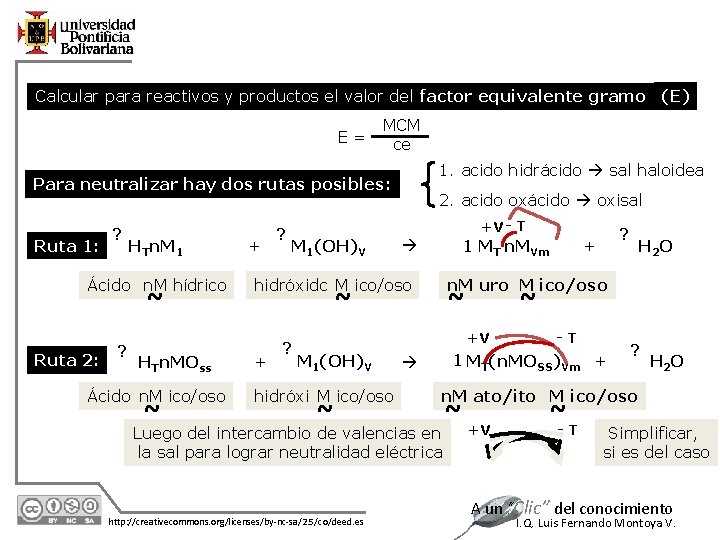
Calcular para reactivos y productos el valor del factor equivalente gramo (E) E= MCM ce 1. acido hidrácido sal haloidea Para neutralizar hay dos rutas posibles: Ruta 1: ? HTn. M 1 Ácido n. M hídrico ~ Ruta 2: ? HTn. MOss Ácido n. M ico/oso ~ + ? 2. acido oxácido oxisal +V - T M 1(OH)V 1 MT n. MVm hidróxido M ico/oso + ~ hidróxido M ico/oso ~ http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es -T 1 MT(n. MOSS)Vm + ? H 2 O n. M ato/ito M ico/oso Luego del intercambio de valencias en la sal para lograr neutralidad eléctrica 12/7/2020 ~ +V M 1(OH)V H 2 O n. M uro M ico/oso ~ ? ? + ~ ~ +V -T Simplificar, si es del caso A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

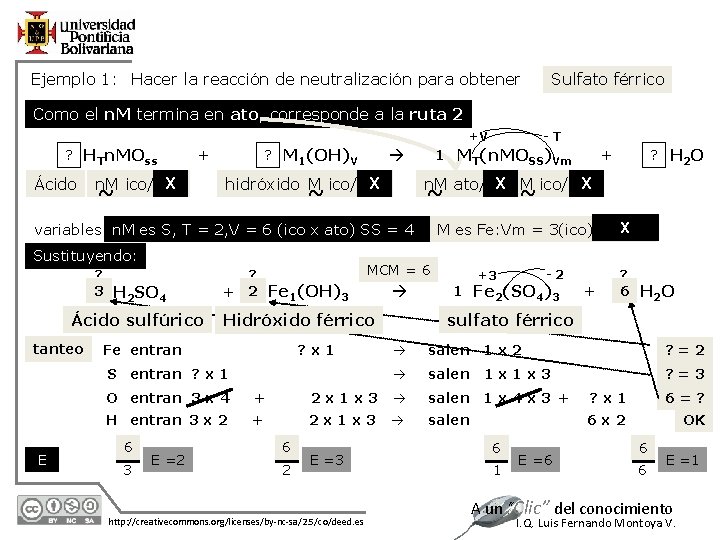
Ejemplo 1: Hacer la reacción de neutralización para obtener Sulfato férrico Como el n. M termina en ato, corresponde a la ruta 2 +V ? HTn. MOss Ácido ? M 1(OH)V + X n. M ico/oso ~ 1 MT(n. MOSS)Vm X hidróxido M ico/oso ~ Ácido sulfúrico tanteo ? 2 Fe 1(OH)3 + ? x 1 S entran ? x 1 E 12/7/2020 MCM = 6 -2 +3 1 Fe 2(SO 4)3 + ? 6 H 2 O sulfato férrico Hidróxido férrico Fe entran ~ X M es Fe: Vm = 3(ico)-2(oso) variables n. M es S, T = 2, V = 6 (ico x ato) SS = 4 ? 3 H 2 SO 4 ? H 2 O + X M ico/oso X n. M ato/ito ~ Sustituyendo: -T salen 1 x 2 ? =2 salen ? =3 1 x 1 x 3 O entran 3 x 4 + 2 x 1 x 3 salen 1 x 4 x 3 + ? x 1 6=? H entran 3 x 2 + 2 x 1 x 3 salen 6 x 2 OK 6 3 E =2 6 2 E =3 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es 6 1 E =6 6 6 E =1 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

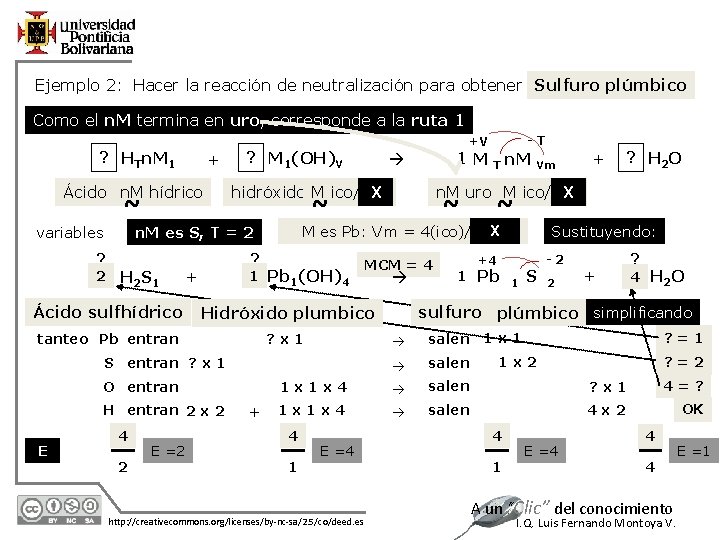
Ejemplo 2: Hacer la reacción de neutralización para obtener Sulfuro plúmbico Como el n. M termina en uro, corresponde a la ruta 1 ? HTn. M 1 + Ácido n. M hídrico ~ variables ? M 1(OH)V 2 H 2 S 1 Hidróxido plumbico tanteo Pb entran ? x 1 E 12/7/2020 4 2 E =2 Vm + ? H 2 O ~ +4 1 Pb 2 1 Sustituyendo: S -2 4 2 + ? 4 H 2 O sulfuro plúmbico simplificando salen 1 x 1 salen 1 x 1 x 4 salen ? x 1 4=? 1 x 1 x 4 salen 4 x 2 OK S entran ? x 1 + ~ MCM = 4 Ácido sulfhídrico H entran 2 x 2 n. M X M es Pb: Vm = 4(ico)/2(oso) 1 Pb 1(OH)4 O entran T X n. M uro M ico/oso ~ ? + 1 M X hidróxido M ico/oso n. M es S, T = 2 ? -T +V 4 1 E =4 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es ? =1 1 x 2 4 1 E =4 ? =2 4 4 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V. E =1

APÉNDICE Justificación del cambio metodológico. En vista de que en los textos existe una serie de metodologías que llevan a errores al aplicarlas y que generan cierto grado de dificultad para que el estudiante se apersone del conocimiento en una forma crítica y analítica, he planteado una metodología más integral que genere en forma general y amena la aplicabilidad para cada caso particular, logrando con ello subsanar los inconvenientes encontrados en las metodologías clásicas. A continuación planteo los casos encontrados en la literatura clásica que generan inconvenientes de aprendizaje y ERRORES DE APLICACIÓN, pero lo más importante no es mostrar problemas sino plantear soluciones a los casos encontrados. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Errores en textos clásicos Caso No. 1, “Ácidos de memoria” En textos como ISBN-9684229852 de origen americano establecen: “Un ácido ternario común (sic) de cada no-metal se designa (en forma arbitraria (sic)) como ácido - ico, es decir, se nombra diciendo la raíz del ácido (sic) terminada en – ico. Los ácidos ternarios de este tipo se indican en la siguiente tabla. No hay ácidos ternarios de terminación - ico para los no metales que se omiten (sic). Es importante aprender los nombres y fórmulas de estos ácidos de memoria (sic) porque los nombres de los demás ácidos ternarios y sales se derivan de ellos”. NOTA: (Sic) significa copia textual aunque no estoy de acuerdo 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

“Grupo periódico de elementos centrales” IIIA IVA VA H 3 BO 3 Ac. Bórico H 2 CO 3 Ac. Carbónico HNO 3 Ac. Nítrico H 4 Si. O 4 Ac. Silícico 12/7/2020 VIA VIIA H 3 PO 4 Ac. Fosfórico H 2 SO 4 Ac. Sulfúrico HCℓO 3 Ac. Clórico H 3 As. O 4 Ac. Arsénico H 2 Se. O 4 Ac. Selénico HBr. O 3 Ac. Brómico H 6 Te. O 6 (Sic) Ac. Telúrico HIO 3 Ac. Yódico http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

COMENTARIOS Sic 1, “Ácido ternario común”. El texto hace referencia al ácido normal o orto pero no menciona los ácidos anormales meta y piro que algunos no metales forman. Sic 2, “en forma arbitraria”. El autor desconoce que el sufijo ICO (indica mayor) y el sufijo OSO (indica menor) son sufijos comparativos y se emplean para indicar con que valor relativo de valencia trabaja el no-metal. Sic 3, “La raíz del ácido terminada en ico”. Todos somos humanos, esto es un eleve, lo que termina en ico es la raíz del nombre del elemento. Sic 4, “No hay ácidos ternarios de terminación –ico para los no metales que se omiten”. Este comentario puede inducir a un sofisma de negar la existencia de algunos ácidos –ico que si existen y que generan sales que también existen como por ejemplo: Ácido Crómico: H 2 Cr. O 4 y ácido Mangánico: H 2 Mn. O 4. 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Nota 1: si el ácido crómico no existiera, no existiría la sal cromato que es de amplio uso en procesos textiles, curtido de cueros, componente en pinturas anticorrosivas para hierro, acero y aleaciones ligeras, tintas, conservador de la madera, etc. Nota 2: si el ácido mangánico no existiera, no existiría la sal manganato que es usada en baterías, en estampado, en fotografía, en purificación de agua, blanqueante de fibras, desinfectante Sic 5, “Es importante aprender los nombres y fórmulas de estos ácidos de memoria”. Con esto lo único que consigue es hacerle creer al los estudiantes que la química está en un pedestal y que el profesor está inalcanzable en dicho pedestal y por lo tanto el “club de amigos de la química” sería una especie en vía de extinción. Esto es un paradigma innecesario. Sic 6, “H 6 Te. O 6 ácido telúrico”. Aquí alguien se equivocó porque el ácido telúrico tiene por fórmula H 2 Te. O 4, pero es dihidratado, H 2 Te. O 4. 2 H 2 O, y a alguien le dió por contar: H hay 6, Te hay 1 y O hay 6 (¿factor común para reducir a la mínima expresión? ) 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

. . . y sigue el texto: “Los ácidos que tienen un átomo de oxígeno menos por átomo central se nombran del mismo modo, con excepción que el sufijo ICO se cambia a OSO” COMENTARIO Esta es una tentativa de relacionar los ácidos – OSO con los ácidos – I CO (¿aprendidos de memoria? ). Sólo existe una discrepancia en el H 6 Te. O 5 cuando en realidad es H 2 Te. O 3. . continúa el texto “Los ácidos ternarios que tienen un átomo de oxígeno menos que los ácidos OSO se nombran usando el prefijo HIPO y el sufijo – OSO” COMENTARIO Esta norma induce a generar los ácidos HIPO-OSO para el Boro, para el Carbono y para el Silicio que no existen, además el ácido Hipoteluroso sería H 6 Te. O 4 que si existe pero su fórmula es H 2 Te. O 2. La efectividad de esta norma es del 67% (8 correctos de 12 posibles). 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

. . . y continúa el texto: “Los ácidos que contienen un átomo de oxígeno mas por átomo de no-metal central que el ácido – ICO se nombran con el prefijo PER y el sufijo – ICO”. COMENTARIO Esta norma induce a generar los ácidos PER-ICO para los no metales que no tienen la valencia per – ico: B, C, Si, N, P, As, S, Se y Te que no existen, también los ácidos PER-ICO para los no metales Cℓ, Br, I que si existen, pero no inducen al ácido Permangánico (HMn. O 4) generador de las sales Permanganato de amplio uso como agente oxidante. Efectividad de esta norma: solo 13% (3 correctos de 13 posibles). Nota: si el permanganato no existiera, que hacer cuando se requiera como: Desinfectante, bactericida, fabricación de sacarina, antídoto en envenenamiento con morfina, curare y fósforo 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Caso No. 2. Ácidos orto, meta y piro, propuesta “general” con muchas excepciones. En textos como ISBN 8430730249 de origen español hacen un intento de definir los ácidos orto (normal) y los anormales meta y piro, así: “Para las columnas impares”: (sic. Se refieren a los elementos de los grupos III, V y VII) PREFIJO FORMA QUE INDICA Meta 1 anhídrido + 1 H 2 O Piro 1 anhídrido + 2 H 2 O Orto 1 anhídrido + 3 H 2 O COMENTARIO Cuando ilustran su uso sólo lo aplican para los no metales B, P y As (los que tienen T = 3), pero nunca para Cℓ, Br, I, N (nosotros ya sabemos que por poseer T=1 estos ácidos son anormales y no existen para estos elementos). 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

. . . sigue el texto: “Para las columnas pares”: (sic, se refieren a los elementos de los grupos IV y VI) PREFIJO FORMA QUE INDICA Meta 1 anhídrido + 1 H 2 O Piro 2 anhídrido + 1 H 2 O Orto 1 anhídrido + 2 H 2 O COMENTARIO Cuando ilustran su uso lo aplican para el S, Se y Te, pero solo la definición orto y piro y nunca la del meta (nosotros ya sabemos que como T = 2 el meta no existe para ellos). Para el Si que si tiene meta (ya que T=4) no pueden usar las definiciones anteriores ya que no cumple la del piro, para el Silicio hay que definir que: Piro = 2 anhídrido + 3 H 2 O 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

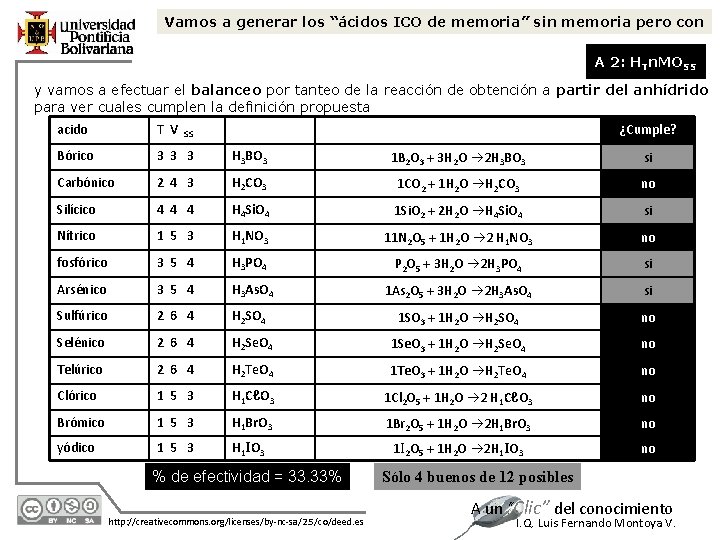
Vamos a generar los “ácidos ICO de memoria” sin memoria pero con A 2: HTn. MOSS y vamos a efectuar el balanceo por tanteo de la reacción de obtención a partir del anhídrido para ver cuales cumplen la definición propuesta acido T V ¿Cumple? Bórico 3 3 3 H 3 BO 3 1 B 2 O 3 + 3 H 2 O 2 H 3 BO 3 si Carbónico 2 4 3 H 2 CO 3 1 CO 2 + 1 H 2 O H 2 CO 3 no Silícico 4 4 4 H 4 Si. O 4 1 Si. O 2 + 2 H 2 O H 4 Si. O 4 si Nítrico 1 5 3 H 1 NO 3 11 N 2 O 5 + 1 H 2 O 2 H 1 NO 3 no fosfórico 3 5 4 H 3 PO 4 P 2 O 5 + 3 H 2 O 2 H 3 PO 4 si Arsénico 3 5 4 H 3 As. O 4 1 As 2 O 5 + 3 H 2 O 2 H 3 As. O 4 si Sulfúrico 2 6 4 H 2 SO 4 1 SO 3 + 1 H 2 O H 2 SO 4 no Selénico 2 6 4 H 2 Se. O 4 1 Se. O 3 + 1 H 2 O H 2 Se. O 4 no Telúrico 2 6 4 H 2 Te. O 4 1 Te. O 3 + 1 H 2 O H 2 Te. O 4 no Clórico 1 5 3 H 1 CℓO 3 1 Cl 2 O 5 + 1 H 2 O 2 H 1 CℓO 3 no Brómico 1 5 3 H 1 Br. O 3 1 Br 2 O 5 + 1 H 2 O 2 H 1 Br. O 3 no yódico 1 5 3 H 1 IO 3 1 I 2 O 5 + 1 H 2 O 2 H 1 IO 3 no SS % de efectividad = 33. 33% 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Sólo 4 buenos de 12 posibles A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Caso No. 3 en la mayoría de los textos elementales y avanzados. Nos afirman que: ”Una vez que usted conozca los números de oxidación (sic) de los diversos iones, podrá vaticinar las fórmulas químicas de cualquiera compuestos que formen. Si usted quiere volverse experto en escribir y nombrar compuestos, deberá memorizar los nombres y símbolos de los iones en la tabla a. Una buena idea es usar fichas. Repase estas fichas a diario hasta que haya memorizado (sic) los nombres y símbolos de los iones” Sic. No es número de oxidación, es carga del ión. “Tabla a: memorizar la siguiente tabla” Cℓ 1 - Cloruro (NO 2)1 - nitrito (SO 4)2 -sulfato (As. O 4)3 - Arseniato F 1 - (NO 3)1 - nitrato (SO 3)2 - sulfito (BO 3)3 - borato Br 1 - Bromuro (CℓO)1 - hipoclorito (CO 3)2 - carbonato (Si. O 4)4 - silicato I 1 - (CℓO 2)1 - clorito (Cr. O 4)2 - cromato (Mn. O 4)2 - manganato (CℓO 3)1 - clorato (PO 4)3 - fosfato (Br. O 3)1 - bromato S 2 - Fluoruro Yoduro Sulfuro Sic: n. M T- n. Muro Sic: (n. MOSS) T- n. M ato/ito Aquí están todos los de la tabla y los que faltan 12/7/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.