NOMENCLATURA DE COMPUESTOS INORGNICOS Bloque 6 Reglas de

NOMENCLATURA DE COMPUESTOS INORGÁNICOS Bloque 6

Reglas de la UIQPA para escribir fórmulas y nombres de los compuestos químicos inorgánicos • El lenguaje de los alquimistas, originó una multitud de sinónimos que dificultaba el estudio de la química, los químicos de mediados del siglo XVIII, como Bergman, Morveau, Berthelot y Berzeliuz entre otros, establecieron una nomenclatura química que les permitiera una mejor comunicación.

Lenguaje de la química • Símbolos y formulas químicas. En la actualidad existen 118 elementos químicos por lo que es conveniente representarlos por medio de símbolos para que permitan la comunicación con toda la comunidad científica. Dentro de los primeros símbolos tenemos los símbolos de los alquimistas y los símbolos de Dalton.
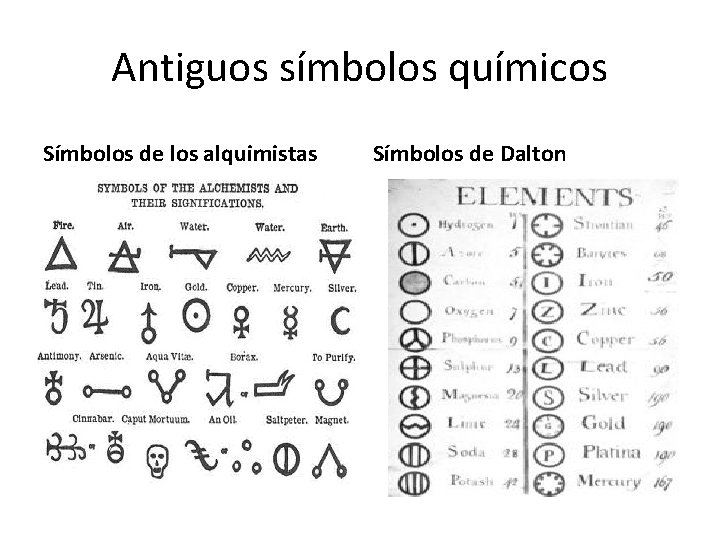
Antiguos símbolos químicos Símbolos de los alquimistas Símbolos de Dalton

EN 1814 J. J. BERZELIUS ( SUECO) PROPUSO REPRESENTAR A LOS ELEMENTOS POR MEDIO DE LETRAS

La IUPAC • Propuso los símbolos se escribieran con 1, 2 o 3 letras ejemplo: • N nitrógeno • Ca Calcio • Unq unnilquadium Los nombres de los elementos pueden cambiar de un idioma a otro pero los símbolos son universales.






Número de oxidación • El número de oxidación es la cantidad de electrones que tiende a ceder o adquirir un átomo de un elemento en una reacción química con otros átomos para poder -de ésa manera- adquirir cierta estabilidad química. El número de oxidación es positivo si el átomo pierde electrones. • Será negativo cuando el átomo gane electrones.

REGLAS PARA ASIGNAR VALENCIA O NÚMERO DE OXIDACIÓN • 1. - TODOS LOS ELEMENTOS SIN COMBINAR TIENE VALENCIA CERO EJEMPLOS : Na 0, K 0, Ca 0, Ba 0, Fe 0 • 2. - LA VALENCIA DEL OXÍGENO ES (-2)EXCEPTO CUANDO FORMA PEROXIDOS (-1) • 3. - EL HIDRÓGENO TIENE VALENCIA (+1) EXCEPTO EN HIDRUROS (-1) • 4. - LOS METALES DEL GRUPO IA Y IIA TIENEN VALENCIA +1 Y +2 RESPECTIVAMENTE.

La suma algebraica de los números de oxidación en un compuesto debe ser cero • Ejemplos: • KMn. O 4 K+1 Mn +7 O 4 -2

IÓN • SUSTANCIA QUE HA PERDIDO O HA GANADO ELECTRONES • SI PIERDE SE CONVIERTE EN CATIÒN • SI GANA SE CONVIERTE EN ANIÒN
IONES MONOATÓMICOS POLIATÓMICOS

MONOATÒMICOS • SON AQUELLOS QUE ESTAN FORMADOS POR UN SOLO ÀTOMO: • K+1, Na+1 , Cl-1 , S-2

POLIATÒMICOS • SON AQUELLOS QUE ESTAN FORMADOS POR 2 Ò MAS ÀTOMOS DE DIFERENTES ELEMENTOS -2 -1 +1 • SO 4 , NO 3 , NH 4

LOS IONES MONOATOMICOS PUEDEN TENER VARIAS VALENCIAS NOMENCLATURA COMÚN • SI TIENE LA MENOR VALENCIA TIENE TERMINACIÒN “OSO” • SI TIENE LA MAYOR VALENCIA TIENE TERMINACIÒN “ICO” • EJEMPLO: Cu+1 / Cu+2 • Cu+1 IÒN CUPROSO Cu+2 IÒN CUPRÌCO

NOMENCLATURA IUPAC O SISTEMÀTICA • SI EL ELEMENTO TIENE VARIAS VALENCIAS ÈSTA SE ESCRIBE CON NÙMERO ROMANO • POR EJEMPLO EL CASO ANTERIOR • Cu+1 / Cu+2 • Cu+1 IÒN COBRE I , Cu+2 IÒN COBRE II • NOTA: SOLO SI EL ELEMENTO TIENE VARIAS VALENCIAS, DE LO CONTRARIO SOLO SE ESCRIBE EL NOMBRE DEL ELEMENTO

TIPS PARA MEMORIZAR LOS NOMBRES DE LOS IONES • LOS ANIONES MONOATÓMICOS TIENEN TERMINACIÓN URO • EJEMPLO: Cl-1 IÓN CLORURO F-1 IÓN FLUORURO N-3 IÓN NITRURO I-1 IÓN IODURO

LOS IONES CON SUFIJO ATO E ITO • INDICAN QUE CONTIENEN OXÍGENO • MAS ÁTOMOS DE OXÍGENO • MENOS ÁTOMOS DE OXÍGENO SO 4 -2 IÓN SULFATO SO 3 -2 IÓN SULFITO ATO ITO

EL PREFIJO BI SIGNIFICA ÁCIDO • HCO 3 -1 IÓN BICARBONATO • HSO 4 -1 IÓN BISULFATO

EL PREFIJO PER ME INDICA QUE TIENE UN OXÍGENO MAS QUE EL ATO • Cl. O 3 -1 IÓN CLORATO • Cl. O 4 -1 IÓN PERCLORATO

EL PREFIJO HIPO ME INDICA QUE TIENE UN OXÍGENO MENOS QUE EL ITO • Cl. O 2 -1 IÓN CLORITO • Cl. O-1 IÓN HIPOCLORITO

FÓRMULA QUÍMICA • ES UNA COMBINACIÓN DE SÍMBOLOS QUE REPRESENTAN LA COMPOSICIÓN DE UN COMPUESTO • H 2 SO 4 COMP: 2 ÁTOMOS DE H 1 ÁTOMO DE AZUFRE 4 ÁTOMOS DE OXÍGENO

• EL SUBINDICE ME INDICA EL NÚMERO DE ÁTOMOS DE CADA ELEMENTO • Y EL COEFICIENTE ME INDICA EL NÚMERO DE MOLÉCULAS. 3 • COEFICIENTE H 2 O SUBINDICE

PARA ESCRIBIR UNA FÓRMULA • PRIMERO SE ESCRIBE EL CATIÓN Y DESPUES EL ANIÓN • Na. Cl KI Cu. O Fe. I 3

SI TENEMOS DOS IONES MONOATÓMICOS CON IGUAL CARGA PERO DIFERENTE SIGNO. • SIMPLEMENTE SE ESCRIBEN TAL CUAL: EJEMPLO • Na. Cl Mg. O Fe. O Cu. S
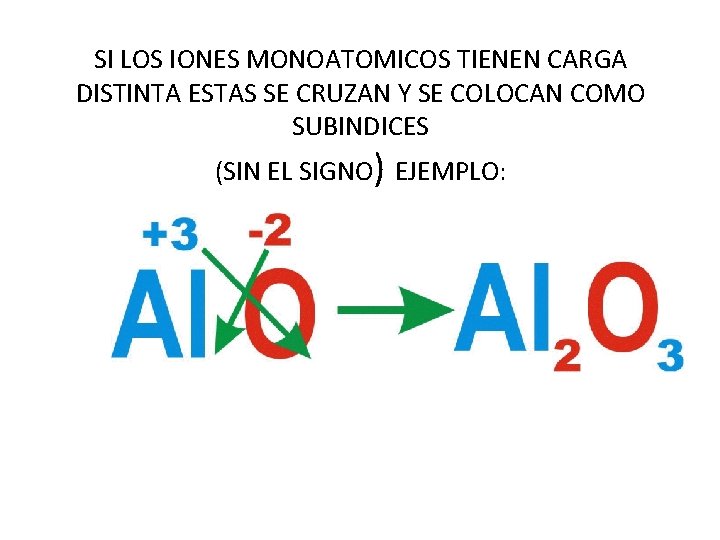
SI LOS IONES MONOATOMICOS TIENEN CARGA DISTINTA ESTAS SE CRUZAN Y SE COLOCAN COMO SUBINDICES (SIN EL SIGNO) EJEMPLO:

CUANDO PONER UN PARÉNTESIS? • EL PARÉNTESIS SE USA CUANDO TENEMOS QUE COLOCAR UN SUBINDICE DE 2 O MAYOR A UN IÓN POLIATOMICO. EJEMPLO: • Fe+3 SO 4 -2 Fe 2 (SO 4)3

LOS COMPUESTOS QUÍMICOS SE PUEDEN CLASIFICAR SEGÚN: EL No. DE ELEMENTOS SU FUNCIÓN QUÍMICA

SEGÚN EL NÚMERO DE ELEMENTOS BINARIOS • 2 ELEMENTOS • Na. Cl, H O, KI 2 TERNARIOS • 3 ELEMENTOS • Na. OH, H SO 2 4 POLIATÓMICOS • 4 ELEMENTOS • Na. HCO , KHSO 3 4

SEGÚN LA FUNCIÓN QUÍMICA ACIDOS BASES O HIDRÓXIDO S SALES OXIDOS HIDRUROS

ÓXIDOS BÁSICOS METAL + OXÍGENO ÓXIDOS ÁCIDOS NO METAL + OXÍGENO

NOMENCLATURA DE ÓXIDOS BÁSICOS • SE ESCRIBEN LAS PALABRAS “ ÓXIDO DE” SEGUIDO DEL NOMBRE DEL CATIÓN. Fe 2 O 3 ÓXIDO DE FIERRO III ÓXIDO FÉRRICO
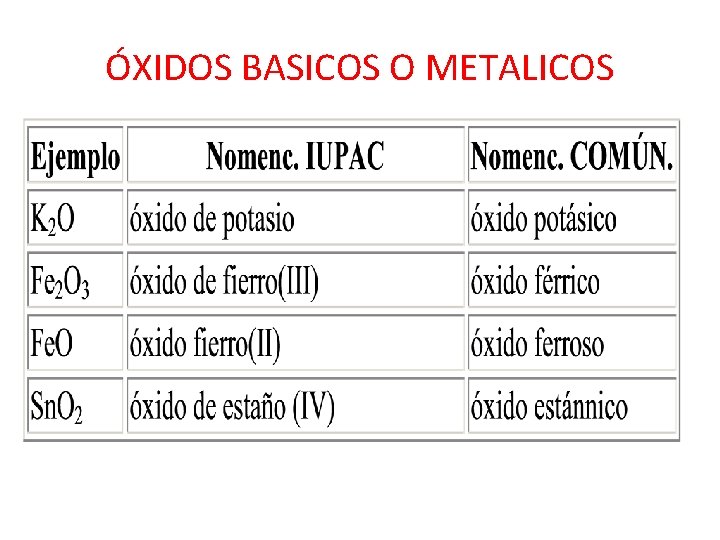
ÓXIDOS BASICOS O METALICOS

NOMENCLATURA DE ÓXIDOS ACIDOS. • SE IDENTIFICA LA CANTIDAD DE OXÍGENOS Y SE EMPLEAN PREFIJOS QUE INDIQUEN LA CANTIDAD DE ÉSTOS. MONO 1 O DI 2 O TRI 3 O TETRA 4 O PENTA 5 O

• SI EL NO METAL TIENE VARIOS ÁTOMOS TAMBIEN SE UTILIZAN LOS MISMOS PREFIJOS. • Cl 2 O 5 PENTAÓXIDO DE DICLORO

OXIDOS ACIDOS O ANHIDRIDOS

HIDRUROS METÁLICOS • SON LA COMBINACIÓN DEL HIDRÓGENO EN SU FORMA DE ANIÓN CON UN ION METÁLICO. • SON BINARIOS • PARA NOMBRAR ESTOS COMPUESTOS SE ANTEPONEN LAS PALABRAS “HIDRURO DE” SEGUIDO DEL NOMBRE DEL IÓN METÁLICO EJEMPLO: • Na H hidruro de sodio • Ca H 2 hidruro de calcio • Mg H 2 hidruro de magnesio

ÁCIDOS • SON SUSTANCIAS QUE TIENEN COMO IÓN CARACTERÍSTICO AL IÓN H 1+ EL CUAL LIBERAN AL DISOLVERSE EN AGUA, TIENEN SABOR AGRIO.
ACIDOS HIDRÁCIDOS ( NO CONTIENEN OXÍGENO) OXIACIDOS ( CONTIENEN OXÍGENO)

HIDRÁCIDOS • SON BINARIOS • SE NOMBRAN CAMBIANDO LA TERMINACIÓN URO DEL ANIÓN POR HÍDRICO Y ANTEPONIENDO LA PALABRA ÁCIDO.
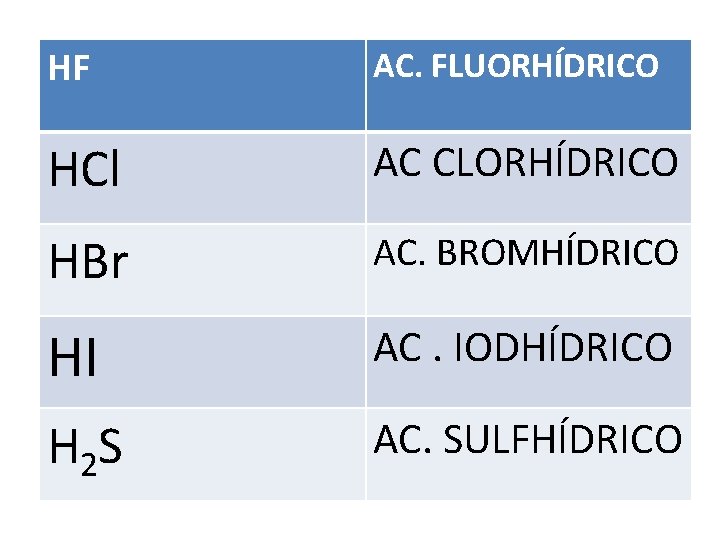
HF AC. FLUORHÍDRICO HCl AC CLORHÍDRICO HBr AC. BROMHÍDRICO HI AC. IODHÍDRICO H 2 S AC. SULFHÍDRICO

OXIACIDOS • SON TERNARIOS • PARA NOMBRARLOS SE ESCRIBE LA PALABRA ACIDO SEGUIDA DEL NOMBRE DEL ANIÓN CAMBIANDO LA TERMINACIÓN ATO X ICO ITO X OSO
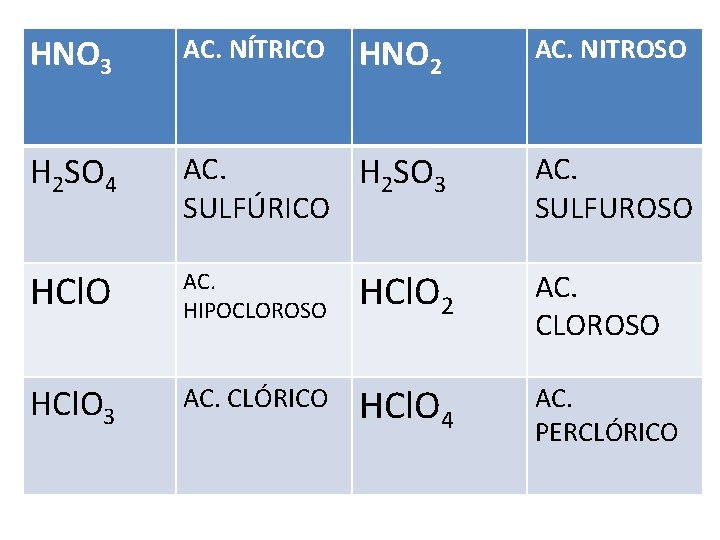
HNO 3 AC. NÍTRICO HNO 2 AC. NITROSO H 2 SO 4 AC. H 2 SO 3 SULFÚRICO AC. SULFUROSO HCl. O AC. HIPOCLOROSO HCl. O 2 AC. CLOROSO HCl. O 3 AC. CLÓRICO HCl. O 4 AC. PERCLÓRICO

SALES • SON SUSTANCIAS FORMADAS POR UN CATIÓN + UN ANIÓN SE FORMAN POR LA SUSTITUCIÓN DE LOS IONES HIDRÓGENO DE UN ÁCIDO POR METALES. • CATIÓN+ ANIÓN

SALES • SALES NEUTRAS. - SE SUSTITUYEN TOTALMENTE TODOS LOS HIDRÓGENOS DEL ACIDO POR METALES. • SALES ACIDAS. - SE SUSTITUYEN PARCIALMENTE LOS IONES HIDRÓGENO DE UN ACIDO POR METALES.
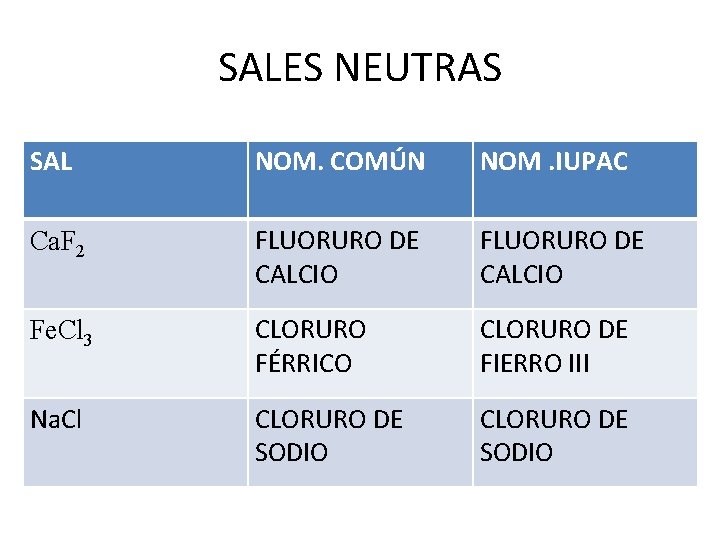
SALES NEUTRAS SAL NOM. COMÚN NOM. IUPAC Ca. F 2 FLUORURO DE CALCIO Fe. Cl 3 CLORURO FÉRRICO CLORURO DE FIERRO III Na. Cl CLORURO DE SODIO
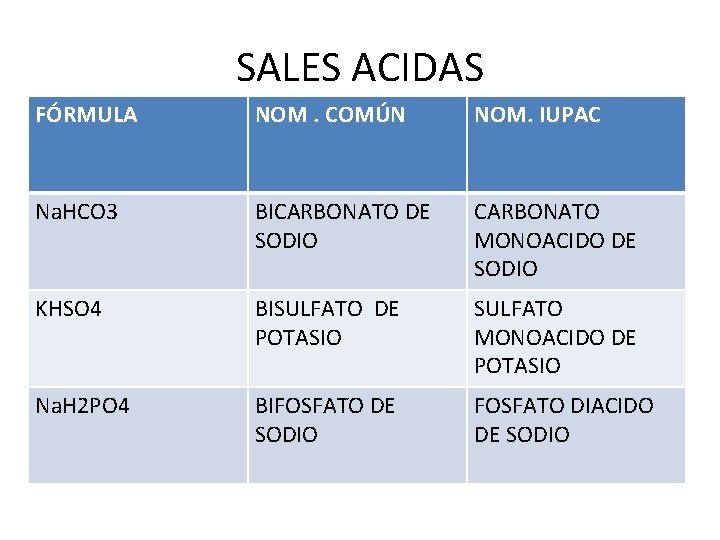
SALES ACIDAS FÓRMULA NOM. COMÚN NOM. IUPAC Na. HCO 3 BICARBONATO DE SODIO CARBONATO MONOACIDO DE SODIO KHSO 4 BISULFATO DE POTASIO SULFATO MONOACIDO DE POTASIO Na. H 2 PO 4 BIFOSFATO DE SODIO FOSFATO DIACIDO DE SODIO

BASES O HIDRÓXIDOS • SON TERNARIOS • SON SUSTANCIAS QUE SE CARACTERIZAN POR TENER UN ION OH- UNIDO A UN IÓN METÁLICO. • SE NOMBRAN ESCRIBIENDO LAS PALABRAS “ HIDRÓXIDO DE” SEGUIDA DEL NOMBRE DEL CATIÓN

EJEMPLOS BASE NOM. COMÚN NOM. IUPAC Na. OH HIDRÓXIDO DE SODIO Fe (OH)3 HIDRÓXIDO FÉRRICO HIDRÓXIDO DE FIERRO III Ca( OH) 2 HIDRÓXIDO DE CALCIO Cu. OH HIDRÓXIDO CUPROSO HIDRÓXIDO DE COBRE I HIDRÓXIDO DE SODIO
- Slides: 54