NKLEER MANYETIK REZONANS SPEKTROSKOPISI Ar Gr rfan apan










- Slides: 32

NÜKLEER MANYETIK REZONANS SPEKTROSKOPISI Arş. Gör. İrfan Çapan

İçerik • NMR nedir? IR ile ne farkı var ? • Hangi Çekirdeklerde Aktiftir? • 1 H-NMR Spektroskopisi • Çekirdeklerin Manyetik alandaki davranışları • Piklerin Oluşumu • Kimyasal Kayma • Örnek Spektrumlar • NMR spektrometresi

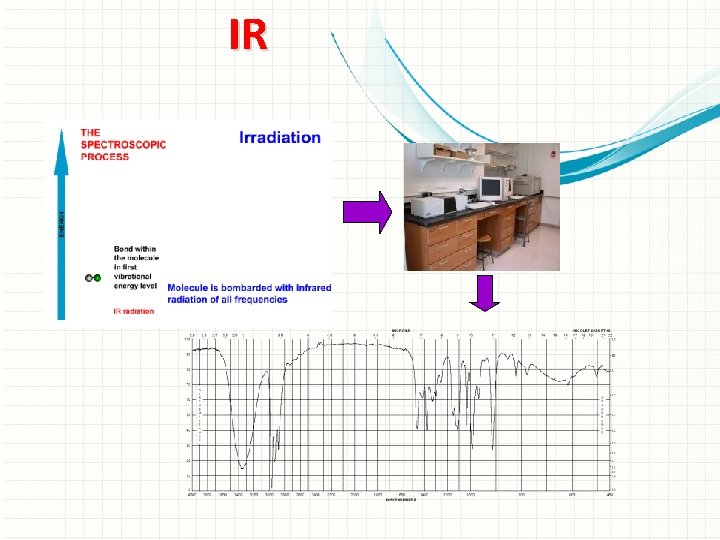
IR

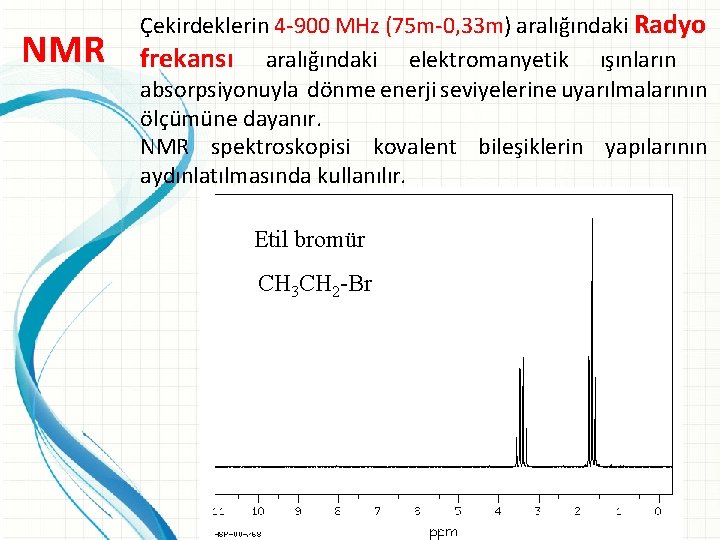
NMR Çekirdeklerin 4 -900 MHz (75 m-0, 33 m) aralığındaki Radyo frekansı aralığındaki elektromanyetik ışınların absorpsiyonuyla dönme enerji seviyelerine uyarılmalarının ölçümüne dayanır. NMR spektroskopisi kovalent bileşiklerin yapılarının aydınlatılmasında kullanılır. Etil bromür CH 3 CH 2 -Br

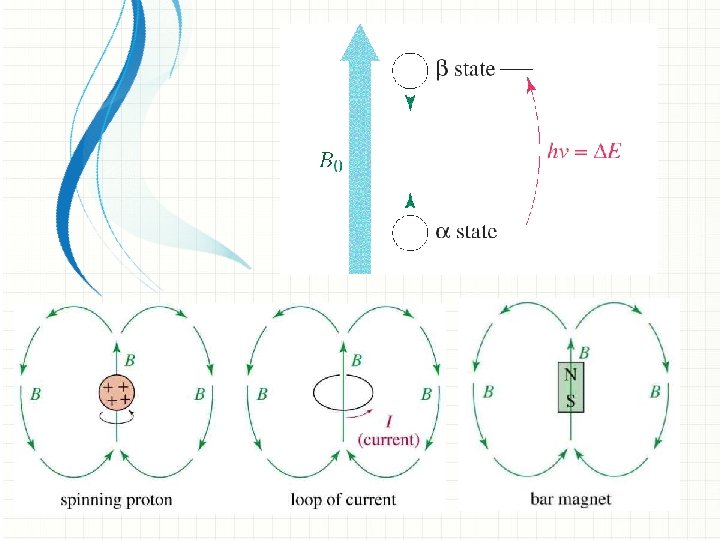
Ø Atom çekirdeği ve elektronlar, atomu oluşturan yüklü taneciklerdir. Ø Elektronlar kendi eksenleri etrafında dönerler yani bir "spin" hareketi yaparlar. Atom çekirdeklerinin çoğu da spin hareketi yapar. + + Ø Elektronun ve en basit çekirdek yapıtaşları olan proton ve nötronun spin kuantum sayısı, I, veya spin değerleri 1/2 dir.

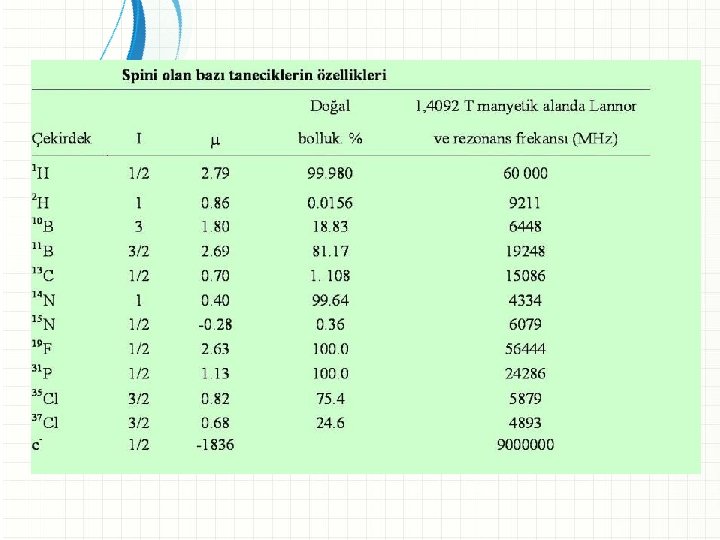
Proton ve nötron sayıları çift sayılı ise (4 He, 12 C, 160 çekirdeklerinde olduğu gibi) bu çekirdeklerin net spini yoktur(I=0). Proton ve nötron sayıları tek sayılı ise yani nötron ve proton sayılarının toplamı çift sayılı ise, çekirdeğin net spini tam sayılıdır. 2 H, 6 Li ve 14 N gibi çekirdeklerin net spini I =1 e, proton sayısı veya nötron sayısı tek sayılı ise spini yarımlı değer alır. Spini 1/2 olan 1 H, 13 C, 15 N, 19 F, 31 P, 57 Fe, spini 3/2 olan 7 Li, 37 CL, 23 Na, 53 Cr, 63 Cu, 61 Ni, spini 5/2 olan 55 Mn … 11 B, 79 Br, 81 Br, 35 Cl,


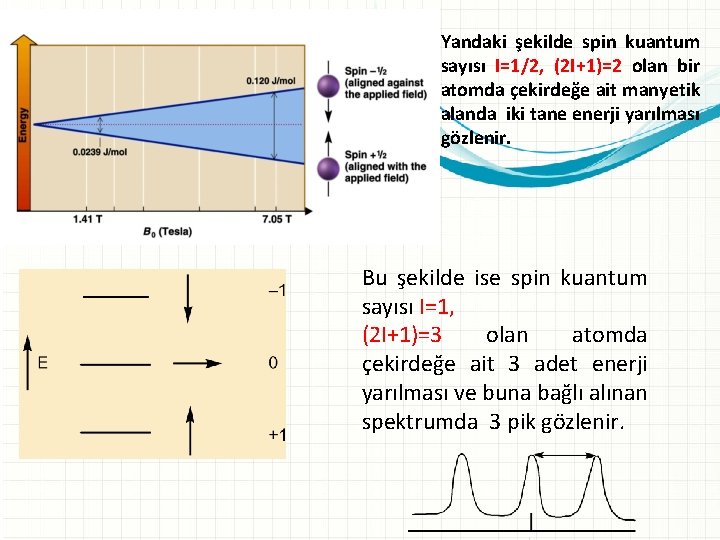
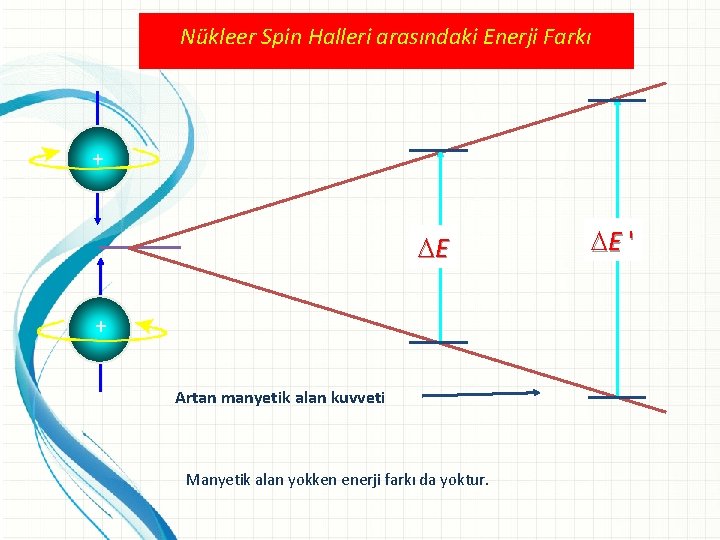
Yandaki şekilde spin kuantum sayısı I=1/2, (2 I+1)=2 olan bir atomda çekirdeğe ait manyetik alanda iki tane enerji yarılması gözlenir. Bu şekilde ise spin kuantum sayısı I=1, (2 I+1)=3 olan atomda çekirdeğe ait 3 adet enerji yarılması ve buna bağlı alınan spektrumda 3 pik gözlenir.

Nükleer Spin Halleri arasındaki Enerji Farkı + E + Artan manyetik alan kuvveti Manyetik alan yokken enerji farkı da yoktur. E '

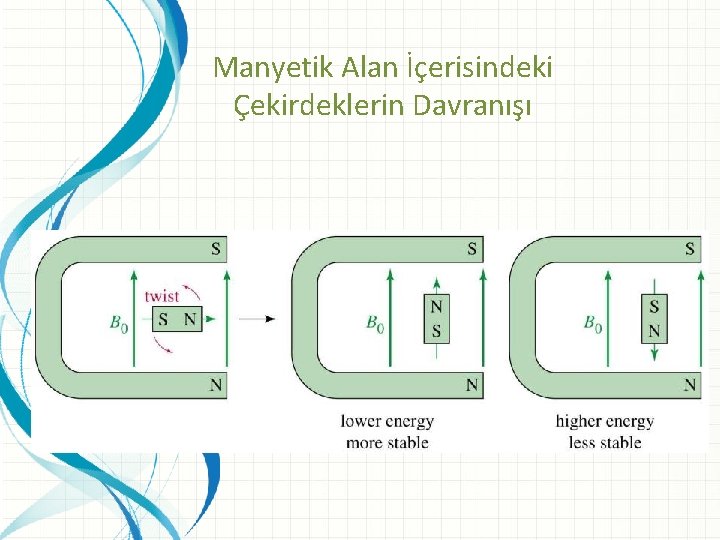
Manyetik Alan İçerisindeki Çekirdeklerin Davranışı


E ve Mıknatıs Kuvveti E = h = h B 0 2 • Farklı enerji seviyeleri arasındaki fark manyetik alan şiddetiyle doğru orantılıdır. • Jiromanyetik oran, , her çekirdek için sabit bir değerdir. (26, 753 s-1 gauss-1 for H). • 14, 092 gauss manyetik alanda, bir protonun üst enerji seviyesine geçmesi için gerekli frekans 60 MHz dir.

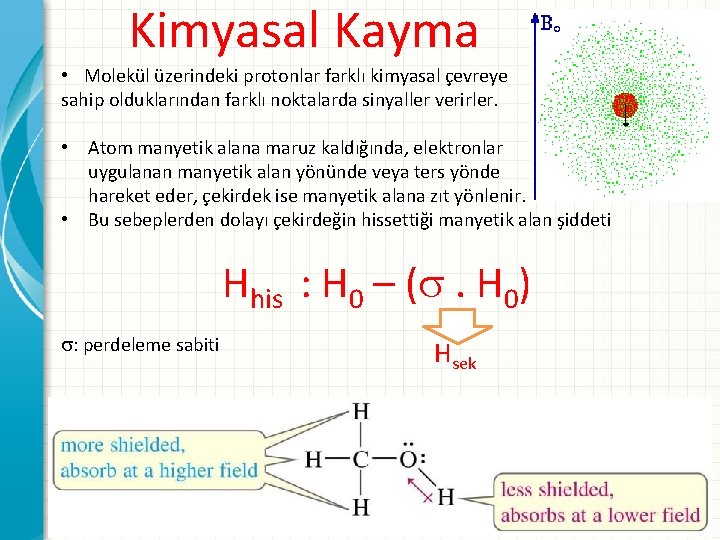
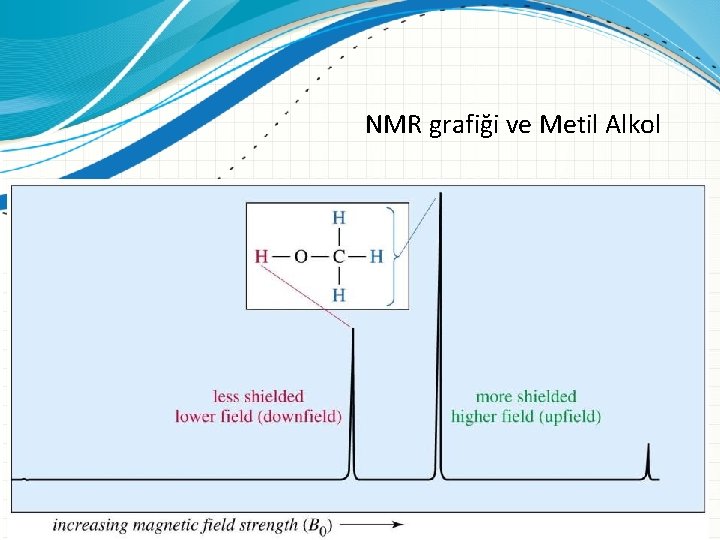
Kimyasal Kayma • Molekül üzerindeki protonlar farklı kimyasal çevreye sahip olduklarından farklı noktalarda sinyaller verirler. • Atom manyetik alana maruz kaldığında, elektronlar uygulanan manyetik alan yönünde veya ters yönde hareket eder, çekirdek ise manyetik alana zıt yönlenir. • Bu sebeplerden dolayı çekirdeğin hissettiği manyetik alan şiddeti Hhis : H 0 – ( . H 0) : perdeleme sabiti Hsek

NMR grafiği ve Metil Alkol

Kimyasal Kayma, (delta) ile ifade edilir. Kimyasal kayma = Sinyalin frekansı-TMS nin frekansı(Hz). 106 Spektrometrede kullanılan radyodalga frekansı(Hz)

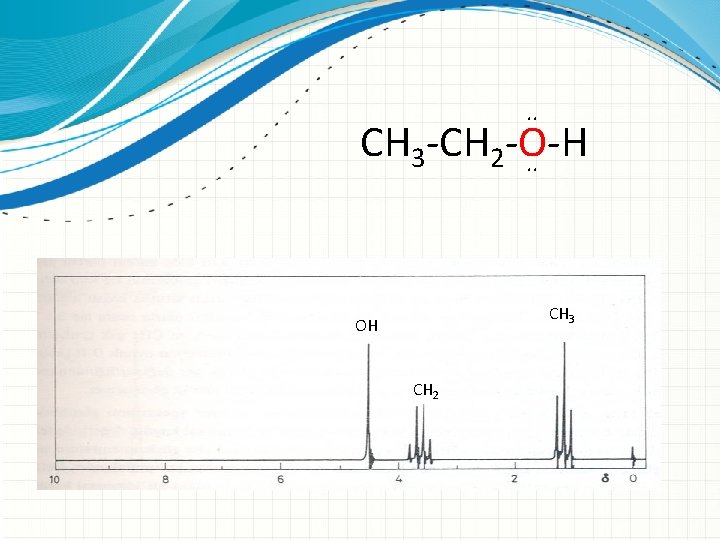
. . CH 3 -CH 2 -O-H. . CH 3 OH CH 2

Spin – Spin Etkileşmesi Piklerin Yarılması Olayı Ø Çekirdeklerin spin enerji düzeyleri bu çekirdeklere komşu ve spini olan başka çekirdekler tarafından değişikliğe uğratılır. Ø Manyetik ve kimyasal çevre yönünden eşdeğer çekirdekler birbirinin NMR sinyallerini etkilemez. Ø Spin-spin etkileşmesi sonucu bir çekirdeğin NMR sinyali, I spin değerine sahip n tane komşu (en fazla 3 bağ uzaklıktaki) çekirdek tarafından (2 n. I + 1) kısma yarılır ve bu pik yarılmasına spin-spin yarılması denir. Ø Buradaki n değeri proton spinini etkileyen eşdeğer ve I = 1/2 spinine sahip çekirdeklerin sayısıdır.

Ø H ler, komşu H sayılarının toplamının 1 fazlasına yarılır. Ø Bu spin-spin yarılmasının miktarı, J ile gösterilen ve birimi Hz olan spin-spin yarılma sabiti ile belirlenir. Ø Buna göre piklerin şiddet oranları aşağıda görülen Pascal üçgeninden bulunabilir

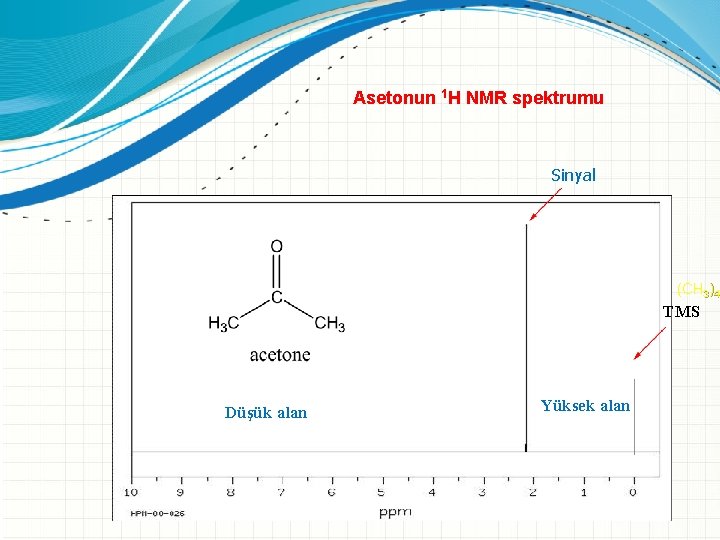
Asetonun 1 H NMR spektrumu Sinyal Düşük alan (CH 3)4 S Yüksek alan TMS Düşük alan Yüksek alan

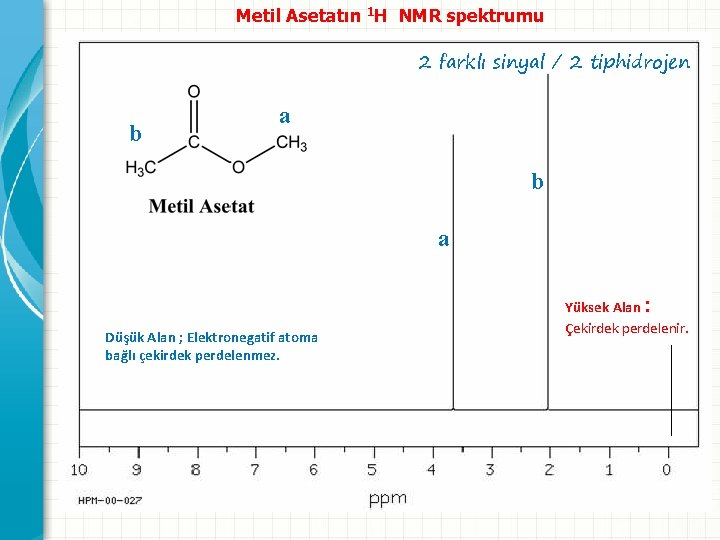
Metil Asetatın 1 H NMR spektrumu 2 farklı sinyal / 2 tiphidrojen b a : Düşük Alan ; Elektronegatif atoma bağlı çekirdek perdelenmez. Yüksek Alan Çekirdek perdelenir.

Bazı Fonksiyonel Gruplara Bağlı Protonların Kimyasal Kayma Değerleri

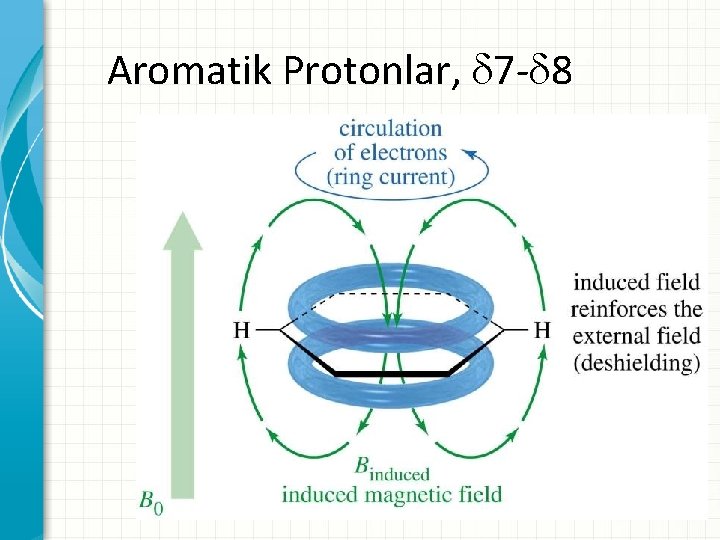
Aromatik Protonlar, 7 - 8

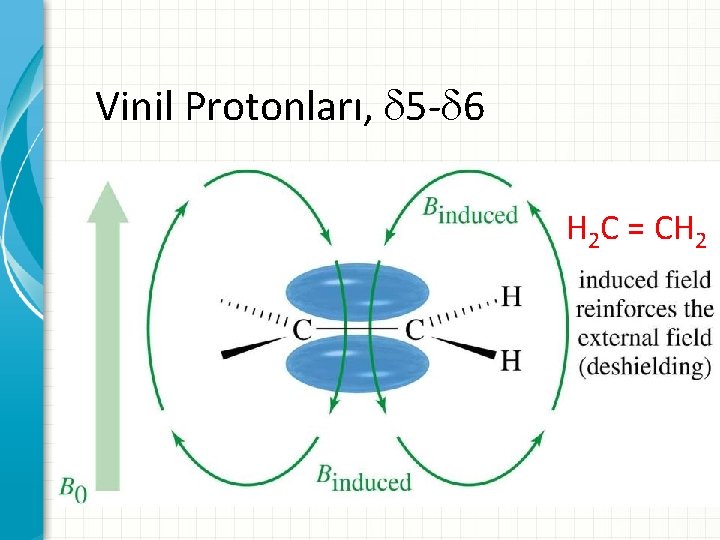
Vinil Protonları, 5 - 6 H 2 C = CH 2

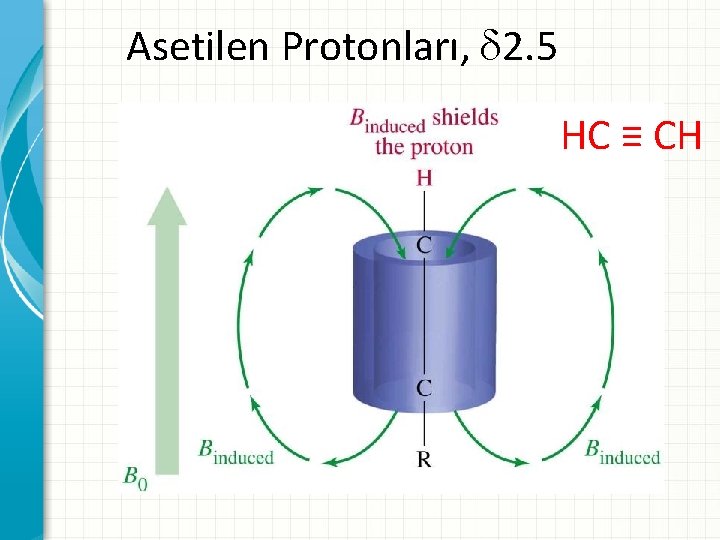
Asetilen Protonları, 2. 5 HC ≡ CH

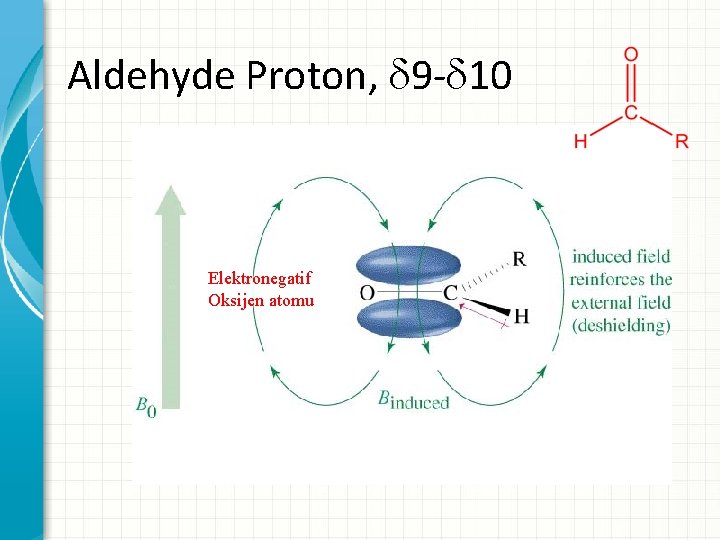
Aldehyde Proton, 9 - 10 Elektronegatif Oksijen atomu

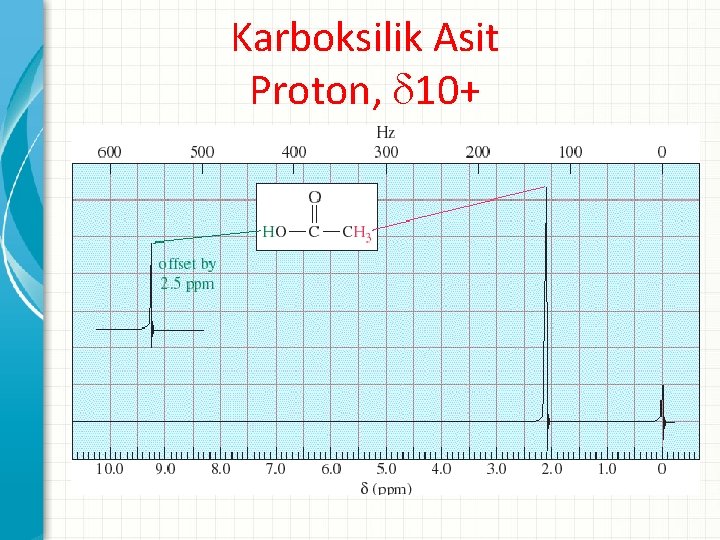
Karboksilik Asit Proton, 10+

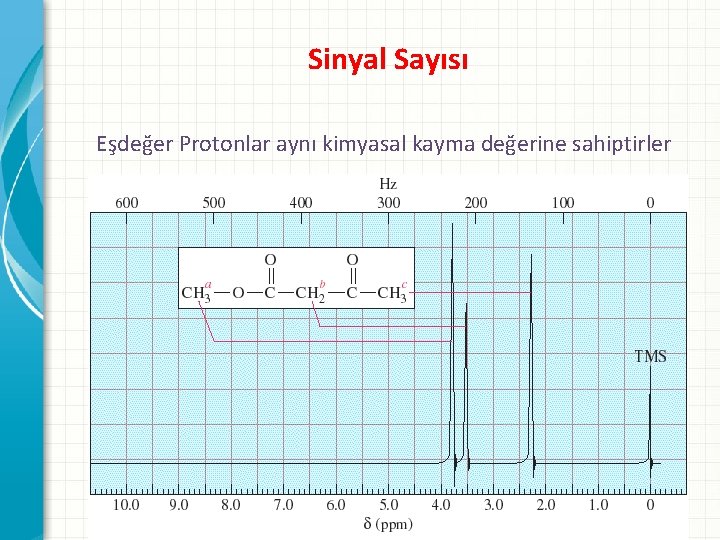
Sinyal Sayısı Eşdeğer Protonlar aynı kimyasal kayma değerine sahiptirler

Sinyal Şiddetleri • Pikin altında kalan, proton sayısını verir • Bu integral yüksekliği olarak bilinir

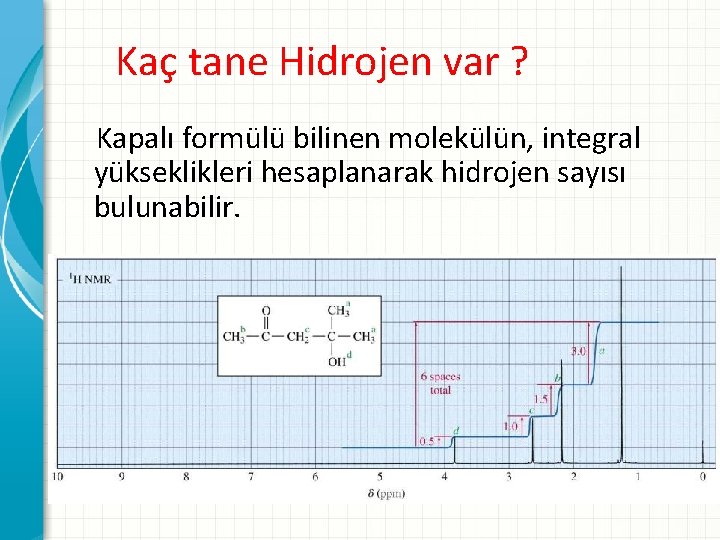
Kaç tane Hidrojen var ? Kapalı formülü bilinen molekülün, integral yükseklikleri hesaplanarak hidrojen sayısı bulunabilir.

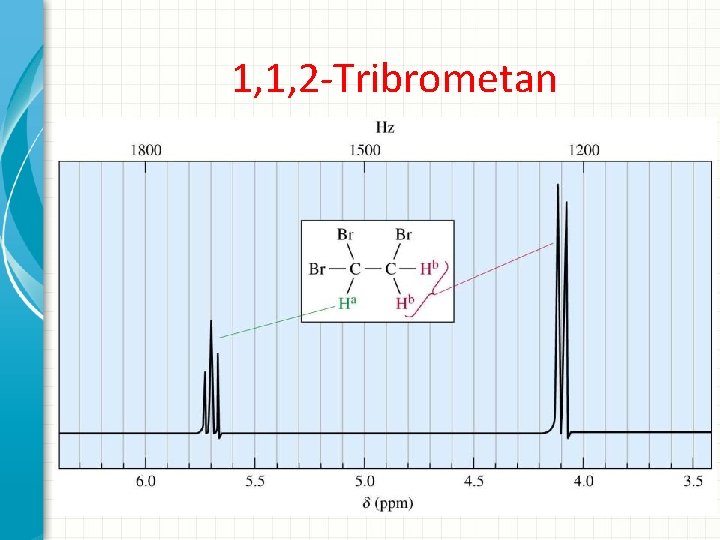
1, 1, 2 -Tribrometan

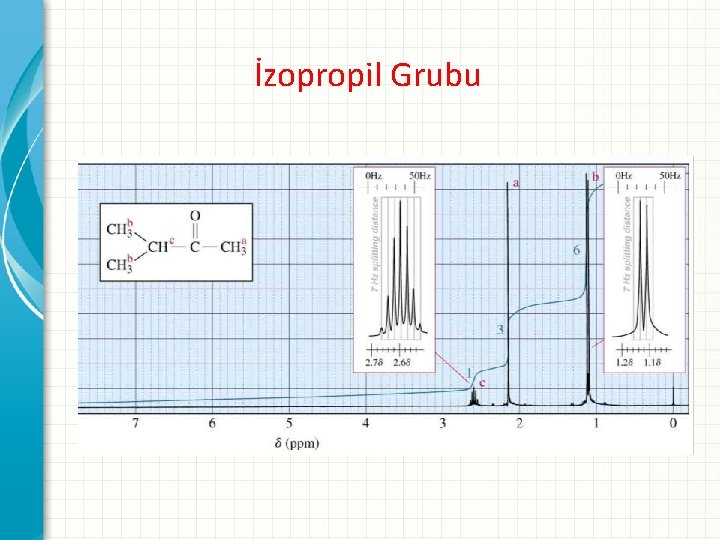
İzopropil Grubu

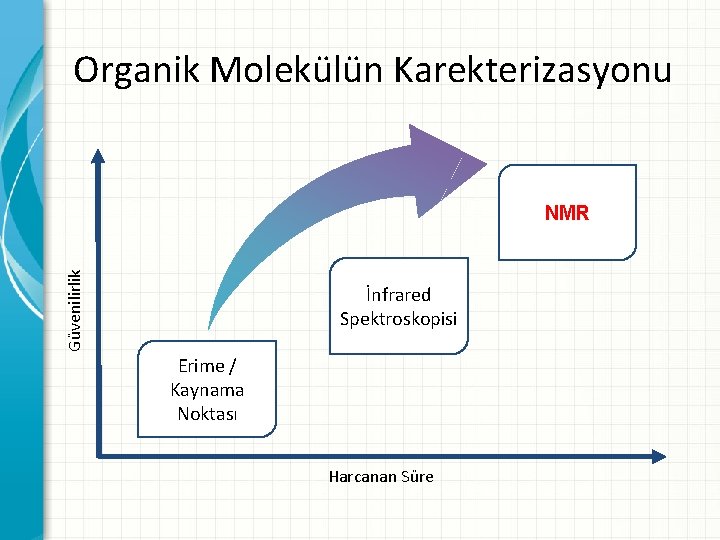
Organik Molekülün Karekterizasyonu Güvenilirlik NMR İnfrared Spektroskopisi Erime / Kaynama Noktası Harcanan Süre