NERNSTOVA JEDNAINA Pripremio Varga Itvan HEMIJSKOPREHRAMBENA SREDNJA KOLA

NERNSTOVA JEDNAČINA Pripremio: Varga Ištvan HEMIJSKO-PREHRAMBENA SREDNJA ŠKOLA ČOKA varga. i@neobee. net

Nernstova jednačina Nemački hemičar i fizičar. Osnivač fizičke hemije. 1906. godine formulisao je treći zakon termodinamike. Na temeljima kvantne teorije, vršio je ispitivanje specifične toplote čvrstih tela na vrlo niskim temperaturama. Nobelovu nagradu dobio je 1921. godine.

Za svaku elektrodu karakterističan je elektrodni potencijal i elektrodna reakcija koja se odigrava na granici faza, a koja se može prikazati sledećom jednačinom: � Mz+ + ze- M Pomoću Nernstove jednačine se može izračunati elektrodni potencijal.

elektrodni potencijal date elektrode, njen standardni ili normalni potencijal, aoks i ared aktivnosti oksidovanog i redukovanog oblika koji se javljaju u elektrohemijskoj reakciji na toj elektrodi.

Prevođenjem prirodnog logaritma u dekadni i uvrštavanjem vrednosti za konstante, na temperaturi 298 K dobija se: Na metalnoj elektrodi u rastvoru sa korespondentnim jonima Nernstova jednačina ima oblik:

U slučaju razblaženih rastvora aktivnost (a) se može zameniti količinskom koncentracijom (c), tada Nernstova jednačina ima oblik: Iz navedene jednačine sledi da i dve iste elektrode potopljene u iste rastvore različite koncentracije mogu obrazovati galvanski element. Ovakvi elementi nazivaju se koncentracioni galvanski elementi.

Elektrohemijski niz elemenata Ako se elementi poređaju po porastu standardnog elektrodnog potencijala dobija se elektrohemijski niz ili naponski red (Voltin niz). � Nula elektrodnog potencijala, odgovara potencijalu standardne vodonične elektrode. �
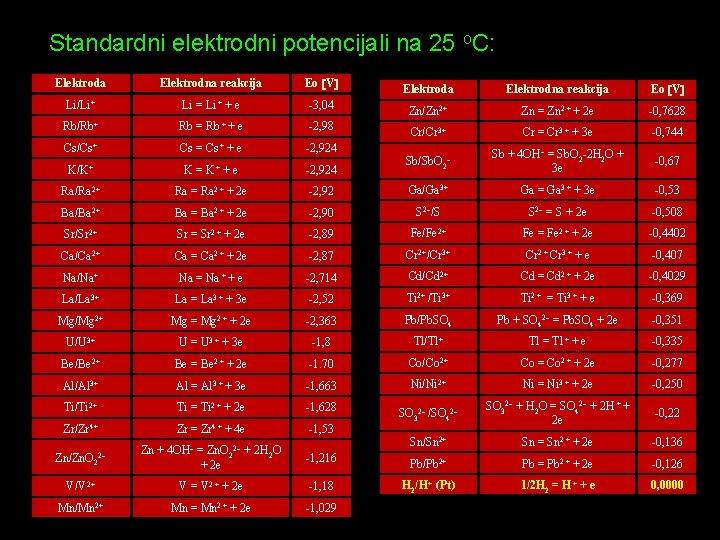
Standardni elektrodni potencijali na 25 o. C: Elektroda Li/Li+ Elektrodna reakcija Eo V -3, 04 Zn/Zn 2+ Zn = Zn 2 + + 2 e -0, 7628 Cr/Cr 3+ Cr = Cr 3 + + 3 e -0, 744 Sb + 4 OH– = Sb. O 2 -2 H 2 O + 3 e -0, 67 Li = Li + + Rb/Rb+ Rb = Rb + + e -2, 98 Cs/Cs+ Cs = Cs + + e -2, 924 K/K+ K = K++ e -2, 924 Sb/Sb. O 2– Ra/Ra 2+ Ra = Ra 2 + + 2 e -2, 92 Ga/Ga 3+ Ga = Ga 3 + + 3 e -0, 53 Ba/Ba 2+ Ba = Ba 2 + + 2 e -2, 90 S 2–/S S 2– = S + 2 e -0, 508 Sr/Sr 2+ Sr = Sr 2 + + 2 e -2, 89 Fe/Fe 2+ Fe = Fe 2 + + 2 e -0, 4402 Ca/Ca 2+ Ca = Ca 2 + + 2 e -2, 87 Cr 2+/Cr 3+ Cr 2 + Cr 3 + + e -0, 407 Na/Na+ Na = Na + + e -2, 714 Cd/Cd 2+ Cd = Cd 2 + + 2 e -0, 4029 La/La 3+ La = La 3 + + 3 e -2, 52 Ti 2+ /Ti 3+ Ti 2 + = Ti 3 + + e -0, 369 Mg/Mg 2+ Mg = Mg 2 + + 2 e -2, 363 Pb/Pb. SO 4 Pb + SO 42– = Pb. SO 4 + 2 e -0, 351 U/U 3+ U = U 3 + + 3 e -1, 8 Tl/Tl+ Tl = Tl + + e -0, 335 Be/Be 2+ Be = Be 2 + + 2 e -1. 70 Co/Co 2+ Co = Co 2 + + 2 e -0, 277 Al/Al 3+ Al = Al 3 + + 3 e -1, 663 Ni/Ni 2+ Ni = Ni 3 + + 2 e -0, 250 Ti/Ti 2+ Ti = Ti 2 + + 2 e -1, 628 SO 32– /SO 42– SO 32– + H 2 O = SO 42– + 2 H + + 2 e -0, 22 Sn/Sn 2+ Sn = Sn 2 + + 2 e -0, 136 Zr/Zr 4+ Zr = Zr 4 + + e Eo V 4 e -1, 53 Zn + 4 OH– = Zn. O 22– + 2 H 2 O + 2 e -1, 216 Pb/Pb 2+ Pb = Pb 2 + + 2 e -0, 126 V/V 2+ V = V 2 + + 2 e -1, 18 H 2/H+ (Pt) 1/2 H 2 = H + + e 0, 0000 Mn/Mn 2+ Mn = Mn 2 + + 2 e -1, 029 Zn/Zn. O 2 2–
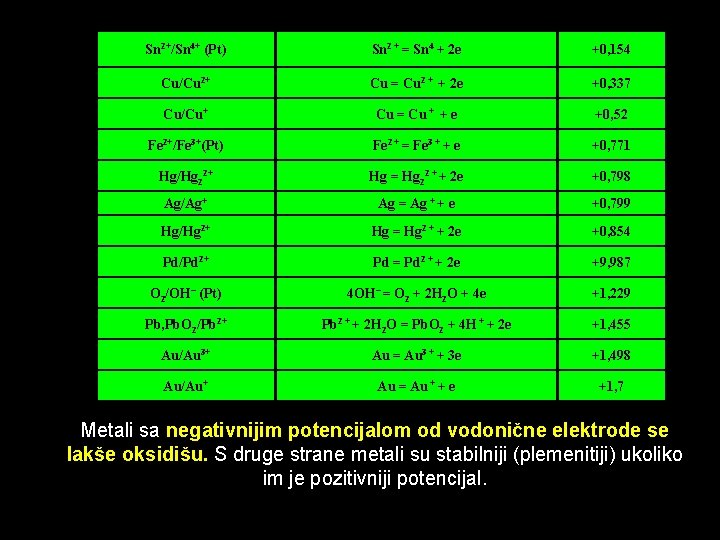
Sn 2+/Sn 4+ (Pt) Sn 2 + = Sn 4 + 2 e +0, 154 Cu/Cu 2+ Cu = Cu 2 + + 2 e +0, 337 Cu/Cu+ Cu = Cu + + e +0, 52 Fe 2+/Fe 3+(Pt) Fe 2 + = Fe 3 + + e +0, 771 Hg/Hg 22+ Hg = Hg 22 + + 2 e +0, 798 Ag/Ag+ Ag = Ag + + e +0, 799 Hg/Hg 2+ Hg = Hg 2 + + 2 e +0, 854 Pd/Pd 2+ Pd = Pd 2 + + 2 e +9, 987 O 2/OH– (Pt) 4 OH– = O 2 + 2 H 2 O + 4 e +1, 229 Pb, Pb. O 2/Pb 2+ Pb 2 + + 2 H 2 O = Pb. O 2 + 4 H + + 2 e +1, 455 Au/Au 3+ Au = Au 3 + + 3 e +1, 498 Au/Au+ Au = Au + + e +1, 7 Metali sa negativnijim potencijalom od vodonične elektrode se lakše oksidišu. S druge strane metali su stabilniji (plemenitiji) ukoliko im je pozitivniji potencijal.

Svaki metal istiskuje iz rastvora jon metala čiji je potencijal pozitivniji od njegovog. � Reakcija istiskivanja jona iz rastvora metalom sa negativnijim potencijalom naziva se cementacija metala (npr. prečišćavanje elektrolita za dobijanje cinka od jona bakra, zlata ili srebra dodavanjem praha cinka). � Metali koji su u elektrohemijskom nizu negativniji od vodonika rastvaraju se u kiselinama oslobađajući vodonik. Metali koji su pozitivniji od vodonika reaguju samo sa kiselinama koje su jaka oksidaciona sredstva (npr. HNO 3) ali bez izdvajanja vodonika. � �

� Oksidaciona sposobnost oksidovanog oblika (katjon, nemetal) raste u smeru porasta elektrodnog potencijala od (–) ka (+), a redukciona sposobnost redukovanog oblika (metal, anjon) raste u smeru od pozitivnog ka negativnom elektrodnom potencijalu.
- Slides: 11