Nebezpen Ltky Nzev opory Fyzikln a chemick vlastnosti

Nebezpečné Látky Název opory – Fyzikální a chemické vlastnosti Látek Josef NAVRÁTIL Operační program Vzdělávání pro konkurenceschopnost Projekt: Vzdělávání pro bezpečnostní systém státu (reg. č. : CZ. 1. 01/2. 2. 00/15. 0070)

Stavy hmoty 3 skupenské stavy Plyny Kapaliny Tuhé látky

Plyny Vyplňují celý prostor, který mají k dispozici Malá hustota Značná tepelná roztažnost a stlačitelnost Rozhraní není ostré

Kapaliny Mají určitý objem Přizpůsobují se tvaru nádob Vyšší hustota Nižší závislost na teplotě a tlaku

Tuhé látky Určitý objem i tvar Nejvyšší hustota Minimální roztažnost a stlačitelnost

LÁTKY A JEJICH SMĚSI

Klasifikace látek Heterogenní x homogenní Chemicky čisté látky – stálé vlastnosti (hustota, bod tání a varu…) Prvky – atomy se stejným protonovým číslem (112) Sloučeniny (8 milionů)

Směsi Směs: látka, obsahující min. 2 složky, je možné je oddělit fyzikálně-chem. metodami Homogenní: má ve všech svých částech stejné vlastnosti (př. : vzduch, roztoky solí), částice < 10 -9 m Heterogenní: skládá se ze dvou nebo více homogenních oblastí ( fází), (př. : směs práškového zinku a práškové síry), částice > 10 -7 m

Směsi Fáze: Homogenní část soustavy, oddělená od ostatních částí rozhraním, na němž se vlastnosti mění skokem Při přechodu z jedné fáze do druhé se prudce mění fyzikální a chemické vlastnosti

Směsi Disperzní soustavy: někdy se řadí k heterogenním směsím ◦ Hrubě disperzní soustavy aerosoly (mlha, kouř, dým) emulze (mléko) suspenze (směs Ca(OH)2 a vody) pěny (šlehačka) ◦ Jemně disperzní soustavy nepravé neboli koloidní roztoky rozptýlené část. se neusazují (vaječný bílek)
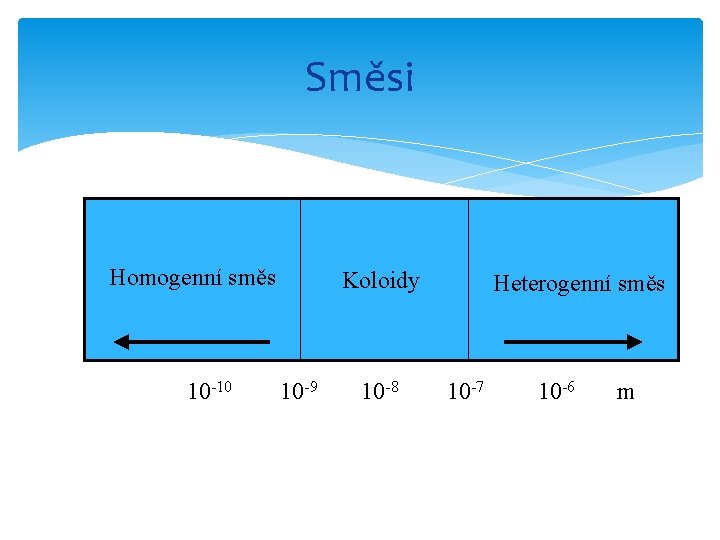
Směsi Homogenní směs 10 -10 Koloidy 10 -9 10 -8 Heterogenní směs 10 -7 10 -6 m

Roztoky Roztoky: homogenní, nejméně dvousložkové soustavy látek Rozpouštění: heterogenní proces za vzniku homogenní směsi (opak: srážení) Rozpouštědlo: látka, která je v roztoku v nadbytku, v soustavě plynkapalina, pevná látka-kapalina je to kapalina

Rozpouštědla - druhy Rozpouštědla: Polární – např. voda, methanol: dobře rozpouští látky s iontovou vazbou, dochází k hydrataci volných iontů Nepolární – např. chloroform, uhlovodíky: nemísí se s vodou

Druhy roztoků Kapalné Tuhé látky v kapalině ( cukr ve vodě) Kapaliny v kapalině (ocet ve vodě) Plyny v kapalině ( kyslík ve vodě) Plynné Plyny v plynu (vzduch) Tuhé látky v tuhé látce (slitiny kovů)

Druhy roztoků Dělení podle vlastností rozpouštěné látky: roztoky neelektrolytů - nevedou el. proud: rozpouštěná látka obsahuje nepolární nebo slabě pol. vazby roztoky elektrolytů - vedou el. proud: rozpouštění iontových sloučenin v polárních rozpouštědlech

Složení roztoků Neomezeně mísitelné látky: vytvoří homogenní směs bez ohledu na poměr - methanol+ethanol Omezeně mísitelné látky: tvoří homogenní směs jen při určitém rozsahu poměrů nenasycené roztoky Rozpustnost: hmotnost látky, která se za daných podmínek rozpustí v určitém množství rozpouštědla za vzniku nasyceného roztoku

Rozpustnost ve vodě Významný parametr Nerozpustné – pod 0, 1 mg/l Tabulkové údaje Křivky rozpustnosti - většinou se stoupající teplotou stoupá rozpustnost

Rozpustnost - koncentrace Koncentrace: množství látky v roztoku Vyjádření: hmotnostní zlomek : w wa = hm. látky / hm. roztoku(látka+rozp. ) hmotnostní procento: w. 100 objemové procento: objem % = objem látky / objem roztoku. 100 molární koncentrace: c. A = počet molů látky / objem roztoku

Látky rozpustné ve vodě Oxidy alkalických kovů alkalických zemin Oxidy nekovů mimo Si. O 2 Hydroxidy alkalických kovů alkalických zemin Všechny dusičnany, většina síranů a chloridů Uhličitany draslíku a sodíku

Nerozpustné Oxidy ostatní Hydroxidy ostatní Dusičnan Bi Sírany Ba, Sr, Ca, Ag, Ra Chloridy Ag, Pb, Hg Většina uhličitanů a fosforečnanů

CHEMICKÉ REAKCE

Chemické reakce - dělení podle vnějších změn: skladné - syntézy (jednodušší molekuly složitější molekuly) rozkladné (složitější molekuly jednodušší molekuly) substituční - vytěsňovací (jedna skupina nahradí jinou) konverze - podvojná záměna ( výměna skupin) neutralizace srážecí reakce Ag. NO 3

Chemické reakce - rozdělení podle skupenství reaktantů: Reakce homogenní plyn + plyn Reakce heterogenní plyn + kapalina

Chemické reakce - rozdělení podle přenášených částic: Reakce acidobazické: zásada sůl kyselina + Reakce oxidačně-redukční: přenos elektronů mezi reagujícími látkami Komplexotvorné: koordinačně kovalentní vazby tvorba

Chemické reakce - termodynamika Fyzikální a chemické děje spojené s energetickými změnami Děj izobarický: za konstantního tlaku - probíhá tak většina laboratorních i průmyslových reakcí Děj izotermický: za konstantní teploty

Chemické reakce - termodynamika Pojmy: Soustava: část prostoru s jeho hmotnou náplní (kádinka a roztok) otevřená - vyměňuje s okolím energii i hmotu uzavřená - vyměňuje s okolím energii izolovaná - neprostupné stěny

Chemické reakce - termodynamika Pojmy: Stavové veličiny: veličiny popisující aktuální stav soustavy extenzivní: závisí na velikosti systému (hmotnost, objem, látkové množství) intenzivní: nezávisí na velikosti systému (hustota, tlak, teplota)

Termochemie Studuje tepelné zabarvení chemické reakce Pojmy: Reakce: exotermní - teplo se uvolňuje endotermní - teplo se spotřebovává Standardní stav: 298, 15 K, 101, 325 k. Pa Entalpie H: extenzivní stavová veličina, popisuje výměnu tepla s okolím, absolutní hodnotu nelze změřit, lze stanovit změnu entalpie vztaženou na std.

Termochemie Množství tepla, které soustava během reakce (konst. p) s okolím vymění reakční teplo Δ H Exotermní děje: Δ H záporná Endotermní děje: Δ H kladná
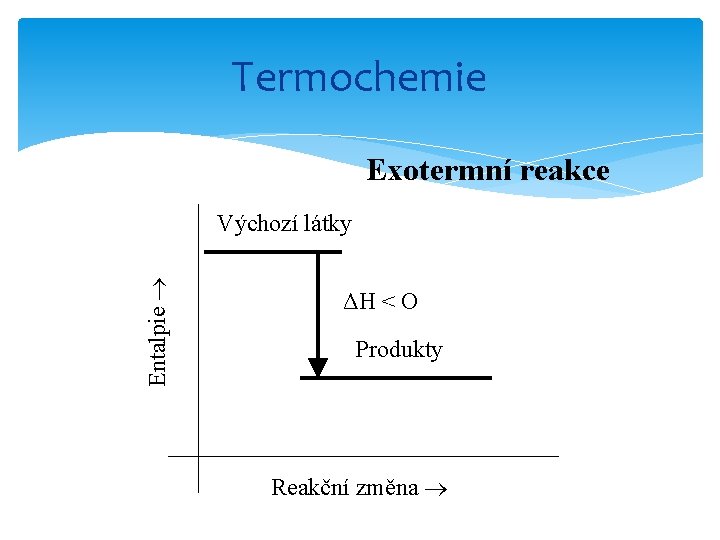
Termochemie Exotermní reakce Entalpie Výchozí látky ΔH < O Produkty Reakční změna
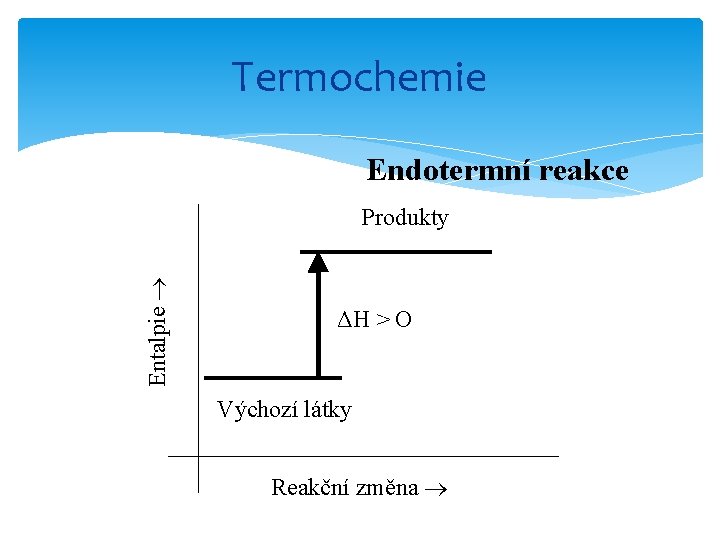
Termochemie Endotermní reakce Entalpie Produkty ΔH > O Výchozí látky Reakční změna

Termochemické zákony I. termochemický zákon (Laplaceův. Lavoisierův): Reakční teplo přímé i zpětné reakce je až na znaménko stejné hoření vodíku v kyslíku : 2 H 2(g) + O 2(g) 2 H 2 O(g) Δ H = -483, 6 k. J rozklad vody: 2 H 2 O(g) 2 H 2(g) + O 2(g) Δ H = 483, 6 k. J

Termochemické zákony II. termochemický zákon (Hessův): Výsledné reakční teplo chemické reakce nezávisí na způsobu jejího průběhu, ale pouze na počátečním a konečném stavu ( výsledné reakční teplo = součet jednotlivých) 1) 2 S(s) + 2 O 2(g) 2 SO 2(g) 2*ΔH = 2*-296, 8 k. J 2) 2 SO 2 (g) + O 2(g) 2 SO 3(g) ΔH = ? ---------------------------- 2 S(s) + 3 O 2(g) 2 SO 3(g) Δ H = -791, 4 k. J 2*(-296, 8 k. J)+ x = -791, 4 k. J x= -197, 8 k. J

Standardní slučovací teplo Označení (Δ H 0298 )sluč Reakční teplo = změna entalpie reakce, při které vzniká 1 mol sloučeniny přímo z prvků Prvky i sloučeniny musí být ve std. stavu Rozměr: k. J/mol Std. slučovací tepla prvků = 0 Výpočet: = Δ H 0 sluč (prod. ) - Δ H 0 sluč (reaktantů) Δ H 0298

Standardní spalné teplo Označení (Δ H 0298 )spal Reakční teplo = změna entalpie reakce, při které je 1 mol látky spálen v nadbytku kyslíku Reaktanty i produkty musí být ve std. stavu Rozměr: k. J/mol Spalná tepla prvků 0 Výpočet: = Δ H 0 spal (reaktantů) - Δ H 0 spal (prod. ) Δ H 0298

Chemické reakce - kinetika Reakční kinetika: popisuje chemické reakce matematickými vztahy Chemická reakce: děj, jehož podstatou jsou srážky molekul reaktantů, zánik některých vazeb a vznik vazeb nových

Chemické reakce - kinetika Teorie aktivních srážek: 1) nutná srážka mezi reag. molekulami 2) částice musí mít dostatečnou energii 3) částice musí mít vhodnou prostorovou orientaci 4) minimální účinná energie aktivační 5) aktivační energie = součtu energií všech zanikajících vazeb
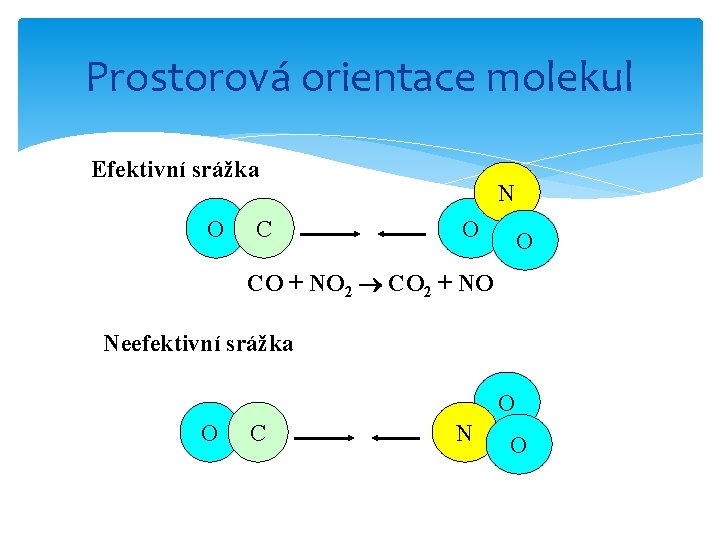
Prostorová orientace molekul Efektivní srážka O C N O O CO + NO 2 CO 2 + NO Neefektivní srážka O O C N O

Chemické reakce - kinetika Rozdíl mezi aktivační energií reakce přímé a zpětné určuje tepelné zabarvení chemické reakce - reakční teplo Δ H
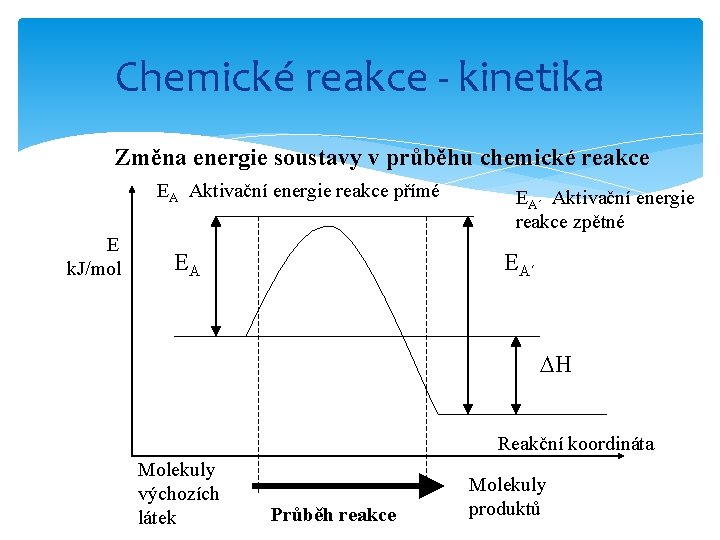
Chemické reakce - kinetika Změna energie soustavy v průběhu chemické reakce EA Aktivační energie reakce přímé E k. J/mol EA EA´ Aktivační energie reakce zpětné EA´ H Reakční koordináta Molekuly výchozích látek Průběh reakce Molekuly produktů
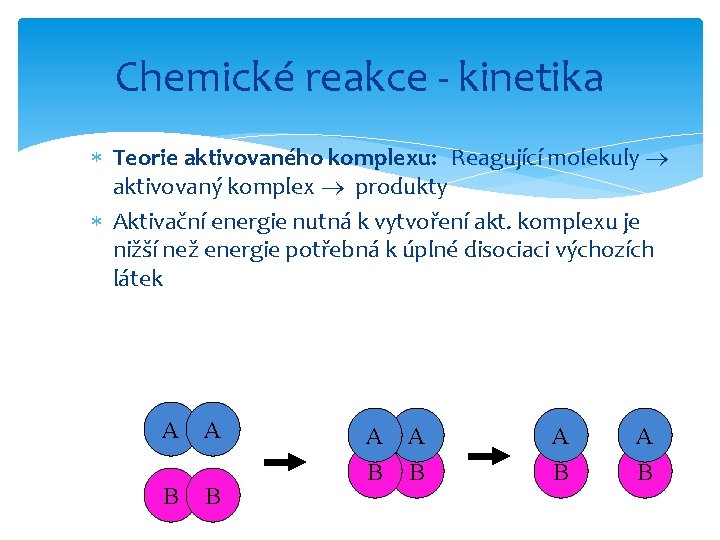
Chemické reakce - kinetika Teorie aktivovaného komplexu: Reagující molekuly aktivovaný komplex produkty Aktivační energie nutná k vytvoření akt. komplexu je nižší než energie potřebná k úplné disociaci výchozích látek A A B B A B A B

Chemické reakce - kinetika Rychlost reakce: Časový úbytek molární koncentrace reaktantu, nebo přírůstek koncentrace produktu a. A + b. B c. C + d. D v 1 a. A + b. B c. C + d. D v 2 A, B reaktanty C, D produkty ustavení dynamické rovnováhy: v 1 = v 2

Chemické reakce - kinetika Vliv koncentrace: Gultberg-Waagův zákon: rychlost reakce je funkcí okamžitých koncentrací reaktantů. Vliv teploty: van´t Hoffovo pravidlo: Zvýšení teploty výchozích látek o 10 °C zvýší rychlost reakce 2 - 4 násobně Vliv katalyzátorů: snižují tzv. aktivační energii potřebnou k provedení reakce katalyzátory x inhibitory

Elektrolytická disociace látek Arrhenius – teorie elektrolytické disociace Iontové sloučeniny a sloučeniny s polárními kovalentními vazbami ve vodných roztocích disociují na ionty Míra štěpení – disociační stupeň a disociační konstanta ( ) = počet disociovaných molekul/počet všech rozpuštěných molekul (0, 1)

Elektrolyty Silné elektrolyty: 1 , HCl, HNO 3, Na. OH, KOH, řada solí Slabé elektrolyty: < 0, 1 H 2 S, HCN, organické kyseliny a zásady

Disociační konstanta Vyjadřuje rovnováhu mezi disociovanými a nedisociovanými látkami BA B+ + A K = (B+). (A-)/(BA) p. K Velikost p. K rozpoznání slabých a silných elektrolytů

Teorie kyselin a zásad Arrhenius: teorie kyselin a zásad (1877) Kyselina: látka, schopná ve vodných roztocích odštěpovat vodíkový kation H+ Zásada: látka, schopná ve vodných roztocích poskytovat anion OH Neutralizace: vzájemná reakce kyseliny a zásady, kdy vzniká sůl a voda Na+OH- + H+Cl - Na+Cl- + H O 2 Neřeší nevodné prostředí

Teorie kyselin a zásad Bronsted-Lowry (1923): Kyselina : látka odštěpující proton (donor protonů) Zásada: látka, schopná přijmou proton (akceptor protonů) Protolytická reakce: dochází k výměně protonů nebo H+ Protolyt: kyseliny a zásady Amfolyt: chová se jako kyselina i zásada

Kyseliny a zásady Kyselina je tím silnější, čím snadněji odštěpuje proton Zásada je tím silnější, čím snadněji váže proton
![Kyseliny a zásady HB + H 2 O H 3 O+ + B] rovnovážná Kyseliny a zásady HB + H 2 O H 3 O+ + B] rovnovážná](http://slidetodoc.com/presentation_image_h/8c31b22632901c40b1471af4fca382d2/image-50.jpg)
Kyseliny a zásady HB + H 2 O H 3 O+ + B] rovnovážná konst. [H 3 O+]. [BK= —————— [HB]. [H 2 O ] pro zředěné roztoky: konstanta acidity [H 3 O+]. [B- ] KA = K [H 2 O ] = ———— —— [HB] čím je KA menší, tím je kyselina slabší
![Kyseliny a zásady pro zředěné roztoky: konstanta bazicity [Z+]. [OH- ] KB = ————— Kyseliny a zásady pro zředěné roztoky: konstanta bazicity [Z+]. [OH- ] KB = —————](http://slidetodoc.com/presentation_image_h/8c31b22632901c40b1471af4fca382d2/image-51.jpg)
Kyseliny a zásady pro zředěné roztoky: konstanta bazicity [Z+]. [OH- ] KB = ————— — [ZOH] čím je KB menší, tím je zásada slabší Síla kyselin ————stoupá———— Hn. XOn+1 ……Hn. XOn+3

Roztoky Kyselé, zásadité, neutrální Koncentrace OH- nebo H 3 O+ Neutrální roztok: molární konc. OH- nebo H 3 O+ je stejná Kyselé roztoky: molární koncentrace H 3 O+ je větší než 1, 0. 10 -7 mol/l Zásadité roztoky: molární koncentrace H 3 O+ je menší než 1, 0. 10 -7 mol/l

Roztoky Vyjádření kyselosti (zásaditosti): p. H -kladná hodnota exponentu koncentrace H 3 O+ Vyjádření kyselosti (zásaditosti): p. OH -kladná hodnota exponentu koncentrace OH p. H + p. OH = 14 Kyselé roztoky: p. H < 7 Zásadité roztoky: p. H > 7 Stanovení p. H: indikátory(barevné), papírky, p. H-metry

Hydrolýza Protolytická reakce solí s vodou Dochází k posunu p. H Silná kyselina + slabá zásada kyselý roztok Slabá kyselina + silná zásada zásaditý roztok Silná kyselina + silná zásada neutrální roztok Ovlivnění teplotou a ředěním
- Slides: 54