NDR MTOKO BYOLOJK OKSDASYON ELEKTRONT AIMA ZNCR OKSDATFF
NDRİ MİTOKO BİYOLOJİK OKSİDASYON ELEKTRONT AŞIMA ZİNCİRİ OKSİDATİFF OSFORİLASYON PROF. DR. ORHAN CANBOLAT 0 C OC
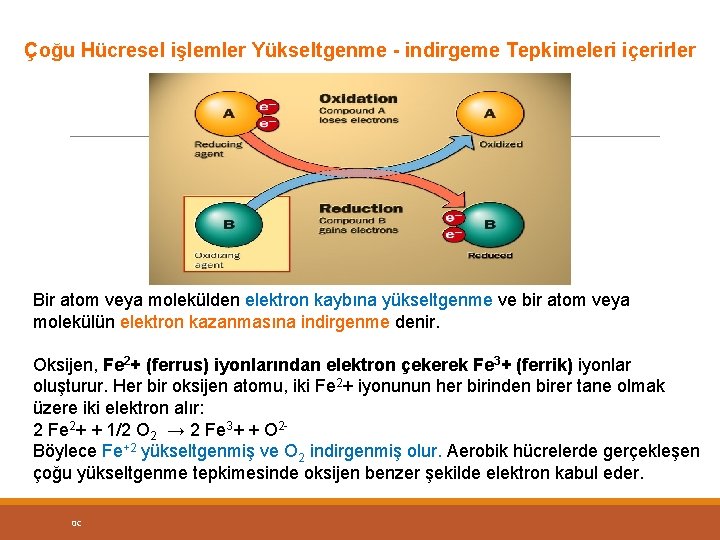
Çoğu Hücresel işlemler Yükseltgenme - indirgeme Tepkimeleri içerirler Bir atom veya molekülden elektron kaybına yükseltgenme ve bir atom veya molekülün elektron kazanmasına indirgenme denir. Oksijen, Fe 2+ (ferrus) iyonlarından elektron çekerek Fe 3+ (ferrik) iyonlar oluşturur. Her bir oksijen atomu, iki Fe 2+ iyonunun her birinden birer tane olmak üzere iki elektron alır: 2 Fe 2+ + 1/2 O 2 → 2 Fe 3+ + O 2 - Böylece Fe+2 yükseltgenmiş ve O 2 indirgenmiş olur. Aerobik hücrelerde gerçekleşen çoğu yükseltgenme tepkimesinde oksijen benzer şekilde elektron kabul eder. 0 C

Yükseltgenme ve İndirgenme tepkimeleri Birçok biyolojik açıdan önemli yükseltgenme ve indirgenme tepkimeleri, yalıtılmış elektronların aktarımından çok, hidrojen atomlarının çıkarılması veya eklenmesini içerir. Elektronlar mutlaka doğrudan bir atom veya molekülden diğerine aktarılmalıdırlar. Elektronlar eşzamanlı olarak daha pozitif indirgenme potansiyeline sahip atomlara ve moleküllere doğru hareket ederler. 0 C
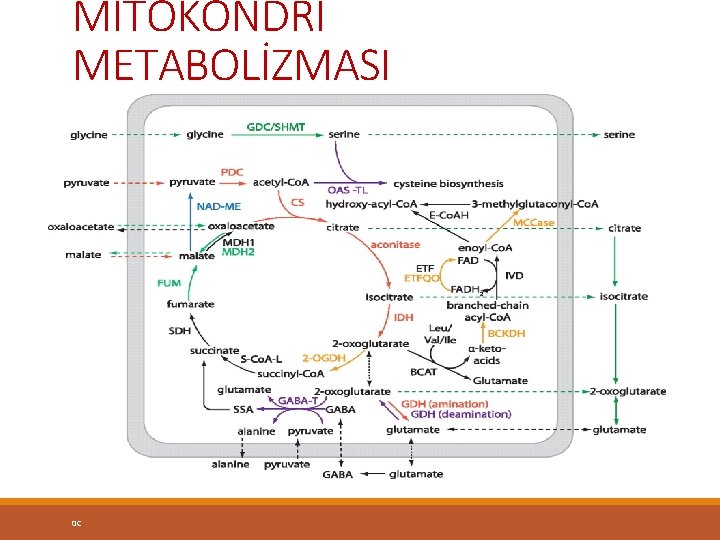
MİTOKONDRİ METABOLİZMASI 0 C

MİTOKONDRİ Şekilleri (veya uzun silindirik) ve büyüklükleri (çap: 0. 2 -1 μm, uzunlukları: 2 -6 μm) farklılıklar gösterir. Mitokondri çift membranla çevrili bir organeldir. Çift membran iki mitokondriyal kompartman oluşturur Membalar arası alan 40 -80 Ao genişliğindedir. Bazı enzimler bulunur. Sayıları değişkendir (1 -2000). Eritrositlerde, bakterilerde ve yeşil alglerde mitokondri yoktur. Hücre içindeki yerleşimleri farklılık gösterir 0 C
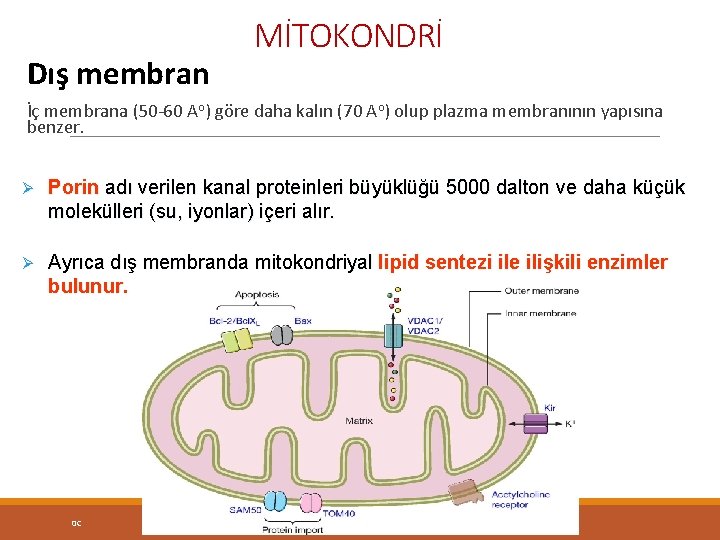
Dış membran MİTOKONDRİ İç membrana (50 -60 Ao) göre daha kalın (70 Ao) olup plazma membranının yapısına benzer. Ø Porin adı verilen kanal proteinleri büyüklüğü 5000 dalton ve daha küçük molekülleri (su, iyonlar) içeri alır. Ø Ayrıca dış membranda mitokondriyal lipid sentezi ile ilişkili enzimler bulunur. 0 C
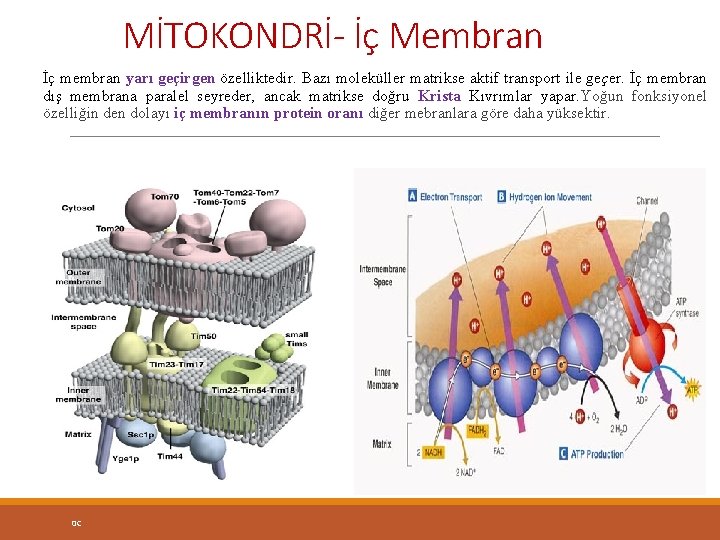
MİTOKONDRİ- İç Membran İç membran yarı geçirgen özelliktedir. Bazı moleküller matrikse aktif transport ile geçer. İç membran dış membrana paralel seyreder, ancak matrikse doğru Krista Kıvrımlar yapar. Yoğun fonksiyonel özelliğin den dolayı iç membranın protein oranı diğer mebranlara göre daha yüksektir. 0 C

MİTOKONDRİ- Matrix İç membranın çevrelediği alandır. Bol miktarda protein molekülü, çeşitli reaksiyon enzimleri , mt. DNA, ribozomlar ve t. RNA bulunur. Ø Matrikste granül sayısı azdır. Hücre içindeki kalsiyum ve magnezyum gibi katyonların fazlası mitokondriye geçerek granüllere bağlanır. Depolanan bu katyonlar gerektiğinde tekrar sitozole geri verilir. 0 C

MİTOKONDRİAL DNA 0 C
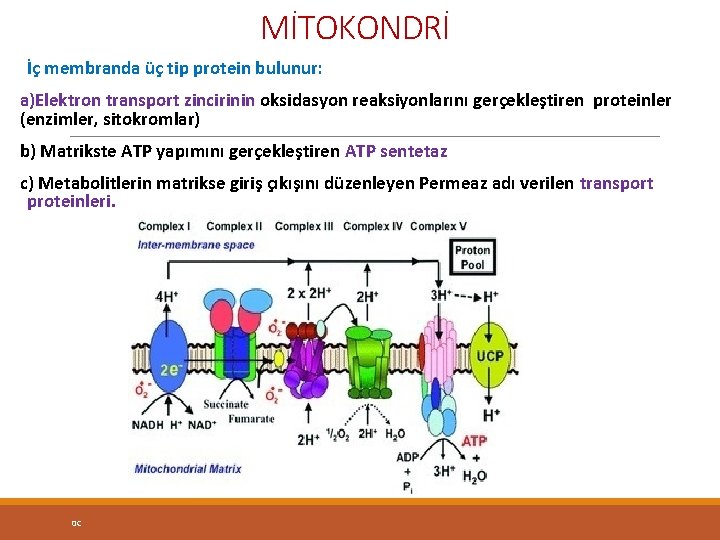
MİTOKONDRİ İç membranda üç tip protein bulunur: a)Elektron transport zincirinin oksidasyon reaksiyonlarını gerçekleştiren proteinler (enzimler, sitokromlar) b) Matrikste ATP yapımını gerçekleştiren ATP sentetaz c) Metabolitlerin matrikse giriş çıkışını düzenleyen Permeaz adı verilen transport proteinleri. 0 C
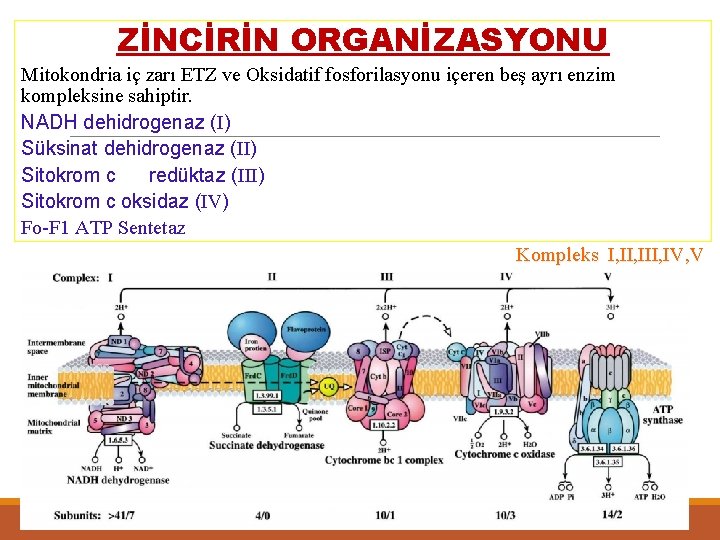
ZİNCİRİN ORGANİZASYONU Mitokondria iç zarı ETZ ve Oksidatif fosforilasyonu içeren beş ayrı enzim kompleksine sahiptir. NADH dehidrogenaz (I) Süksinat dehidrogenaz (II) Sitokrom c redüktaz (III) Sitokrom c oksidaz (IV) Fo-F 1 ATP Sentetaz Kompleks I, III, IV, V İntermembran Alanı 0 C

ETZ KOMPENENTLERİ NADH Flavoprotein FMN, FMNH 2, FAD, Demir-sülfür proteini ( Fe - S ) Ubikinon ( CO - Q ) Sitokromlar( a, a , b, b , c, c ) Cu 0 C
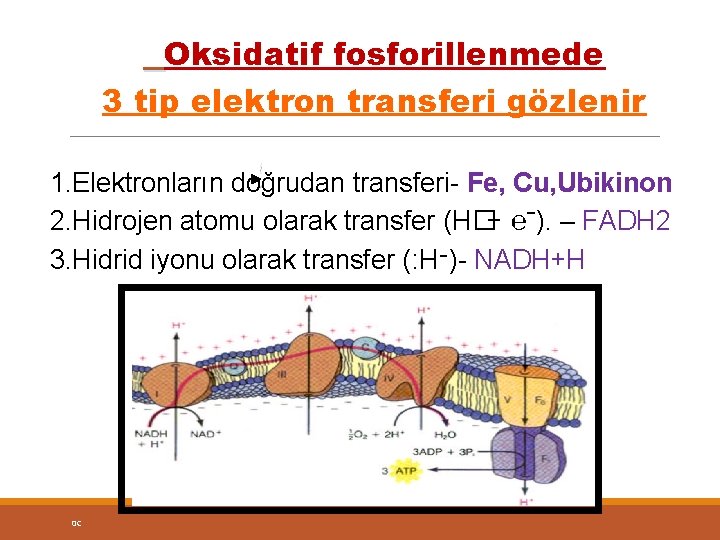
Oksidatif fosforillenmede 3 tip elektron transferi gözlenir 1. Elektronların doğrudan transferi- Fe, Cu, Ubikinon 2. Hidrojen atomu olarak transfer (H�+ ℮ˉ). – FADH 2 3. Hidrid iyonu olarak transfer (: H )־ - NADH+H 0 C
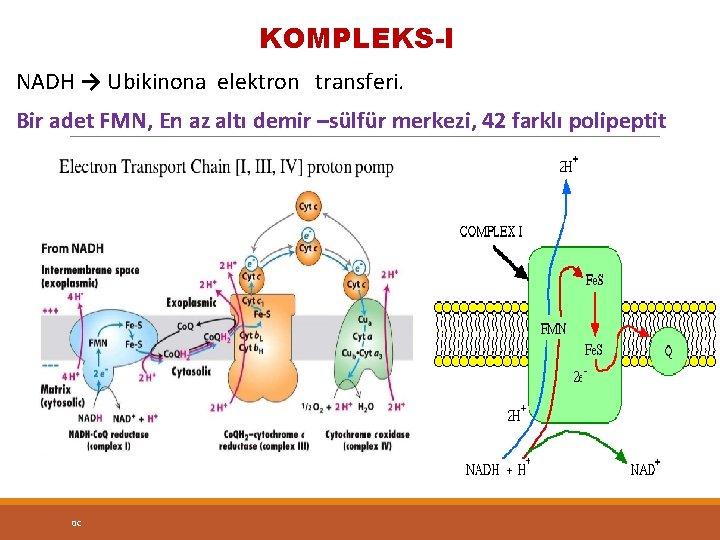
KOMPLEKS-I NADH → Ubikinona elektron transferi. Bir adet FMN, En az altı demir –sülfür merkezi, 42 farklı polipeptit 0 C
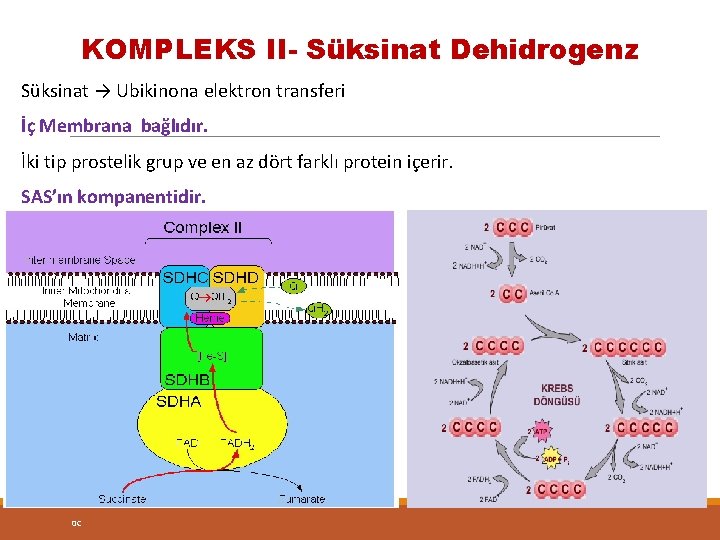
KOMPLEKS II- Süksinat Dehidrogenz Süksinat → Ubikinona elektron transferi İç Membrana bağlıdır. İki tip prostelik grup ve en az dört farklı protein içerir. SAS’ın kompanentidir. 0 C
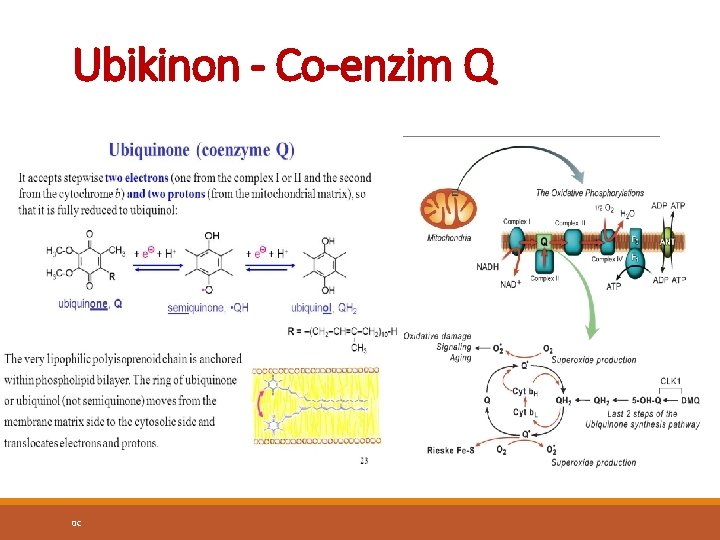
Ubikinon - Co-enzim Q 0 C
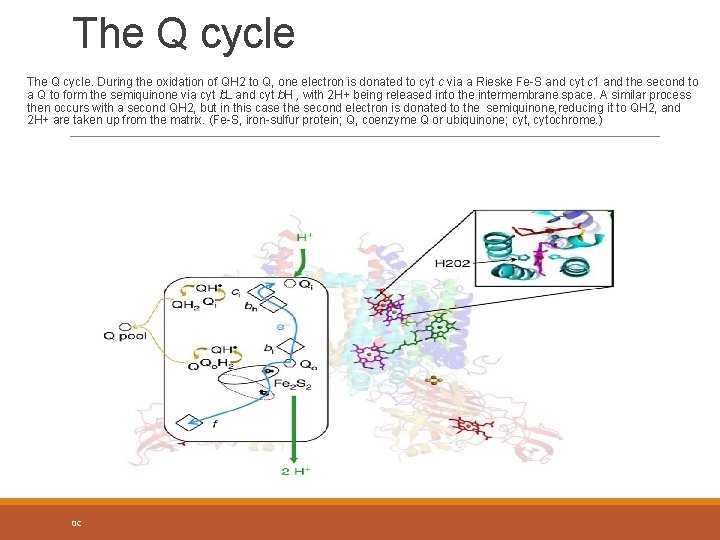
The Q cycle. During the oxidation of QH 2 to Q, one electron is donated to cyt c via a Rieske Fe-S and cyt c 1 and the second to a Q to form the semiquinone via cyt b. L and cyt b. H , with 2 H+ being released into the intermembrane space. A similar process then occurs with a second QH 2, but in this case the second electron is donated to the semiquinone, reducing it to QH 2, and 2 H+ are taken up from the matrix. (Fe-S, iron-sulfur protein; Q, coenzyme Q or ubiquinone; cyt, cytochrome. ) 0 C
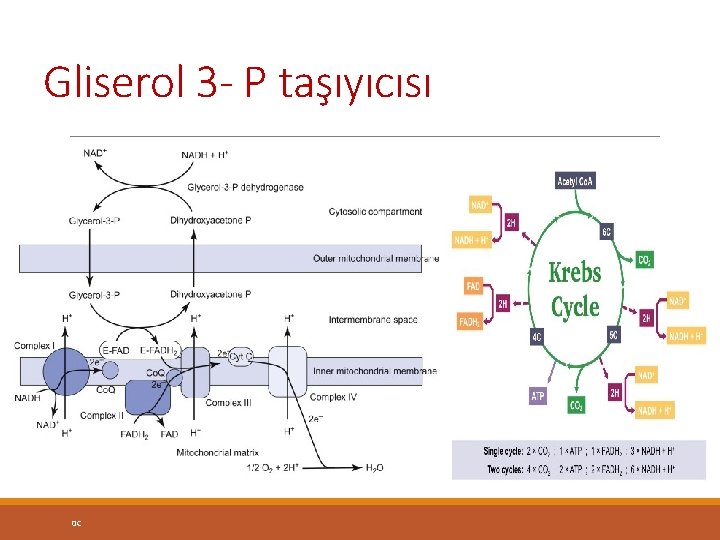
Gliserol 3 - P taşıyıcısı 0 C
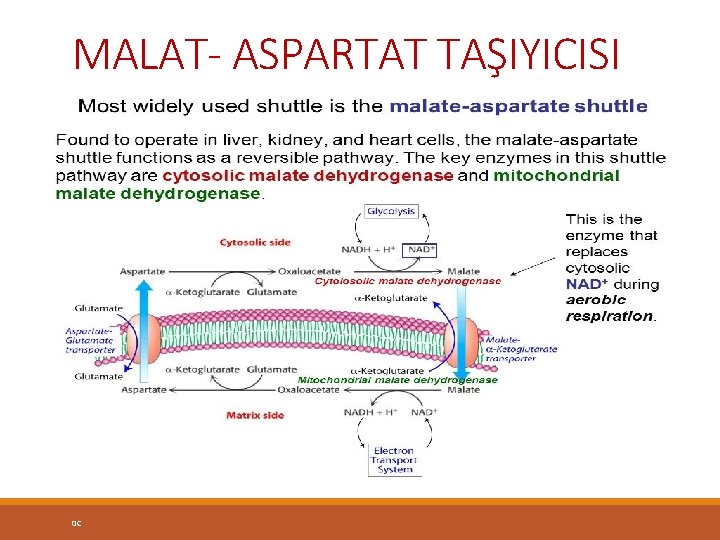
MALAT- ASPARTAT TAŞIYICISI 0 C
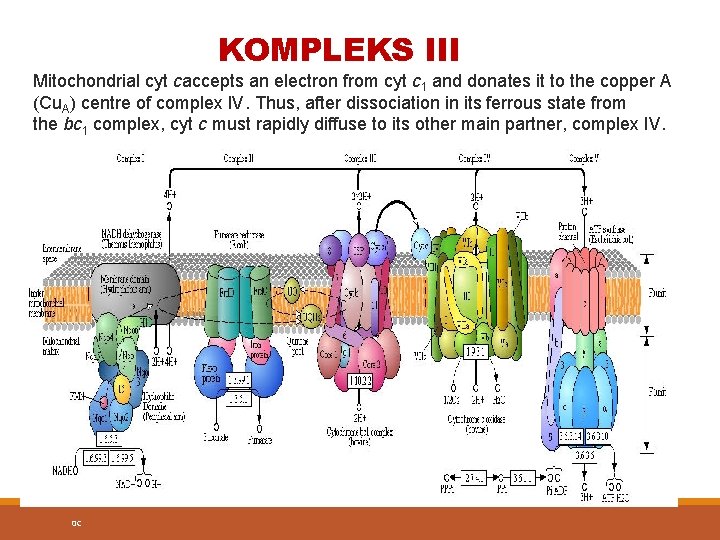
KOMPLEKS III Mitochondrial cyt caccepts an electron from cyt c 1 and donates it to the copper A (Cu. A) centre of complex IV. Thus, after dissociation in its ferrous state from the bc 1 complex, cyt c must rapidly diffuse to its other main partner, complex IV. 0 C
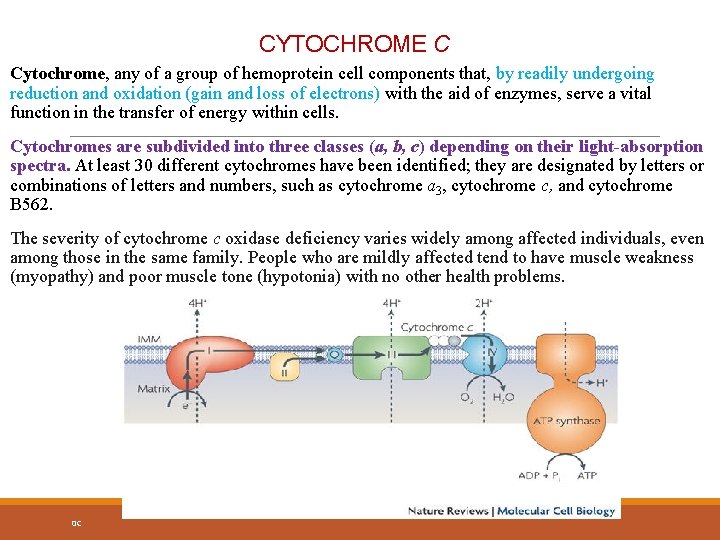
CYTOCHROME C Cytochrome, any of a group of hemoprotein cell components that, by readily undergoing reduction and oxidation (gain and loss of electrons) with the aid of enzymes, serve a vital function in the transfer of energy within cells. Cytochromes are subdivided into three classes (a, b, c) depending on their light-absorption spectra. At least 30 different cytochromes have been identified; they are designated by letters or combinations of letters and numbers, such as cytochrome a 3, cytochrome c, and cytochrome B 562. The severity of cytochrome c oxidase deficiency varies widely among affected individuals, even among those in the same family. People who are mildly affected tend to have muscle weakness (myopathy) and poor muscle tone (hypotonia) with no other health problems. 0 C
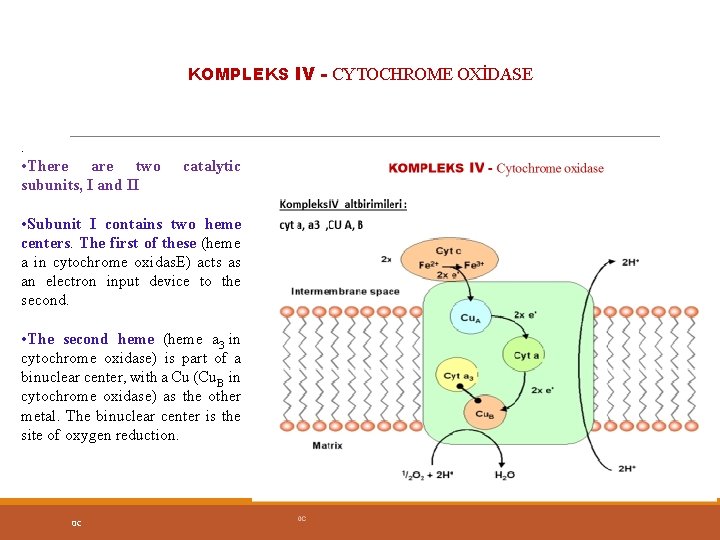
KOMPLEKS IV - CYTOCHROME OXİDASE . • There are two subunits, I and II catalytic • Subunit I contains two heme centers. The first of these (heme a in cytochrome oxidas. E) acts as an electron input device to the second. • The second heme (heme a 3 in cytochrome oxidase) is part of a binuclear center, with a Cu (Cu. B in cytochrome oxidase) as the other metal. The binuclear center is the site of oxygen reduction. 0 C
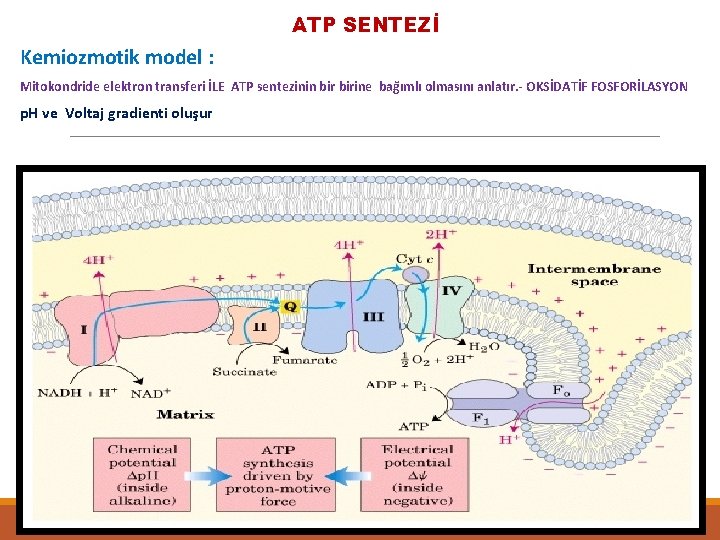
ATP SENTEZİ Kemiozmotik model : Mitokondride elektron transferi İLE ATP sentezinin birine bağımlı olmasını anlatır. - OKSİDATİF FOSFORİLASYON p. H ve Voltaj gradienti oluşur 0 C
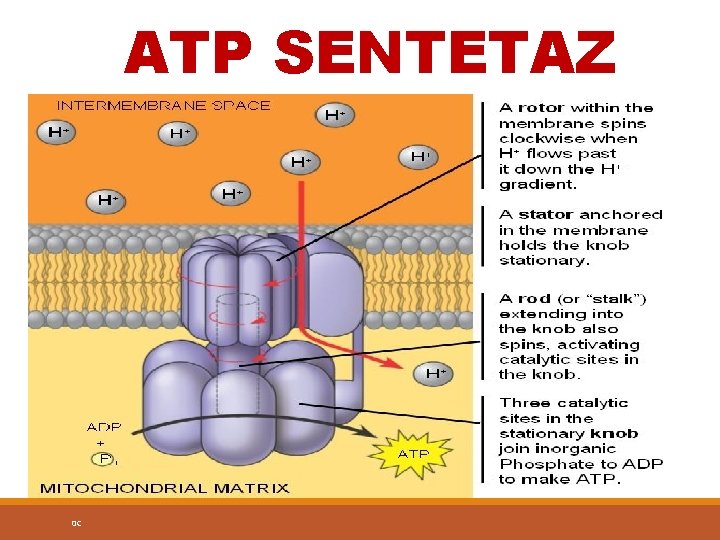
ATP SENTETAZ 0 C
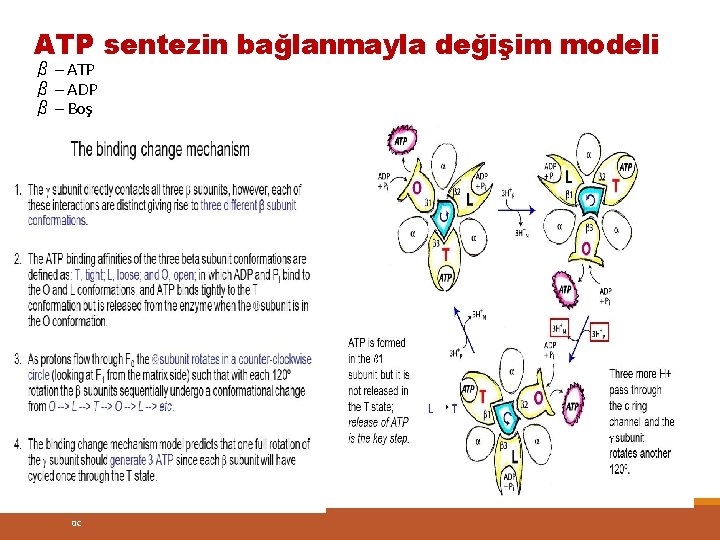
ATP sentezin bağlanmayla değişim modeli β – ATP β – ADP β – Boş 0 C

Enerji Bilançosu- Aerobik Solunum 0 C
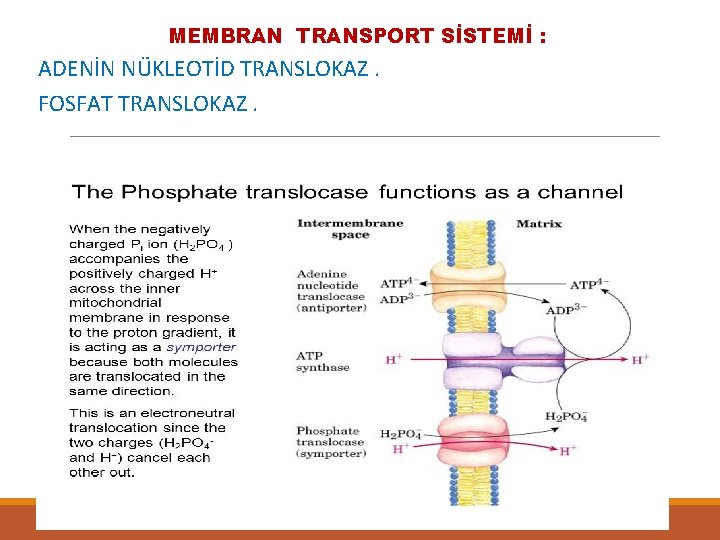
MEMBRAN TRANSPORT SİSTEMİ : ADENİN NÜKLEOTİD TRANSLOKAZ. FOSFAT TRANSLOKAZ. 0 C
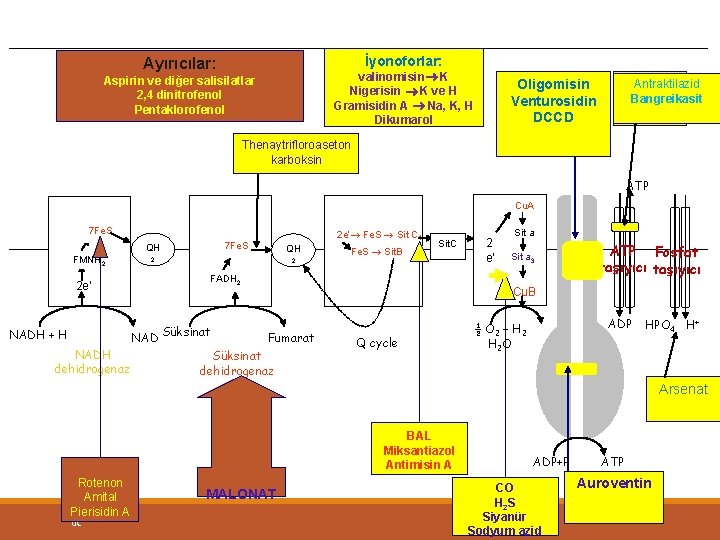
İyonoforlar: Ayırıcılar: valinomisin K Nigerisin K ve H Gramisidin A Na, K, H Dikumarol Aspirin ve diğer salisilatlar 2, 4 dinitrofenol Pentaklorofenol Oligomisin Venturosidin DCCD Antraktilazid Bangreikasit FCCP Thenaytrifloroaseton karboksin ATP Cu. A 7 Fe. S QH FMNH 2 2 e’ NADH dehidrogenaz QH 2 Fe. S Sit. B Sit. C 2 FADH 2 NAD Süksinat NADH + H 2 e’ Fe. S Sit C 1 2 e’ Sit a 3 ATP Fosfat taşıyıcı Cu. B Fumarat Süksinat dehidrogenaz Q cycle ADP ½ O 2 + H 2 O HPO 4 H+ Arsenat BAL Miksantiazol Antimisin A Rotenon Amital Pierisidin A 0 C MALONAT ADP+P CO H 2 S Siyanür Sodyum azid ATP Auroventin


MANY POISONS INHIBIT THE RESPIRATORY CHAIN Barbiturates such as amobarbital inhibit electron transport via Complex I by blocking the transfer from Fe-S to Q. At sufficient dosage, they are fatal in vivo. Antimycin A and dimercaprol inhibit the respiratory chain at Complex III. The classic poisons H 2 S, carbon monoxide and cyanide inhibit. Complex IV and can therefore totally arrest respiration. Malonate is a competitive inhibitor of Complex II. Atractyloside inhibits oxidative phosphorylation by inhibiting the transporter of ADP into and ATP out of the mitochondrion (Figure 13– 10). The antibiotic oligomycin completely blocks oxidation and phosphorylation by blocking the flow of protons through ATP synthase (Figure 13– 9). Uncouplers dissociate oxidation in the respiratory chain from phosphorylation (Figure 13– 7). These compounds are toxic in vivo, causing respiration to become uncontrolled, since the rate is no longer limited by the concentration of ADP or Pi. The uncoupler that has been used most frequently is 2, 4 - dinitrophenol, but other compounds act in a similar manner. Thermogenin (or the uncoupling protein) is a physiological uncoupler found in brown adipose tissue that functions to generate body heat, particularly for the newborn and during hibernation in animals 0 C
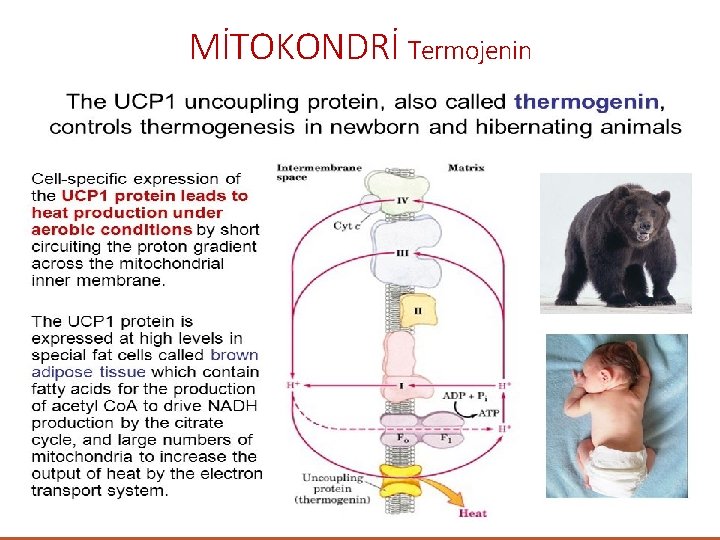
MİTOKONDRİ Termojenin 0 C

Mitokondrinin Genetik Yapısı 1. Sirkülerdir 2. Katlanmış bir yapı sergilemez 3. İntron yapısı yoktur 4. Mitokondriyal m. RA’nın başna (Cap) ve sonuna (poli. A) eklentiler yapılmaz 5. Bazı mitokondriyal genom kodonları nükleer genom kodonlarından farklı anlam taşır 0 C

0 C
0 C

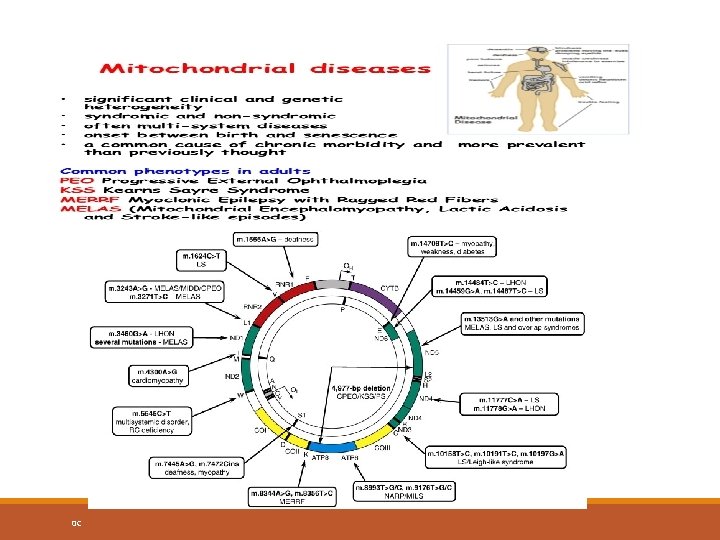
Mitokondriyal Hastalıklar Bazı dokular ; kalp, iskelet kası, merkez sinir sistemi, böbrek , mitokondriyal enerji üretimine yüksek oranda bağlı olduğundan mt. DNA mutasyonlarından nokta mutasyonları, delesyonlar, dublikasyonlardan daha fazla etkilenirler. Başlıca klinik bulgular; hipotoni, gelişme geriliği, mental gerilik, konvülsiyon nöbetleri ve ataksidir. Vucut sıvılarında laktik asit düzeyinin artması en önemli laboratuar bulgusudur. Ø Ø Chinnery PF and Gomez-Duran A , Oldies but Goldies, mt. DNA Population Variants, and Neurodegenerative Diseases. Front. Neurosci. 12: 682. , 2018. Oldies but Goldies mt. DNA Population Variants and Neurodegenerative Diseases. 0 C

Mitokondriyal Hastalıklar Çeşitli hastalıklarda görülen mt. DNA mutasyonları 4 gruba ayrılabilir; 1. Missense mutasyonları ; LHON, Leigh sendromu 2. Protein sentezi (t. RNA mutasyonları) mutasyonları; MELAS, MERRF 3. İnsersiyon/Delesyon mutasyonları ; Pearson, Kearns-Sayre 4. Kopya sayısı mutasyonları 0 C
Leber’in Herediter Optik Nöropatisi (LHON): Maternal geçişli Genç, erkek Retinal ganglion hücrelerde selektif kayıp, santral görme kaybı, optik atrofi Mitokondrial nokta mutasyonları: G 11778 A/ND 4 G 3460 A /ND 1 T 14484 C/ND 6 Solunum zincirine e- ların giriş yeri olan kompleks I’in alt ünitelerinde etkilenmeye yol açmakta kompleks III ve IV ‘de etkilemektedir 0 C

Nörojenik Kas Güçsüzlüğü, Ataksi ve Retinitis Pigmentosa (NARP): 0 C
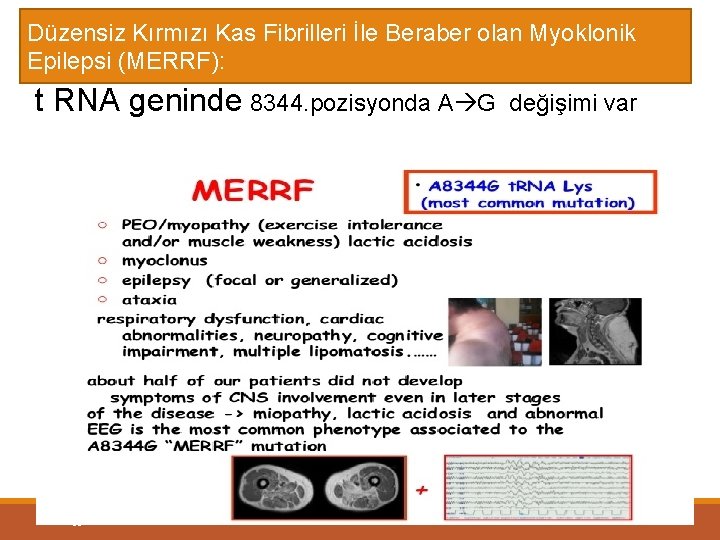
Düzensiz Kırmızı Kas Fibrilleri İle Beraber olan Myoklonik Epilepsi (MERRF): t RNA geninde 8344. pozisyonda A G değişimi var 0 C
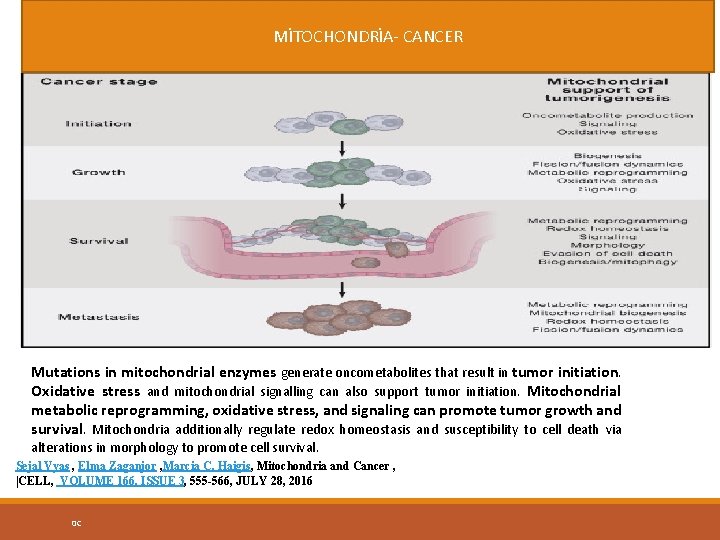
MİTOCHONDRİA- CANCER Mutations in mitochondrial enzymes generate oncometabolites that result in tumor initiation. Oxidative stress and mitochondrial signalling can also support tumor initiation. Mitochondrial metabolic reprogramming, oxidative stress, and signaling can promote tumor growth and survival. Mitochondria additionally regulate redox homeostasis and susceptibility to cell death via alterations in morphology to promote cell survival. Sejal Vyas , Elma Zaganjor , Marcia C. Haigis, Mitochondria and Cancer , |CELL, VOLUME 166, ISSUE 3, 555 -566, JULY 28, 2016 0 C
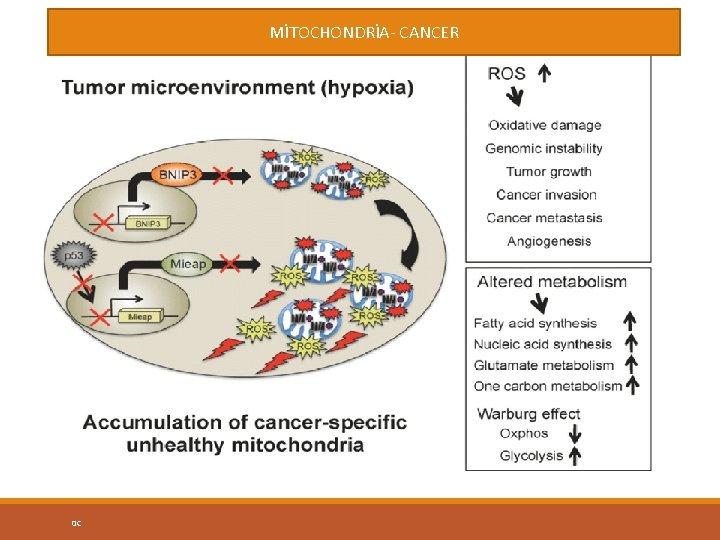
MİTOCHONDRİA- CANCER 0 C
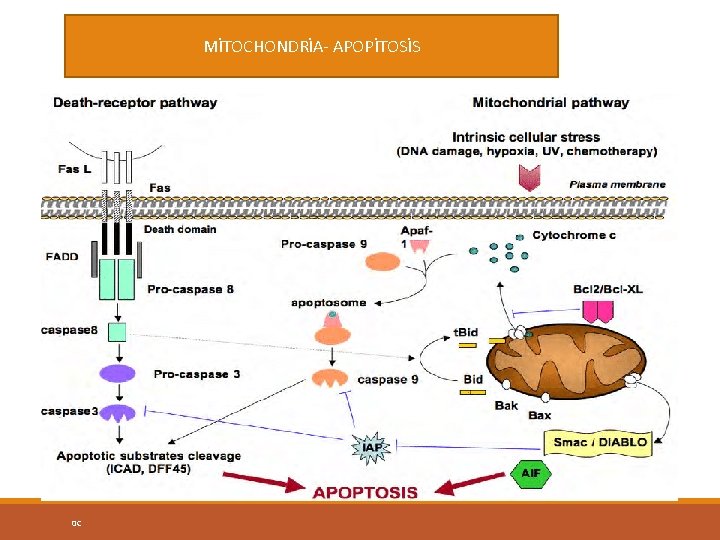
MİTOCHONDRİA- APOPİTOSİS 0 C
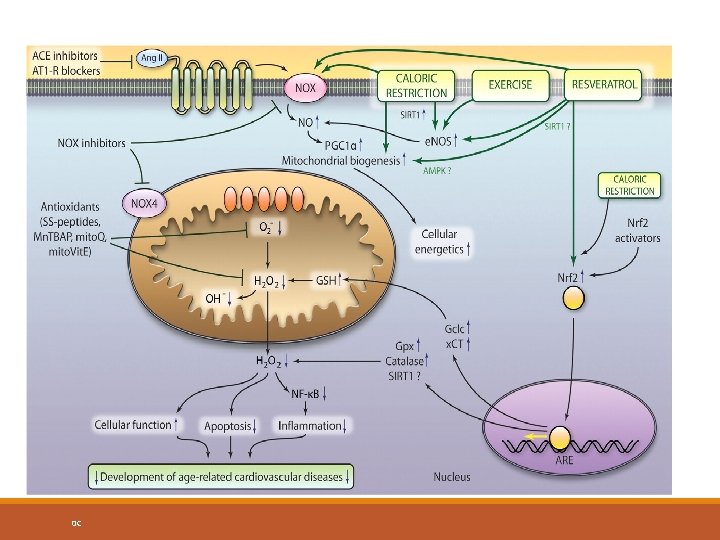
0 C
- Slides: 43