Nastavni predmet 1 Organska kemija s vjebama 2

• Nastavni predmet: 1. Organska kemija s vježbama • 2. Organska kemija • Nastavni plan i program/Kurikulum: Aspirin • 1. Kemijski tehničar • 2. Ekološki tehničar • Razred: treći • Trajanje: 3 sata • Pripremila: Kata Marković, dipl. ing.
Dragi učenici, U ovoj prezentaciji upoznati ćete kemijsku formulu aspirina, njegovu primjenu i način dobivanja u kemijskom laboratoriju. Uvod Ponoviti ćete također i neke procese i postupke koji se primjenjuju u laboratoriju prilikom sinteze nekog proizvoda. Nadam se da će to ponavljanje i upoznavanje novih procesa biti uspješno. Sretno!

Objašnjava upotrebu laboratorijskoga posuđa i pribora. Razlikuje značenje piktograma. Primjenjuje pravila sigurnoga ponašanja prilikom rukovanja kemikalijama, posuđem i priborom. Ishodi Izvodi postupke razdvajanja sastojaka iz smjese. Određuje talište, gustoću, topljivost tvari. Primjenjuje stehiometrijske odnose množine tvari na temelju jednadžbe kemijskih reakcija. Prikazuje podatke prikupljene pokusom tablicama i grafovima.
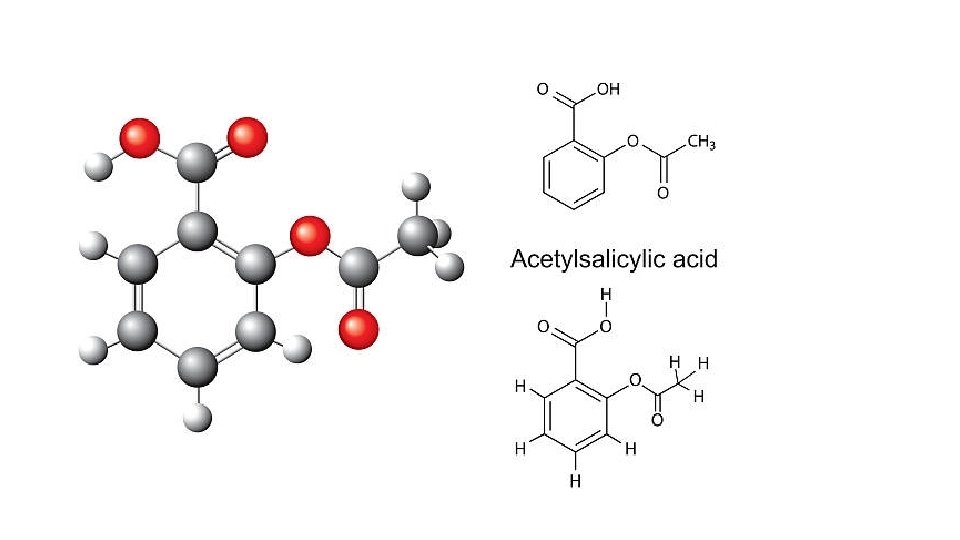

Aspirin

Bayerov aspirin Godišnje se u Bayerovim pogonima proizvede više od 50. 000 tona Aspirina, odnosno od 2, 3 do 2, 5 milijardi tableta, njih do 6000 u minuti. Poredane jedna do druge, petstomiligramske tablete Aspirina proizvedene u jednoj godini činile bi niz do Mjeseca i natrag.

Dugo je upotrebljavan kao lijek: Za prevenciju: glavobolje prehlade srčanog udara karcinoma …

Nepoželjna djelovanja aspirina Aspirin, usprkos svojoj popularnosti, nije lijek pogodan uvijek i za svakoga. Najčešće nuspojave uzimanja aspirina su iritacija i ulceracija sluznice želuca i crijeva, unutarnje krvarenje, probavne smetnje, mučnina i šum u ušima, naročito kod uzimanja visokih doza.

Dobivanje aspirina u školskom laboratoriju Može se sintetizirati i u našem školskom laboratoriju. Možete li proučavajući formulu acetilsalicilne kiseline (ASPIRINA) zaključiti što bi mogle biti polazne sirovine za dobivanje aspirina i kojim postupkom bi ga mogli dobiti? Sirovine: salicilna kiselina, anhidrid octene kiseline Postupak: esterifikacija
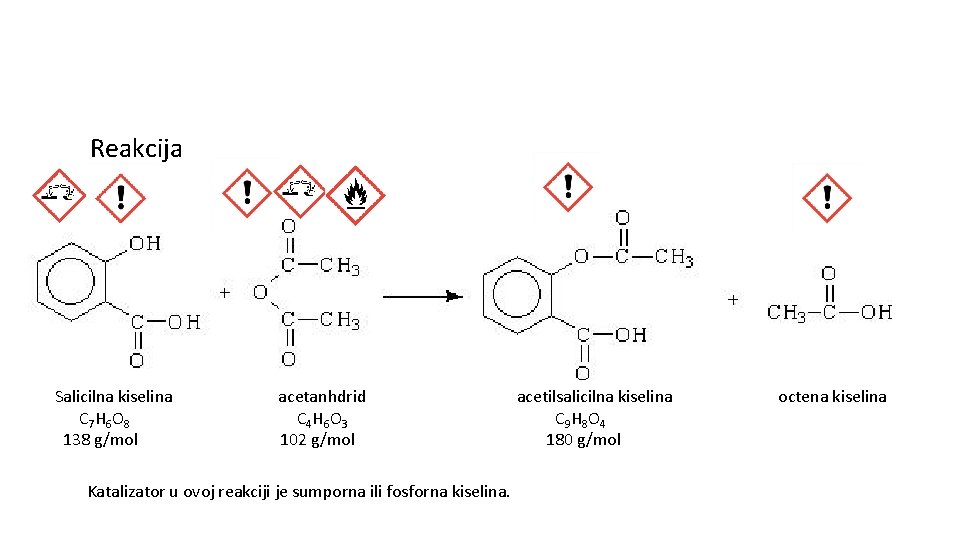
Reakcija Salicilna kiselina acetanhdrid acetilsalicilna kiselina octena kiselina C 7 H 6 O 8 C 4 H 6 O 3 C 9 H 8 O 4 138 g/mol 102 g/mol 180 g/mol Katalizator u ovoj reakciji je sumporna ili fosforna kiselina.

Pokušajte razmisliti *1 Zašto se u ovom procesu esterifikacije upotrebljava anhidrid octene kiseline?

Priprema Aspirina Odmjeri se 2, 4 g salicilne kiseline i prenese u okruglu tikvicu od 100 m. L. Odmjerenu masu potrebno je zabilježiti. U tikvicu s salicilnom kiselinom doda se 6 m. L anhidrida octene kiseline koji ima gustoću 1, 08 g/cm 3. Potom se doda 3 do 4 kapi konc. sumporne ili fosforne kiseline. Smjesa se zagrijava oko 15 -25 minuta u vodenoj kupelji.
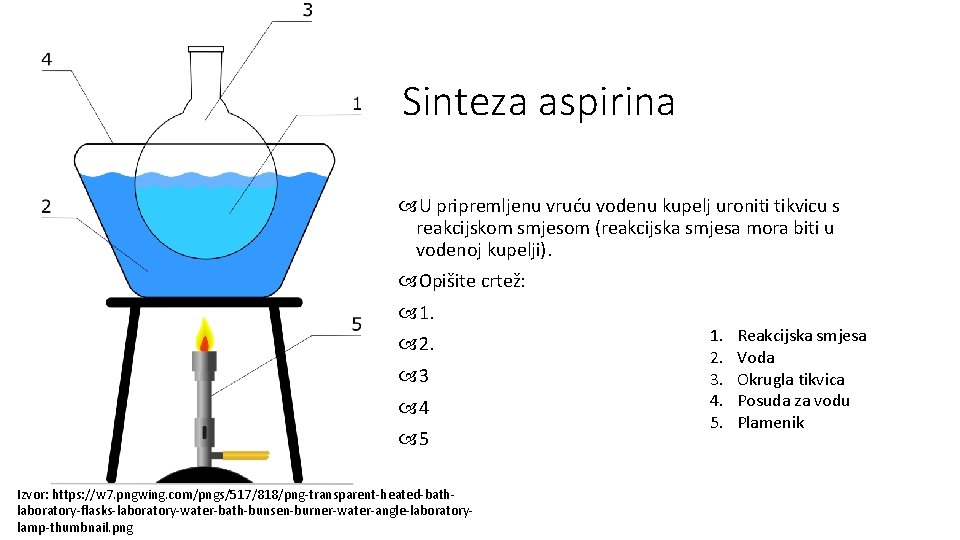
Sinteza aspirina U pripremljenu vruću vodenu kupelj uroniti tikvicu s reakcijskom smjesom (reakcijska smjesa mora biti u vodenoj kupelji). Opišite crtež: 1. 2. 3 4 5 Izvor: https: //w 7. pngwing. com/pngs/517/818/png-transparent-heated-bathlaboratory-flasks-laboratory-water-bath-bunsen-burner-water-angle-laboratorylamp-thumbnail. png 1. 2. 3. 4. 5. Reakcijska smjesa Voda Okrugla tikvica Posuda za vodu Plamenik

Aparatura za sintezu aspirina Na grlo tikvice tijekom zagrijavanja staviti Vigreux-ovu kolonu. *2 Možete li predvidjeti zašto? Zagrijavati do 15 -25 minuta ( temperatura oko 85 o. C )

Postupak nakon provedene reakcije Dok se tikvica još nalazi u vodenoj kupelji, polako dodajte 2 ml destilirane vode u tikvicu. Potom, izvadite tikvicu iz vodene kupelji i dodajte 20 ml destilirane vode. Pustite da se tikvica sa smjesom ohladi na sobnu temperaturu. Kad se otopina hladi, pojavit će se kristali aspirina. Za što bolje hlađenje smjese tj. što bolju kristalizaciju tikvicu je potrebno staviti u ledenu kupelj. *3Što je kristalizacija i o čemu ovisi?

Odvajanje aspirina iz smjese vakuum filtracijom Budući da je octena kiselina topiva u vodi, lako se odvaja od produkta aspirina. Postupak odvajanja kristala acetilsalicilne kiseline iz smjese je vakuum filtracija. Izvor: https: //www. fkit. unizg. hr/_download/repository/Praktikum_preparativne_organske_ke mije. pdf

Izolirani aspirin Aspirin izoliran u ovom koraku je "sirovi proizvod". "Pročišćeni proizvod" može se dobiti putem prekristalizacije sirovog produkta u vrućem etanolu. *4 Što je prekristalizacija i kako bi je proveli?
Čistoća aspirina *5 Čistoća proizvoda može se analizirati. Pokušajte razmisliti kako?

Masa salicilne kiseline (a) = 2, 40 g Masa filtrirnog papira i satnog stakla (b) = 32, 96 g Rezultati mjerenja Masa sušenog, prekristaliziranog aspirina, filtrirnog papira i satnog stakla (c) = 34, 41 g Masa osušenog, prekristaliziranog aspirina (d) = (c) - (b) = 34, 41 - 32, 96 = 1, 45 g

*6 Iskorištenje (Izračunajte prinos navedene reakcije) *6. 1. Broj molova salicilne kiseline stavljene u reakciju = ? M(salicine kiseline) = 138 g/ mol *6. 2. Broj molova anhidrida octene kiseline stavljenog u reakciju = ? *6. 3. Mjerodavni reaktant = ? *6. 4. Očekivani broj molova aspirina = ? M(aspirina) = 180 g/ mol * 6. 5. Očekivana masa aspirina = ? *6. 6. Dobivena masa aspirina = ? * Iskorištenje = ?

Podaci o čistoći aspirina Temperaturni raspon taljenja = 134, 2 ° C do 136, 1 ° C Izgled Bijeli, tanki, pahuljasti kristali *7Što se može zaključiti iz ovih podataka?

Provjerite svoje odgovore

*1 Zašto anhidrid? Preferira se anhidrid octene kiseline jer dobro reagira, manje je opasan, relativno jeftin, a octena kiselina dobivena kao nusprodukt može se ponovo prevesti u anhidrid.

*2 Zašto Vigreux-ova kolona Tijekom reakcije razvijaju se pare koje se kondenziraju i vraćaju u reakciju.

*3 Što je kristalizacija? Izdvajanje čvrste otopljene tvari iz otopine. Za proces kristalizacije važna je koncentracija otopljene tvari u otopini i temperatura.

*4 Prekristalizacija ŠTO JE PREKRISTALIZACIJA? ØNajpogodniji i najbrži načina za pročišćavanje neke tvari. ØTvar koja se pročišćava otapa se u vrućem prikladnom otapalu. ØHlađenjem otopine otopljena tvar kristalizira. ØOnečišćenja ostaju u otopini. POSTUPAK Ø Odabrati otapalo Ø Otopiti tvar u otapalu Ø Provesti kristalizaciju Ø Odvojiti i isprati kristale Ø Osušiti kristale

*5 Procjena čistoće ØTalište karakterizira spoj (raspon tališta označava čistoću spoja). ØPoteciometrijska titracija (acetilsalicilnu kiselinu titrirati jakom bazom). ØInfracrvena spektroskopija Otopiti tvar u pogodnom otapalu i dobiti IR-spektar te usporediti s referentnim spektrom … https: //www. researchgate. net/profile/C_Muthuselvi 2/publication/319327699/figure/fig 4/AS: 532555059261440@150398 2428053/Powder-diffraction-pattern-of-aspirin-crystal_Q 320. jpg

*Iskorištenje

*7Čistoća dobivenog aspirina Iz dobivenih podataka da se zaključiti da je dobiveni aspirin dobre čistoće.
HVALA
- Slides: 31