Najwiksze i najmniejsze cz I Budowa atomu Jony

Największe i najmniejsze (cz. I) Ø Budowa atomu Ø Jony Ø Izotopy

Budowa materii v. Materia ma budowę ziarnistą (nieciągłą), potwierdzeniem jest zjawisko dyfuzji v. Dyfuzja – zjawisko polegające na samorzutnym rozprzestrzenianiu się substancji w danej objętości Ø dyfuzja zachodzi we wszystkich stanach skupienia: ü najszybciej w stanie gazowym ü najwolniej w stenie stałym Jednostki stosowane do wyrażenia rozmiarów atomów, cząsteczek, długości wiązań pikometr angstrem nanometr 1 pm = 10 -12 m 1Å = 10 -10 m 1 nm = 10 -9 m

Atomy – promień atomowy v Zmiana promienia atomowego a położenie pierwiastka w układzie okresowym pierwiastków chemicznych Ø W grupach – promień atomowy wzrasta wraz ze wzrostem liczby atomowej Z pierwiastka: ü r 1 H = 30 pm; r 3 Li = 152 pm; r 11 Na = 186 pm; r 19 K = 227 pm; r 37 Rb = 248 pm; r 55 Cs = 265 pm; r 87 Fr = 270 pm Ø W okresach – promień atomowy maleje wraz ze wzrostem liczby atomowej Z pierwiastka (wyjątek stanowią helowce, których promienie są większe od promieni fluorowców ale mniejsze od promieni litowców): ü r 3 Li = 152 pm; r 4 Be = 114 pm; r 5 B = 88 pm; r 6 C = 77 pm; r 7 N = 70 pm; r 8 O = 66 pm; r 9 F = 58 pm; r 10 Ne = 160 pm

Promień jonowy H (30 pm) H+ (1∙ 10 -5 pm) H- (154 pm) Na (186 pm) Na+ ( 98 pm) - Cl ( 181 pm) - Cl- (181 pm) Ø Zmiana promienia jonowego wynika z liczby przyciąganych elektronów przez ten sam ładunek jądra atomowego
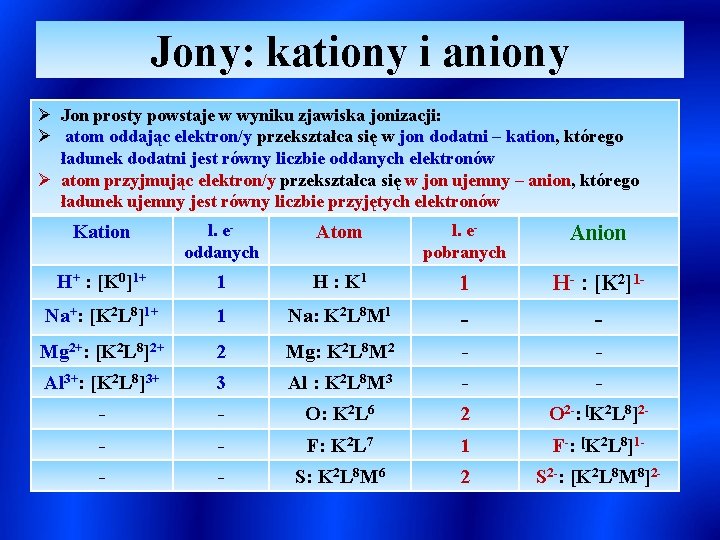
Jony: kationy i aniony Ø Jon prosty powstaje w wyniku zjawiska jonizacji: Ø atom oddając elektron/y przekształca się w jon dodatni – kation, którego ładunek dodatni jest równy liczbie oddanych elektronów Ø atom przyjmując elektron/y przekształca się w jon ujemny – anion, którego ładunek ujemny jest równy liczbie przyjętych elektronów Kation l. eoddanych Atom l. epobranych Anion H+ : [K 0]1+ 1 H : K 1 1 H- : [K 2]1 - Na+: [K 2 L 8]1+ 1 Na: K 2 L 8 M 1 - - Mg 2+: [K 2 L 8]2+ 2 Mg: K 2 L 8 M 2 - - Al 3+: [K 2 L 8]3+ 3 Al : K 2 L 8 M 3 - - O: K 2 L 6 2 O 2 -: [K 2 L 8]2 - - - F: K 2 L 7 1 F-: [K 2 L 8]1 - - - S: K 2 L 8 M 6 2 S 2 -: [K 2 L 8 M 8]2 -

Budowa atomu Cząstki elementarne atomu i ich parametry Nazwa proton Symbol i średnica p ; p+ ; 1 p 1 Masa (1 u = 1, 66 ∙ 10 -24 g) Ładunek jednostkowy 1 u +1 +1, 602∙ 10 -19 C 1 u 0 1/1840 u -1 -1, 602∙ 10 -19 C ok. 2, 5∙ 10 -15 m neutron n ; n 0 ; 1 n 0 ok. 2, 5∙ 10 -15 m elektron e- ; 0 e -1 < 10 -22 m Masa atomu skupiona jest w jądrze atomowym (ponad 99, 9%), którego gęstość jest bardzo duża: 1014 g/cm 3
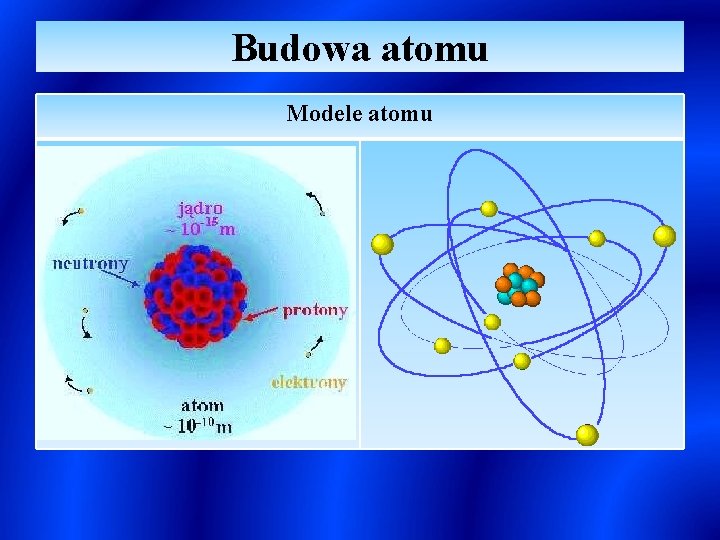
Budowa atomu Modele atomu

Izotopy v Izotopy – odmiany tego samego pierwiastka – nuklidy o: Ø tej samej liczbie atomowej Z (tej samej liczbie protonów) Ø różniej liczbie masowej A (różnej liczbie neutronów) N+Z=A A–N =Z Z = liczba porządkowa = liczba atomowa = liczba elektronów = ładunek jądra atomowego A = liczba masowa = liczba protonów + liczba neutronów = liczba nukleonów E Przykład – izotopy wodoru 1 1 E; 2 2 E ; 3 1 E; 1 1 H 2 1 H ; 1 1 P 2 ; 1 D 3 1 H ; 3 1 T Z=1 A=1 N=0 99, 985% Z=1 A=2 N=1 0, 015% Z=1 A=3 N=2 10 -16% ; P – prot ; ; D – deuter T – tryt

Zastosowanie izotopów v Jądra izotopów pierwiastków promieniotwórczych (radioaktywnych) są nietrwałe – ulegają samorzutnemu rozpadowi emitując trzy rodzaje promieniowania: α; β; γ v Zastosowanie izotopów promieniotwórczych Ø Źródła energii – paliwo jądrowe w reaktorach atomowych elektrowni i silników łodzi podwodnych oraz lodołamaczy: [ 235 U (1 kg/300 T węgla), 239 Pu ] Ø Ładunki nuklearne broni Ø Radioterapia nowotworów: 89 Sr, 153 Sm, 32 P, 192 Ir, 137 Cs, 60 Co, 226 Ra, 90 Y Ø Urządzenia techniczne – detektory dymu: 238 Pu, 241 Am Ø Przyrządy kontrolno-pomiarowe – defektoskopy: 75 Se; 169 Yb; 192 Ir Ø Badania naukowe – metoda wskaźników izotopowych (badania mechanizmu reakcji chemicznych): 13 C, 18 O Ø Datowanie znalezisk archeologicznych i geologicznych: 14 C, 40 K
- Slides: 9