Nachweisreaktionen Grundlagen Eine Nachweisreaktion ist eine chemische Reaktion

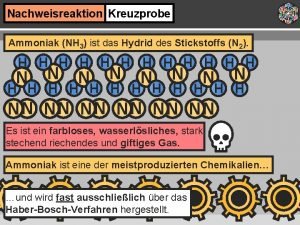
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Flammenprobe [Kationen] So bringt man die unbekannte Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Flammenprobe [Kationen] So bringt man die unbekannte](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-4.jpg)
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Bei der Kriechprobe Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Bei der Kriechprobe](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-7.jpg)
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Wenn die Probe Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Wenn die Probe](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-8.jpg)
![Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Beispiel: Silbernitratprobe [Silbernitratlösung als Reagens] 1 Ag+ Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Beispiel: Silbernitratprobe [Silbernitratlösung als Reagens] 1 Ag+](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-13.jpg)

- Slides: 18

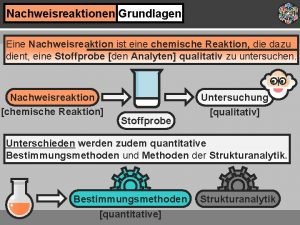
Nachweisreaktionen Grundlagen Eine Nachweisreaktion ist eine chemische Reaktion, die dazu dient, eine Stoffprobe [den Analyten] qualitativ zu untersuchen. Nachweisreaktion [chemische Reaktion] Stoffprobe Untersuchung [qualitativ] Unterschieden werden zudem quantitative Bestimmungsmethoden und Methoden der Strukturanalytik. Bestimmungsmethoden [quantitative] Strukturanalytik

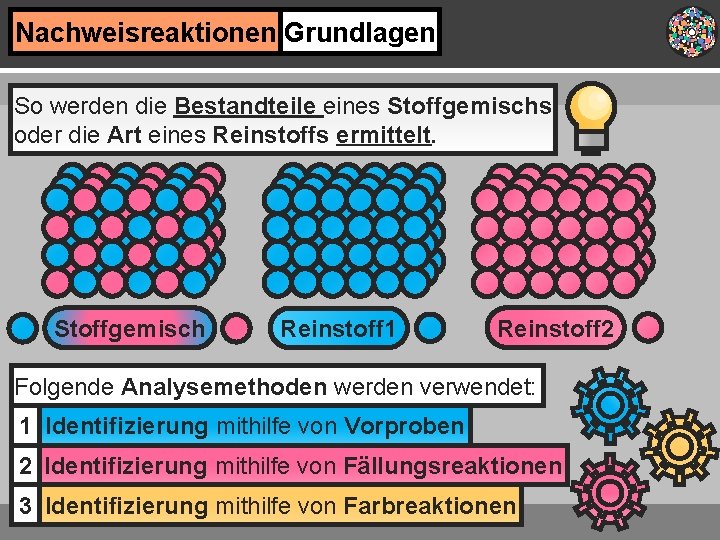
Nachweisreaktionen Grundlagen So werden die Bestandteile eines Stoffgemischs oder die Art eines Reinstoffs ermittelt. Stoffgemisch Reinstoff 1 Reinstoff 2 Folgende Analysemethoden werden verwendet: 1 Identifizierung mithilfe von Vorproben 2 Identifizierung mithilfe von Fällungsreaktionen 3 Identifizierung mithilfe von Farbreaktionen

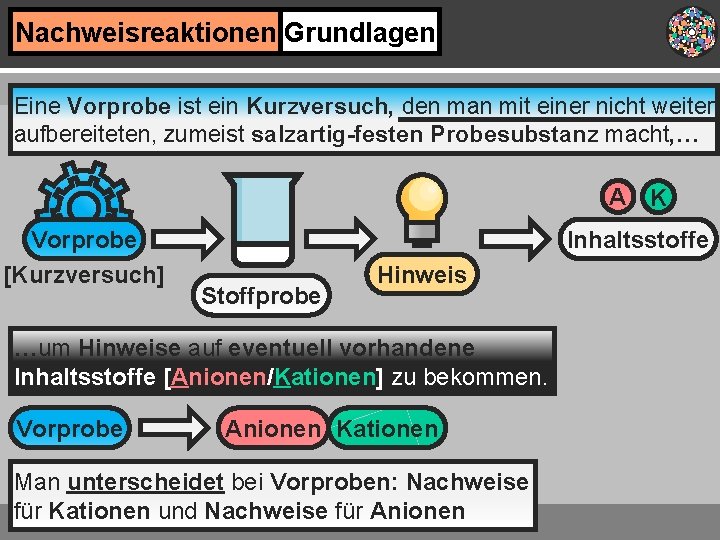
Nachweisreaktionen Grundlagen Eine Vorprobe ist ein Kurzversuch, den man mit einer nicht weiter aufbereiteten, zumeist salzartig-festen Probesubstanz macht, … A K Vorprobe [Kurzversuch] Inhaltsstoffe Stoffprobe Hinweis …um Hinweise auf eventuell vorhandene Inhaltsstoffe [Anionen/Kationen] zu bekommen. Vorprobe Anionen Kationen Man unterscheidet bei Vorproben: Nachweise für Kationen und Nachweise für Anionen
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben Flammenprobe Kationen So bringt man die unbekannte Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Flammenprobe [Kationen] So bringt man die unbekannte](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-4.jpg)
Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Flammenprobe [Kationen] So bringt man die unbekannte Probe auf einem [Na] [Rb] [Sr] Magnesiastäbchen in die nichtleuchtende… [Ca] [Ba] [Cs] [Ca] Probe [unbekannt] Flamme …Flamme des Bunsenbrenners. Die Flamme verfärbt sich, wenn bestimmte Ionen durch die Flamme angeregt werden. [K] [Cu] [Li]

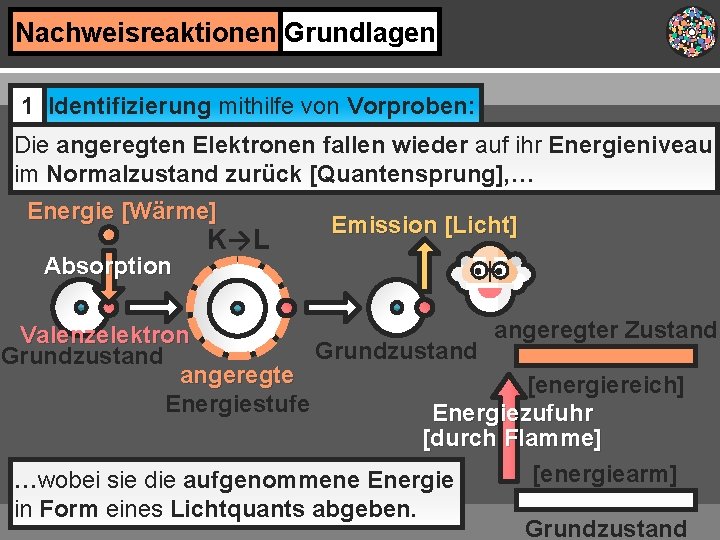
Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Die angeregten Elektronen fallen wieder auf ihr Energieniveau im Normalzustand zurück [Quantensprung], … Energie [Wärme] Absorption K→L Emission [Licht] angeregter Zustand Valenzelektron Grundzustand angeregte [energiereich] Energiestufe Energiezufuhr [durch Flamme] [energiearm] …wobei sie die aufgenommene Energie in Form eines Lichtquants abgeben. Grundzustand

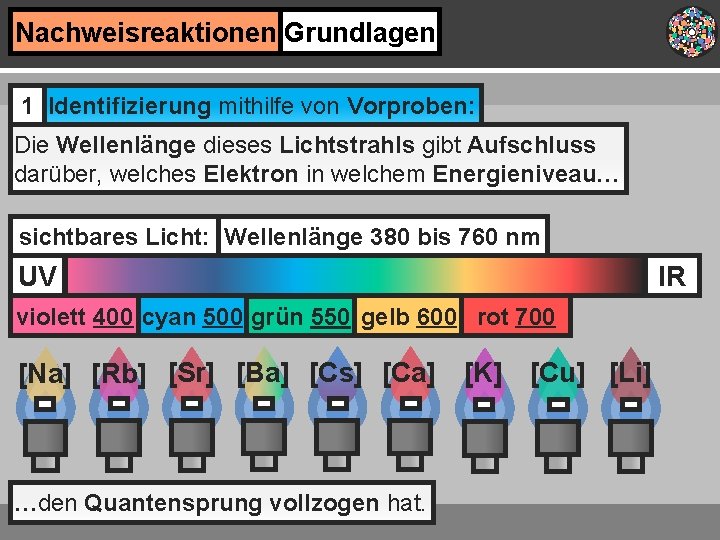
Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Die Wellenlänge dieses Lichtstrahls gibt Aufschluss darüber, welches Elektron in welchem Energieniveau… sichtbares Licht: Wellenlänge 380 bis 760 nm UV violett 400 cyan 500 grün 550 gelb 600 rot 700 [Na] [Rb] [Sr] [Ba] [Cs] [Ca] [K] [Cu] [Li] …den Quantensprung vollzogen hat. IR
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben Kriechprobe Anionen auf Fluoridionen Bei der Kriechprobe Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Bei der Kriechprobe](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-7.jpg)
Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Bei der Kriechprobe gibt man eine kleine Menge der zu untersuchenden Substanz zusammen… O H O S O H O Probe [unbekannt] Schwefelsäure [H 2 SO 4] …mit konzentrierter Schwefelsäure in ein Reagenzglas.
![Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben Kriechprobe Anionen auf Fluoridionen Wenn die Probe Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Wenn die Probe](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-8.jpg)
Nachweisreaktionen Grundlagen 1 Identifizierung mithilfe von Vorproben: Kriechprobe [Anionen] auf Fluoridionen Wenn die Probe Fluorid enthält, dann bildet sich Fluorwasserstoffsäure [HF]. O F H O S O H H F O Probe [unbekannt] Schwefelsäure [H 2 SO 4] Diese ätzt die Glaswand an und kriecht an ihr hoch.

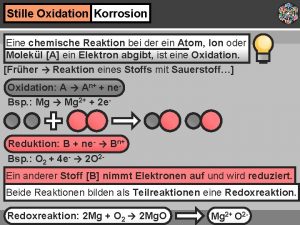
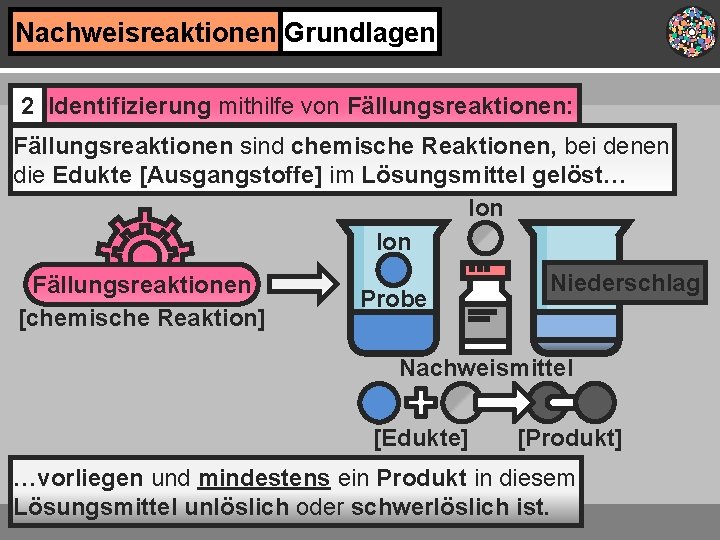
Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Fällungsreaktionen sind chemische Reaktionen, bei denen die Edukte [Ausgangstoffe] im Lösungsmittel gelöst… Ion Fällungsreaktionen [chemische Reaktion] Probe Niederschlag Nachweismittel [Edukte] [Produkt] …vorliegen und mindestens ein Produkt in diesem Lösungsmittel unlöslich oder schwerlöslich ist.

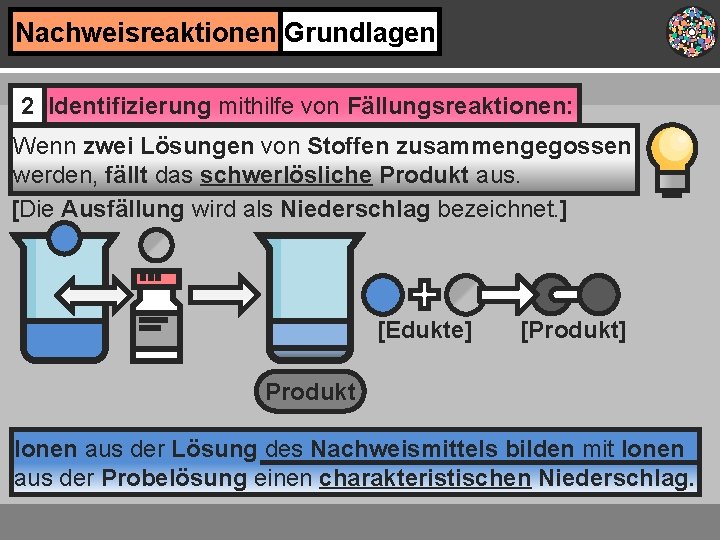
Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Wenn zwei Lösungen von Stoffen zusammengegossen werden, fällt das schwerlösliche Produkt aus. [Die Ausfällung wird als Niederschlag bezeichnet. ] [Edukte] [Produkt] Produkt Ionen aus der Lösung des Nachweismittels bilden mit Ionen aus der Probelösung einen charakteristischen Niederschlag.

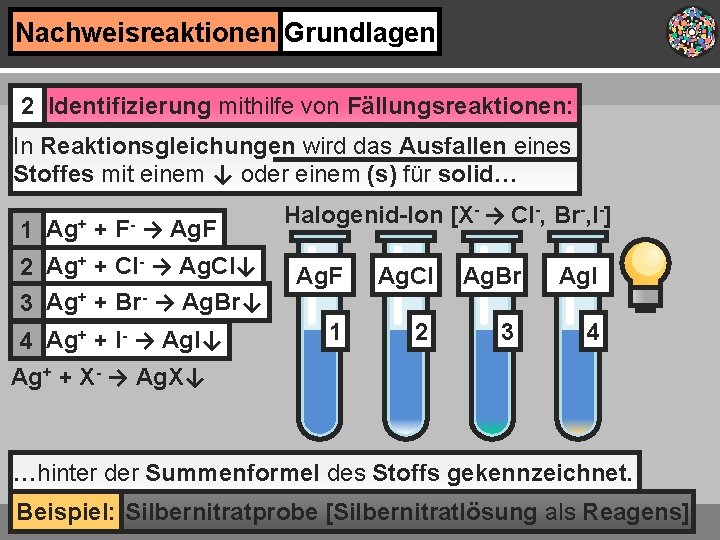
Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: In Reaktionsgleichungen wird das Ausfallen eines Stoffes mit einem ↓ oder einem (s) für solid… 1 Ag+ + F- → Ag. F 2 Ag+ + Cl- → Ag. Cl↓ 3 Ag+ + Br- → Ag. Br↓ 4 Ag+ + I- → Ag. I↓ Halogenid-Ion [X- → Cl-, Br-, I-] Ag. F Ag. Cl Ag. Br Ag. I 1 2 3 4 Ag+ + X- → Ag. X↓ …hinter der Summenformel des Stoffs gekennzeichnet. Beispiel: Silbernitratprobe [Silbernitratlösung als Reagens]

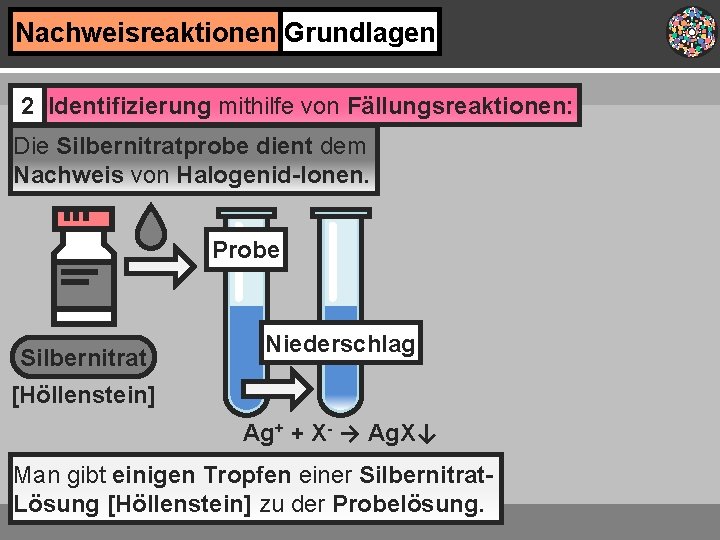
Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Die Silbernitratprobe dient dem Nachweis von Halogenid-Ionen. Probe Silbernitrat Niederschlag [Höllenstein] Ag+ + X- → Ag. X↓ Man gibt einigen Tropfen einer Silbernitrat. Lösung [Höllenstein] zu der Probelösung.
![Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen Beispiel Silbernitratprobe Silbernitratlösung als Reagens 1 Ag Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Beispiel: Silbernitratprobe [Silbernitratlösung als Reagens] 1 Ag+](https://slidetodoc.com/presentation_image_h/166fb4d9aa078f14a742f0f4f682aa3c/image-13.jpg)
Nachweisreaktionen Grundlagen 2 Identifizierung mithilfe von Fällungsreaktionen: Beispiel: Silbernitratprobe [Silbernitratlösung als Reagens] 1 Ag+ + F- → Ag. F 2 Ag+ + Cl- → Ag. Cl↓ 3 Ag+ + Br- → Ag. Br↓ 4 Ag+ + I- → Ag. I↓ Halogenid-Ion [X- → Cl-, Br-, I-] Ag. F Ag. Cl Ag. Br Ag. I 1 2 3 4 Ag+ + X- → Ag. X↓ Fluoridionen lassen sich durch Niederschlag nicht nachweisen, da Ag. F als einziges Silberhalogenid gut wasserlöslich ist.

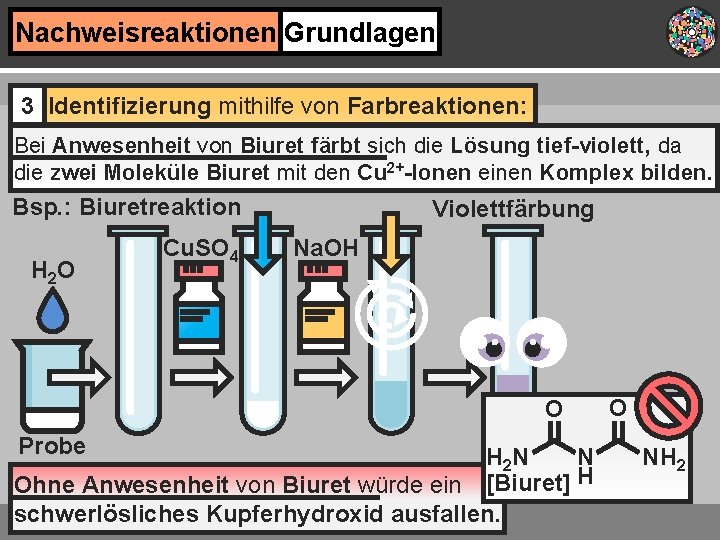
Nachweisreaktionen Grundlagen 3 Identifizierung mithilfe von Farbreaktionen: Farbänderung Reaktionen, bei denen durch Zusammengießen von Lösungen eine Farbänderung auftritt, ohne dass ein Niederschlag ausfällt. Farbreaktion p. H-Wert 6 -7 Eine Farbreaktion ist auch das Eintauchen von Indikatorpapieren in Lösungen [Bestimmung des p. H- Werts]. 1 2 3 4 5 6 7 8 9 10 11 12 13 14

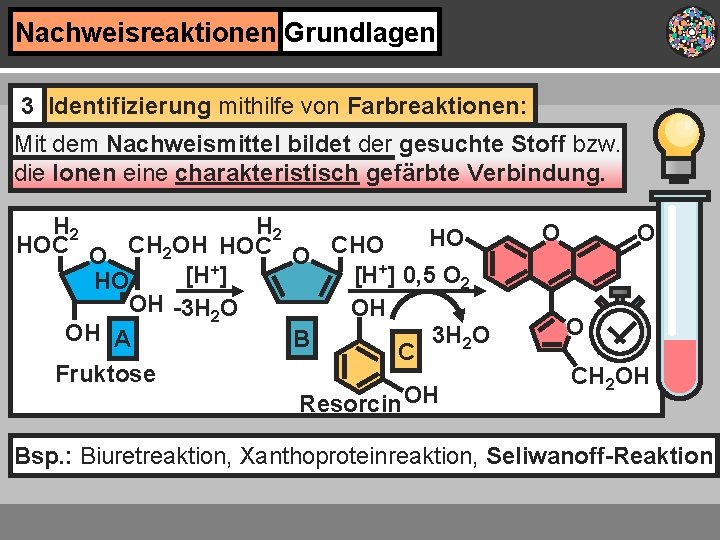
Nachweisreaktionen Grundlagen 3 Identifizierung mithilfe von Farbreaktionen: Mit dem Nachweismittel bildet der gesuchte Stoff bzw. die Ionen eine charakteristisch gefärbte Verbindung. H 2 HO HOC O CH 2 OH HOC O CHO +] 0, 5 O +] [H [H 2 HO OH -3 H 2 O OH OH A 3 H 2 O B C Fruktose Resorcin OH O O O CH 2 OH Bsp. : Biuretreaktion, Xanthoproteinreaktion, Seliwanoff-Reaktion

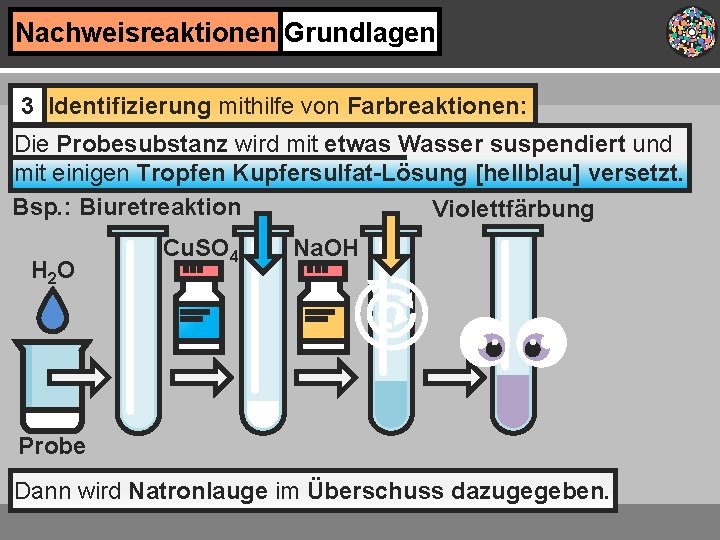
Nachweisreaktionen Grundlagen 3 Identifizierung mithilfe von Farbreaktionen: Die Probesubstanz wird mit etwas Wasser suspendiert und mit einigen Tropfen Kupfersulfat-Lösung [hellblau] versetzt. Bsp. : Biuretreaktion Violettfärbung H 2 O Cu. SO 4 Na. OH Probe Dann wird Natronlauge im Überschuss dazugegeben.

Nachweisreaktionen Grundlagen 3 Identifizierung mithilfe von Farbreaktionen: Bei Anwesenheit von Biuret färbt sich die Lösung tief-violett, da die zwei Moleküle Biuret mit den Cu 2+-Ionen einen Komplex bilden. Bsp. : Biuretreaktion H 2 O Cu. SO 4 Violettfärbung Na. OH O Probe N H 2 N Ohne Anwesenheit von Biuret würde ein [Biuret] H schwerlösliches Kupferhydroxid ausfallen. O NH 2

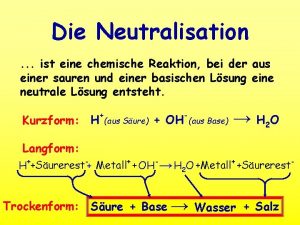
Nachweisreaktionen Grundlagen Zusammenfassung: Eine Nachweisreaktion ist eine chemische Reaktion, die dazu dient, eine Stoffprobe [den Analyten] qualitativ zu untersuchen. Nachweisreaktionen können mit einfachen apparativen Mitteln durchgeführt werden.
 Was ist eine nachweisreaktion
Was ist eine nachweisreaktion Zinnnitrat
Zinnnitrat Zuordnung oder funktion
Zuordnung oder funktion Kalkwasserprobe
Kalkwasserprobe Voorbeelden van chemische energie
Voorbeelden van chemische energie Chemische reacties
Chemische reacties Das chemische dreieck
Das chemische dreieck Chemische formel schokolade
Chemische formel schokolade Mefigyn
Mefigyn Interneuronale synapse
Interneuronale synapse Bindung
Bindung Grenzwinkel holland
Grenzwinkel holland Meilenstein definition din 69900
Meilenstein definition din 69900 Erwerbswirtschaftliches prinzip
Erwerbswirtschaftliches prinzip Die liebe ist eine himmelsmacht
Die liebe ist eine himmelsmacht Musik ist eine sprache die jeder mensch versteht
Musik ist eine sprache die jeder mensch versteht Lichtquellen und beleuchtete körper
Lichtquellen und beleuchtete körper Erörterung aufbau sanduhr
Erörterung aufbau sanduhr Die waage der baleks interpretation
Die waage der baleks interpretation