Myelodysplastiskt syndrom Johanna Ungerstedt Docent Specialistlkare Hematologiskt Centrum

























- Slides: 39

Myelodysplastiskt syndrom Johanna Ungerstedt Docent, Specialistläkare Hematologiskt Centrum Karolinska Universitetssjukhuset

Oftast smygande debut Trötthet, svaghet, dyspné Anemi Inflammatoriska symtom Paramalignt Ibland men ovanligt, förekommer akut debut med tex svår infektion pga grav neutropeni, eller blödning och tom DIC bild pga grav trombocytopeni.

Vad betyder myelodysplastiskt syndrom (MDS)? § ”Myelo” Benmärg § ”Dysplasi” Onormal mognad av celler Missväxt § ”Syndrom” Diagnosen ställs med benmärgsprov. För riskbedömning behövs också kromosomanalys.


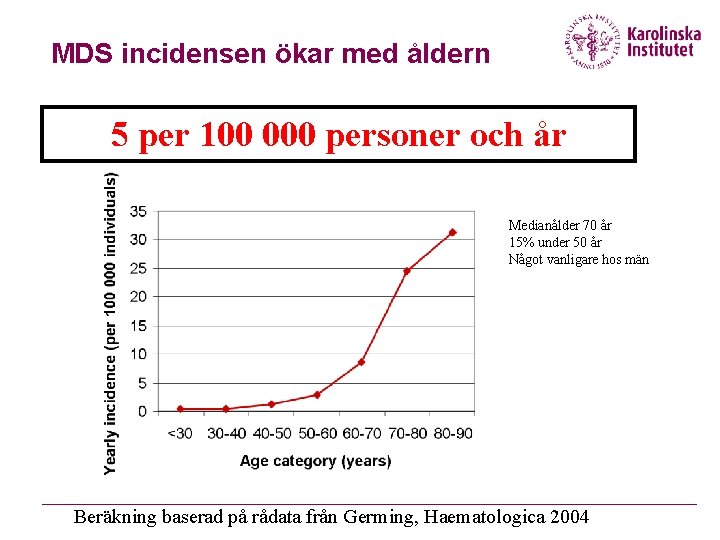
MDS incidensen ökar med åldern 5 per 100 000 personer och år Medianålder 70 år 15% under 50 år Något vanligare hos män Beräkning baserad på rådata från Germing, Haematologica 2004

När skall man misstänka MDS? § Oklar anemi, trombocytopeni eller neutropeni Oftast makrocytär anemi Förhöjt ferritin som tecken på en ineffektiv erytropoes § Ökar om järnet inte används § Hos vilka personer? Äldre Hos patienter som tidigare fått cytostatika

Patientfall 1 • 77 -årig kvinna med tablettbehandlad diabetes, f. ö. frisk. Vid rutinkontroll på vårdcentral upptäcks Hb 105 g/l. Patienten har inga symtom av anemin. LPK och TPK ua. Anemin är makrocytär. (MCV 102).

Patientfall 1 • 77 -årig kvinna med tablettbehandlad diabetes, f. ö. frisk. Vid rutinkontroll på vårdcentral upptäcks Hb 105 g/l. Patienten har inga symtom av anemin. LPK och TPK ua. Anemin är makrocytär. § Differential diagnoser: B 12 / folat brist, möjligen järnbrist thyroidea Toxisk påverkan t. ex. alkohol, cytostatika, andra läkemedel Myeloproliferativ sjukdom § Patienten negerar alkohol, inga mediciner förutom metformin. Informeras om möjlig MDS. § Hur går vi vidare?

Patientfall 2 § 70 årig rökande man, tid op för godartad prostataförstoring, söker vårdcentralen pga trötthet. § I lab noteras Hb 87, även sänkt LPK på 2, 9 x 109/l och TPK 87 x 109/l. B 12 och folat ua. § Remitteras till hematologisk klinik där benmärgsundersökning utförs.

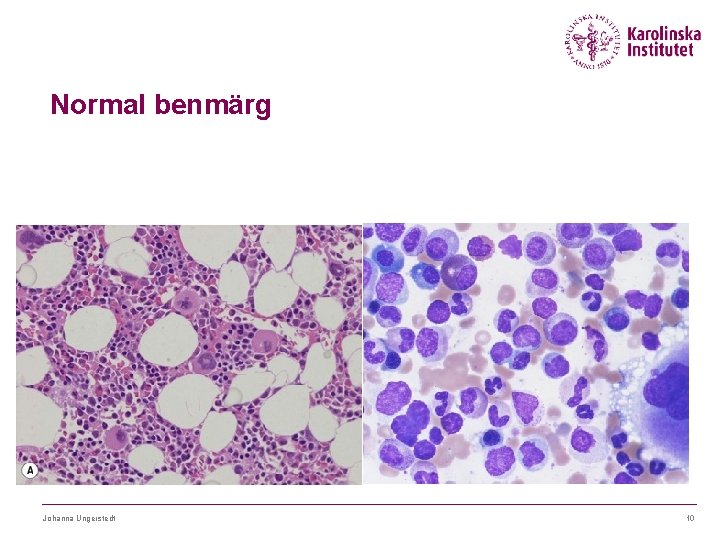
Normal benmärg Johanna Ungerstedt 10

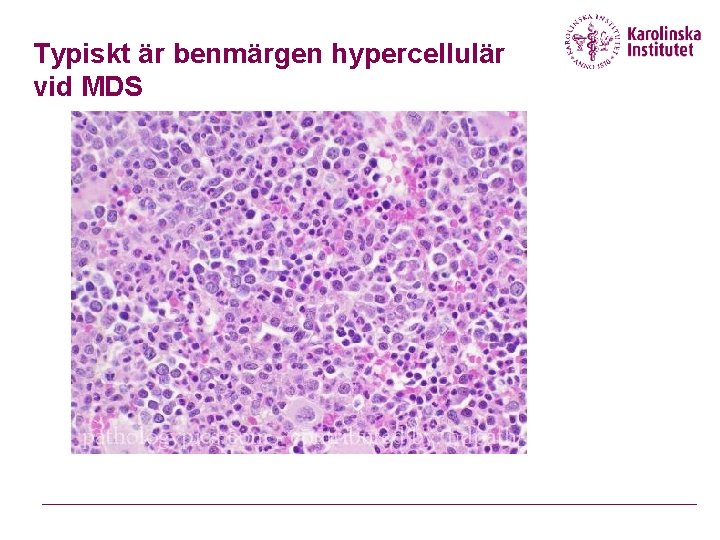
Typiskt är benmärgen hypercellulär vid MDS

Patientfall 1 Benmärgsmorfologi Dysplasi i erytro-, granulocyto- och trombocytopoesen. normalt antal blaster Signifikanta dysplasier i minst en av de tre poeserna ses vid MDS

Dysplastisk neutrofil granulocyt - pseudo-Pelger anomali

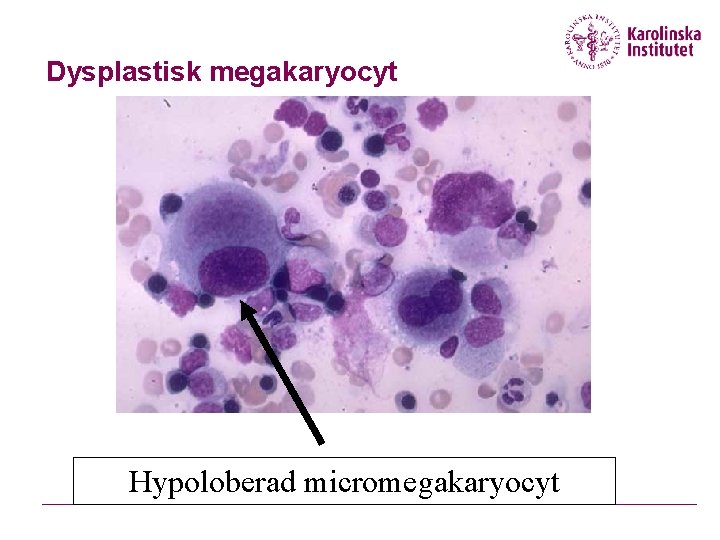
Dysplastisk megakaryocyt Hypoloberad micromegakaryocyt

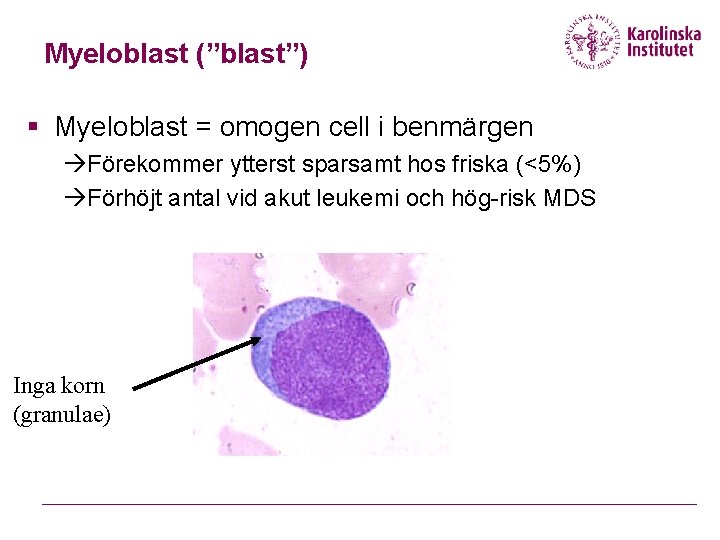
Myeloblast (”blast”) § Myeloblast = omogen cell i benmärgen Förekommer ytterst sparsamt hos friska (<5%) Förhöjt antal vid akut leukemi och hög-risk MDS Inga korn (granulae)

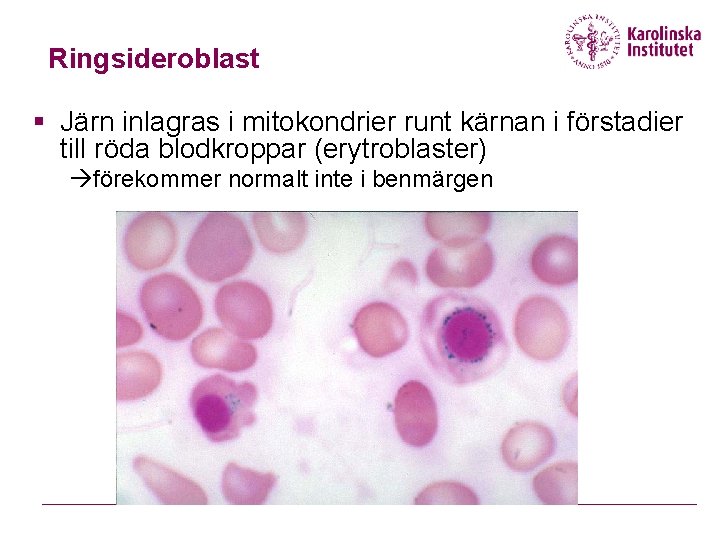
Ringsideroblast § Järn inlagras i mitokondrier runt kärnan i förstadier till röda blodkroppar (erytroblaster) förekommer normalt inte i benmärgen

Diagnos / Klassifikation § Ny benmärg evter 1 -3 månader för att fastställa diagnosen § kromosomanalys normal § Klassifikation enligt WHO! Varför? Ger information om viktiga särdrag i olika undergrupper av MDS Baserar sig på: § benmärgsmorfologi (vilka cellinjer som är dysplastiska), samt ev förekomst av ringsideroblaster § andel blaster § kromosomavvikelser § hur låga de perifera blodvärdena är

WHO klassifikation 2016 MDS subtyper D Arber et al Blood 2016 Namn Efternamn 18

Kromosomerna centrala för prognosen Avvikelser ses hos 50 % av MDS-patienterna Heterogena och varierande abnormaliteter Kromosomavvikelserna har olika prognostisk innebörd Greenberg, Blood 2012

IPSS-R Prognos Score MDS baseras på: -cytogenetik -blast % -Hb -TPK -Neutrofila 20

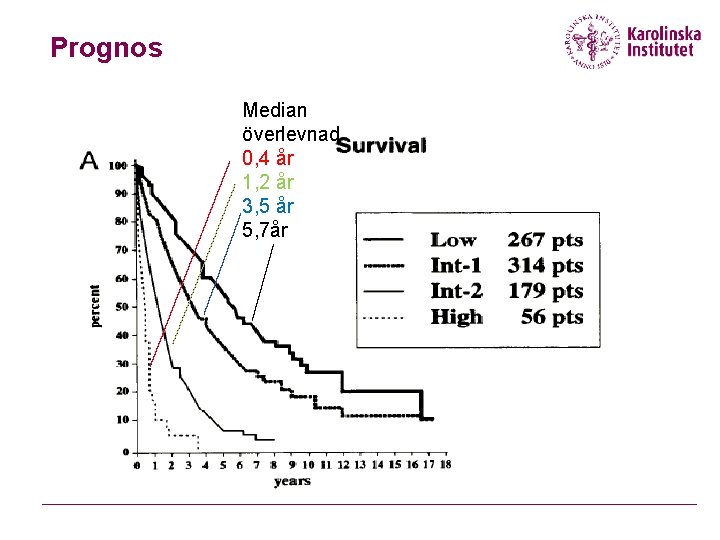
Prognos Median överlevnad 0, 4 år 1, 2 år 3, 5 år 5, 7år

Förenklad riskindelning § ”Lågrisk MDS” <10% blaster IPSS Low eller Int-1 § ”Högrisk MDS” 10 -19% blaster* IPSS Int-2 eller High alternativt lägre blasttal men med högrisk kromosomavvikelser § Har betydelse för hur vi kommunicerar prognos med patienten uppföljning/behandling *om ≥ 20% blaster så definitionsmässigt AML

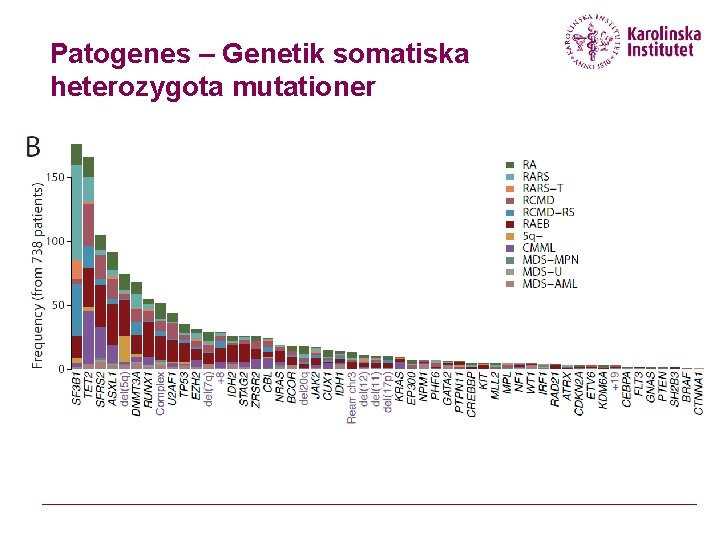
Patogenes – Genetik somatiska heterozygota mutationer

MDS är klonala stamcellssjukdomar

Ökad apoptos under utmognaden Benmärg: Ökat antal omogna celler. Hypercellulär benmärg Under utmognaden går cellerna i apoptos innan de mognar ut till färdiga, differentierade celler. Blod: Ökad apoptos leder till cytopeni (anemi, neutropeni, trombocytopeni)

MDS epidemiologi / riskfaktorer § Medianålder vid insjuknande: 70 år § Män / kvinnor = 1. 4 / 1 § En liten ärftlig komponent, ingen praktisk betydelse. Sällsynta ärftliga former finns § Cytostatika – den starkaste riskfaktorn Alkylerande (te x cyklofosfamid, melfalan) Topoisomeras II hämmare (te x etoposid, antracykliner) 20% av alla MDS fall anses vara terapirelaterade § Joniserande strålning 2 gångers riskökning, dosberoende § Hög exposition för organiska lösningsmedel 2, 1 gångers riskökning § Rökning 1, 7 gångers riskökning § Alkohol Ingen riskökning. Rödvin eventuellt mindre risk. Strom, Leukemia 2005, Sem in Hematology 2008

Myelodysplasi kan förekomma vid många tillstånd § Alkoholöverkonsumtion § Brist på vitaminer / spårämnen B 12, folat, koppar § § § Hypothyreos Infektioner (EBV, CMV, parvovirus, HIV, hepatit mm) SLE, leversjukdom, vissa andra blodsjukdomar Behandling med cytostatika / strålning Läkemedelsbiverkan trimetoprim, kloramfenikol, immunosuppressiva § Förgiftning (bly, arsenik m fl) § MDS kräver att sekundära orsaker till dysplasi utesluts

Utredning misstänkt MDS § Blodstatus och diff § Ferritin, F-Hb, B 12, folat, homocystein, njurfunktion, leverfunktion, TSH, DIC-prover § Hemolysprover (reticulocyter, LD, bilirubin, haptoglobin, DAT) § Virusdiagnostik HIV, hepatit B/C § i särskilda fall parvovirus B 19, EBV, CMV § Benmärgsanalys – dysplasier? Morfologi och histopatologi § OBS biopsi viktig § Kromosomanalys (benmärg) § S-erytropoetin, HLA-typning

Kliniska problem vid MDS Anemi 90% • Transfusionsbehov • Sänkt livskvalitet • Järnöverskott Neutropeni 50% • 5% grav (<0, 2 x 109/l) • Infektioner Trombocytopeni 50% • 10% grav (<20 x 109/l) • Blödningar AML-utveckling 30% av alla MDS Inflammatoriska symtom 10% • ledbesvär • hudutslag • SLE-liknande

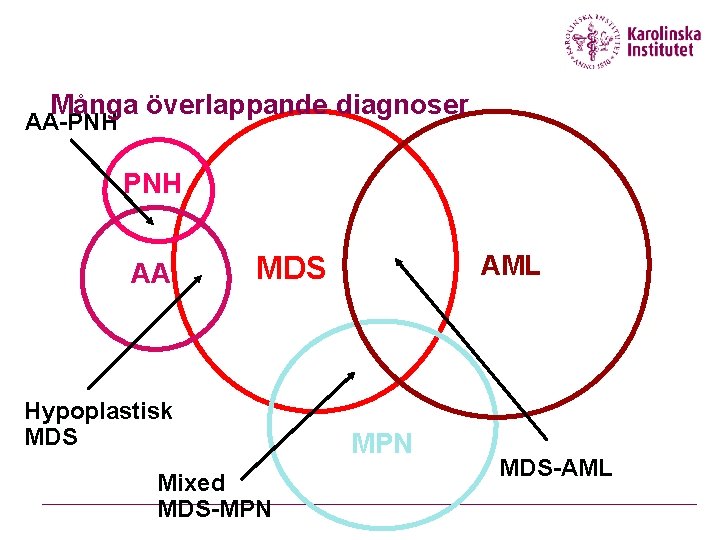
Många överlappande diagnoser AA-PNH AA MDS Hypoplastisk MDS Mixed MDS-MPN AML MPN MDS-AML

g n i l d n a DS beh M LIVSKVALITET ÖVERLEVNAD

Lågrisk MDS - behandling

Hematopoetiska tillväxtfaktorer vid MDS § Erytropoetinanaloger Epoetin (EPO) och darbepoetin (DAR; långverkande) Indicerat vid lågrisk MDS och signifikant anemi Totalt 20 -40% svarsfrekvens (70% vid noggrant patienturval) § Högt endogent S-EPO och stort transfusionsbehov negativa prediktorer för svar I snitt 2 års svarsduration § Tillägg av G-CSF om uteblivet svar Synergistisk effekt; ökar chansen till svar

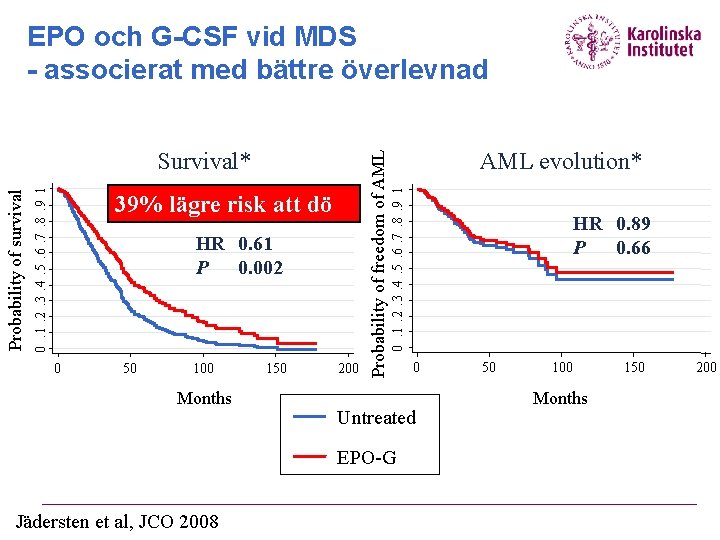
39% lägre risk att dö HR 0. 61 P 0. 002 0 50 100 Months 150 200 AML evolution* 0. 1. 2. 3. 4. 5. 6. 7. 8. 9 1 Probability of survival Survival* Probability of freedom of AML EPO och G-CSF vid MDS - associerat med bättre överlevnad 0 Untreated EPO-G Jädersten et al, JCO 2008 HR 0. 89 P 0. 66 50 100 Months 150 200

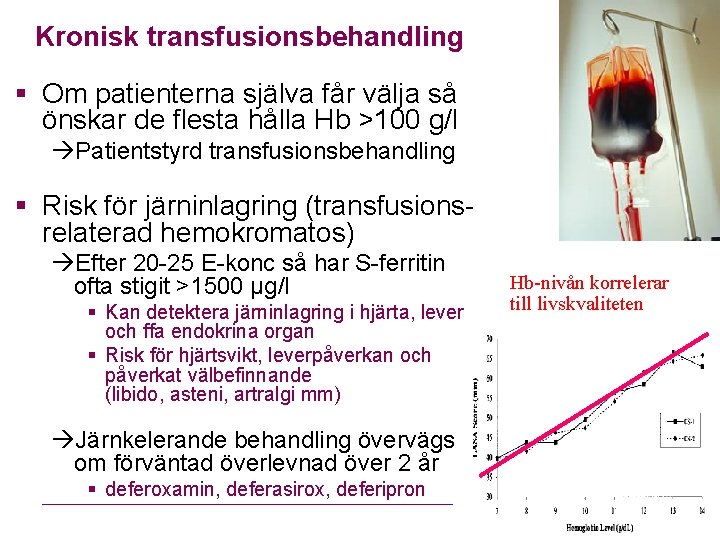
Kronisk transfusionsbehandling § Om patienterna själva får välja så önskar de flesta hålla Hb >100 g/l Patientstyrd transfusionsbehandling § Risk för järninlagring (transfusionsrelaterad hemokromatos) Efter 20 -25 E-konc så har S-ferritin ofta stigit >1500 µg/l § Kan detektera järninlagring i hjärta, lever och ffa endokrina organ § Risk för hjärtsvikt, leverpåverkan och påverkat välbefinnande (libido, asteni, artralgi mm) Järnkelerande behandling övervägs om förväntad överlevnad över 2 år § deferoxamin, deferasirox, deferipron Hb-nivån korrelerar till livskvaliteten

Högrisk MDS - behandling

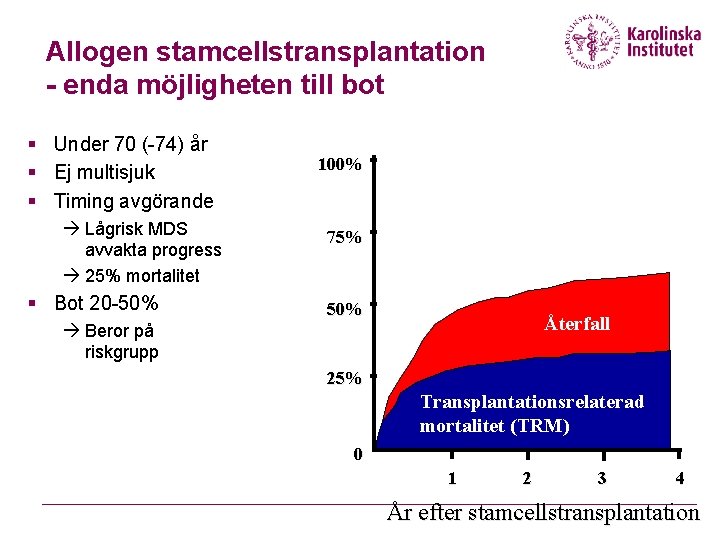
Allogen stamcellstransplantation - enda möjligheten till bot § Under 70 (-74) år § Ej multisjuk § Timing avgörande Lågrisk MDS avvakta progress 25% mortalitet § Bot 20 -50% 100% 75% 50% Återfall Beror på riskgrupp 25% Transplantationsrelaterad mortalitet (TRM) 0 1 2 3 4 År efter stamcellstransplantation

Hypometylerande behandling Azacytidin (Vidaza®) § § 5 -azacytidin 60% förbättrar sina blodvärden Endast 10 -20% kompletta remissioner § Hålls i schack men elimineras inte Svarsduration i snitt 15 månader Proportion surviving 1. 0 § 0. 9 0. 8 0. 7 Förbättrar överlevnaden vs standardbehandling* Medianöverlevnad 24 vs. 15 månader, P<0. 001 Hazard ratio 0. 58 (42% mindre risk attt dö) 0. 6 24. 4 months 0. 5 15 months 0. 4 Difference: 9. 4 months 0. 3 Azacytidin Supportive care / Cytostatics 0. 2 0. 1 0. 0 0 5 10 15 20 25 Time (months) from randomisation 30 35 40 Fenaux, Lancet Oncology 2009

MDS behandling - sammanfattning § § Nonchalera inte en oklar anemi hos äldre eller patienter som tidigare behandlats med cytostatika ell strålning tänk på MDS Beakta differentialdiagnoser Riskstratifierad behandling – livskvalitet viktigt Primum non nocere Tänk alltid på möjligheten till botande allogen SCT Måste göras i rätt tid; inte för tidigt, inte för sent § Lågrisk MDS – förbättra blodvärdena och sträva efter god livskvalitet Blodtransfusion och behandling av järnöverskott Tillväxtfaktorer: EPO +/- G-CSF Immunmodulerande eller immunosupprimerande § Högrisk MDS – slå tillbaka maligna klonen Allogen stamcells transplantation Hypometylerande droger Cytostatika, lågdos eller AML-liknande Palliativ and understödjande behandling
 Paramalignt syndrom
Paramalignt syndrom Johanna ungerstedt
Johanna ungerstedt Mircea oprica
Mircea oprica Mitoshämmare
Mitoshämmare Osiris zuyd
Osiris zuyd Escalatieladder beginnend docent
Escalatieladder beginnend docent Milijana novovic buric
Milijana novovic buric Simon burgers docent
Simon burgers docent Mortuis vivos docent
Mortuis vivos docent Maja maričić docent
Maja maričić docent Doçent ek ders ücreti
Doçent ek ders ücreti Från student till docent
Från student till docent Define docent
Define docent Magister dorenweerd
Magister dorenweerd Admissio borsa personal docent
Admissio borsa personal docent Amelia earhart birth
Amelia earhart birth Abrufvertrag rahmenvertrag
Abrufvertrag rahmenvertrag Johanna lattu
Johanna lattu Johanna waldau
Johanna waldau Johanna londoño modelo
Johanna londoño modelo Johanna chan md
Johanna chan md Avanne ja alkoholi
Avanne ja alkoholi Does christina forgive tris for killing will
Does christina forgive tris for killing will Johanna bobrowski
Johanna bobrowski Johanna marroig
Johanna marroig Porvoon kaupunki vanhuspalvelut
Porvoon kaupunki vanhuspalvelut 33 and 34
33 and 34 Etkl
Etkl Johanna snickars
Johanna snickars Johanna chan pack
Johanna chan pack Prof. johanna haberer
Prof. johanna haberer Organigramme école maternelle
Organigramme école maternelle Johanna will-orava
Johanna will-orava Johanna spyri biografia
Johanna spyri biografia Johanna hade
Johanna hade Johanna eia
Johanna eia Johanna breyne
Johanna breyne Johanna nguyen
Johanna nguyen Johanna rönn
Johanna rönn Johanna wyn
Johanna wyn