Myelodysplastisk syndrom Behandling av hyrisiko sykdom Synne Torkildsen

Myelodysplastisk syndrom Behandling av høyrisiko sykdom Synne Torkildsen, 19. september 2017

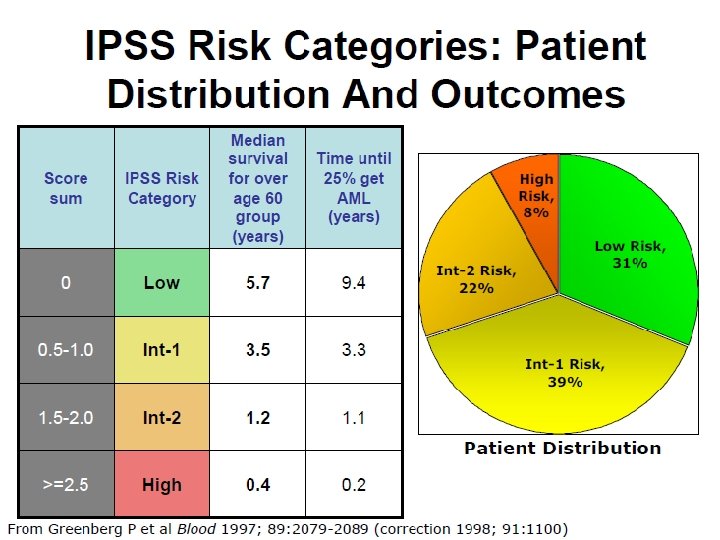
Risikogrupper Forventet risiko for å utvikle AML og forventet overlevelse. Redskap for å velge beste behandlingsalternativ. Vanligste scorings-systemer brukt i dag: IPSS (International Prognostic Scoring system) Lav risiko Lav og Int-1 Høy risiko Int-2 og Høy (> 1, 5) IPSS-R (Revised International Prognostic Scoring system) Lav risiko Intermediær Høy risiko (>4, 5)
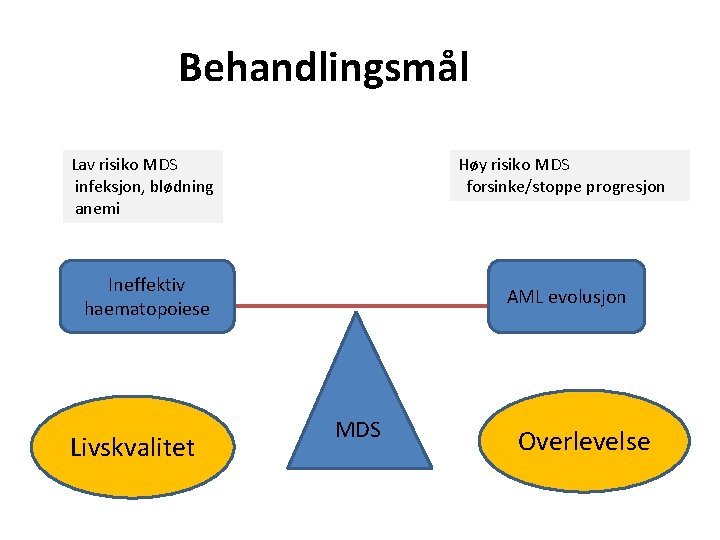
Behandlingsmål Lav risiko MDS infeksjon, blødning anemi Høy risiko MDS forsinke/stoppe progresjon Ineffektiv haematopoiese Livskvalitet AML evolusjon MDS Overlevelse

Behandling høyrisiko 1. Støttebehandling; målet er å få kontroll på symptomer. 2. Lav intensitetsbehandling; målet er å forsinke sykdomsutviklingen. a) Hypometylerende, b) Immunmodulerende c) Lavdose cellegift 1. Intensiv cellegiftsbehandling; 2. Allogen stamcelletransplantasjon: Den eneste behandlingen med mulighet for kurasjon

2. Lav intensitet Målet er å forsinke sykdomsutviklingen. Behandle sykdommen med så få bivirkninger som mulig, og på den måten opprettholde en god livskvalitet. a) Hypometylerende behandling: Azacitidine (Vidaza) – førstehåndsbehandling i ca. 10 år Godkjent for behandling av int-2/ høyrisk MDS, og MDS- AML med 20 -30% blaster. For høyrisk pasienter uegnet for transplantation, evt. som en “bro” til transplantasjon.

Azacitidine • Påvirker kreftceller på DNA nivå, hvilket kan «slå gener av og på» . • Kan «slå på» tumor suppressor gener som har blitt stille i MDS. • Tumor suppressor gener lager proteiner som normalt forhindrer kreftutvikling. • Ved MDS, har tumor suppressor gener ofte blitt stille grunnet tillegg av » methyl grupper» på DNA (epigenetisk modifisering). • Forhindrer tillegg av methyl grupper, vekker tumor ekspresjons gener - som igjen presser MDS celler vekk.

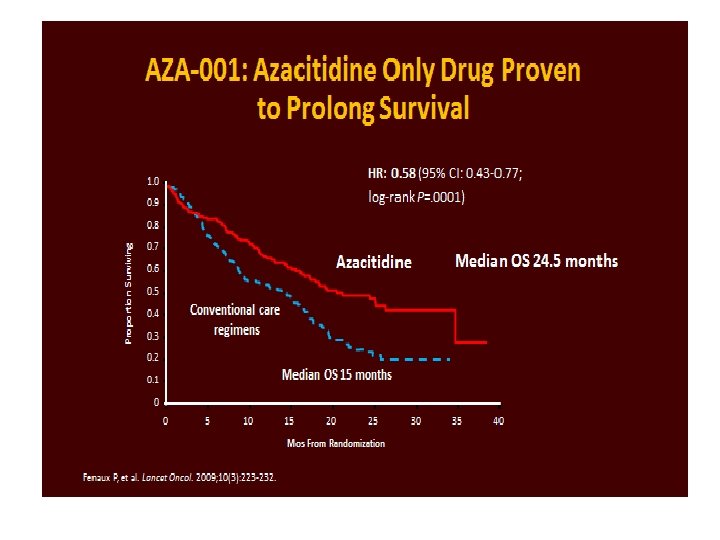
Azacitidine - Langsom behandling, trenger måneder for respons. - Må brukes på ubestemt tid for å være effektiv. - Ikke kurativ Kan resultere i: • Redusert behov for transfusjoner og mindre infeksjoner. • Forsinke utvikling til mer alvorlig sykdom • I store studier vist å bremse utviklingen fra MDS til akutt leukemi, av og til i mange år, samt gi forlenget overlevelse. • Kan også gi økt overlevelse og forbedre livskvalitet, sammenliknet med støttebehandling alene.

Azacitidine • Gis under huden, på abdomen, armer eller ben, evt. Intravenøst • Medikamentet gis i 5 (100 mg/m^2) eller 7 dager(75 mg/m^2) hver 28 dag. • Evaluering av respons etter 6 sykler, med mindre tegn til sykdomsprogresjon før. • Kan gå opp til 6 sykler før man ser respons. • Behandlingen skal fortsette frem til klare tegn på tap av effekt, eller til progresjon.

Azacitidine Lav dose, godt tolerert, få bivirkninger- selv hos svært gamle pasienter. Vanligste bivirkninger; • Litt muskel- og leddsmerter • kvalme, • Forstoppelse eller diare, • myelosuppresjon • lokale reaksjoner rundt innstikksted.

Decitabine • Hypometylerende middel som Azacitidine, tilsvarende behandlingsmekanisme og resultat. • Noe mildere bivirkninger. • Ved MDS Int-2 og høyrisk, hvis Azacitidine ikke kan brukes på grunn av bivirkninger. • 15 mg/m^2 intravenøst over 3 timer, hver 8. time, dag 1 -3, hver 6. uke. • Evt. 20 mg/m^2 intravenøst over 1 time i 5 påfølgende dager, hver 4. uke. • Responsevaluering etter 4 -6 sykler, med mindre klare tegn til progresjon før. • Behandlingen fortsetter frem til progresjon.

c). Lavdose kjemoterapi: Hos enkelte pasienter kan lavdosert kjemoterapi bli brukt til å redusere antall hvite blodceller, blaster, og bedre pancytopenien. • Alkeran tabletter; • Symptomatisk behandling av høyrisk MDS og MDS-AML med normal karyotype og hypo/normocellulær benmarg. • Lav-dose cytarabin • Symptomatisk behandling av cytopeni hos selekterte høyrisk pasienter. Lav responsrate hvis lavt platetall og kromosomavvik ved diagnose.

3. Intensiv cellegiftsbehandling • Utslette en signifikant andel syke celler i benmargen, for å gi den mulighet til å fungere normalt igjen (remisjon). • Aktuelt for noen pasienter med; • - høyrisk MDS, • - sykdomsprogresjon til AML • - høy andel leukemiceller (blaster) i benmargen. • Liknende regime som ved akutt myelogen leukemi. • Krever sykehusinnleggelse. • Endel bivirkninger, spesielt relatert til cytopenier, - men også kvalme/oppkast, diare, såre slimhinner, hud forandringer, hårtap, dårlig matlyst.

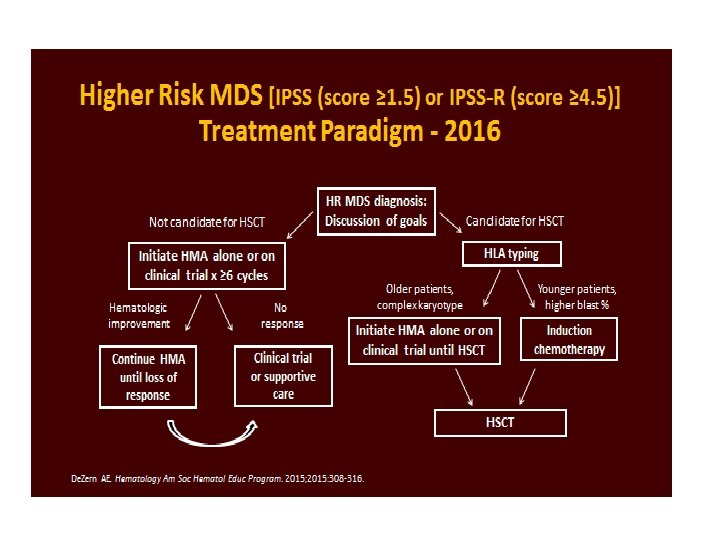
Intensiv cellegiftsbehandling • Anbefalt hvis pasienten er forholdsvis ung (f. eks under 60 år) og i god klinisk form – etterfulgt av • allogen stamcelletransplantasjon. • Vanligvis ikke anbefalt til pasienter med dårlig klinisk status, spesielt hvis > 65, eller hvis > 75 år. • Hos eldre, der azacitidine har sviktet (eller > 30% blaster) – hvis god klinisk status, og gode prognostiske funn. • Kan også være aktuelt for pasienter aktuelle for benmargstransplantasjon, uten egnet giver.

Konklusjon • Behandling basert på risiko for sykdom; lavrisk vs. høyrisk. • Allogen stamcelletransplantasjon er eneste potensielt kurative behandling per idag – men ikke for alle. • Azacitidine er generelt anbefalt som førstevalg for høyrisk MDS samt MDS/AML med 20 – 30% blaster • Evt. AML lik behandling hvis pasienten er ung med godt prognostisk utgangspunkt for å kunne oppnå respons. • Enkelte har best nytte av støttebehandling også i denne gruppen. • I retning av mer persontilpasset og individualisert behandling – men fortsatt et stykke frem.

Takk for oppmerksomheten
- Slides: 19