Myelodisplastik Sendrom Yksek Riskli Hasta Takip ve Tedavisi








































- Slides: 65

Myelodisplastik Sendrom Yüksek Riskli Hasta Takip ve Tedavisi Dr. Fahri ŞAHİN Ege Üniversitesi Tıp Fakültesi İç Hastalıkları AD, Hematoloji BD


Ne demek Yüksek riskli hasta? • Ortalama yaşam beklentisi < 1 yıl • AML’ ye dönüşüm riski yüksek • IPSS’e göre: Orta II ve Yüksek risk grubu hastalar

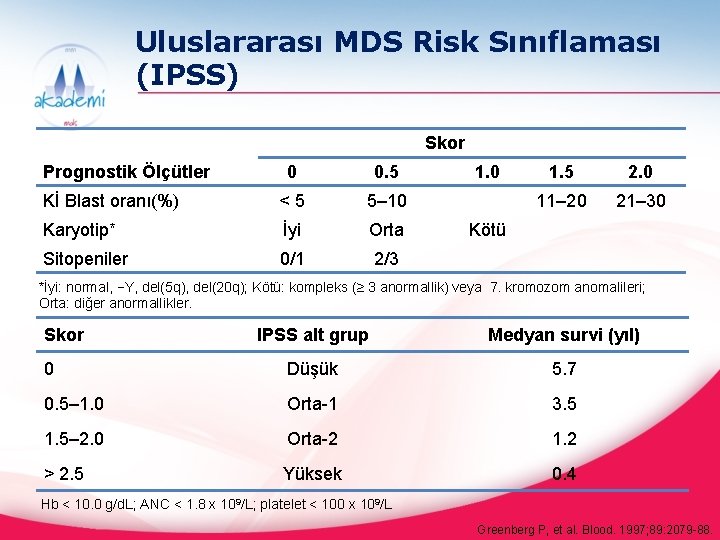
Uluslararası MDS Risk Sınıflaması (IPSS) Skor Prognostik Ölçütler 0 0. 5 Kİ Blast oranı(%) <5 5– 10 Karyotip* İyi Orta Sitopeniler 0/1 2/3 1. 0 1. 5 2. 0 11– 20 21– 30 Kötü *İyi: normal, −Y, del(5 q), del(20 q); Kötü: kompleks (≥ 3 anormallik) veya 7. kromozom anomalileri; Orta: diğer anormallikler. Skor IPSS alt grup Medyan survi (yıl) 0 Düşük 5. 7 0. 5– 1. 0 Orta-1 3. 5 1. 5– 2. 0 Orta-2 1. 2 > 2. 5 Yüksek 0. 4 Hb < 10. 0 g/d. L; ANC < 1. 8 x 109/L; platelet < 100 x 109/L Greenberg P, et al. Blood. 1997; 89: 2079 -88.

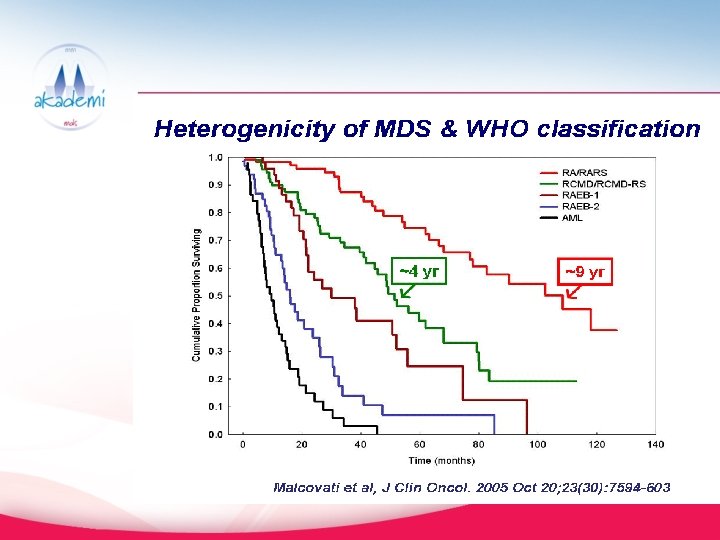
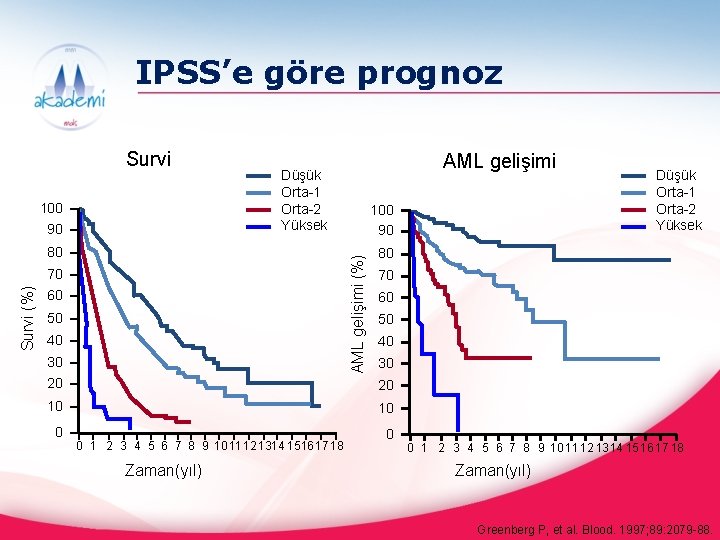
IPSS’e göre prognoz Survi 100 90 AML gelişimi (%) 80 70 Survi (%) AML gelişimi Düşük Orta-1 Orta-2 Yüksek 60 50 40 30 80 70 60 50 40 30 20 20 10 10 0 0 1 2 3 4 5 6 7 8 9 10 1112 1314 151617 18 Zaman(yıl) Düşük Orta-1 Orta-2 Yüksek 0 0 1 2 3 4 5 6 7 8 9 10 11 12 1314 1516 17 18 Zaman(yıl) Greenberg P, et al. Blood. 1997; 89: 2079 -88.

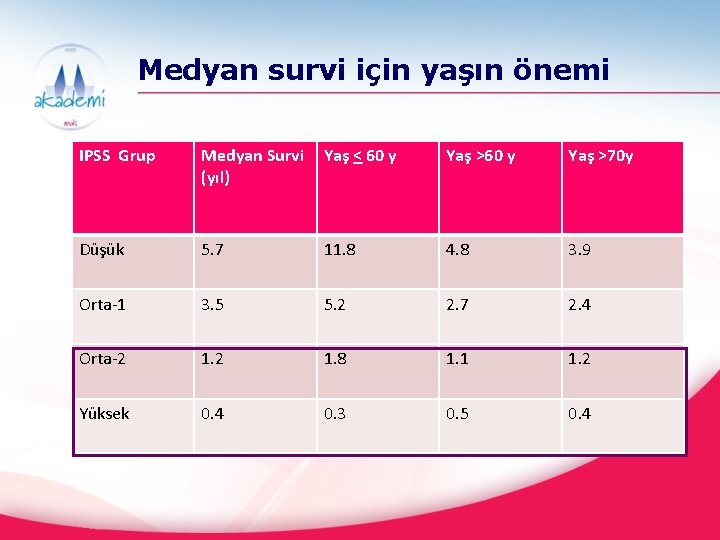
Medyan survi için yaşın önemi IPSS Grup Medyan Survi (yıl) Yaş < 60 y Yaş >70 y Düşük 5. 7 11. 8 4. 8 3. 9 Orta-1 3. 5 5. 2 2. 7 2. 4 Orta-2 1. 8 1. 1 1. 2 Yüksek 0. 4 0. 3 0. 5 0. 4



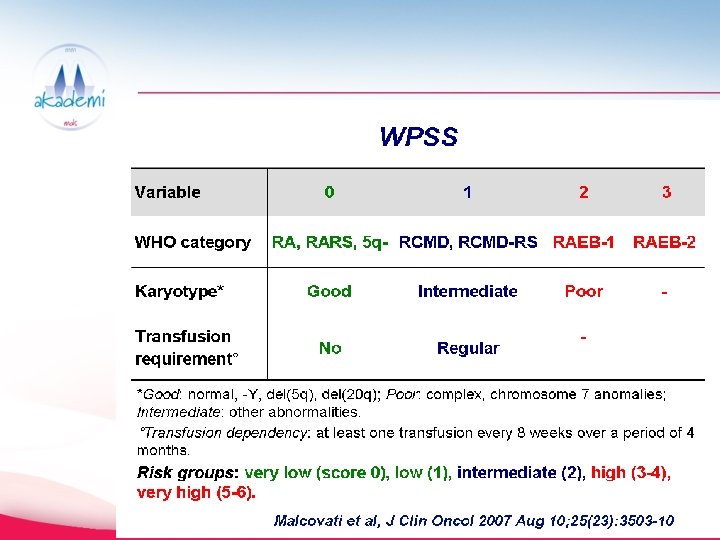
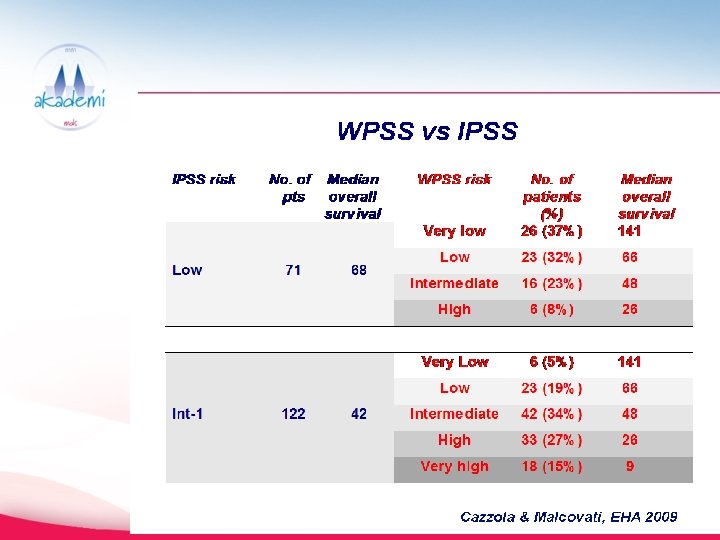
Ne demek Yüksek riskli hasta? • Ortalama yaşam beklentisi < 1 yıl • AML’ ye dönüşüm riski yüksek • IPSS’e göre: Orta II ve Yüksek risk grubu hastalar • WPSS’e göre: Yüksek ve Çok Yüksek risk grubu hastalar

IPSS Risk Kategori Dağılımı Yüksek %8 Düşük %31 Orta-2 %22 Orta-1 %39 Greenberg PL et al. Blood. 1997; 89: 2079

Yüksek riskli hastayı belirlemek • WHO sınıfı, Kemik iliği blast oranı • Karyotipi • Sitopeni durumu • Transfüzyon ihtiyacı

Yüksek Riskli Hasta Tedavisi

Tedavi hedefleri • Yaşamı uzatmak (kaliteli yaşamı) • Progresyonu durdurmak • AML ye dönüşümü geciktirmek • Tam remisyon elde etmek • Minimal yan etki

MDS: Tedavi Seçenekleri • “En iyi destek tedavisi”, demir şelasyonu • Hematopoietik büyüme faktörleri Düşük • Immünsüpresif tedavi • Immünmodulatuar ilaçlar • Arsenik trioksit • Düşük doz kemoterapi • Epigenetik tedaviler • Farnesiltransferaz inhibitörleri • Yoğun kemoterapi Çok Yüksek • Allo-KHN

Myelodisplastik Sendrom Epigenetik ve Hipometile Edici Ajanlar

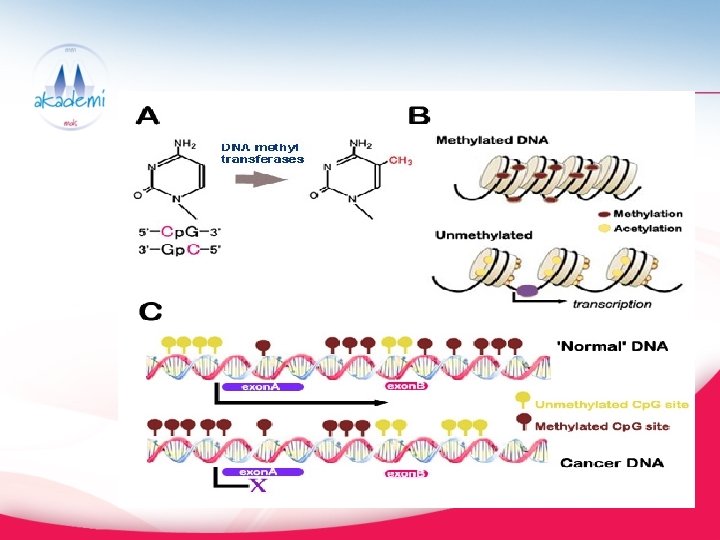
DNA METİLASYONU • Post-replikatif bir mekanizmadır • DNA düzeyinde yapılan modifikasyonla karakterize epigenetik mekanizmadır • DNA metiltransferaz görev alır • İnsanda % 90 oranında metillenen nükleotidler Cp. G dinükleotididir


MDS de Genlerin Hipermetilasyon Durumu • p 15 INK 4 A (~65%) – hücre siklus kontrolü • DAP kinaz (~47%) – Apoptozis • Frajil histidin triad (FHIT) geni • SOCS 1 – sitokin regülasyonu • E-cadherin – adezyon • Alfa catenin (del 5 q)

Hipometile Edici Sitozin Analogları Sitozin 5 -metilsitozin Riboz Deoksiriboz 5 -azasitidin 5 -aza-2’deoksisitidin

• Desitabin ve Azasitidin 1964'te Çekoslovakya’da sentezlenmiştir 1 • Her iki ajan da 1960'lı yılların sonlarında (preklinik)2 ve 1970'li yıllarda (klinik)3 araştırılmıştır • Desitabin ve Azasitidin 2004 ve 2006 yılında MDS ve KMML için FDA onayı almıştır • Peki bu ilaçların geliştirilmesinde neden bu kadar gecikme oldu? 1. Plimi and Sorm. Coll. Czech. Chem. Commum. 29: 2576, 1964 2. Piskala and Sorm. Coll. Czech. Chem. Commum. 29: 2060, 1964 3. Hrodek and Vesely. Neoplasma 18: 493, 1971

• 1980'li yıllarda yüksek dozlar o Lösemide azasitidin çalışmaları (kür başına 750 -1500 mg/m 2) o Desitabin için MTD kür başına 2000 mg/m 2 • Sonraki yıllarda daha düşük dozlar o MDS’de azasitidin (kür başına 525 mg/m 2' - orijinal dozun 1/3 ila 1/4'ü) (Silverman) o Desitabin (kür başına 50 -135 mg/m 2' - orijinal dozun 1/20'si)

AZASİTİDİN

• Sitidin nükleozid analoğu • DNA ve RNA’ya inkorpore olur • 1 -2 log düşük doz uygulamasında o Geri dönüşümsüz DNA metiltransferaz inhibisyonu

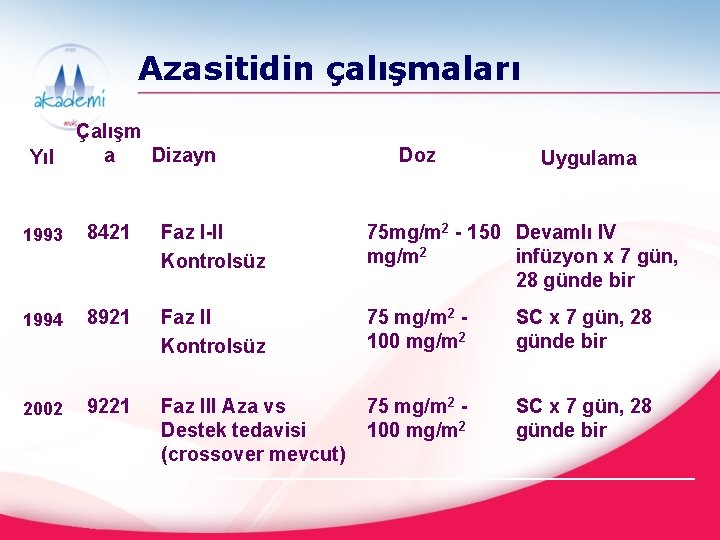
Azasitidin çalışmaları Yıl Çalışm a Dizayn Doz Uygulama 1993 8421 Faz I-II Kontrolsüz 75 mg/m 2 - 150 Devamlı IV mg/m 2 infüzyon x 7 gün, 28 günde bir 1994 8921 Faz II Kontrolsüz 75 mg/m 2 100 mg/m 2 SC x 7 gün, 28 günde bir 2002 9221 Faz III Aza vs Destek tedavisi (crossover mevcut) 75 mg/m 2 100 mg/m 2 SC x 7 gün, 28 günde bir

Azasitidin Yüksek Riskli MDS'de Sağkalımda İyileşme Sağlar AZA 75 mg/m 2/g x 7 g, 28 günde bir N=179 Randomizasyon Araştırıcı tarafından CCR tedavisi seçilmesi N=179 Yalnızca en iyi destekleyici bakım Düşük doz Ara-C (20 mg/m 2/g x 14 g, 28 -42 günde bir) Standart KT (7+3) AZA-001 Fenaux. Lancet Oncology 20: 223, 2009

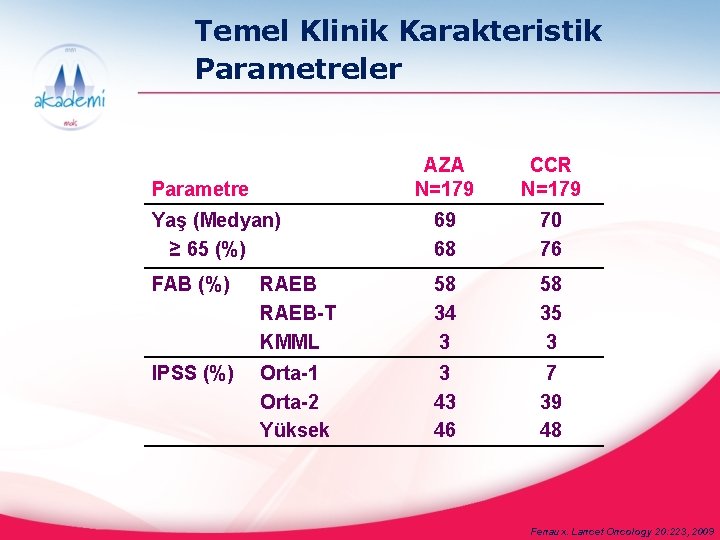
Temel Klinik Karakteristik Parametreler AZA N=179 CCR N=179 Yaş (Medyan) ≥ 65 (%) 69 68 70 76 FAB (%) RAEB-T KMML 58 34 3 58 35 3 IPSS (%) Orta-1 Orta-2 Yüksek 3 43 46 7 39 48 Parametre Fenaux. Lancet Oncology 20: 223, 2009

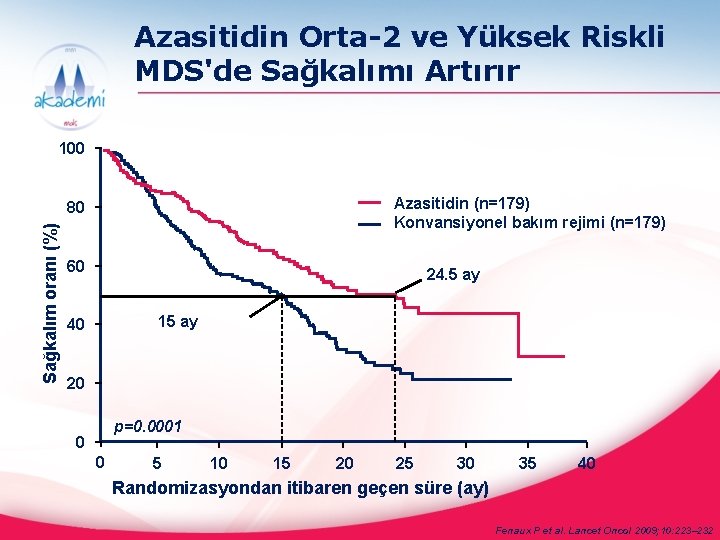
Azasitidin Orta-2 ve Yüksek Riskli MDS'de Sağkalımı Artırır 100 Azasitidin (n=179) Konvansiyonel bakım rejimi (n=179) Sağkalım oranı (%) 80 60 24. 5 ay 15 ay 40 20 p=0. 0001 0 0 5 10 15 20 25 30 35 40 Randomizasyondan itibaren geçen süre (ay) Fenaux P et al. Lancet Oncol 2009; 10: 223– 232

Primer Sonlanım Noktaları: Sonuçlar • Medyan sağkalım: o 24. 4 ay azasitidin grubunda vs 15 ay konvansiyonel tedavi rejimlerinde(CCR) (p< 0. 0001) o 9. 4 ay medyan sağkalım avantajı Azasitidin alan hastalar vs CCR • Toplam Sağkalımı %74 oranında uzatır o HR =0. 58 (95% CI: 0. 43 -0. 77) • 2 yıllık sağkalım avantajı oranı: o %50. 8 Azasitidin grubu vs %26. 2 CCR grubu (p<0. 0001) Fenaux P et al. Lancet Oncol 2009; 10: 223– 232

Sekonder Sonlanım Noktaları: Sonuçlar • AML’ye ya da ölüme kadar geçen süre o 13 ay AZA grubunda vs 7. 6 ay CCR grubunda, p=0. 003 • AML’ye kadar geçen süre o 26. 1 ay AZA grubunda vs 12. 4 ay CCR grubunda, p=0. 004 • RBC Transfüzyon Bağımsızlığı o 45% AZA grubu vs 11% CCR grubu, p<0. 0001 Fenaux P et al. Lancet Oncol 2009; 10: 223– 232

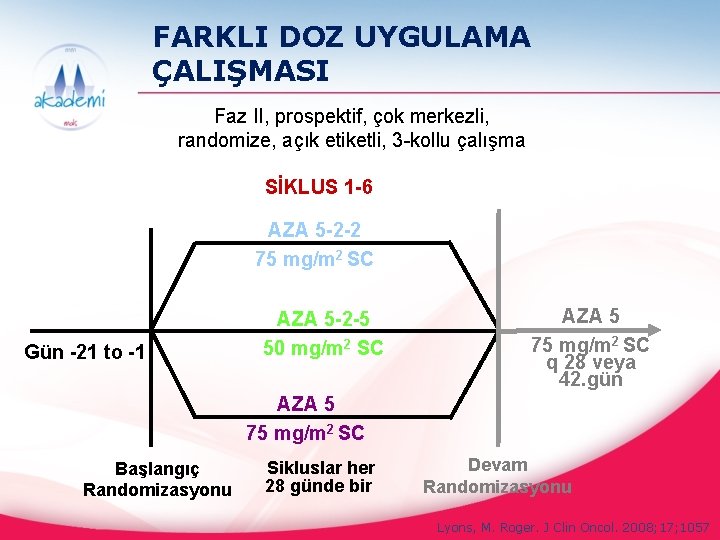
FARKLI DOZ UYGULAMA ÇALIŞMASI Faz II, prospektif, çok merkezli, randomize, açık etiketli, 3 -kollu çalışma SİKLUS 1 -6 AZA 5 -2 -2 75 mg/m 2 SC Gün -21 to -1 AZA 5 -2 -5 50 mg/m 2 SC AZA 5 75 mg/m 2 SC q 28 veya 42. gün AZA 5 75 mg/m 2 SC Başlangıç Randomizasyonu Sikluslar her 28 günde bir Devam Randomizasyonu Lyons, M. Roger. J Clin Oncol. 2008; 17; 1057

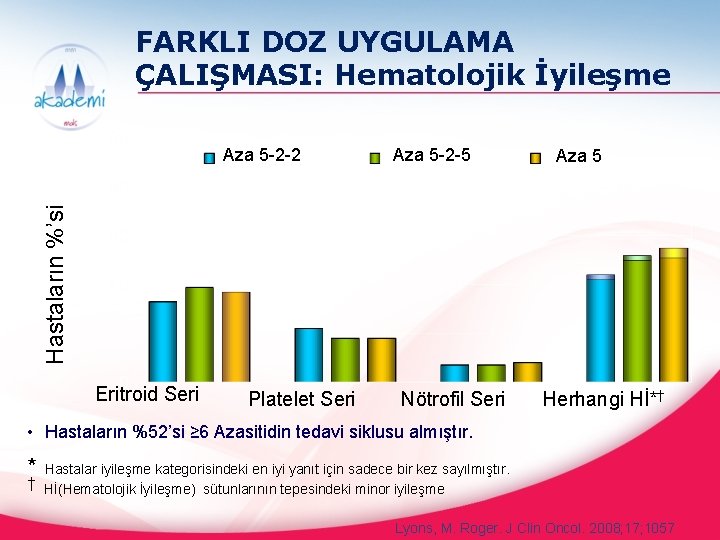
FARKLI DOZ UYGULAMA ÇALIŞMASI: Hematolojik İyileşme Aza 5 -2 -5 Aza 5 Hastaların %’si Aza 5 -2 -2 Eritroid Seri Platelet Seri Nötrofil Seri Herhangi Hİ*† • Hastaların %52’si ≥ 6 Azasitidin tedavi siklusu almıştır. * Hastalar iyileşme kategorisindeki en iyi yanıt için sadece bir kez sayılmıştır. † Hİ(Hematolojik İyileşme) sütunlarının tepesindeki minor iyileşme Lyons, M. Roger. J Clin Oncol. 2008; 17; 1057

DESİTABİN

Etki Mekanizması Metiltransferaz enzimini inhibe eder HİPOMETİLASYON SONUÇ • • Sessiz genlerin transkripsiyonu Tümör baskılayıcı genlerin aktive olması Malin hücrelere karşı immün yanıtın güçlenmesi Hücre farklılaşmasının indüklenmesi

D-0007 Çalışması Desitabin faz III tasarımı Çalışma 0007 (N=170) R A N D O M İ Z A S Y O N Destekleyici Bakım + Desitabin (N=89) Destekleyici Bakım (N=81) Kantarjian. Cancer 106: 1794, 2006.

D-0007 Çalışması Genel bilgiler • Açık, randomize 1: 1 • 22 merkez • Hastalar o n=170 o IPSS orta-1, orta-2 veya yüksek risk • Desitabin dozu 15 mg/m 2 q 8 h (toplam: 45 mg/m 2/g), 3 gün süreyle

D-0007 Çalışması Sonlanım noktaları • Çalışmanın birincil sonlanım noktaları o Toplam yanıt oranı (tam ve kısmi yanıt) o AML dönüşümüne veya ölüme kadar geçen süre • Tedaviyi kesme kriterleri o o Hastalığın ilerlemesi (>%30 blast oranı) 6 kür sonrası kısmi yanıt alınamaması 8 kür sonrası tam yanıt alınamaması Tam yanıtın 2 kür devam etmemesi

D-0007 Çalışması Yanıt değerlendirmesi • Desitabine yanıt veren hastalarda (CR ve PR) AML’ye veya ölüme kadar geçen süre 17. 5 ay iken, yanıt vermeyen hastalarda 9. 8 ay olmuştur (p=0. 01) • Desitabine yanıt veren hastalarda sağkalım 23. 5 ay iken, yanıt vermeyen hastalarda 13. 7 ay olarak belirlenmiştir (p=0. 007) Kantarjian H. et al. Decitabine Improves Patient Outcomes in Myelodysplastic Syndromes: Results of a Phase III Randomized Study. Cancer 2006; 106: 1794– 80.

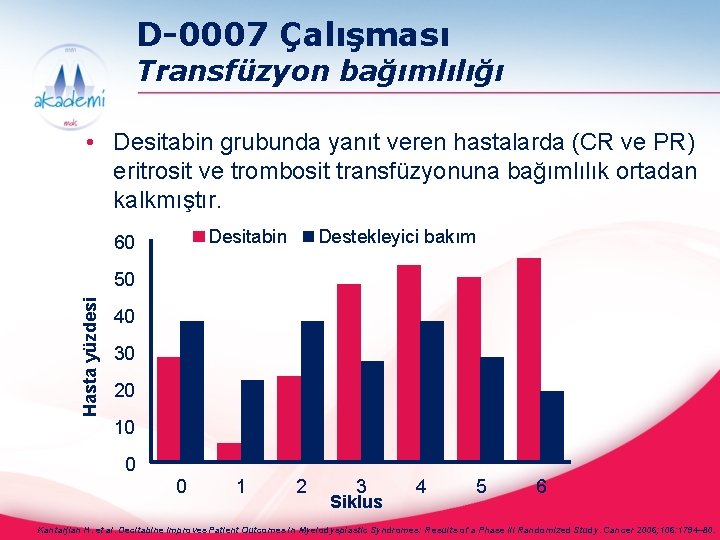
D-0007 Çalışması Transfüzyon bağımlılığı • Desitabin grubunda yanıt veren hastalarda (CR ve PR) eritrosit ve trombosit transfüzyonuna bağımlılık ortadan kalkmıştır. Desitabin 60 Destekleyici bakım Hasta yüzdesi 50 40 30 20 10 0 0 1 2 3 Siklus 4 5 6 Kantarjian H. et al. Decitabine Improves Patient Outcomes in Myelodysplastic Syndromes: Results of a Phase III Randomized Study. Cancer 2006; 106: 1794– 80.

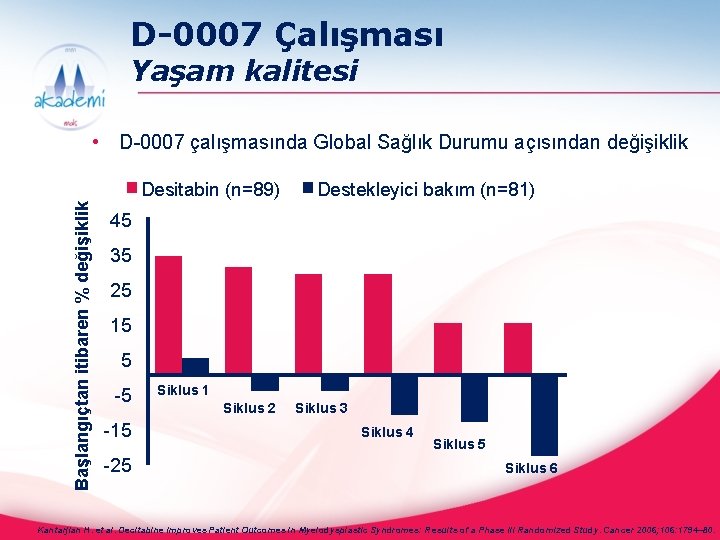
D-0007 Çalışması Yaşam kalitesi • D-0007 çalışmasında Global Sağlık Durumu açısından değişiklik Başlangıçtan itibaren % değişiklik Desitabin (n=89) Destekleyici bakım (n=81) 45 35 25 15 5 -5 -15 -25 Siklus 1 Siklus 2 Siklus 3 Siklus 4 Siklus 5 Siklus 6 Kantarjian H. et al. Decitabine Improves Patient Outcomes in Myelodysplastic Syndromes: Results of a Phase III Randomized Study. Cancer 2006; 106: 1794– 80.

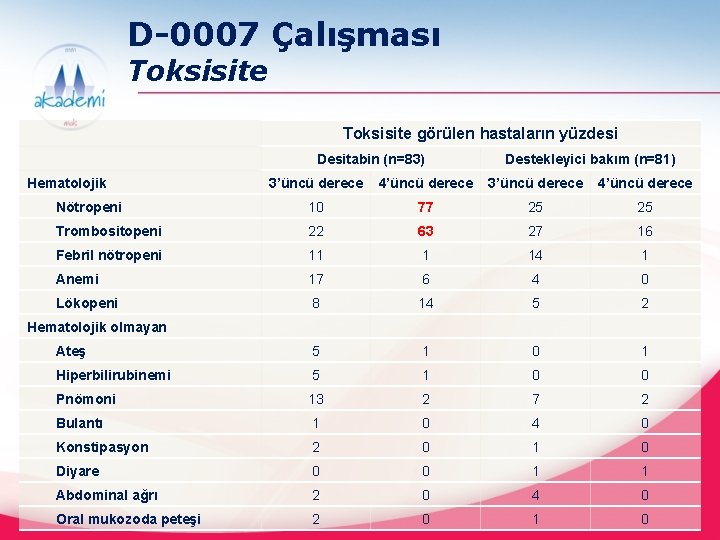
D-0007 Çalışması Toksisite görülen hastaların yüzdesi Desitabin (n=83) Hematolojik Destekleyici bakım (n=81) 3’üncü derece 4’üncü derece Nötropeni 10 77 25 25 Trombositopeni 22 63 27 16 Febril nötropeni 11 1 14 1 Anemi 17 6 4 0 Lökopeni 8 14 5 2 Ateş 5 1 0 1 Hiperbilirubinemi 5 1 0 0 Pnömoni 13 2 7 2 Bulantı 1 0 4 0 Konstipasyon 2 0 1 0 Diyare 0 0 1 1 Abdominal ağrı 2 0 4 0 Oral mukozoda peteşi 2 0 1 0 Hematolojik olmayan

ADOPT Çalışması Miyelodisplastik Sendromlu Erişkinlere 4 Haftada Bir 5 Gün Süreyle Günlük Desitabin Uygulamasının Çokmerkezli Çalışması: Ayakta Tedavi İçin Alternatif Dozaj (ADOPT) Çalışması David P. Steensma, Maria R. Baer, James L. Slack, Rena Buckstein, Lucy A. Godley, Guillermo Garcia-Manero, Maher Albitar, Julie S. Larsen, Sujata Arora, Michael T. Cullen ve Hagop Kantarjian J Clin Oncol. 2009. DOI: 10. 1200/JCO. 2008. 19. 6550. Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

ADOPT Çalışması Çalışma tasarımı • Çok merkezli, randomize olmayan, açık etiketli çalışma • Kuzey Amerika’dan 28 merkez, 99 hasta • ≥ 18 yaş; Medyan yaş 72 (34 -87) • Kronik miyelomonositik lösemi dahil (BK<12 x 109/L) herhangi bir FAB alt sınıfına ait MDS tanısı konmuş (yeni veya sekonder) • Her 4 haftada bir, 5 ardışık gün süresince 1 saat süresi ile desitabin 20 mg/m 2/gün IV infüzyon Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

ADOPT Çalışması Sonlanım noktaları • Primer sonlanım noktası o Toplam yanıt oranı (IWG 2006 yanıt kriterleri) • Sekonder sonlanım noktaları o o o Sitogenetik yanıt Hematolojik iyileşme Yanıt süresi Sağkalım Güvenlilik Transfüzyon ihtiyacı Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

ADOPT Çalışması IWG kriterine göre yanıt • 5 günlük desitabin tedavisi, hastaların yarısından fazlasında gösterdiği iyileşmeyle MDS hastalarında anlamlı klinik yarar sağlamıştır • Medyan kullanım siklus sayısı 5 (0 -17) 2006 IWG kriterine göre yanıt ITT popülasyonu Hasta sayısı Yüzde Toplam tam yanıt oranı, CR+m. CR 32 32 Toplam yanıt oranı, CR+m. CR+PR 32 32 Toplam düzelme oranı, CR+m. CR+PR+HI 50 51 Stabil ya da daha iyi hastalık durumu oranı, CR+m. CR+PR+HI+SD 74 75 CR 17 17 HI 18 18 Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

ADOPT Çalışması Yanıt hızı ve süresi • İlk yanıtlar, vakaların %82’sinde 2. kürün sonunda gözlendi • Klinik iyileşme gösteren 50 hastanın %54’ü en iyi yanıta ilk 2 kürde ulaştı İlk yanıta ve en iyi yanıta kadar geçen süre Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

ADOPT Çalışması Güvenlilik verileri • Hastaların %10 ve daha fazlasında oluşan advers olayların özeti Hastaların yüzdesi Hematolojik olay 1 -2’nci derece ≥ 3’üncü derece Nötropeni 1 31 Trombositopeni 2 18 Febril nötropeni 3 14 Anemi 5* 12 Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

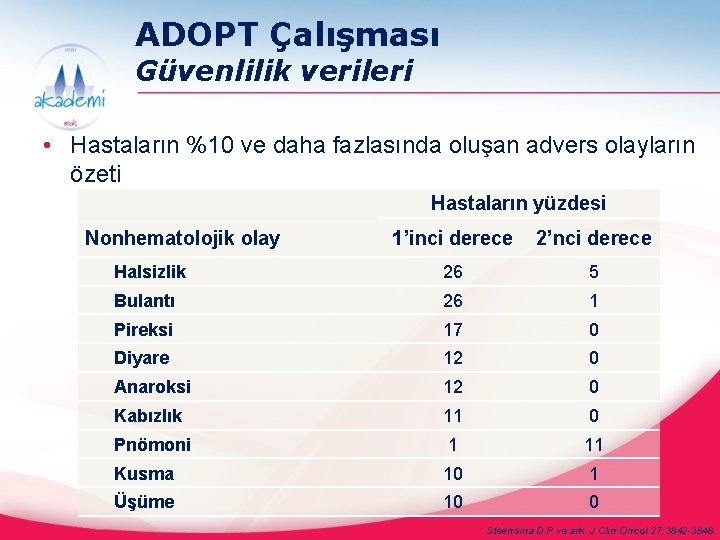
ADOPT Çalışması Güvenlilik verileri • Hastaların %10 ve daha fazlasında oluşan advers olayların özeti Hastaların yüzdesi Nonhematolojik olay 1’inci derece 2’nci derece Halsizlik 26 5 Bulantı 26 1 Pireksi 17 0 Diyare 12 0 Anaroksi 12 0 Kabızlık 11 0 Pnömoni 1 11 Kusma 10 1 Üşüme 10 0 Steensma D. P ve ark. J Clin Oncol 27: 3842 -3848.

Üç Kollu Desitabin Çalışması • Desitabin tedavi kolları o 1 saat boyunca günde 10 mg/m 2 IV x 10 o 1 saat boyunca günde 20 mg/m 2 IV x 5 o Günde 20 mg/m 2 SC (10 mg SC BID) x 5 Kantarjian Blood 109: 52, 2007

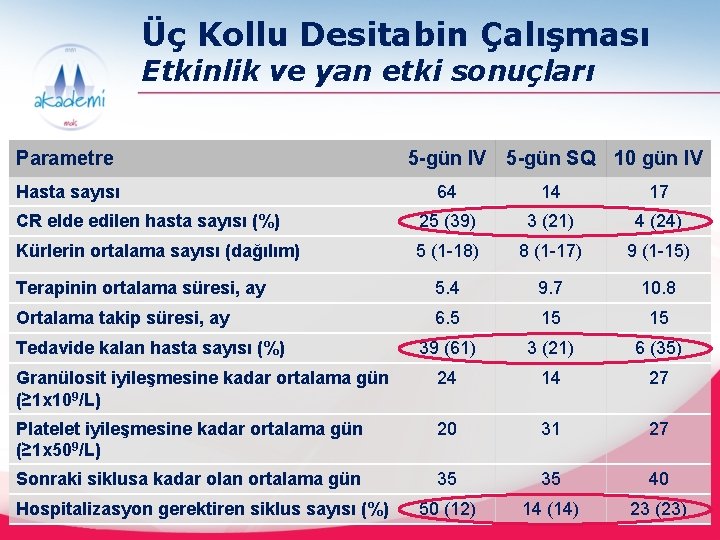
Üç Kollu Desitabin Çalışması Etkinlik ve yan etki sonuçları Parametre Hasta sayısı 5 -gün IV 5 -gün SQ 10 gün IV 64 14 17 CR elde edilen hasta sayısı (%) 25 (39) 3 (21) 4 (24) Kürlerin ortalama sayısı (dağılım) 5 (1 -18) 8 (1 -17) 9 (1 -15) Terapinin ortalama süresi, ay 5. 4 9. 7 10. 8 Ortalama takip süresi, ay 6. 5 15 15 39 (61) 3 (21) 6 (35) Granülosit iyileşmesine kadar ortalama gün (≥ 1 x 109/L) 24 14 27 Platelet iyileşmesine kadar ortalama gün (≥ 1 x 509/L) 20 31 27 Sonraki siklusa kadar olan ortalama gün 35 35 40 50 (12) 14 (14) 23 (23) Tedavide kalan hasta sayısı (%) Hospitalizasyon gerektiren siklus sayısı (%)

MDS'de Desitabin Yoğun kemoterapiyle karşılaştırma

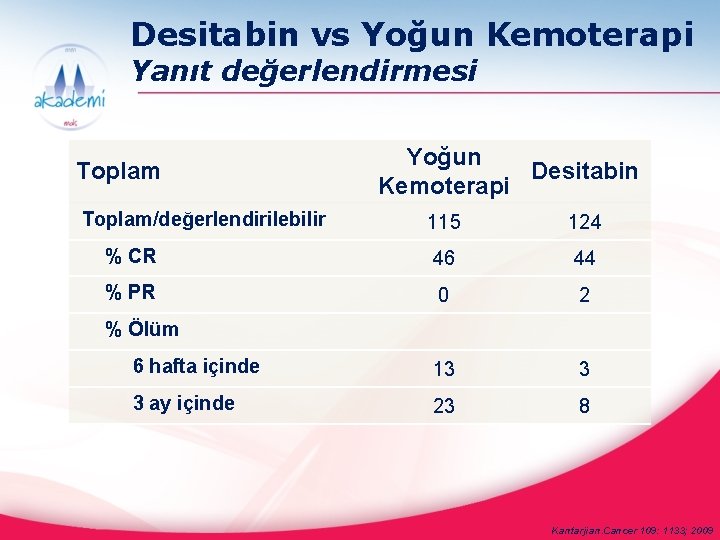
Desitabin vs Yoğun Kemoterapi Yanıt değerlendirmesi Toplam/değerlendirilebilir Yoğun Desitabin Kemoterapi 115 124 % CR 46 44 % PR 0 2 6 hafta içinde 13 3 3 ay içinde 23 8 % Ölüm Kantarjian. Cancer 109: 1133; 2009

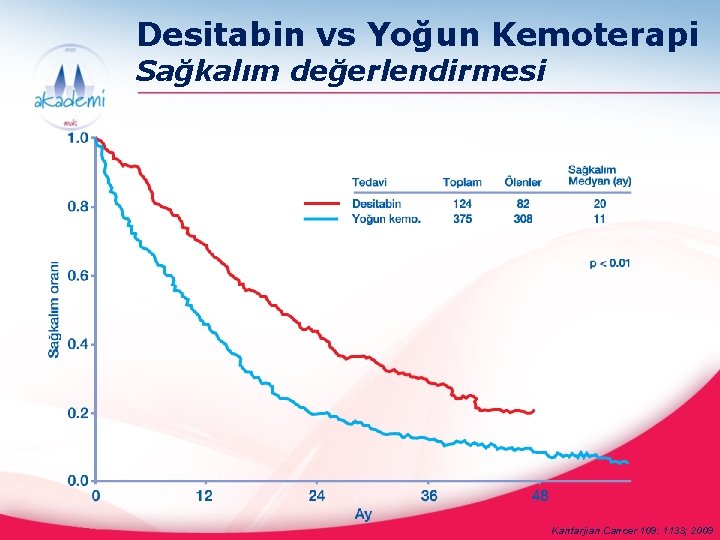
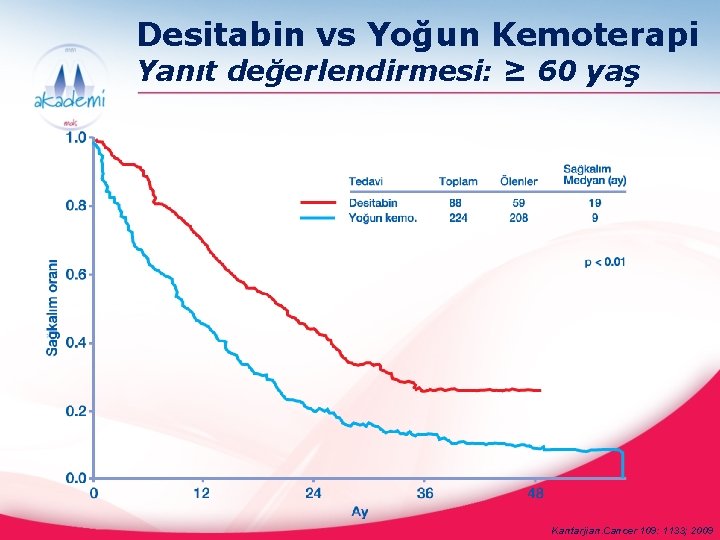
Desitabin vs Yoğun Kemoterapi Sağkalım değerlendirmesi Kantarjian. Cancer 109: 1133; 2009

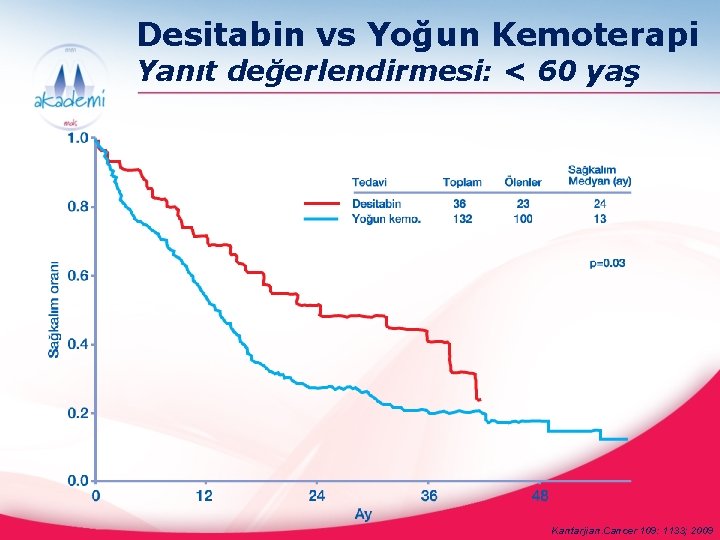
Desitabin vs Yoğun Kemoterapi Yanıt değerlendirmesi: < 60 yaş Kantarjian. Cancer 109: 1133; 2009

Desitabin vs Yoğun Kemoterapi Yanıt değerlendirmesi: ≥ 60 yaş Kantarjian. Cancer 109: 1133; 2009

Myelodisplastik Sendrom Yoğun Kemoterapi ve Transplantasyon


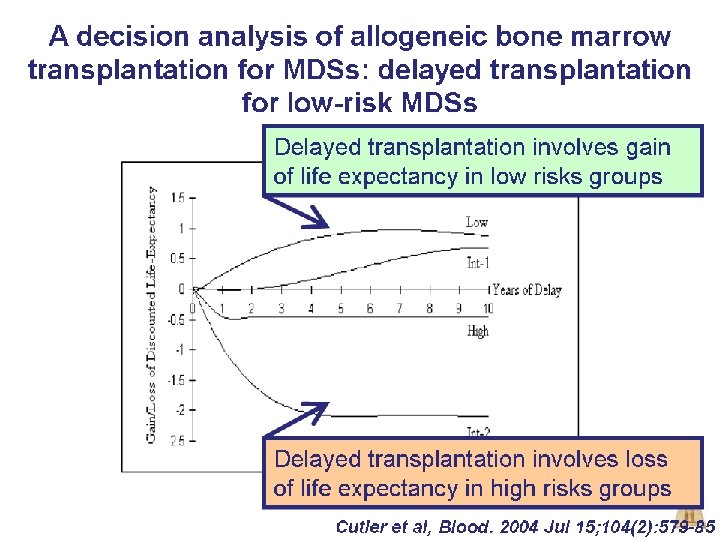
MDS için Allojeneik KHT 1. Orta-2, yüksek risk hastalar: hemen transplantasyon 2. Orta-1, düşük risk o Progresyon olunca transplantasyon o Progresyon tanımı: • Klinik olarak önemli sitopeni • % ilik blastlarda artış • Yeni kromozomal anormallik

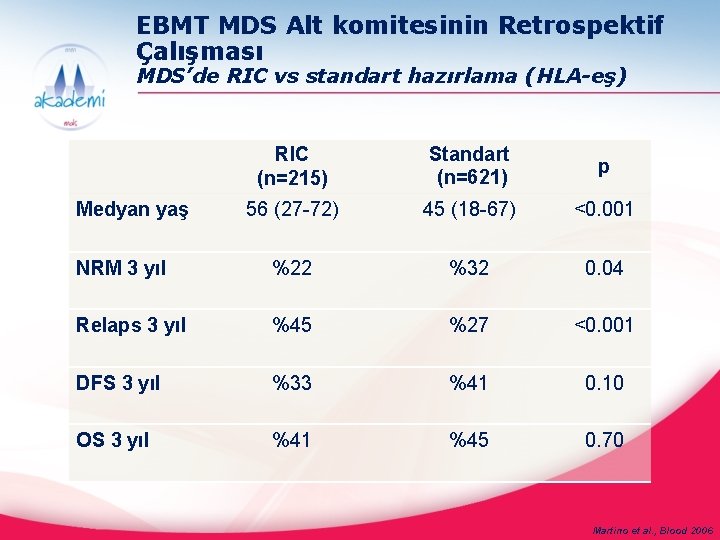
EBMT MDS Alt komitesinin Retrospektif Çalışması MDS’de RIC vs standart hazırlama (HLA-eş) RIC (n=215) Standart (n=621) p 56 (27 -72) 45 (18 -67) <0. 001 NRM 3 yıl %22 %32 0. 04 Relaps 3 yıl %45 %27 <0. 001 DFS 3 yıl %33 %41 0. 10 OS 3 yıl %41 %45 0. 70 Medyan yaş Martino et al. , Blood 2006

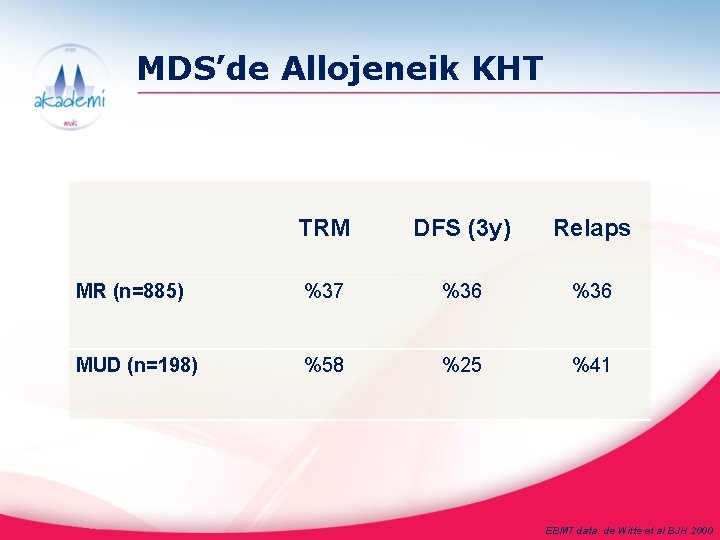
MDS’de Allojeneik KHT TRM DFS (3 y) Relaps MR (n=885) %37 %36 MUD (n=198) %58 %25 %41 EBMT data: de Witte et al BJH 2000

Yeni arayışlar • • • Zebularine Vorinostat Depsipeptid(Romidepsin) Etinostat Panobinostat DMTIs + Talidomid DMTIs + Lenalidomid DMTIs + Bortezomib DMTIs + Gemtuzumab ozogamisin

Endikasyon • Vidaza ve Dacogen, o RAEB-1 ve RAEB-2 tedavisinde o Diğer MDS alt tiplerinde eşlik eden sitogenetik kötü risk, ağır dishematopoez, yoğun enfeksiyonlarla seyreden lökopeni, klinik kanamalara neden olabilecek trombositopeni ve transfüzyonlarla düzeltilemeyen derin refrakter anemi hallerinde ENDİKEDİR

6. 2. 14. C- Özel düzenleme yapılan ilaçlar; (Değişik: 01/03/2011 -27861/9 md. Yürürlük: 11/03/2011) h) Azasitidin ve Decitabin; A. Miyelodisplastik Sendromda (MDS) görülen dirençli anemi tedavisinde; 1 - Kemik iliği blast oranının %5 in üzerinde artmış olduğunun belirtildiği, içinde en az bir hematoloji uzmanının bulunduğu 4 ay süre ile geçerli sağlık kurulu raporu ile 18 yaş üstü hastalarda kullanılmak üzere hematoloji uzmanı tarafından en fazla birer (1 er) aylık tedavi miktarında reçete edilebilir.

6. 2. 14. C- Özel düzenleme yapılan ilaçlar; 2 - Azasitidin veya Decitabini 4 ay alan hastalarda yanıt değerlendirilmesi yapılır. Blast oranı %5 ve altına inen hastalar ile tedaviye başlandığındaki ilk değerine göre blast oranında %50 den daha az azalma olan hastalarda tedavi kesilir. Blast oranı tedaviye başlandığındaki ilk değerine göre %50 ve daha fazla azalan (ancak Blast oranı %5 in üstünde kalan) hastalarda bu durumu belirten yeni bir rapor düzenlenerek yalnızca 3 ay daha tedaviye devam edilir. Relaps olan hastalarda başlama kriterlerine uygun olarak tedaviye tekrar başlanabilir.

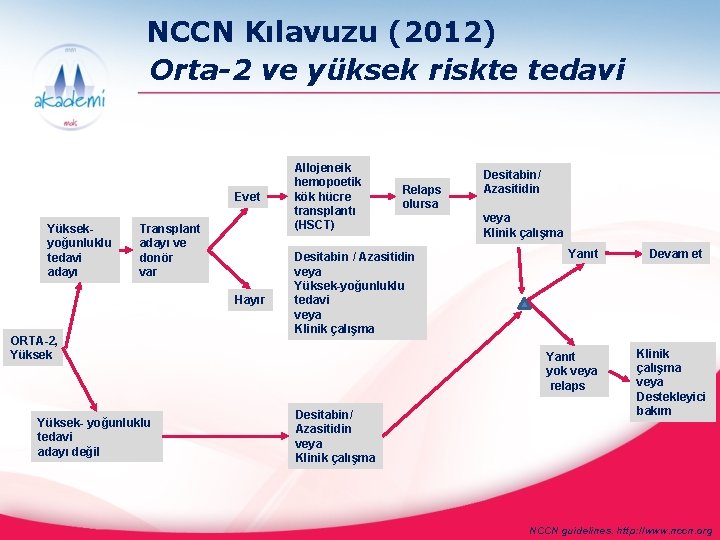
NCCN Kılavuzu (2012) Orta-2 ve yüksek riskte tedavi Evet Yüksekyoğunluklu tedavi adayı Transplant adayı ve donör var Hayır ORTA-2, Yüksek- yoğunluklu tedavi adayı değil Allojeneik hemopoetik kök hücre transplantı (HSCT) Relaps olursa Desitabin / Azasitidin veya Yüksek-yoğunluklu tedavi veya Klinik çalışma Desitabin/ Azasitidin veya Klinik çalışma Yanıt yok veya relaps Desitabin/ Azasitidin veya Klinik çalışma Devam et Klinik çalışma veya Destekleyici bakım NCCN guidelines. http: //www. nccn. org
