Mycoplasmas y Ureaplasmas El orden Mycoplasmatales se subdivide

Mycoplasmas y Ureaplasmas

El orden Mycoplasmatales se subdivide en cuatro géneros: Eperythrozoon, Haemobartonella, Mycoplasma Ureaplasma.

Los géneros con mayor signifiación clínica son Mycoplasma (125 especies) y Ureaplasma (7 especies), y la especie más importante es Mycoplasma pneumoniae (llamado también agente de Eaton por el investigador que lo aisló por primera vez). M. pneumoniae causa enfermedades del aparato respiratorio, como la traqueobronquitis y la neumonía (cuadro 40 -1 ). Otros patógenos que se aíslan con frecuencia son Mycoplasma genitalium, Mycoplasma hominis y Ureaplasma urealyticum

FISIOLOGIA Y ESTRUCTURA Son las bacterias más pequeñas de vida libre. Son peculiares debido a la ausencia de pared celular y a la presencia de esteroles en su membrana celular. Su ausencia le confiere resistencia a los micoplasmas frente a las penicilinas, las cefalosporinas, la vancomicina y otros antibióticos que interfieren en la síntesis de la pared celular. Los micoplasmas adoptan formas pleomorfas, que van desde cocos de 0, 2 -0, 3 mm hasta bacilos de 0, 1 -0, 2 mm de ancho y 1 -2 mm de longitud. Estos microorganismos se dividen por fisión binaria (típico de todas las bacterias), crecen en medios artificiales acelulares y contienen tanto ácido ribonucleico (ARN) como ácido desoxirribonucleico (ADN). Los micoplasmas son anaerobios facultativos (excepto M. pneumoniae, que es un aerobio estricto) y necesitan esteroles exógenos que les proporciona el suero animal que se añade al medio de crecimiento. Los micoplasmas crecen lentamente, con un tiempo de generación de 1 a 6 horas, y la mayoría forma colonias pequeñas que resultan difíciles de detectar sin una incubación prolongada. Debido a la ausencia de pared celular en Mycoplasmatales, los principales determinantes antigénicos son los glucolípidos y las proteínas de membrana. Estos antígenos tienen reactividad cruzada con los tejidos del ser humano y con otras bacterias.
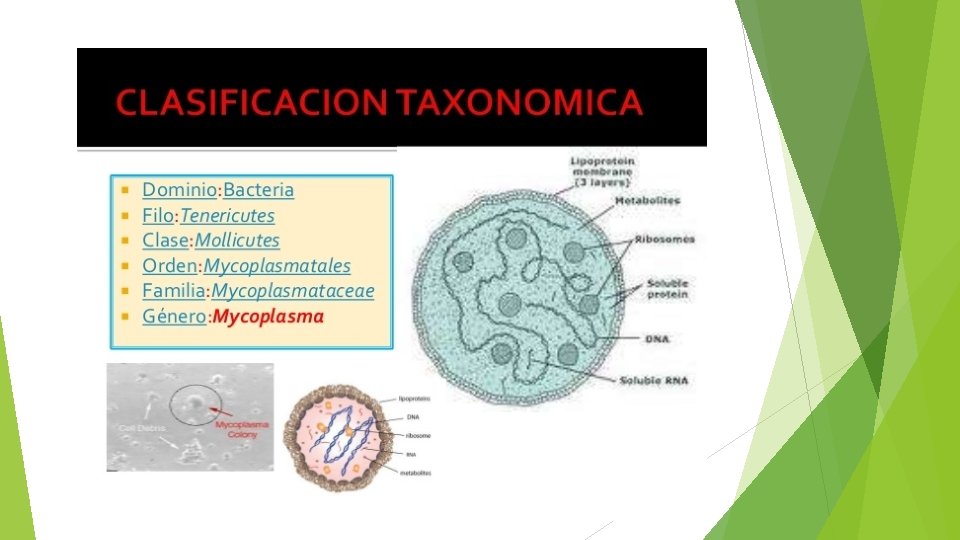

morfologia Pleomorficos. No poseen pared celular. Tienen triple menbrana con pared celular con: Aerobios. Anaerobios facultativos. Glucosa positivos. Proteinas. Temperatura de crecimiento 37 c Lipidos. PH 7. 6 a 8. 0. Colesterol. Citoplasma con abundantes granulos de acido ribonucleico. Requieren lipidos y colesterol. Membrana con redes de acido ribonucleicos. Reduccion lenta de azul de metileno. Reducen el tetrazolio. Movilidad deslizante. Tienen ligera producion de: Tincion con giencia. GRAM negativos acido sulfidrico. Hemolisis beta o alfa.

Patogenia e Inmunidad M. pneumoniae es un patógeno extracelular que se adhiere al epitelio respiratorio mediante una estructura de anclaje especializada, que se forma en un extremo de la célula. Esta estructura está constituida por un complejo de proteínas para adherencia, en la que destaca la adhesina P 1 como la más importante. Las adhesinas interactúan de manera específica con los receptores de glucoproteínas sialidadas en la base de los cilios de la superficie de las células epiteliales (así como en la superficie de los eritrocitos). A continuación tiene lugar la ciliostasis, tras la que son destruidos en primer lugar los cilios y posteriormente las células del epitelio ciliar. La pérdida de estas células interfiere en el aclaramiento normal de las vías respiratorias superiores y permite que las vías respiratorias inferiores se contaminen con microorganismos y sufran una irritación mecánica. Este proceso es el responsable de la tos persistente que tienen los pacientes con enfermedad sintomática. M. pneumoniae funciona como un superantígeno y estimula la migración de las células inflamatorias al lugar de la infección y la liberación de citosinas por las mismas, inicialmente factor de necrosis tumoral a e interleucina 1 (IL-1) y posteriormente IL-6. Este proceso participa tanto en la eliminación de las bacterias como en la enfermedad. Varias especies de Mycoplasma son capaces de cambiar rápidamente la expresión de las lipoproteínas de superficie, lo que probablemente tenga importancia para evadir la respuesta inmunitaria del hospedador y establecer infecciones persistentes o crónicas.

EPIDEMIOLOGIA M. pneumoniae es un patógeno humano estricto. La enfermedad respiratoria (es decir, traqueobronquitis, neumonía) producida por M. pneumoniae tiene una distribución universal durante todo el año, sin que exista ningún aumento de la actividad de carácter estacional. Sin embargo, puesto que la neumonía causada por otros agentes infecciosos (p. ej. , Streptococcus pneumoniae, virus) es más frecuente durante los meses de invierno, la enfermedad por M. pneumoniae es proporcionalmente más frecuente en verano y en otoño. La enfermedad epidémica se produce cada 4 -8 años. La enfermedad es más frecuente en los niños en edad escolar y en los adultos jóvenes (de 5 a 15 años), aunque todos los grupos de edad son susceptibles.

M. pneumoniae coloniza la nariz, la garganta, la tráquea y las vías aéreas inferiores de los sujetos infectados y se disemina a través de las gotículas respiratorias más grandes durante los episodios de tos. La infección se suele diseminar entre compañeros de clase, familiares o contactos estrechos. La tasa de ataque es mayor en niños que en adultos (media global, alrededor del 60%), probablemente debido a que la mayoría de los adultos disfruta de una inmunidad parcial como consecuencia de una exposición previa. El período de incubación y el tiempo de infectividad son prolongados; por tanto, la enfermedad puede persistir durante meses. Los niños, especialmente las niñas, están colonizados cuando nacen por M. hominis, M. genitalium y especies del género Ureaplasma, aunque son estas últimas las que se aíslan con una frecuencia mayor. Aunque el estado de portador de estos micoplasmas no suele ser persistente, una pequeña población de niños prepúberes está colonizada. La incidencia de micoplasmas genitales aumenta después de la pubertad, lo que se corresponde con la actividad sexual. Alrededor del 15% de los hombres y de las mujeres sexualmente activos están colonizados por M. hominis, mientras que una proporción comprendida entre el 45% y el 75% lo está por Ureaplasma. La incidencia del estado de portador en adultos que son sexualmente inactivos no supera a la de los niños en la etapa prepuberal. M. pneumoniae no forma parte de la microbiota normal de las mucosas en humanos; sin embargo, se describen portadores prolongados tras la enfermedad sintomática.
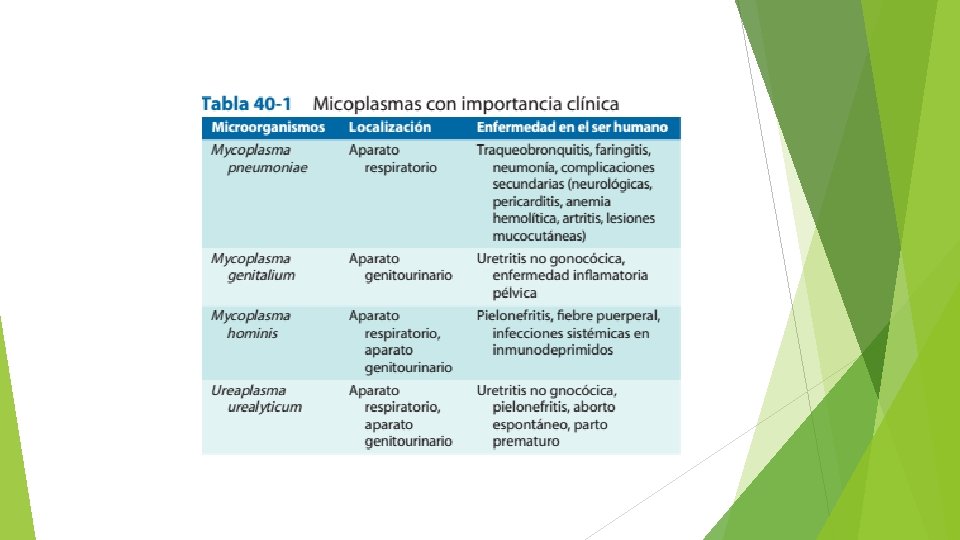

ENFERMEDADES CLINICAS La exposición a M. pneumoniae produce típicamente un estado de portador asintomático. La presentación clínica más frecuente de la infección por M. pneumoniae es la traqueobronquitis. A las 2 -3 semanas de la exposición aparece febrícula, malestar, cefalea y tos seca sin expectoración. faringitis aguda. neumonía atípica primaria o neumonía «ambulatoria» ), en la que se observa una neumonía parcheada en las radiografías de tórax que característicamente es más llamativa de lo que lo son los hallazgos físicos. Las mialgias y los síntomas digestivos son infrecuentes. Las complicaciones secundarias incluyen alteraciones neurológicas (p. ej. , meningoencefalitis, parálisis y mielitis), pericarditis, anemia hemolítica, artritis y lesiones mucocutáneas. Como la vía genitourinaria se coloniza por otras especies de Mycoplasma y Ureaplasma, resulta difícil determinar la implicación de estos microorganismos en un paciente concreto. Sin embargo, se acepta en general que M. genitalium produce uretritis no gonocócica (UNG) y enfermedad inflmatoria pélvica; U. urealyticum puede ocasionar UNG, pielonefritis y abortos espontáneos o partos prematuros, y M. hominis puede ser causa de pielonefritis, fiebres puerperales e infecciones sistémicas en inmunodeprimidos. Los indicios que relacionan estos microorganismos con estas enfermedades se basan en 1) el aislamiento de las bacterias de las muestras de los pacientes infectados, 2) una respuesta serológica frente al microorganismo, 3) la mejoría clínica después del tratamiento con los antibióticos específicos, 4) la demostración de la enfermedad en un modelo animal o 5) una combinación de estos hallazgos.
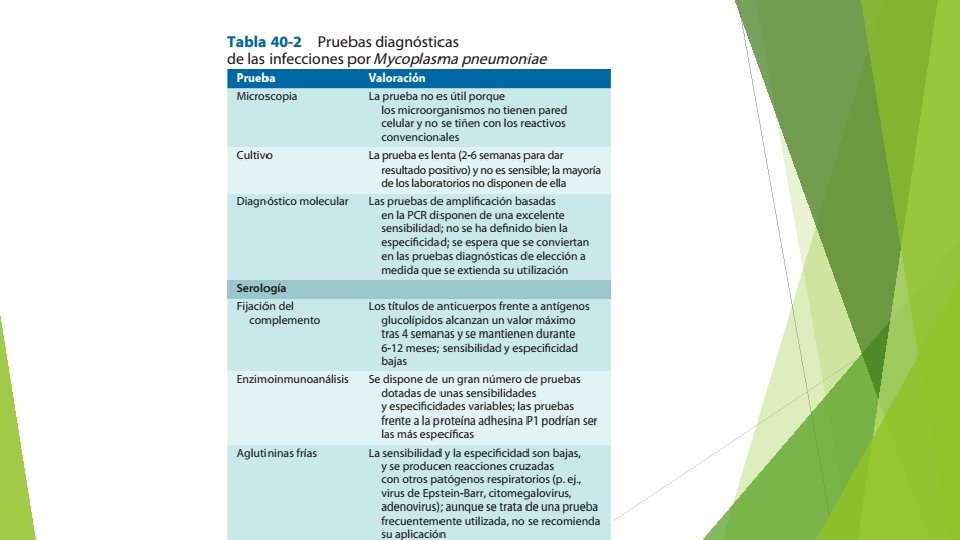
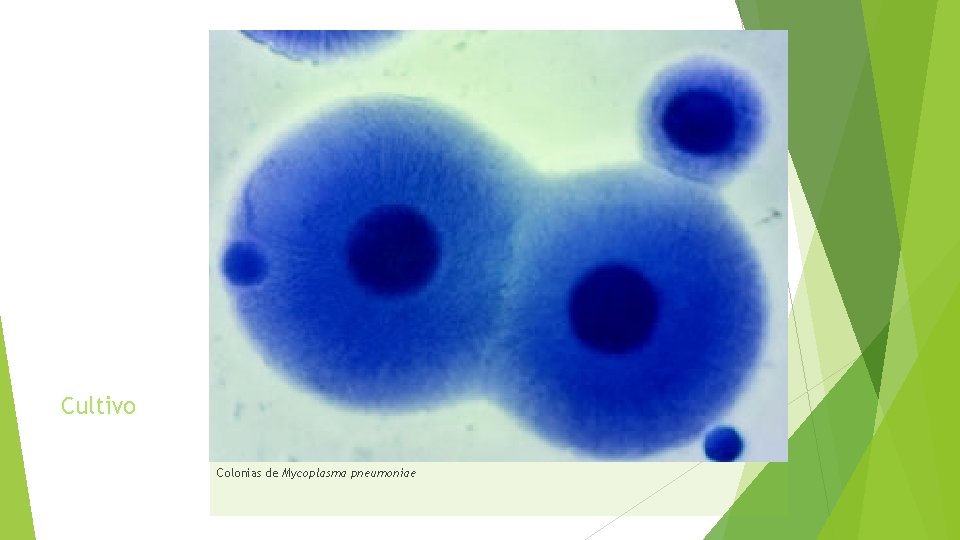
Cultivo Colonias de Mycoplasma pneumoniae

Tratamiento y prevención La eritromicina , las tetraciclinas (especialmente la doxiciclina) y las floroquinolonas más modernas son igual de eficaces para tratar las infecciones por M. pneumoniae, aunque las tetraciclinas y las floroquinolonas se reservan para los adultos. Las tetraciclinas tienen la ventaja de ser eficaces frente a la mayoría de los otros micoplasmas y clamidias, una causa frecuente de UNG. La eritromicina y las tetraciclinas se usan para tratar las infecciones por Ureaplasma. Al contrario que otros micoplasmas, M. hominis es resistente a la eritromicina y algunas veces a las tetraciclinas. Se ha usado la clindamicina para tratar las infecciones producidas por estas cepas resistentes.

La prevención de la enfermedad por Mycoplasma es problemática. Las infecciones por M. pneumoniae se propagan por contacto estrecho; por tanto, el aislamiento de las personas infectadas teóricamente reduciría el riesgo de infección. Sin embargo, el aislamiento es impracticable, puesto que los pacientes suelen ser infecciosos durante un período de tiempo prolongado, incluso mientras están recibiendo antibióticos. Tanto las vacunas inactivadas como las vivas atenuadas han presentado malos resultados. La inmunidad protectora que confiere esta infección es baja. Las infecciones por M. hominis, M. genitalium y Ureaplasma se transmiten por contacto sexual. Por tanto, estas enfermedades se pueden prevenir evitando los contactos sexuales sin protección.
UREAPLASMA UREALYRICUM • Filamentoso. • Carecen de pared celular. • Anaerobios facultativos. • Para su crecimiento en cultivos requieren de medios especiales con: • Urea. • Esteroles.

patogenia La ausencia de una pared celular permite adherencia estrecha entre el micoplasma y la celula hospedera. Se encuentra en la mucosas genitales. En la mucosa produce lisis celular.
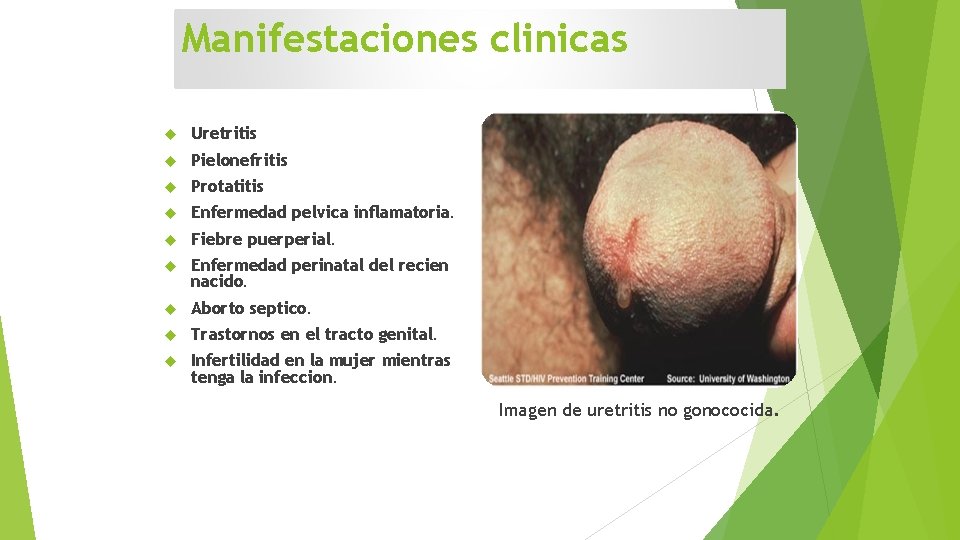
Manifestaciones clinicas Uretritis Pielonefritis Protatitis Enfermedad pelvica inflamatoria. Fiebre puerperial. Enfermedad perinatal del recien nacido. Aborto septico. Trastornos en el tracto genital. Infertilidad en la mujer mientras tenga la infeccion. Imagen de uretritis no gonococida.

diagnostico Secreciones de la vias genitales. Raspado de la via genital. Medio de cultivo con urea. Resiembra a corto plazo Condiccional un buffer para mantener el PH. Serologico: Elisa.

tratamiento Macrolidos. Eritromicinas. Miocamicina. Clindamicina. Roxitromicina. Azitromicina.

Chlamydia y Chlamydophila La familia Chlamydiaceae incluye dos géneros con importancia clínica, Chlamydia y Chlamydophila, con tres especies responsables de enfermedad en el ser humano: Chlamydia trachomatis, Chlamydophila psittaci y Chlamydophila pneumoniae. Otras especies se han incluido dentro de estos dos géneros, pero son patógenos humanos poco frecuentes. Las bacterias de la familia Chlamydiaceae son parásitos intracelulares obligatorios, estos microorganismos tienen las siguientes características de las bacterias: 1) poseen una membrana interna y otra externa semejantes a las de las bacterias gramnegativas; 2) contienen ácido desoxirribonucleico (ADN) y ácido ribonucleico (ARN); 3) poseen ribosomas procariotas; 4) sintetizan sus propias proteínas, ácidos nucleicos y lípidos, 5) son sensibles a numerosos antibióticos antibacterianos. Al contrario de lo que ocurre con otras bacterias, las clamidias presentan un ciclo vital peculiar, ya que pasan por formas infecciosas inactivas desde el punto de vista metabólico (cuerpos elementales [CE]) y por formas no infecciosas con actividad metabólica (cuerpos reticulados [CR]).


Fisiología y estructura De un modo parecido a una espora, los CE son resistentes a muchos factores ambientales estresantes. Aunque estas bacterias no cuentan con la capa de peptidoglucanos rígida que existe en la mayor parte de las restantes bacterias, su núcleo denso central se rodea de una membrana citoplasmática y de una membrana externa de doble capa. La pared celular contiene un lipopolisacárido (LPS) que es común a todos los miembros de la familia. El LPS sólo tiene una actividad débil como endotoxina. La proteína principal de la membrana externa (MOMP) de la pared celular es un componente estructural importante de la membrana externa y es única de cada especie.

Una segunda proteína de membrana externa muy conservada, OMP 2, es compartida por todos los miembros de la familia Chlamydiaceae. Esta proteína rica en cisteína es responsable de los extensos puentes disulfuro que dan estabilidad a los CE. Los CE no se pueden replicar, pero son infecciosos, de forma que se pueden ligar a receptores en las células hospedadoras y estimular su captación por la célula infectada. En esta localización intracelular, los CE se convierten en CR, la forma de clamidia con actividad metabólica que se replica. Dado que en los cuerpos reticulares no existen proteínas con extensos enlaces cruzados, esta forma resulta frágil a nivel osmótico; sin embargo, se protegen por su localización intracelular.

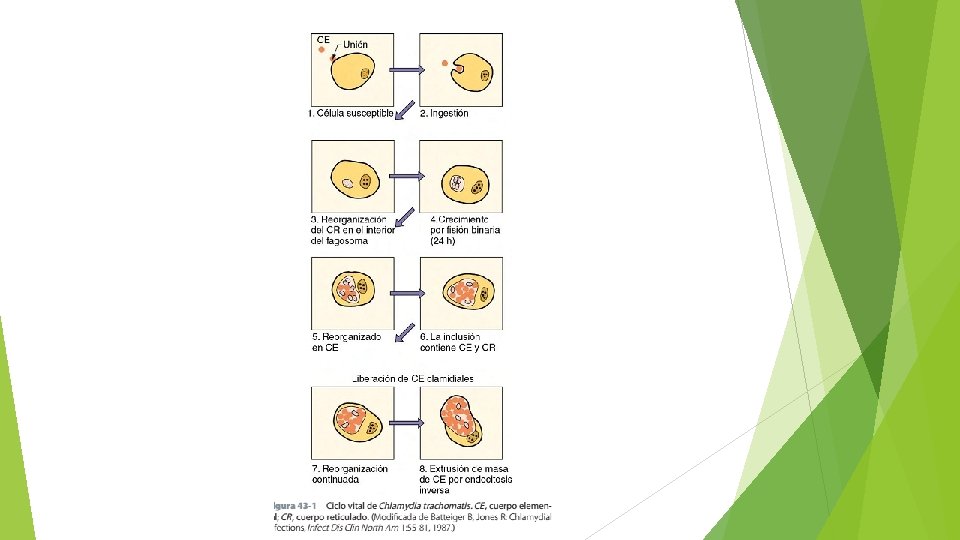
Las Chlamydiaceae se replican gracias a un ciclo de crecimiento único que se produce dentro de las células hospedadoras susceptibles. Este ciclo se inicia cuando los CE infecciosos pequeños (300 -400 nm) se unen a las microvellosidades de las células susceptibles, tras lo cual se produce una penetración activa en la célula hospedadora.

Tras ser internalizadas, las bacterias permanecen dentro de los fagosomas citoplasmáticos, en los que tiene lugar el ciclo de replicación. Si la membrana externa del CE está intacta, se inhibirá la fusión de los lisosomas celulares con los fagosomas que contienen los CE, lo que evitará la destrucción intracelular. Si la membrana externa se lesiona o se inactivan las bacterias mediante calor o recubrimiento por anticuerpos, se produce la fusión del fagolisosoma con la consiguiente destrucción de las bacterias.

A las 6 -8 horas de entrar en la célula, los cuerpos elementales se reorganizan en CR más grandes (800 -1. 000 nm) y con actividad metabólica. Las Chlamydiaceae son parásitos de energía porque emplean la adenosina trifosfato de la célula hospedadora para satisfacer sus necesidades energéticas. Algunas cepas pueden depender también del hospedador para que les aporten aminoácidos específicos. Los CR se replican mediante fisión binaria, igual que otras bacterias, y las tinciones histológicas pueden detectar con facilidad el fagosoma con los CR acumulados, que se llaman inclusión. Unas 18 -24 horas después de la infección, los CR se empiezan a reorganizar en CE de menor tamaño y entre 48 y 72 horas después la célula se rompe y libera las bacterias infecciosas.

Chlamydia trachomatis C. trachomatis tiene una serie de hospedadores limitados y las infecciones sólo se producen en personas. Las especies responsables de enfermedad humana se subdividen en dos biovariedades: tracoma y linfogranuloma venéreo (LGV). Estas biovariedades se dividen a su vez en serovariedades según las diferencias antigénicas en la proteína principal de la membrana externa (MOMP). Las serovariedades específicas se asocian con enfermedades específicas.

Enfermedades causadas por C. Trachomatis Tiene 3 categorias de enfermedades en el hombre causadas por este tipo de bacteria: Tracomona. Enfermedad transmitida en forma directa(contacto sexual. ) e indirectamente. Linfogranuloma Venereo. La capacidad de una sola specie para causar tal variedad de enfermedades surge de las diferentes varaciones leves en virulencia o en la afinidad de los tejidos del huesped por los serotipos diferentes de este micorbio

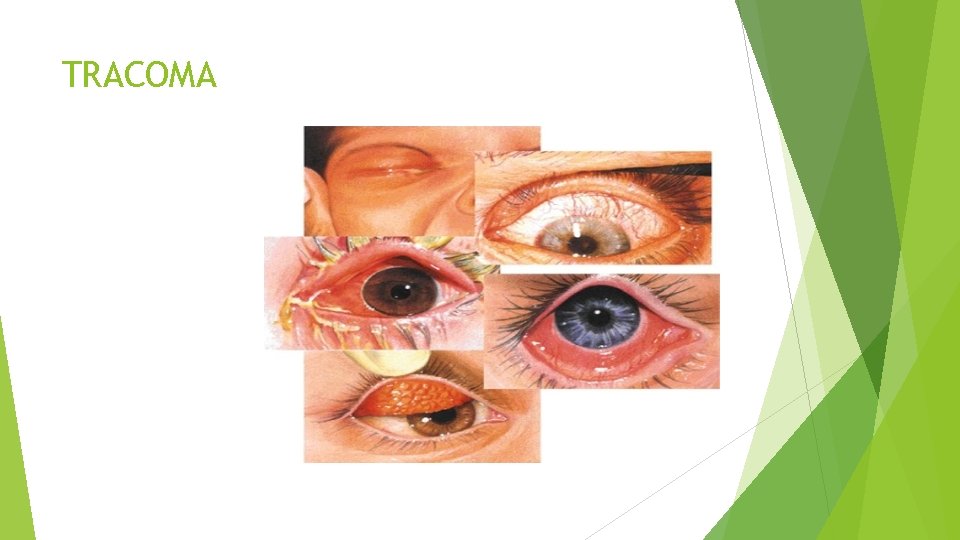
TRACOMA

TRACOMA El tracoma es una enfermedad crónica producida por las serovariedades A, B, Ba y C. Inicialmente, los pacientes tienen una conjuntivitis folicular con inflamación difusa que afecta a toda la conjuntiva. La conjuntiva va presentando cicatrices conforme progresa la enfermedad, haciendo que el párpado del paciente se retraiga. Las pestañas que crecen hacia dentro producen excoriaciones en la córnea y finalmente ocasionan una ulceración corneal, cicatrización, formación de pannus (invasión de los vasos de la córnea) y pérdida de visión. Es frecuente que el tracoma recurra después de una supuesta curación, probablemente debido a las infecciones subclínicas que se han documentado en los niños de las zonas endémicas y en los inmigrantes en EE. UU. que adquirieron el tracoma en sus países de origen durante la infancia.

Conjuntivitis de inclusión en los adultos En los adultos sexualmente activos se ha observado una conjuntivitis aguda folicular producida por las cepas de C. trachomatis que se asocian a las infecciones genitales (A, B, Ba, D a K). La infección se caracteriza por la presencia de secreciones mucopurulentas, queratitis, infitrados corneales y, en algunos casos, un cierto grado de vascularización corneal. Se han observado cicatrices en los pacientes con infección crónica.

Conjuntivitis neonatal Las infecciones oculares se producen también en los niños expuestos a C. trachomatis durante el parto. Después de una incubación de 5 a 12 días, los párpados del niño se hinchan, con hiperemia y abundantes secreciones purulentas. Las infecciones no tratadas pueden durar hasta 12 meses, durante los cuales se produce cicatrización y vascularización corneal. Los niños que no se tratan o reciben únicamente un tratamiento tópico tienen riesgo de presentar una neumonía por C. trachomatis. Neumonía del lactante El período de incubación de la neumonía del lactante es variable, pero suele comenzar entre 2 y 3 semanas después del nacimiento. Inicialmente se observa rinitis, y después aparece una tos en staccato típica. El niño permanece afebril durante la enfermedad clínica, la cual se prolonga varias semanas. Los signos radiológicos de la infección pueden durar varios meses.

Linfogranulona Venereo Las serovariedades del LGV de C. trachomatis se han visto implicadas en la conjuntivitis oculoglandular de Parinaud, una inflamación de la conjuntiva que se asocia a linfadenopatías preauriculares, submandibulares y cervicales

Infecciones urogenitales La mayoría de las infecciones del aparato genital en las mujeres son asintomáticas (hasta el 80%), pero se pueden volver sintomáticas; entre sus manifestaciones clínicas están la bartolinitis, la cervicitis, la endometritis, la perihepatitis, la salpingitis y la uretritis. Los pacientes asintomáticos infectados por clamidias son un importante reservorio para la diseminación de C. trachomatis. En los pacientes con infecciones sintomáticas se ven secreciones mucopurulentas y sus muestras suelen contener un número más elevado de microorganismos en los cultivos que las muestras de las pacientes con infecciones asintomáticas. La uretritis por C. trachomatis puede tener lugar con o sin infección cervical acompañante. La mayor parte de las infecciones por C. trachomatis en los hombres son sintomáticas; sin embargo, hasta el 25% de las infecciones pueden permanecer asintomáticas. Aproximadamente entre el 35% y el 50% de los casos de uretritis no gonocócicas están producidas por C. trachomatis; no son infrecuentes las infecciones mixtas por C. trachomatis y Neisseria gonorrhoeae. Los síntomas de la infección por clamidias aparecen después del tratamiento satisfactorio de la gonorrea, ya que el período de incubación es más largo y el uso de antibióticos b-lactámicos para tratar la gonorrea es ineficaz frente a C. trachomatis. Aunque el exudado es menos purulento en los pacientes con infecciones uretrales por clamidias, estas infecciones no se pueden distinguir de una manera fiable de la gonorrea, por lo que se deben llevar a cabo pruebas para ambos microorganismos.

Se cree que el síndrome de Reiter (uretritis, conjuntivitis, poliartritis y lesiones mucocutáneas) se inicia con la infección genital por C. trachomatis. Aunque no se han aislado clamidias del líquido sinovial de estos pacientes, se han observado CE en el líquido sinovial o en las muestras de tejido de los hombres con artritis reactiva adquirida por transmisión sexual. Esta enfermedad suele ocurrir en varones blancos jóvenes. Alrededor del 50% al 65% de los pacientes con síndrome de Reiter tienen una infección genital por clamidias al inicio de la artritis, y los estudios serológicos ponen de manifisto que más del 80% de los hombres con síndrome de Reiter muestran indicios de una infección previa o concomitante por C. trachomatis.

Linfogranuloma venéreo Tras un período de incubación de 1 a 4 semanas, en los pacientes con LGV aparece una lesión inicial en el lugar de la infección (p. ej. , pene, uretra, glande, escroto, pared vaginal, cérvix, vulva). Sin embargo, la lesión (pápula o úlcera) pasa inadvertida, porque es pequeña, indolora, no llama la atención y remite rápidamente. La ausencia de dolor diferencia a estas úlceras de las que se observan en la sífilis o las infecciones por herpes simple. El paciente puede presentar fiebre, cefalea y mialgias mientras está presente la lesión. La segunda fase de la infección viene marcada por la inflamación y la tumefacción de los ganglios linfáticos que drenan el lugar de la infección inicial. Los ganglios inguinales suelen estar afectados, y se tornan bubones fluctuantes dolorosos que van aumentando de tamaño hasta romperse y formar fístulas de drenaje. Las manifestaciones sistémicas son fiebre, escalofríos, anorexia, cefalea, meningismo, mialgias y artralgias. La proctitis es frecuente en las mujeres con LGV como consecuencia de la extensión linfática desde el cérvix o desde la vagina. La proctitis se produce en los hombres después del coito anal o como resultado de la diseminación linfática desde la uretra. El LGV que no se trata se puede resolver en esta fase o puede progresar a una fase crónica ulcerativa en la que se forman úlceras genitales, fístulas, estenosis o elefantiasis genital.

Diagnóstico de laboratorio La infección por C. trachomatis se puede diagnosticar 1) por los hallazgos citológicos, serológicos o de cultivo; 2) mediante la detección directa del antígeno en las muestras clínicas, y 3) por el uso de pruebas de ácidos nucleicos. las infecciones sintomáticas son generalmente más fáciles de diagnosticar que las asintomáticas, porque hay más clamidias presentes en las muestras. También es importante la calidad de la muestra. No es adecuada una muestra de pus o de exudado uretral, en donde puede haber un número relativamente escaso de microorganismos. Las clamidias infectan las células del epitelio columnar o escamosocolumnar; por tanto, se deben recoger muestras endocervicales, pero no vaginales. Se ha calculado que alrededor de un tercio de las muestras que se remiten para su estudio en los pacientes con sospecha de infección por Chlamydia no son las apropiadas.
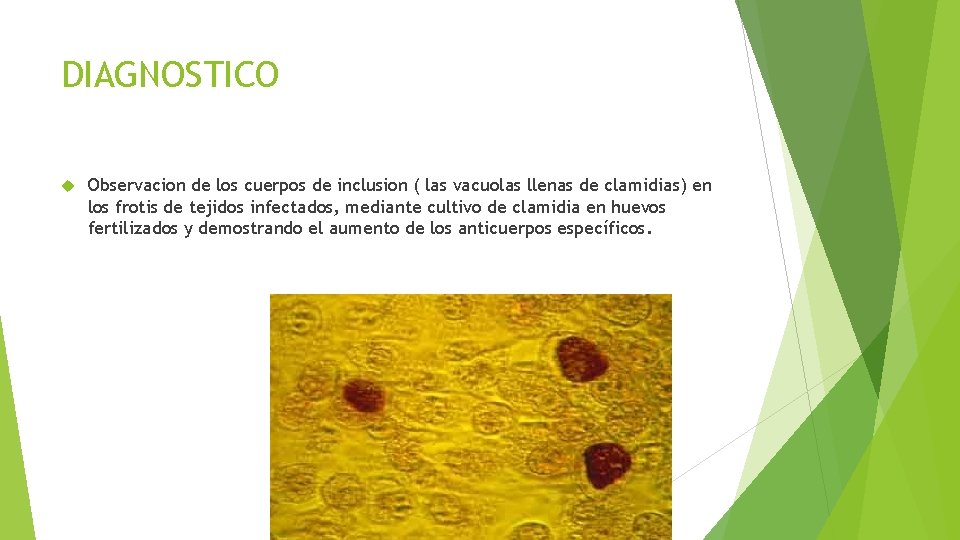
DIAGNOSTICO Observacion de los cuerpos de inclusion ( las vacuolas llenas de clamidias) en los frotis de tejidos infectados, mediante cultivo de clamidia en huevos fertilizados y demostrando el aumento de los anticuerpos específicos.

TRATAMIENTO Sulfonamidas Tetraciclinas Rifampicina

Resumen de Chlamydia trachomatis Biología, virulencia y enfermedad: Bacilos gramnegativos pequeños sin capa de peptidoglucanos en su pared celular. Parásitos intracelulares estrictos en el ser humano Dos formas distintas: cuerpos elementales infecciosos y cuerpos reticulares no infecciosos El antígeno de lipopolisacárido lo comparte con otras especies de Chlamydia y de Chlamydophila Las principales proteínas de la membrana externa son específicas de especie Dos biovariedades se asocian a enfermedad en el ser humano: tracoma y LGV Infecta las células epiteliales cilíndricas no ciliadas, cuboidales y transicionales Evita la fusión del fagosoma con los lisosomas celulares Los efectos patológicos del tracoma se deben a las infecciones repetidas Diagnóstico El cultivo es muy específico pero relativamente insensible Las pruebas de antígeno (DFA, ELISA) son relativamente insensibles Las pruebas de amplificación molecular son las más sensibles y específicas de las que puede disponerse actualmente Tratamiento, prevención y control El LGV se trata con doxiciclina o eritromicina Las infecciones oculares o genitales se tratan con azitromicina o doxiciclina La conjuntivitis y la neumonía del recién nacido se tratan} con eritromicina Las prácticas sexuales seguras y el tratamiento precoz de las parejas sexuales ayudan al control de las infecciones


Chlamydophila pneumoniae C. pneumoniae es un patógeno del ser humano que causa sinusitis, faringitis, bronquitis y neumonía. Se cree que las infecciones se transmiten de una persona a otra mediante las secreciones respiratorias. La prevalencia de infección resulta muy discutida y en la bibliografía se recogen amplias variaciones, en gran parte por la notable variación de los métodos diagnósticos. La mayor parte de las infecciones por C. pneumoniae son asintomáticas o leves, y producen tos persistente y malestar; la mayoría de los pacientes no necesita hospitalización. Las infecciones respiratorias más graves afectan generalmente a un único lóbulo pulmonar. Estas infecciones no se pueden distinguir de otras neumonías atípicas, como las producidas por Mycoplasma pneumoniae, Legionella pneumophila y los virus respiratorios.

El diagnóstico de las infecciones por C. pneumoniae es complejo. Los microorganismos no crecen en las líneas celulares que se usan para el aislamiento de C. trachomatis, y aunque lo hacen en la línea HEp-2, dicha línea no se usa en la mayor parte de los laboratorios clínicos. La detección de C. pneumoniae mediante NAAT ha obtenido resultados satisfactorios; sin embargo, se han descrito notables variaciones entre los laboratorios con experiencia en el uso de estas pruebas. La prueba de MIF es la única aceptable para el diagnóstico serológico. Los criterios para el diagnóstico de una infección aguda por C. pneumoniae son un título único de Ig. M mayor de 1: 16 o un aumento al cuádruple del título de Ig. G. Un título elevado de Ig. G de forma aislada no es diagnóstico. Dado que los anticuerpos Ig. G no aparecen hasta 6 -8 semanas tras la infección, las pruebas serológicas tienen un valor limitado en el diagnóstico de la infección aguda.

Los macrólidos (azitromicina, eritromicina, claritromicina), la doxiciclina o el levoflxacino se recomiendan para el tratamiento de las infecciones por C. pneumoniae, aunque las evidencias a favor de su uso son limitadas.
chlamydophila p. Sittaci Chlamydophila psittaci

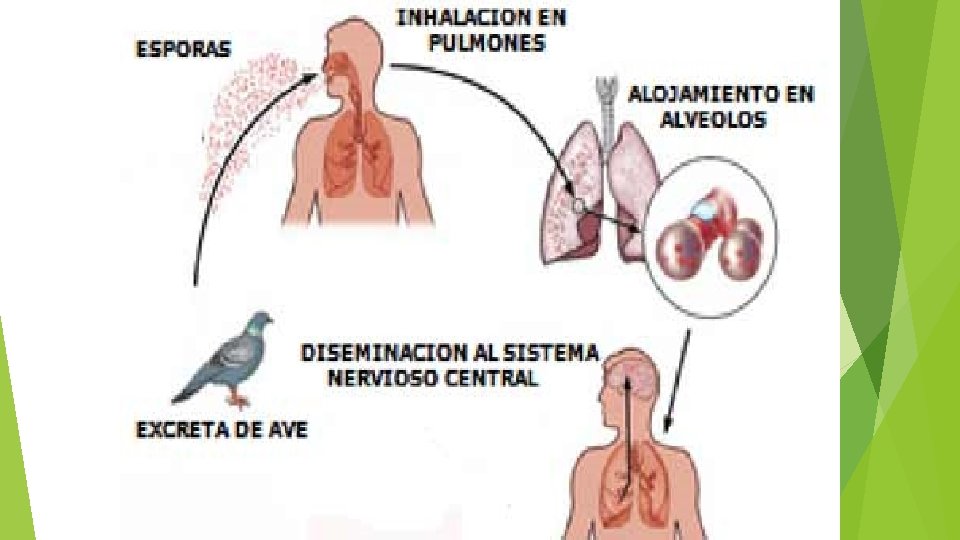
C. psittaci es la causa de la psitacosis (fiebre del loro), que se puede transmitir al ser humano. No obstante, el reservorio natural de C. psittaci es casi cualquier especie de ave, y la enfermedad se ha denominado más correctamente como ornitosis. El microorganismo está presente en la sangre, los tejidos, las heces y las plumas de los animales infectados, que pueden parecer enfermos o sanos. La infección penetra a través del aparato respiratorio, desde donde las bacterias se diseminan a las células reticuloendoteliales del hígado y del bazo. Los microorganismos se multiplican en estas localizaciones, produciendo una necrosis focal. Los pulmones y otros órganos se ven afectados como consecuencia de la diseminación hematógena, que produce fundamentalmente una respuesta inflamatoria linfocitaria en los alvéolos y en los espacios intersticiales. En estas localizaciones aparece edema, engrosamiento de la pared alveolar, infiltración de macrófagos, necrosis y algunas veces hemorragia. En los bronquiolos se forman tapones de mucosidad, que producen cianosis y anoxia.
Causa una enfermedad infecciosa que suele ser transmitida a los humanos por las aves pertenecientes a las familias de los loros, pavos y palomas. La enfermedad es llamada psitacosis
Manifestaciones clínicas: La psitacosis es una infección aguda y febril de vías respiratorias y signos generalizados que suelen incluir fiebre, tos no productiva, cefalea y malestar general.

La bacteria se suele transmitir al ser humano a través de la inhalación de los excrementos secos, de la orina o de las secreciones respiratorias de las aves del tipo del loro (p. ej. , loros, periquitos, guacamayos, cacatúas). La transmisión de una persona a otra es infrecuente. Los veterinarios, los cuidadores del zoológico, los trabajadores de las tiendas de mascotas y los empleados de las plantas de procesamiento de las aves de corral presentan un mayor riesgo de padecer esta infección. La enfermedad se produce tras un período de incubación de 5 a 14 días, y se suele manifestar con cefalea, fiebre alta, escalofríos, malestar general y mialgias. Los signos pulmonares son tos no productiva, crepitantes y consolidación. Es frecuente la afectación del sistema nervioso central, que consiste generalmente en cefalea, aunque puede ocurrir encefalitis, convulsiones, coma e incluso la muerte en los casos graves que no se tratan. Los pacientes presentan síntomas gastrointestinales como náuseas, vómitos y diarrea. Otros síntomas sistémicos son carditis, hepatomegalia, esplenomegalia y queratoconjuntivitis folicular.

A veces hay neumonía intersticial extensa con cambios radiográficos que de manera característica son más intensos de lo que cabría esperar con base en los signos de exploración física

Complicaciones raras Pericarditis Miocarditis Endocarditis Tromboflebitis superficial Hepatitis Encefalopatía
Síntomas HUMANOS Falta de apetito Fiebre Apariencia desgreñada Dolor de cabeza Secreción ocular Escalofríos Nasal Neumonía Diarrea AVES
Suele presentarse en trabajadores de tiendas de mascotas y personas que han comprado un ave infectada. Campesinos y en trabajadores de mataderos donde se procesan pavos. Se contagia por la inhalación de polvo de material fecal seco de jaulas de las aves. Manipulación de aves infectadas en mataderos.

ANTIBIOTICOS como Tetraciclina, Eritromicina, Macrolidos Azitromicina dihidratada Claritromicina Cloranfenicol 12 a 14 días cono mínimo después que la fiebre haya mostrado defervescencia

Diagnostico Es de tipo serológico, en que se advierte un incremento cuádruple del titulo de anticuerpos, y para ello se usa el estudio de fijación de complemento, en muestras de la fase aguda y de convalecencia obtenidas con una diferencia de dos a tres semanas

Enfermedades por Rickettsia.

Historia Ø En 1906 Howard Taylor Ricketts (1871 -1910) estudió una enfermedad que se manifestaba con cierta frecuencia en la zona noroeste de los Estados Unidos, logrando demostrar que la enfermedad se transmite por la picadura de la garrapata del Pacífico o Dermacentor occidentalis. Ø En 1909, el mismo Ricketts, anunció el descubrimiento de dos diminutos cuerpos de aspecto lanceolado como causantes de la enfermedad. Ø Casi a la vez, el austriaco Stanislaus Von Prowazek confirmó los hallazgos de Ricketts respecto al vector y al agente causante y, como él, también se infectó y falleció en 1915. Ø Un año más tarde, el brasileño Henrique da Rocha-Lima identificó el agente causante del tifus transmitido por el piojo y denominó a la bacteria Rickettsia prowazekii en homenaje a los dos fallecidos.

Morfología y estructura. • Pertenece a la familia Rickettsiaceae. • Las proteínas de la membrana externa se extienden a la superficie celular, donde se encuentran presentes en cantidades más abundantes. • Son bacterias intracelulares obligados. • Son muy pequeñas. • Son Gram negativas. • Son causantes de enfermedades infecciosas transmitidas por aerosoles, mordeduras, picaduras, rasguños, aguas y alimentos contaminados. Son altamente pleomórficas pues se pueden presentar como: • cocos (0, 1 μm de diámetro) • bacilos (1 -4 μm de longitud) • hilos (10 μm de largo) • No formadoras de esporas. • Se demuestra mejor su presencia por medio de técnicas de inmunofluorescencia específica. • La pared celular contiene lipopolisacáridos y al menos dos proteínas grandes en la membrana externa, así como peptidoglucano.

Crecimiento y metabolismo • Las rickettsias crecen libremente en el citoplasma de células eucariotas, donde presentan una adaptación notable. • La infección de la célula hospedadora inicia por la inducción de un proceso de endocitosis, que es muy similar a la fagocitosis, pero que requiere el consumo de energía por parte de Rickettsia. • No sobrevive fuera de la célula. Cultivo. El aislamiento de las rickettsias es difícil, por lo tanto es solo de utilidad limitada en el diagnóstico. Se inoculan embriones de pollo o caballos con sangre total; la muestra debe ser obtenida preferiblemente al inicio de la enfermedad.
Factores de virulencia ENDOTOXINAS FOSFOLIPASA A HEMOLISINAS (lisis de los eritrocitos, leucocitos y plaquetas mediante la producción de poros en la membrana citoplasmática)

serología v Para detectar rickettsias en garrapatas y fragmentos de tejido se utilizan pruebas directas con anticuerpos inmunofluorescentes. v En cualquier rickettsiosis, la evidencia serológica de la infección aparece después de la segunda semana de la enfermedad. v Existen pruebas de laboratorio que se necesita de poco antígeno y son sencillas que sirve para detetectar el Ig. M y el Ig. G.

Histopatología v Las rickettsias se multiplican en las células endoteliales de los vasos sanguíneos pequeños y generan vasculitis. v v v Las células se edematizan y necrosan. v Las lesiones vasculares son evidentes en la piel, pero también ocurre vasculitis en muchos órganos. v Se acompaña de coagulación intravascular diseminada y obstrucción vascular. Nodulos tíficos. El corazón exhibe lesiones similares en los vasos sanguíneos y algunas veces las lesiones se extienden hasta otros órganos.
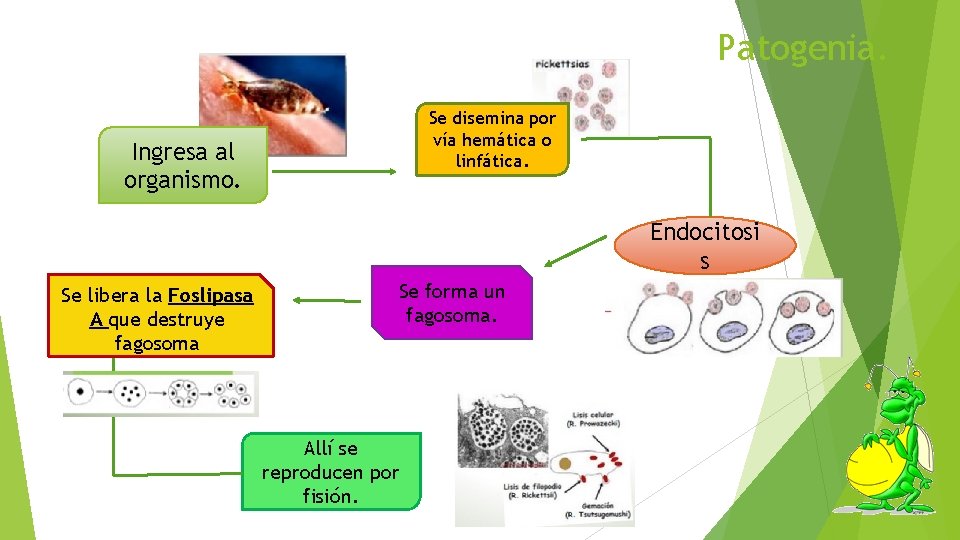
Patogenia. Se disemina por vía hemática o linfática. Ingresa al organismo. Endocitosi s Se libera la Foslipasa A que destruye fagosoma Se forma un fagosoma. Allí se reproducen por fisión.

Clasificación.
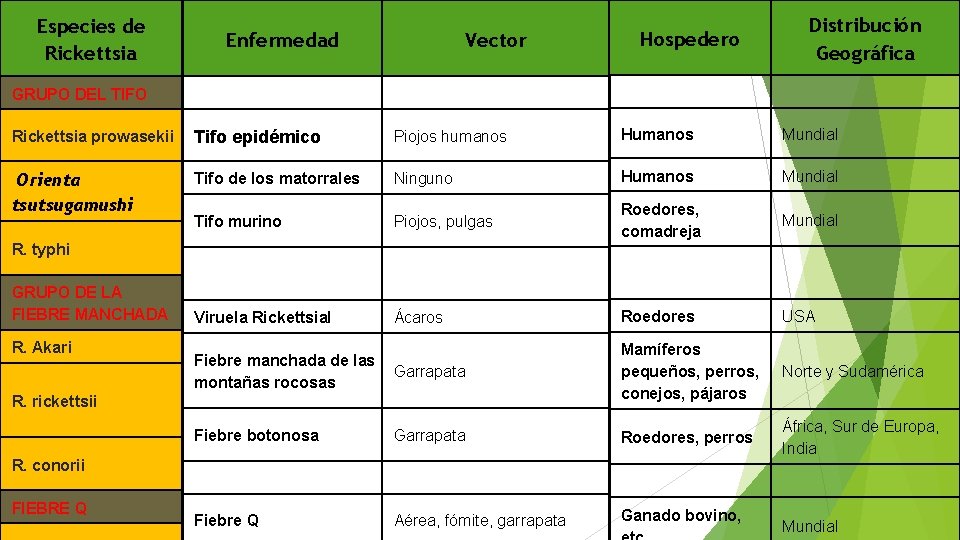
Especies de Rickettsia Enfermedad Distribución Geográfica Hospedero Vector GRUPO DEL TIFO Rickettsia prowasekii Tifo epidémico Piojos humanos Humanos Mundial Orienta Tifo de los matorrales Ninguno Humanos Mundial Tifo murino Piojos, pulgas Roedores, comadreja Mundial Viruela Rickettsial Ácaros Roedores USA Fiebre manchada de las Garrapata montañas rocosas Mamíferos pequeños, perros, conejos, pájaros Norte y Sudamérica Fiebre botonosa Garrapata Roedores, perros África, Sur de Europa, India Fiebre Q Aérea, fómite, garrapata Ganado bovino, tsutsugamushi R. typhi GRUPO DE LA FIEBRE MANCHADA R. Akari R. rickettsii R. conorii FIEBRE Q Mundial

Manifestaciones clínicas Con excepción de la fiebre Q, en la que no existen lesiones cutáneas, las rickettsiosis se caracterizan por fiebre, cefalea, malestar general, postración, exantema cutáneo y hepatoesplenomegalia. A. Grupo del tifus B. Grupo de fiebres exantemáticas. C. Fiebre Q

A. Grupo del tifus 1. Tifus epidémico (Rickettsia prowazekii). • Tífus epidémico es una enfermedad transmitida por el piojo del cuerpo humano. • Cuando un piojo infectado pica a una persona, defeca y las bacterias se encuentran en las heces. La irritación causada por la picadura hace que la persona al rascarse inoculen las bacterias en la piel erosionada. • Reservorio principal: los seres humanos. . • Tifus epidémico se produce entre personas que viven en condiciones desfavorables. • No se produce la transmisión transovárica del piojo (mueren entre 2 -3 semanas después de haberse infectado) • Se presenta principalmente en centro América, Sudamérica, áfrica y con menor frecuencia en EEUU
Modo de transmisión. • Los piojos infectados secretan Rickettsias en las heces, y por lo común, defecan en el momento de alimentarse. • Las personas se infectan al frotar las heces o triturar el piojo sobre el sitio de la picadura. • Las Rickettsias pueden sobrevivir durante semanas en el piojo muerto.

Cuadro clínico. § El Tifus epidémico se caracteriza por la aparición repentina de fiebre, escalofríos, dolor de cabeza, mialgias y artralgias, después de un período de incubación promedio de 8 días. § La erupción de tifus epidémico se desarrolla en el tronco primero y se extiende a las extremidades (propagación centrífuga). § Las complicaciones incluyen: miocarditis, estupor y delirio. § La tasa de mortalidad varía, pero puede ser bastante alto (60 - 70%) en algunas epidemias severas.
Medidas de prevención. Aplicar polvo insecticida residual y eficaz, en forma manual o por medio de un pulverizador mecánico, a la ropa y a las personas de grupos de población que viven en condiciones que facilitan la infestación por los piojos. TRATAMIENT O Tetraciclina Diagnóstico: La prueba de la MIF (Microinmunofluorescencia) es el método diagnóstico de elección para demostrar la enfermedad por R. prowazekii. Cloranfenicol

2. Tifus endémico (Rickettsia typhi). • Las ratas son el reservorio principal para la enfermedad que se transmite por el vector de la pulga de la rata. • El ciclo normal es la rata, las pulgas de las ratas y seres humanos que se infectan accidentalmente. • Las bacterias se encuentran en las heces de las pulgas y se inoculan en la piel erosionada por rascarse el área irritada por la mordedura.
La infección persiste en la naturaleza por el ciclo: Rata Pulga Existen 2 modos de transmisión: Pulga Rata Hombre Rata
Cuadro clínico. • Fiebre • Escalofríos • Dolor de cabeza. • Mialgia aparecen bruscamente de 1 - 2 semanas después de la infección. • La erupción comienza en el tronco y se extiende a las extremidades, • La enfermedad es leve y se resuelve dentro de 3 semanas, incluso sin tratamiento.
Se usa una prueba de fluorescencia indirecta (IFA) específica de R. typhi para confirmar el diagnóstico de tifus murino. Medidas de prevención. -Controlar el depósito de roedores, es útil en la prevención de la infección. -No existe vacuna eficaz. Tratamiento Diagnóstico: Tetraciclina Doxiciclina Cloranfenicol

3. Tifus de los matorrales (Orienta tsutsugamushi). • La enfermedad se transmite a los humanos por los ácaros. • El ácaro es a la vez el depósito y el vector de las bacterias pasando a la generación siguiente transováricamente. • Los roedores también pueden actuar como un depósito. • El ciclo normal es de ácaro a roedores, y de ácaros a seres humanos, los cuales se infectan accidentalmente. • Se da en el este de Asia, Australia, Japón, otras islas del oeste del Pacifico y EEUU como enfermedad v Tiene un período de incubación de 6 a 18 días importada. (media, de 10 a 12 días).
TRATAMIENT O Cuadro clínico. v Aparición repentina de fiebre escalofríos v Dolor de cabeza v Mialgia 1 -3 semanas después de contraer la bacteria. v La erupción aparece primero en el tronco y se extiende a las extremidades (propagación centrífuga). Tetraciclina Cloranfenicol Las complicaciones del tifus de los matorrales pueden incluir meningoencefalitis, hepatitis, neumonitis y miocarditis. El fallo de uno o más órganos principales también es posible. Complicaciones.

B. Fiebres exantemáticas. 1. R. rickettsii • Es la más común en los Estados Unidos, con 400 a 800 casos que ocurren anualmente. • Aunque la enfermedad fue descrita originalmente en los estados de las Montañas Rocosas, ahora es más común en los estados del centro-sur, incluyendo Carolina del Sur. • El M. O se transmite a través de la picadura de una garrapata infectada, esto ocurre, mayoritariamente, a partir de abril y septiembre. • Los M. O avirulentos latentes se activan por infestación de sangre caliente que posteriormente se liberaran a través de la saliva, para penetrar en el torrente circulatorio del huésped humano. • El individuo para ser infectado debe estar expuesto a un periodo de tiempo prolongado (2448 horas).
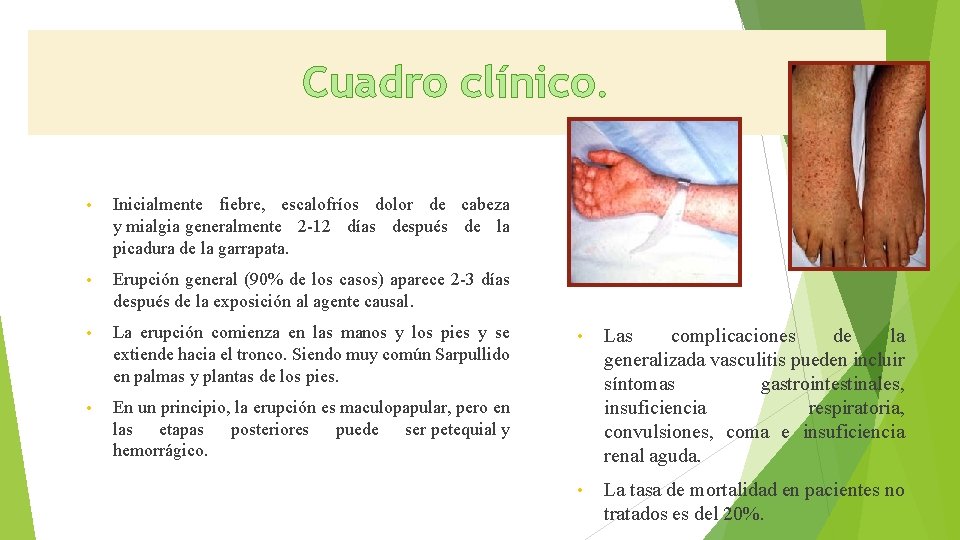
Cuadro clínico. • Inicialmente fiebre, escalofríos dolor de cabeza y mialgia generalmente 2 -12 días después de la picadura de la garrapata. • Erupción general (90% de los casos) aparece 2 -3 días después de la exposición al agente causal. • La erupción comienza en las manos y los pies y se extiende hacia el tronco. Siendo muy común Sarpullido en palmas y plantas de los pies. • En un principio, la erupción es maculopapular, pero en las etapas posteriores puede ser petequial y hemorrágico. • Las complicaciones de la generalizada vasculitis pueden incluir síntomas gastrointestinales, insuficiencia respiratoria, convulsiones, coma e insuficiencia renal aguda. • La tasa de mortalidad en pacientes no tratados es del 20%.
Medidas de prevención. -Controlar el depósito de roedores, es útil en la prevención de la infección. -No existe vacuna eficaz. TRATAMIENT O Tetraciclina Diagnóstico. Se puede diagnosticar la presencia de R. Rickettsii mediante la tinción de Giemsa y de Giménez. También mediante la técnica de la PCR o mediante la prueba de Weil-Félix, que implica la aglutinación de los antígenos de la bacteria. Cloranfenicol

C. Fiebre Q C. burnetti. • La infección se produce por la inhalación de partículas en el aire. • El microorganismo se multiplica en los pulmones y se difunde a otros órganos. • C. burnetii es extremadamente estable en el medio ambiente y tiene características "similares a esporas". • C. burnetii infecta a una amplia variedad de animales, incluyendo conejos, cabras, ganado ovino y gatos. Se reconocen dos fases antigénicas: 1. La fase I, que se encuentra en la naturaleza (organismo de los animales o de las garrapatas. 2. La fase II, avirulenta, después de múltiples pasos de laboratorio en huevos o cultivos celulares. El agente puede estar presente en artrópodos infectados, y en la sangre, orina, heces, leche y tejidos de animales o humanos infectados. • La inmunidad celular es importante en la recuperación de la enfermedad.

Manifestaciones clínicas. Clínicamente se pueden distinguir 2 fases: Aguda: fiebre, dolor de cabeza, escalofríos y mialgia. Hepática: formación de granulomas (hasta un tercio de los casos se puede complicar con hepatitis).

Diagnóstico El diagnóstico de laboratorio se hace por el incremento de anticuerpos Ig. M específicos entre las fases agudas y de convalecencia, por medio de inmunofluorescencia, microaglutinación, fijación del complemento o ELISA. Tratamiento Fiebre Q aguda: Tetraciclina. Fiebre Q crónica: combinación de antibióticos como Doxiciclina, Trimetropin y Sulfametoxazol.

tratamiento Las tetraciclinas son eficaces siempre y cuando se instituyan en una etapa incipiente; se administran diariamente por vía oral y se prolongan durante tres a cuatro días después de la defervescencia. En los pacientes graves, las primeras dosis se administran por vía intramuscular. El cloranfenicol también es efectivo. Las sulfonamidas agravan la enfermedad y están contraindicadas. Los anticuerpos no eliminan a las rickettsias del cuerpo, pero suprimen su proliferación.

Datos de laboratorio. v Desde el punto de vista técnico es difícil aislar a las rickettsias y su utilidad para el diagnóstico es limitada. v v Las rickettsias se recuperan con más frecuencia en la sangre que se extrae poco después de iniciada la enfermedad. Las pruebas serológicas más utilizadas son la inmunofluorescencia indirecta y la fijación del complemento. v v Algunas rickettsias infectan ratones y éstas también se observan en los frotis de exudado peritoneal. Es necesario demostrar que los anticuerpos se elevan durante la evolución de la enfermedad.
Prevención A. Prevención de la transmisión rompiendo la cadena de la infección 1. Tifus epidémico. Desparasitación con insecticida. 2. Tifus murino. Acondicionar los edificios para que sean a prueba de ratas y utilizar venenos contra ratas. 3. Tifus de los matorrales. Eliminar en los campamentos la vegetación secundaria en la que pudieran habitar ratas y ácaros.
4. Fiebres exantemáticas. Limpiar la tierra infestada, profilaxis personal en forma de ropa protectora como botas, calcetines sobre los pantalones, repelentes de ácaros; y retirar con frecuencia las garrapatas adheridas. 5. Rickettsiosis vesiculosa. Eliminar roedores y sus parásitos en las viviendas.

B. Prevención de la transmisión de la fiebre Q por medio de la pasteurización correcta de la leche. Las recomendaciones actuales para la pasteurización con “alta temperatura y tiempo corto” a 71. 5°C durante 15 s es suficiente para destruir a la Coxiella viable. C. Prevención vacunación por medio de No existe vacuna contra la fiebre exantemática americana, otras enfermedades del grupo de las fiebres exantemáticas ni contra las enfermedades del grupo del tifus. Se está investigando una vacuna contra C. burnetii elaborada a partir de sacos vitelinos de huevo. Esta vacuna se ha utilizado en empleados de laboratorio que trabajan con C. burnetii vivos.



- Slides: 95