Mutarotcia je veobecne acidobzicky katalyzovan vzjomn premena anomrnotautomrnych

Mutarotácia je všeobecne acidobázicky katalyzovaná vzájomná premena anomérno-tautomérnych foriem redukujúceho sacharidu cez jeho acyklickú formu prebiehajúca v čerstvom roztoku sacharidu až do ustálenia rovnováhy. Táto premena sa navonok prejavuje ako časová zmena optickej otáčavosti [ ]D z počiatočnej do rovnovážnej hodnoty a schématicky sa označuje vodorovnou šípkou (napr. pre -anomér D -glukózy [ ]D +111º +53º (voda)).

Mutarotácia zahrňuje anomerizáciu a tautomerizáciu α-D-glukopyranóza β-D-glukopyranóza Zdroj: Monosaccharides. Their Chemistry and Their Roles in Natural Products, P. M. Collins, R. J. Ferrier, Wiley, Chichester, 1995.

Mutarotácia zahrňuje anomerizáciu a tautomerizáciu α-D-glukopyranóza β-D-glukopyranóza 38 % 62 % A aaaaldehydoα-D-glukofuranóza 0, 05 % aaa. D-glukózahydrát glukaaaa+aaaaaa aldehydoaaa. D-glukóza 0, 02 % β-D-glukofuranóza 0, 14 %
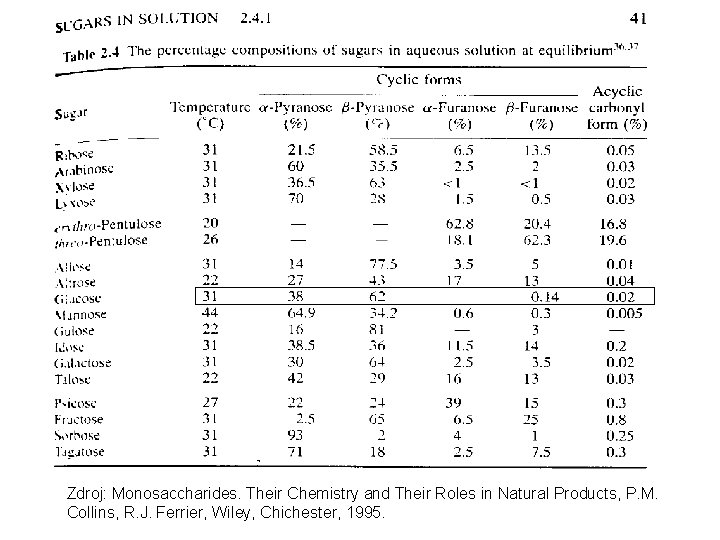
Zdroj: Monosaccharides. Their Chemistry and Their Roles in Natural Products, P. M. Collins, R. J. Ferrier, Wiley, Chichester, 1995.
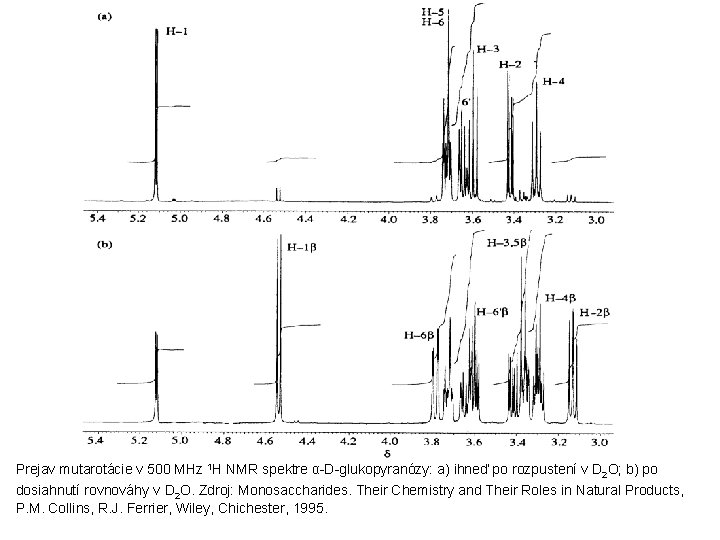
Prejav mutarotácie v 500 MHz 1 H NMR spektre α-D-glukopyranózy: a) ihneď po rozpustení v D 2 O; b) po dosiahnutí rovnováhy v D 2 O. Zdroj: Monosaccharides. Their Chemistry and Their Roles in Natural Products, P. M. Collins, R. J. Ferrier, Wiley, Chichester, 1995.
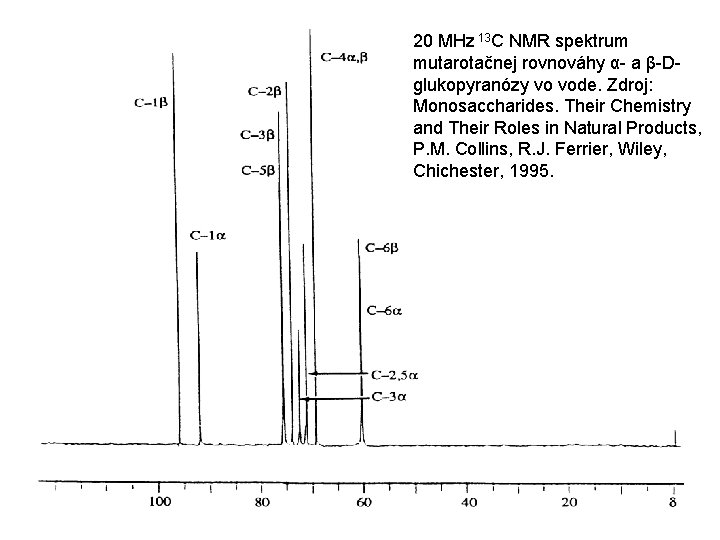
20 MHz 13 C NMR spektrum mutarotačnej rovnováhy α- a β-Dglukopyranózy vo vode. Zdroj: Monosaccharides. Their Chemistry and Their Roles in Natural Products, P. M. Collins, R. J. Ferrier, Wiley, Chichester, 1995.

Lobry de Bruyn-Alberda van Ekensteinova reakcia bázicky katalyzovaná nerovnovážna izomerizačnoepimerizačná vzájomná premena dvojice epimérnych aldóz a odpovedajúcej ketózy prebiehajúca cez endiolový intermediát. Reakcia sa v preparatívnom meradle využíva na prípravu ketóz z aldóz; výťažky epimérnej aldózy sú nízke. V závislosti na podmienkach môže táto reakcia prebiehať po celom reťazci a jej výsledkom je potom zložitá zmes aldóz a ketóz. Namiesto vodných roztokov alkalických zemín, ktoré katalyzujú aj ďalšie reakcie, sa ako reakčné prostredie obvykle používa vlhký pyridín.
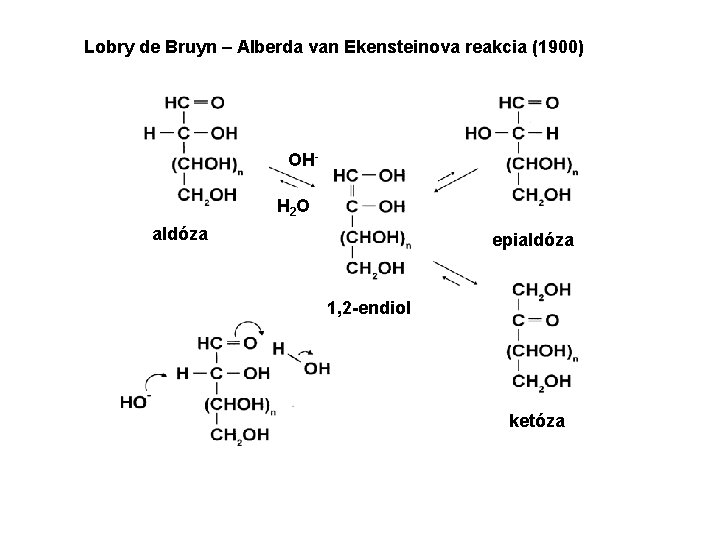
Lobry de Bruyn – Alberda van Ekensteinova reakcia (1900) OHH 2 O aldóza epialdóza 1, 2 -endiol ketóza
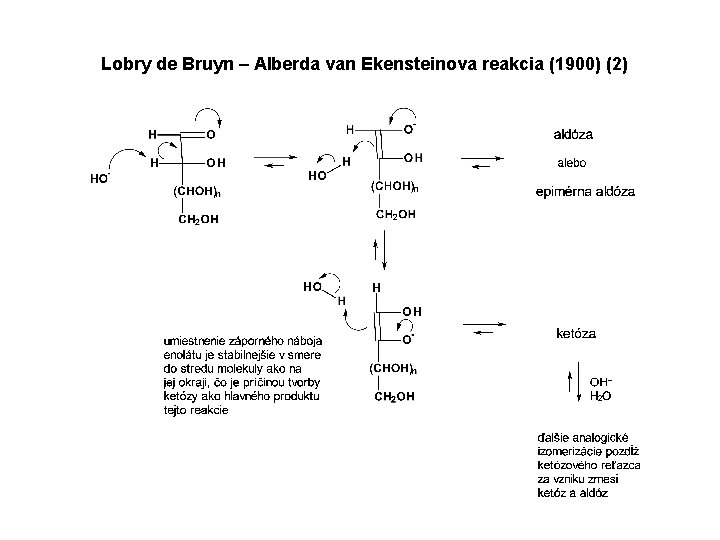
Lobry de Bruyn – Alberda van Ekensteinova reakcia (1900) (2)

epimerizácia - vo všeobecnosti reakcia, ktorou sa dosahuje vzájomná premena epimérnych sacharidov. Na prípravu epimérnych aldóz sa najvýhodnejšie využíva Bílikova reakcia. Epimerizácia aldóz a ketóz sa v menšom rozsahu vyskytuje v Lobry de Bruyn-Alberda van Ekensteinovej reakcii. Epimerizácii v bázickom prostredí podliehajú aj kyseliny aldónové.
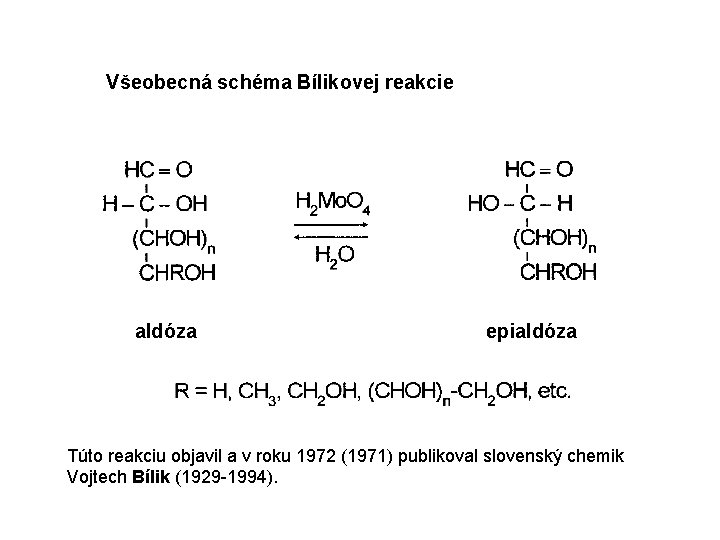
Všeobecná schéma Bílikovej reakcie aldóza epialdóza Túto reakciu objavil a v roku 1972 (1971) publikoval slovenský chemik Vojtech Bílik (1929 -1994).

Bílikova reakcia - všeobecná vnútromolekulová reakcia aldóz prebiehajúca vo vodných roztokoch v prítomnosti katalytického množstva kyseliny molybdénovej, v dôsledku ktorej vzniká v priebehu 2 až 8 hodín pri teplote 70 až 90 o. C rovnovážna zmes dvojice epimérnych aldóz. Zloženie rovnovážnych zmesí je pre dvojice epimérnych D-aldóz: D-treóza D-arabinóza D-xylóza D-glukóza D-galaktóza D-alóza atď. : : : D-erytróza D-ribóza D-lyxóza D-manóza D-talóza D-altróza 4 2 7 3 4 3 : : : 3 1 5 1 1 2 Rovnovážne pomery sú rovnaké aj pre epimérne dvojice L-aldóz. Reakcia má veľký preparatívny význam; využíva sa na výrobu resp. prípravu mnohých aldóz (napr. D-manózy, D-talózy, D-lyxózy, D-ribózy, L-ribózy, atď.

Všobecné podmienky C-2 epimerizácie aldóz katalyzovanej molybdénanovými iónmi • 10 -20 % vodný roztok aldózy (0, 06 -1, 1 mol/L) v 0, 1 % vodnej kyseline molybdénovej (0, 006 mol/L) • p. H 2, 9, 80 -95 ºC D-glukóza 90 ºC 2 h D-glukóza + D-manóza 73 % 27 % 90 ºC 10 h D-manóza
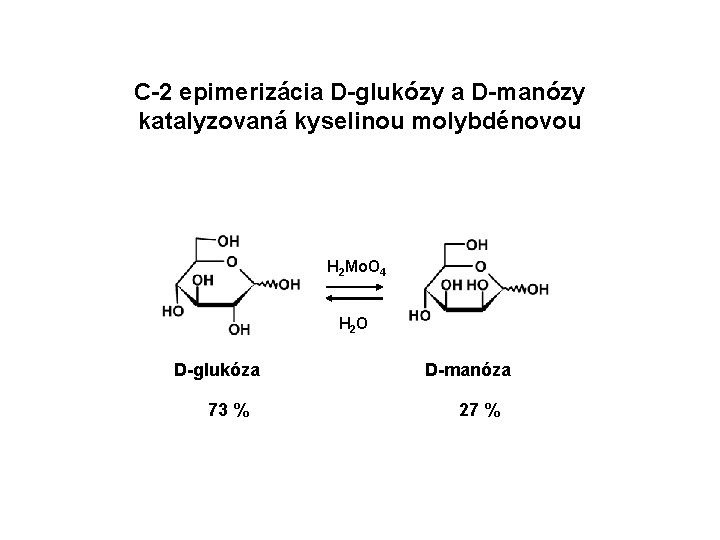
C-2 epimerizácia D-glukózy a D-manózy katalyzovaná kyselinou molybdénovou H 2 Mo. O 4 H 2 O D-glukóza 73 % D-manóza 27 %

Bílikova reakcia je molekulový prešmyk aldóz, pri ktorom dochádza k zániku väzby C-2 C-3 za súčasného vzniku väzby C-1 C-3, čo bolo dokázané nasledovnými premenami: Zdroj: Hayes ML, Pennings NJ, Serianni AS, Barker R (1982) J Am Chem Soc 104: 6764
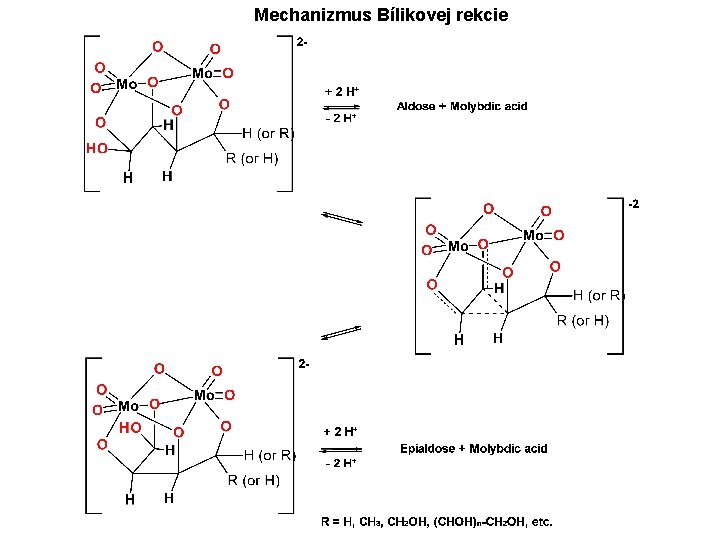
Mechanizmus Bílikovej rekcie
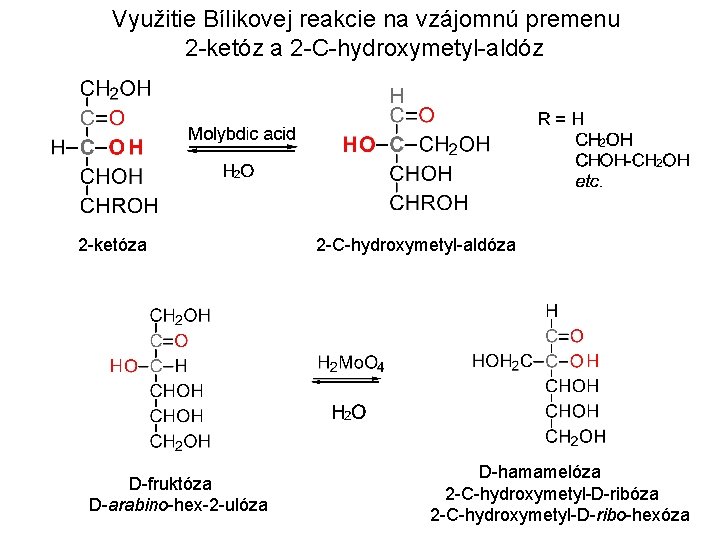
Využitie Bílikovej reakcie na vzájomnú premenu 2 -ketóz a 2 -C-hydroxymetyl-aldóz 2 -ketóza D-fruktóza D-arabino-hex-2 -ulóza 2 -C-hydroxymetyl-aldóza D-hamamelóza 2 -C-hydroxymetyl-D-ribo-hexóza
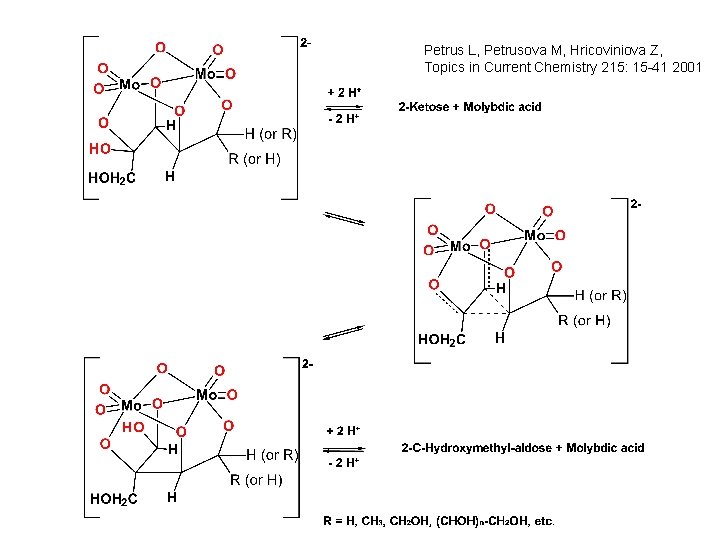
Petrus L, Petrusova M, Hricoviniova Z, Topics in Current Chemistry 215: 15 -41 2001
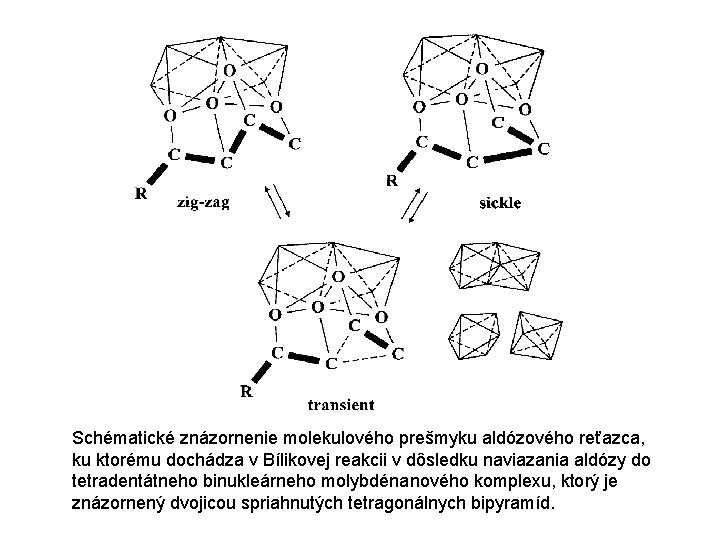
Schématické znázornenie molekulového prešmyku aldózového reťazca, ku ktorému dochádza v Bílikovej reakcii v dôsledku naviazania aldózy do tetradentátneho binukleárneho molybdénanového komplexu, ktorý je znázornený dvojicou spriahnutých tetragonálnych bipyramíd.
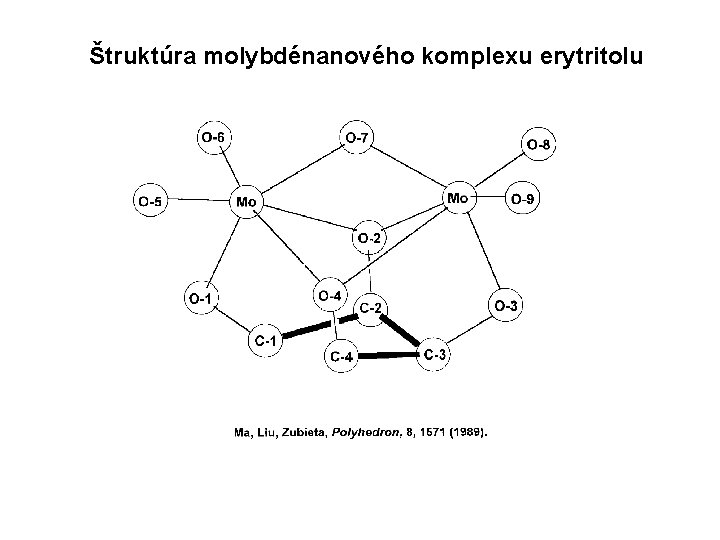
Štruktúra molybdénanového komplexu erytritolu
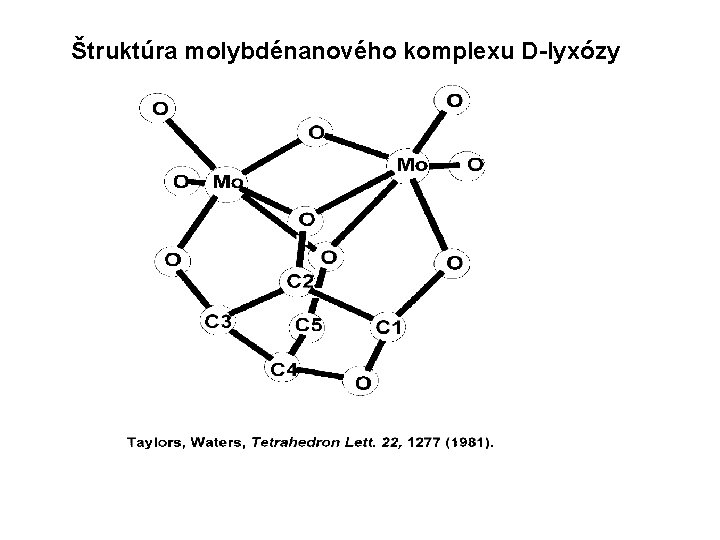
Štruktúra molybdénanového komplexu D-lyxózy
![Ostatné známe katalytické systémy pre C-1 -C-2 transpozičnú C-2 “epimerizáciu” aldóz D-[1 -13 C]glukóza Ostatné známe katalytické systémy pre C-1 -C-2 transpozičnú C-2 “epimerizáciu” aldóz D-[1 -13 C]glukóza](http://slidetodoc.com/presentation_image_h/83f56a79f03e342086bbcc703b9c3f96/image-22.jpg)
Ostatné známe katalytické systémy pre C-1 -C-2 transpozičnú C-2 “epimerizáciu” aldóz D-[1 -13 C]glukóza - D-[2 -13 C]manóza Ni(II) – N-alkylovaný etyléndiamín 1 Co(II) – N-alkylovaný etyléndiamín 2 Ca(OH)2, čiastočne Sr(OH)2 ref. 3 La(OAc)3 vo vodnom Na. OHref. 4
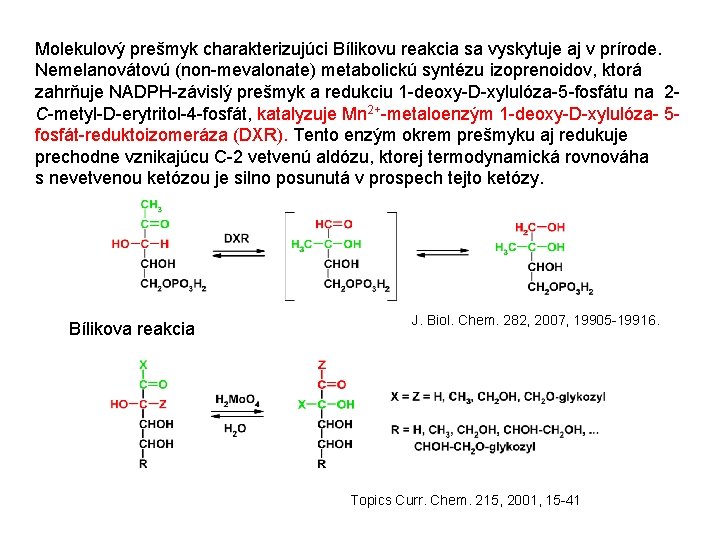
Molekulový prešmyk charakterizujúci Bílikovu reakcia sa vyskytuje aj v prírode. Nemelanovátovú (non-mevalonate) metabolickú syntézu izoprenoidov, ktorá zahrňuje NADPH-závislý prešmyk a redukciu 1 -deoxy-D-xylulóza-5 -fosfátu na 2 C-metyl-D-erytritol-4 -fosfát, katalyzuje Mn 2+-metaloenzým 1 -deoxy-D-xylulóza- 5 fosfát-reduktoizomeráza (DXR). Tento enzým okrem prešmyku aj redukuje prechodne vznikajúcu C-2 vetvenú aldózu, ktorej termodynamická rovnováha s nevetvenou ketózou je silno posunutá v prospech tejto ketózy. Bílikova reakcia J. Biol. Chem. 282, 2007, 19905 -19916. Topics Curr. Chem. 215, 2001, 15 -41

Katalýza transpozičného prešmyku redukujúcich sacharidov bola pozorovaná len s komplexami prvkov (kovov), ktoré majú d-orbitály. Tieto d-orbitály sú pravdepodobne nevyhnutné na priebeh tohto prešmyku, ktorý zrejme spočíva v delokalizácii karbonylovej skupiny redukujúceho sacharidu na atóm uhlíka susediaci s jeho karbonylovou skupinou, a to prostredníctvom interakcie d-orbitálov katalytického prvku s p-orbitálmi zúčastnených atómov uhlíka a kyslíka redukujúceho cukru.

Učivo Chémie sacharidov na ďalších obrázkoch je nad rámec predmetu Chémia prírodných látok
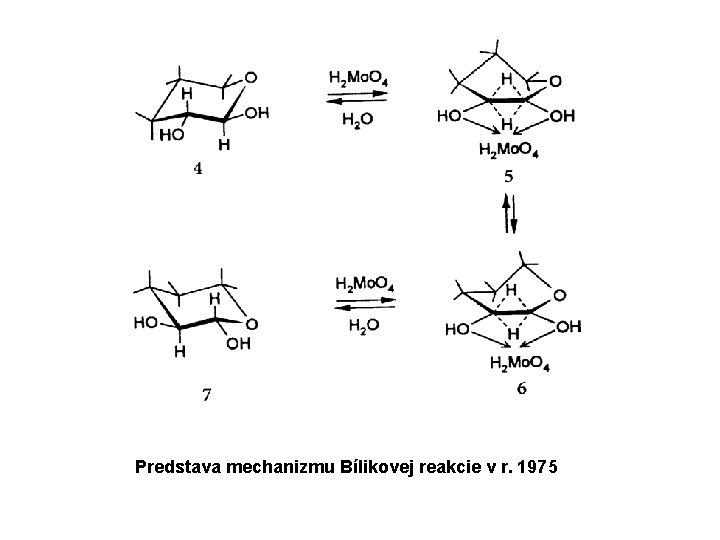
Predstava mechanizmu Bílikovej reakcie v r. 1975
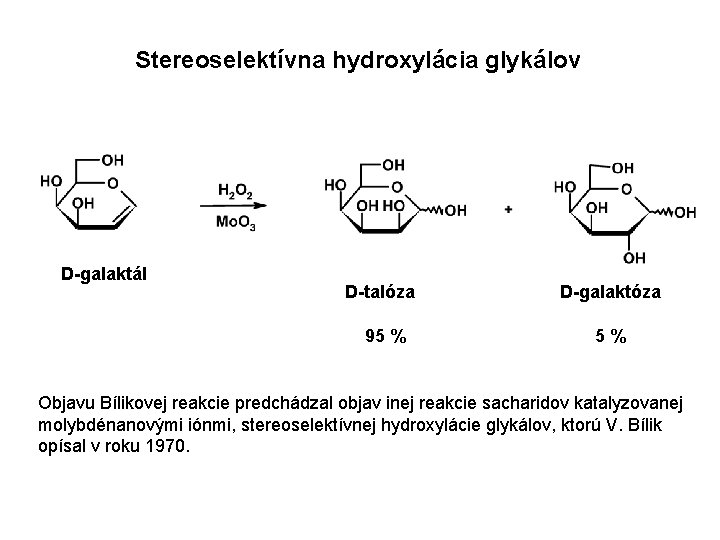
Stereoselektívna hydroxylácia glykálov D-galaktál D-talóza 95 % D-galaktóza 5% Objavu Bílikovej reakcie predchádzal objav inej reakcie sacharidov katalyzovanej molybdénanovými iónmi, stereoselektívnej hydroxylácie glykálov, ktorú V. Bílik opísal v roku 1970.

Rovnovážne pomery epimérnych aldóz v Bílikovej reakcii

- Slides: 29