Muskelgewebe Dvid Csaba Semmelweis Universitt Anatomisches Histologisches und
Muskelgewebe Dávid Csaba Semmelweis Universität Anatomisches, Histologisches und Embryologisches Institut Nagyobbrészt Dr. H-Minkó Krisztina diáiból

Generelle Eigenschaften • Funktion: Kontraktion • Viele Zellen, wenig extrazelluläre Matrix • Kontraktile Filamente – Aktin, Myosin • Komplexes Zytoskelett • Großer Energiebedarf – Mitokondrien • Großaer Ca 2+-bedarf – glattes ER, Ca 2+-Kanäle, Ca 2+-Pumpen • Membrana basalis

Typen • Quesrgestreifte Muskulatur Skelettmuskel: -Einheit: vielkerniger Muskelfaser -Ursprung, Ansatz: fas immer an Skelettelemente (Knochen, Knorpel) -Regulation der Kontraktion durch Nervenendigungen Eingeweide: -Einheit: vielkerniger Muskelfaser -oft unabhängig von Skelettelemente (Speiseröhre) -Regulation der Kontraktion durch Nervenendigungen • Herzmuskel (quergestreifet muskel. ZELLEN) • Glatte Muskulatur (keine Querstreifung) Andere kontraktile Zellen (kein Muskelgewebe!) Myoepithel (Drüsen) Myofibroblast (Perizyt, Mesangiale Zellen)
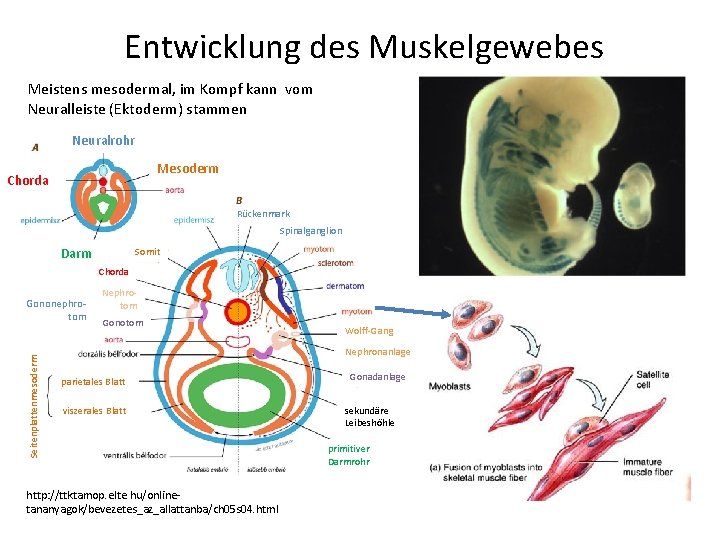
Entwicklung des Muskelgewebes Meistens mesodermal, im Kompf kann vom Neuralleiste (Ektoderm) stammen Neuralrohr Mesoderm Chorda Rückenmark Spinalganglion Darm Somit Chorda Seitenplattenmesoderm Gononephrotom Nephrotom Gonotom Wolff-Gang Nephronanlage parietales Blatt viszerales Blatt http: //ttktamop. elte. hu/onlinetananyagok/bevezetes_az_allattanba/ch 05 s 04. html Gonadanlage sekundäre Leibeshöhle primitiver Darmrohr
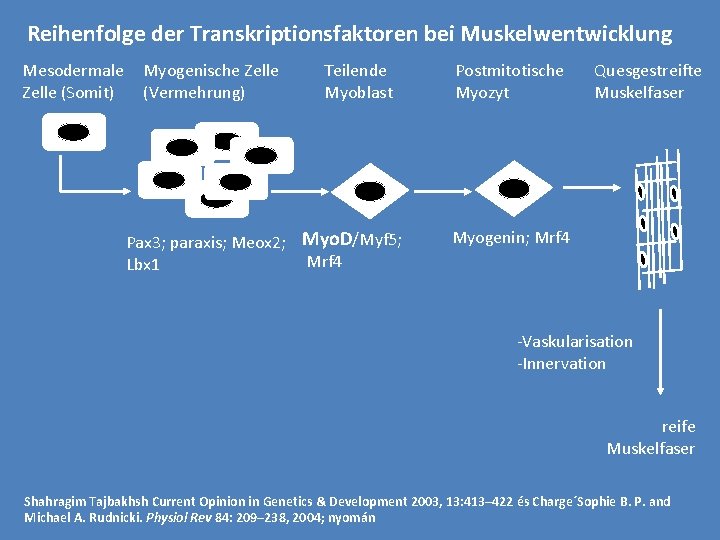
Reihenfolge der Transkriptionsfaktoren bei Muskelwentwicklung Mesodermale Zelle (Somit) Myogenische Zelle (Vermehrung) Teilende Myoblast Pax 3; paraxis; Meox 2; Myo. D/Myf 5; Mrf 4 Lbx 1 Postmitotische Myozyt Quesgestreifte Muskelfaser Myogenin; Mrf 4 -Vaskularisation -Innervation reife Muskelfaser Shahragim Tajbakhsh Current Opinion in Genetics & Development 2003, 13: 413– 422 és Charge´Sophie B. P. and Michael A. Rudnicki. Physiol Rev 84: 209– 238, 2004; nyomán

Quergestreifte Muskelgewebe

Mehrkernige Riesenzelle (Synzytium) – Muskelfaser Membrana basalis Ersatzzelle – Satelittenzelle Plasmamembran - Sarkolemma Cytoplazma - Sarkoplazma Glattes ER– Sarkoplasmatisches Retikulum Mitochondrium - Sarkosoma Kontraktile Einheit - Sarkomer

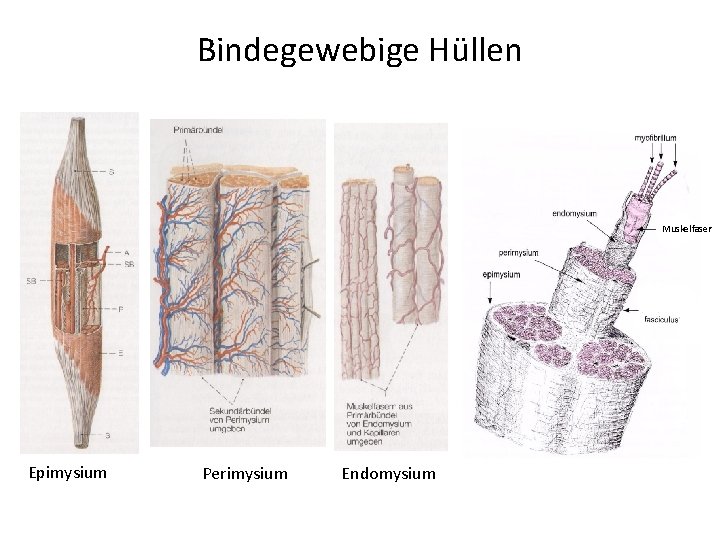
Bindegewebige Hüllen Muskelfaser Epimysium Perimysium Endomysium


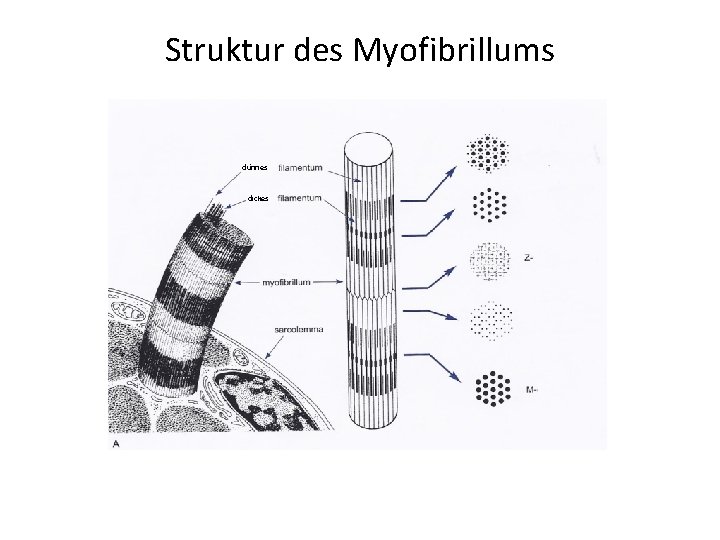
Struktur des Myofibrillums dünnes dickes

SARKOMER A-Streifen Anisotrop I-Streifen Isotrop H-Zone Hensen Z Mittelzone Zwischenscheibe (Z-Linie)
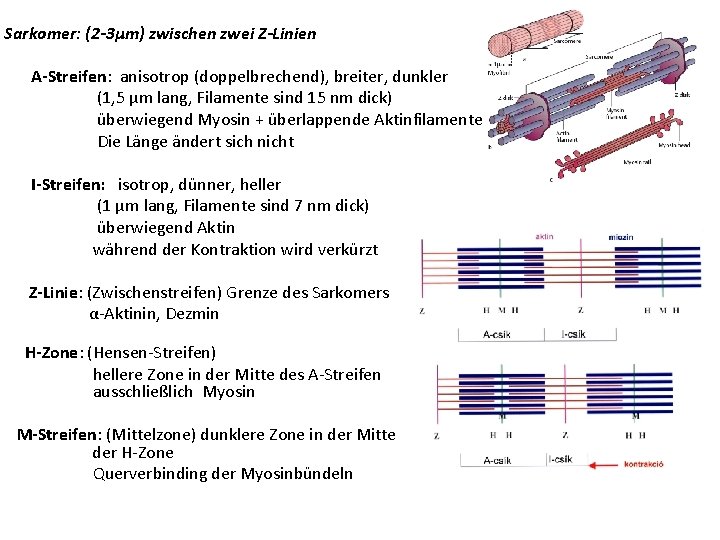
Sarkomer: (2 -3µm) zwischen zwei Z-Linien A-Streifen: anisotrop (doppelbrechend), breiter, dunkler (1, 5 µm lang, Filamente sind 15 nm dick) überwiegend Myosin + überlappende Aktinfilamente Die Länge ändert sich nicht I-Streifen: isotrop, dünner, heller (1 µm lang, Filamente sind 7 nm dick) überwiegend Aktin während der Kontraktion wird verkürzt Z-Linie: (Zwischenstreifen) Grenze des Sarkomers α-Aktinin, Dezmin H-Zone: (Hensen-Streifen) hellere Zone in der Mitte des A-Streifen ausschließlich Myosin M-Streifen: (Mittelzone) dunklere Zone in der Mitte der H-Zone Querverbinding der Myosinbündeln
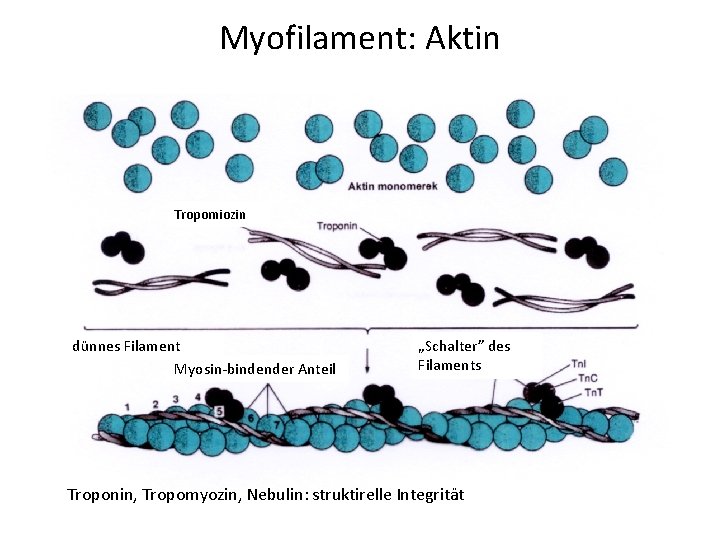
Myofilament: Aktin Tropomiozin dünnes Filament Myosin-bindender Anteil „Schalter” des Filaments Troponin, Tropomyozin, Nebulin: struktirelle Integrität

Aktin felfedezése Szent-Györgyi Albert
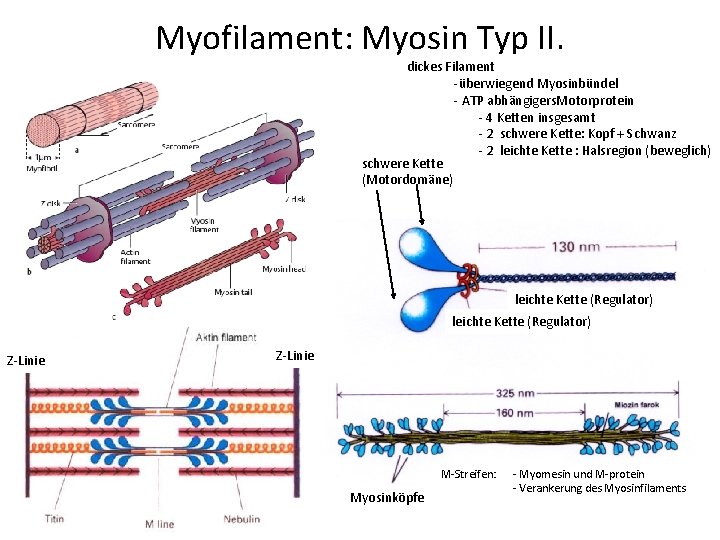
Myofilament: Myosin Typ II. dickes Filament -überwiegend Myosinbündel - ATP abhängigers. Motorprotein - 4 Ketten insgesamt - 2 schwere Kette: Kopf + Schwanz - 2 leichte Kette : Halsregion (beweglich) schwere Kette (Motordomäne) leichte Kette (Regulator) Z-Linie M-Streifen: Myosinköpfe - Myomesin und M-protein - Verankerung des Myosinfilaments

Mechanismus der Kontraktion Theorie der gleitenden Filamente In der chemischen Bindung gespeicherte Energie des ATPs wird als kinetische Aribet freigegeben A-Streifen I-Streifen I-Str Kontraktion
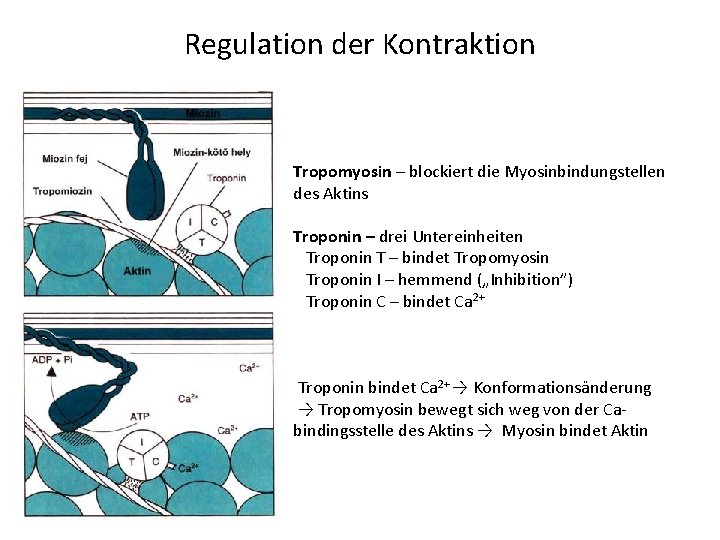
Regulation der Kontraktion Tropomyosin – blockiert die Myosinbindungstellen des Aktins Troponin – drei Untereinheiten Troponin T – bindet Tropomyosin Troponin I – hemmend („Inhibition”) Troponin C – bindet Ca 2+ Troponin bindet Ca 2+ → Konformationsänderung → Tropomyosin bewegt sich weg von der Cabindingsstelle des Aktins → Myosin bindet Aktin

Transversal (T)–Tubulus, Triad Kopplung der Erregung und Kontraktion -sarkoplasmatisches Retikulum - speichert Ca 2+ -enthält Ca 2+-Pumpen - eigentlich g. ER T-tubulus -tiefe Invagination der Zellmembran Freisetzung des Ca 2+ vom sarkoplasmatischen Retikulum startet die Kontraktion Nach der Kontraktion Ca 2+ wird durch sarkoplasmatisches Retikulum aufgenommen


Muscle Contraction Process Molecular Mechanism 3 D Animation https: //www. youtube. com/watch? v=YAJ-9 n. PSqw. A
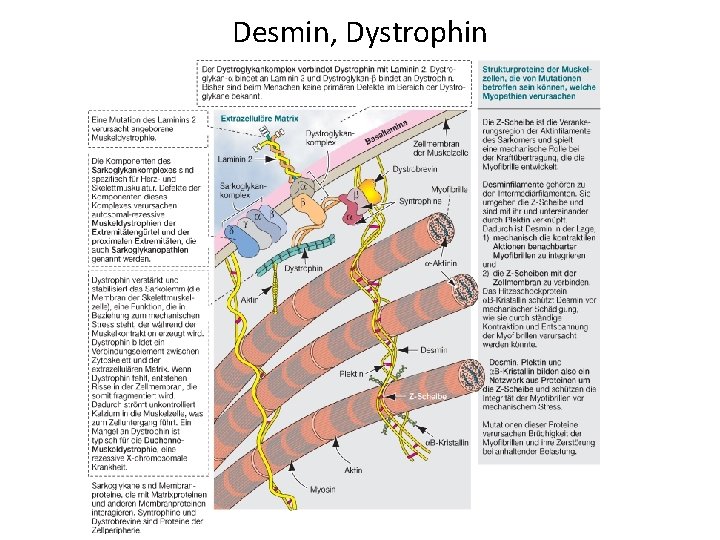
Desmin, Dystrophin
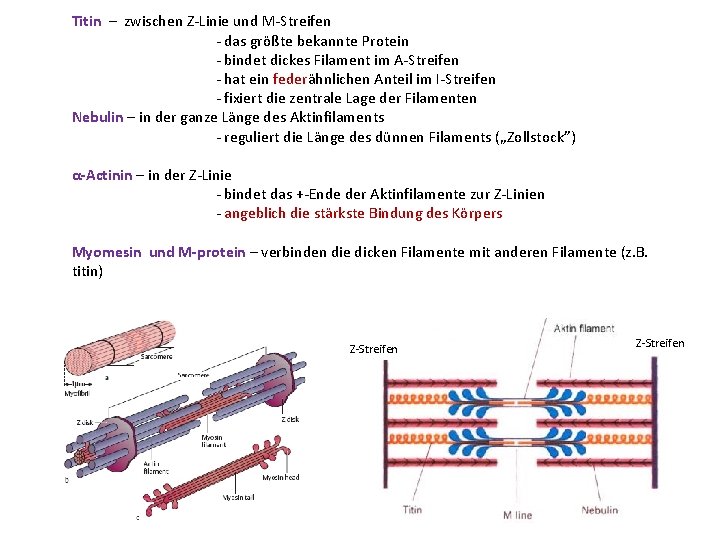
Titin – zwischen Z-Linie und M-Streifen - das größte bekannte Protein - bindet dickes Filament im A-Streifen - hat ein federähnlichen Anteil im I-Streifen - fixiert die zentrale Lage der Filamenten Nebulin – in der ganze Länge des Aktinfilaments - reguliert die Länge des dünnen Filaments („Zollstock”) α-Actinin – in der Z-Linie - bindet das +-Ende der Aktinfilamente zur Z-Linien - angeblich die stärkste Bindung des Körpers Myomesin und M-protein – verbinden die dicken Filamente mit anderen Filamente (z. B. titin) Z-Streifen
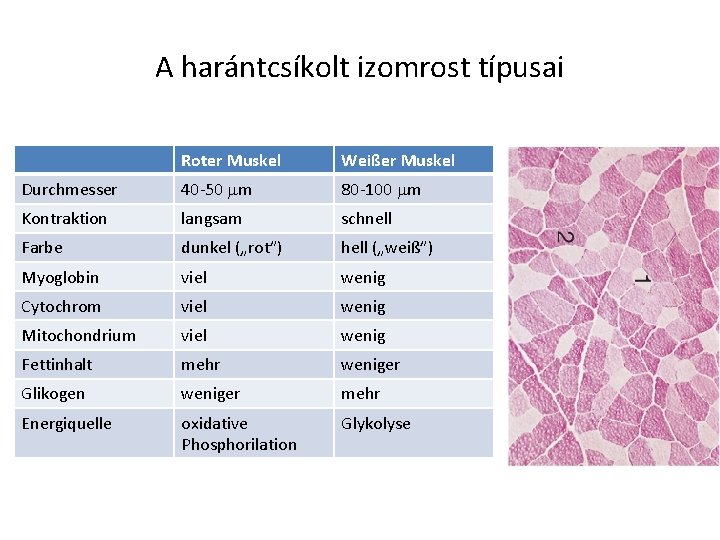
A harántcsíkolt izomrost típusai Roter Muskel Weißer Muskel Durchmesser 40 -50 mm 80 -100 mm Kontraktion langsam schnell Farbe dunkel („rot”) hell („weiß”) Myoglobin viel wenig Cytochrom viel wenig Mitochondrium viel wenig Fettinhalt mehr weniger Glikogen weniger mehr Energiquelle oxidative Phosphorilation Glykolyse
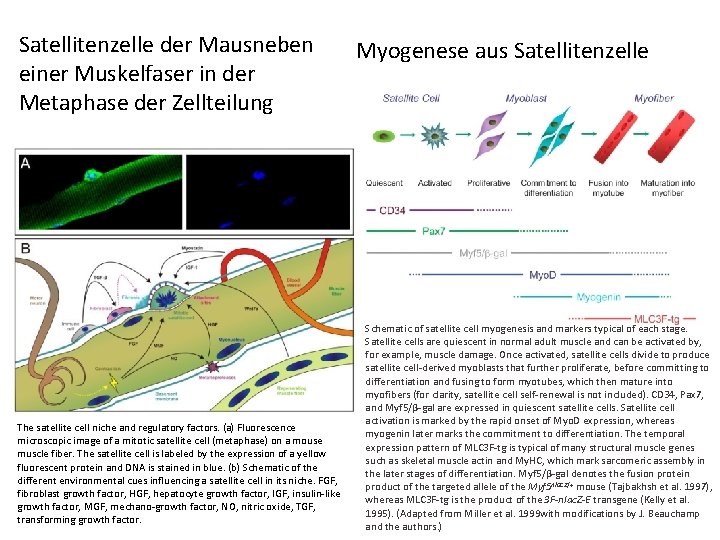
Satellitenzelle der Mausneben einer Muskelfaser in der Metaphase der Zellteilung The satellite cell niche and regulatory factors. (a) Fluorescence microscopic image of a mitotic satellite cell (metaphase) on a mouse muscle fiber. The satellite cell is labeled by the expression of a yellow fluorescent protein and DNA is stained in blue. (b) Schematic of the different environmental cues influencing a satellite cell in its niche. FGF, fibroblast growth factor, HGF, hepatocyte growth factor, IGF, insulin-like growth factor, MGF, mechano-growth factor, NO, nitric oxide, TGF, transforming growth factor. Myogenese aus Satellitenzelle Schematic of satellite cell myogenesis and markers typical of each stage. Satellite cells are quiescent in normal adult muscle and can be activated by, for example, muscle damage. Once activated, satellite cells divide to produce satellite cell-derived myoblasts that further proliferate, before committing to differentiation and fusing to form myotubes, which then mature into myofibers (for clarity, satellite cell self-renewal is not included). CD 34, Pax 7, and Myf 5/β-gal are expressed in quiescent satellite cells. Satellite cell activation is marked by the rapid onset of Myo. D expression, whereas myogenin later marks the commitment to differentiation. The temporal expression pattern of MLC 3 F-tg is typical of many structural muscle genes such as skeletal muscle actin and My. HC, which mark sarcomeric assembly in the later stages of differentiation. Myf 5/β-gal denotes the fusion protein product of the targeted allele of the Myf 5 nlac. Z/+ mouse (Tajbakhsh et al. 1997), whereas MLC 3 F-tg is the product of the 3 F-nlac. Z-E transgene (Kelly et al. 1995). (Adapted from Miller et al. 1999 with modifications by J. Beauchamp and the authors. )

Herzmuskulatur
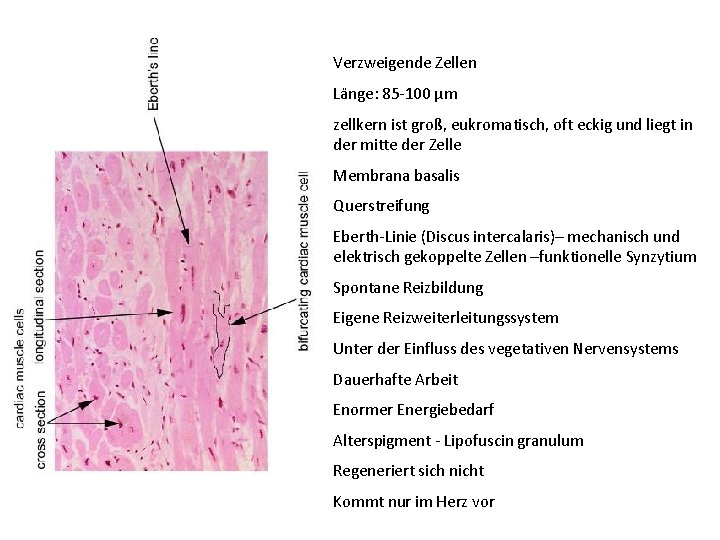
Verzweigende Zellen Länge: 85 -100 μm zellkern ist groß, eukromatisch, oft eckig und liegt in der mitte der Zelle Membrana basalis Querstreifung Eberth-Linie (Discus intercalaris)– mechanisch und elektrisch gekoppelte Zellen –funktionelle Synzytium Spontane Reizbildung Eigene Reizweiterleitungssystem Unter der Einfluss des vegetativen Nervensystems Dauerhafte Arbeit Enormer Energiebedarf Alterspigment - Lipofuscin granulum Regeneriert sich nicht Kommt nur im Herz vor

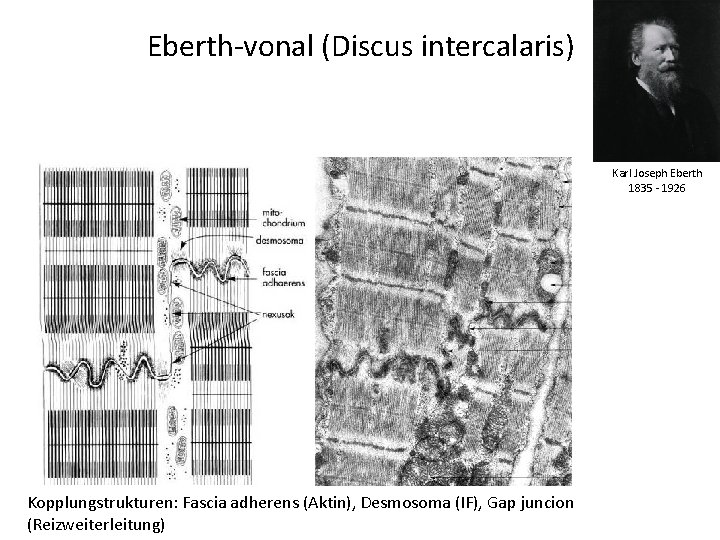
Eberth-vonal (Discus intercalaris) Karl Joseph Eberth 1835 - 1926 Kopplungstrukturen: Fascia adherens (Aktin), Desmosoma (IF), Gap juncion (Reizweiterleitung)
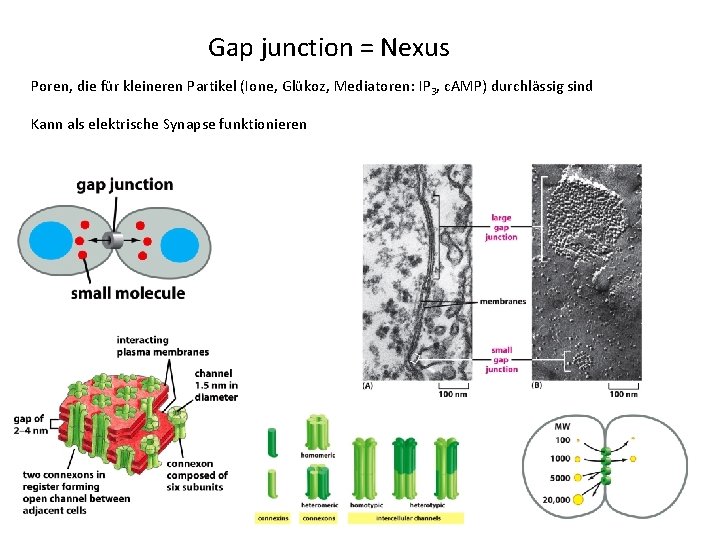
Gap junction = Nexus Poren, die für kleineren Partikel (Ione, Glükoz, Mediatoren: IP 3, c. AMP) durchlässig sind Kann als elektrische Synapse funktionieren
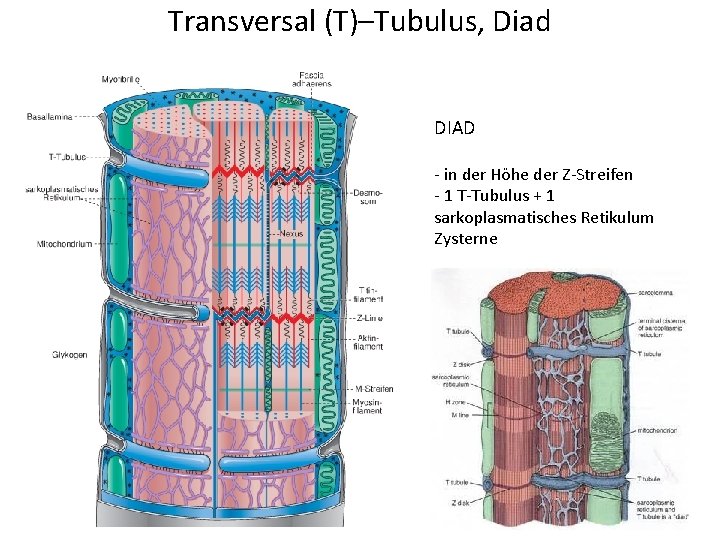
Transversal (T)–Tubulus, Diad DIAD - in der Höhe der Z-Streifen - 1 T-Tubulus + 1 sarkoplasmatisches Retikulum Zysterne
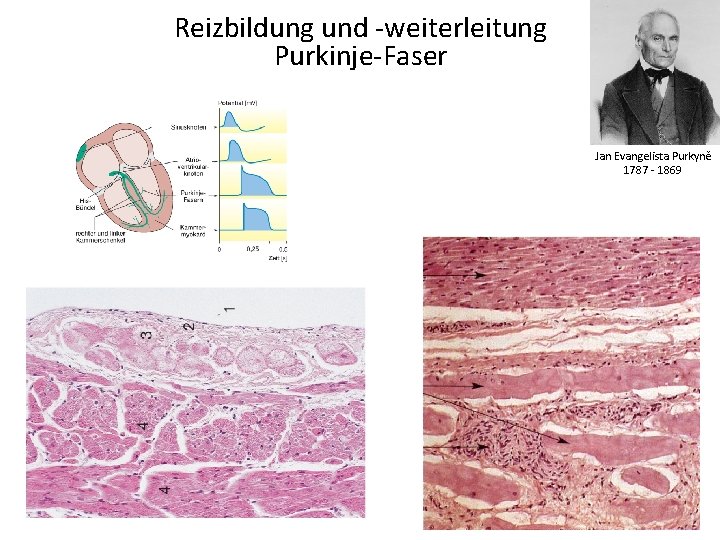
Reizbildung und -weiterleitung Purkinje-Faser Jan Evangelista Purkyně 1787 - 1869
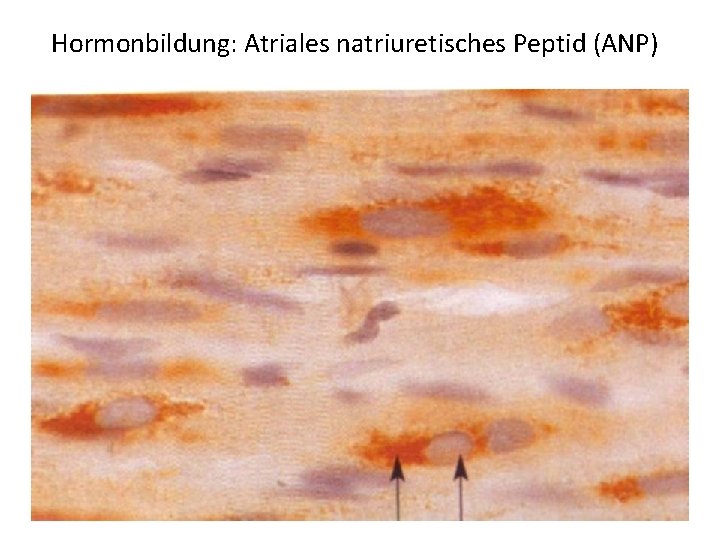
Hormonbildung: Atriales natriuretisches Peptid (ANP)

Glatte Muskulatur
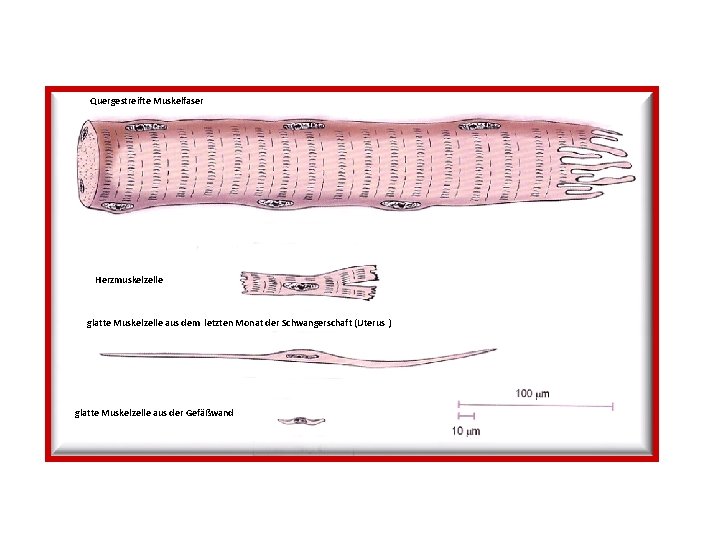
Quergestreifte Muskelfaser Herzmuskelzelle glatte Muskelzelle aus dem letzten Monat der Schwangerschaft (Uterus ) glatte Muskelzelle aus der Gefäßwand
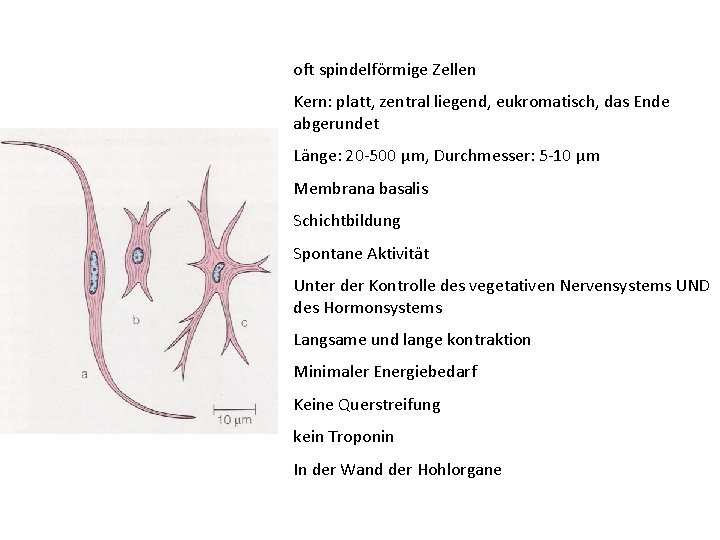
oft spindelförmige Zellen Kern: platt, zentral liegend, eukromatisch, das Ende abgerundet Länge: 20 -500 μm, Durchmesser: 5 -10 μm Membrana basalis Schichtbildung Spontane Aktivität Unter der Kontrolle des vegetativen Nervensystems UND des Hormonsystems Langsame und lange kontraktion Minimaler Energiebedarf Keine Querstreifung kein Troponin In der Wand der Hohlorgane



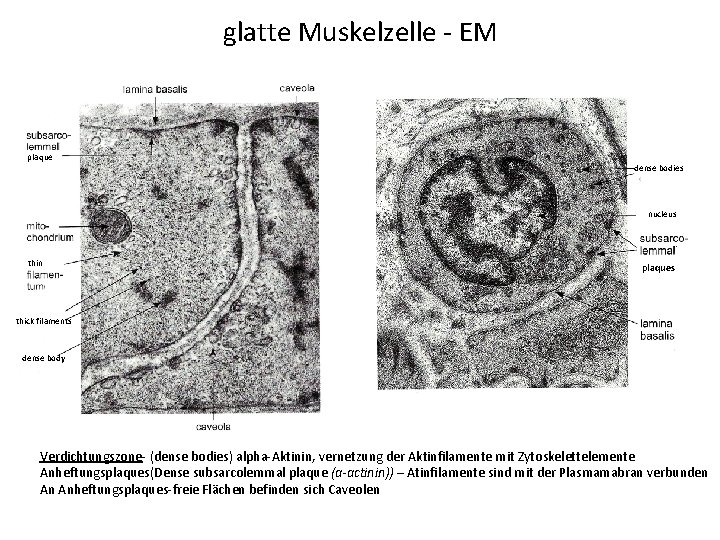
glatte Muskelzelle - EM plaque dense bodies nucleus thin plaques thick filaments dense body Verdichtungszone- (dense bodies) alpha-Aktinin, vernetzung der Aktinfilamente mit Zytoskelettelemente Anheftungsplaques(Dense subsarcolemmal plaque (ɑ-actinin)) – Atinfilamente sind mit der Plasmamabran verbunden An Anheftungsplaques-freie Flächen befinden sich Caveolen

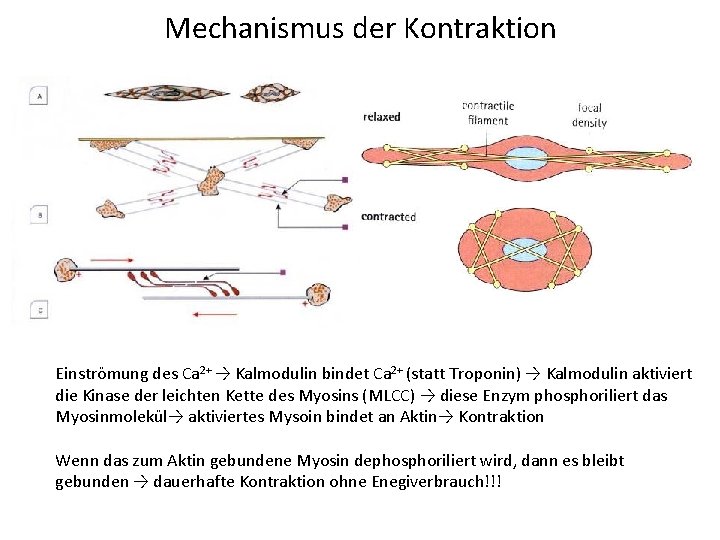
Mechanismus der Kontraktion Einströmung des Ca 2+ → Kalmodulin bindet Ca 2+ (statt Troponin) → Kalmodulin aktiviert die Kinase der leichten Kette des Myosins (MLCC) → diese Enzym phosphoriliert das Myosinmolekül→ aktiviertes Mysoin bindet an Aktin→ Kontraktion Wenn das zum Aktin gebundene Myosin dephosphoriliert wird, dann es bleibt gebunden → dauerhafte Kontraktion ohne Enegiverbrauch!!!

Typen der glatten Muskelzelle Multiunit: - eigenständige Zellen mit separierter Innervation (keine elektrische Kopplung) - fein Regulierbar - Kontraktion nur durch der Innervation Beispiel: m. sphincter pupillae, m. ciliaris Single unit: - elektrische und mechanische Kopplung (Gap junction) - funktionelle Einheit, funktionelle Synzytium - Innervation ist weniger wichtig -fast alle glatte Muskeln Beispeil: Wand der Hohlorgane

Danke für Ihre Aufmerksamkeit!

Literatur • Renate Lüllmann-Rauch : Histologie, 2. Auflage, Thieme, Stuttgart • Ulrich Welsch : Sobotta Lehrbuch Histologie, 2. Auflage Urban & Fischer Verlag • Röhlich Pál: Szövettan. Budapest, 1999 • A szövettani képek nagy része az Anatómiai, Szövet- és Fejlődéstani Intézet gyűjteményéből származik. • L. C. Junqueira et al. : Basic Histology • A. Faller, M. Schuenke: The Human Body, 2004, Thieme, Stuttgart-New York • Carola R, Harley JP, Noback CR: Human Anatomy & Physiology, Mc. Graw-Hill Inc. , USA, 1990 • Berne R et al: Physiology, 5 th edition, 2004, Elsevier Inc. • Von der Vorlesungen von Dr. Nemeskéri Ágnes, Dr. Szabó Arnold, Dr. H-Minkó Krisztina
- Slides: 46