MTODOS DE SEPARACIN MEZCLAS HOMOGNEAS OBJETIVO Conocer y

MÉTODOS DE SEPARACIÓN MEZCLAS HOMOGÉNEAS

OBJETIVO • _ Conocer y aplicar los métodos de separación de las mezclas homogéneas. • _ Discriminar cuando es posible usar un método u otro
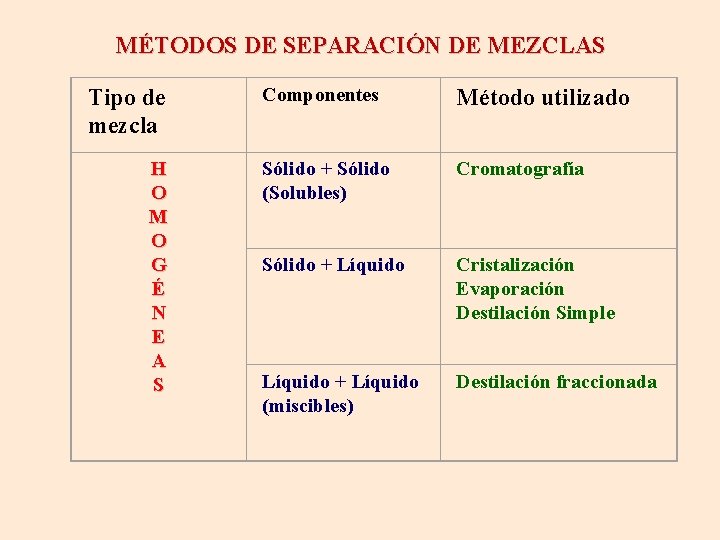
MÉTODOS DE SEPARACIÓN DE MEZCLAS Tipo de mezcla H O M O G É N E A S Componentes Método utilizado Sólido + Sólido (Solubles) Cromatografía Sólido + Líquido Cristalización Evaporación Destilación Simple Líquido + Líquido (miscibles) Destilación fraccionada
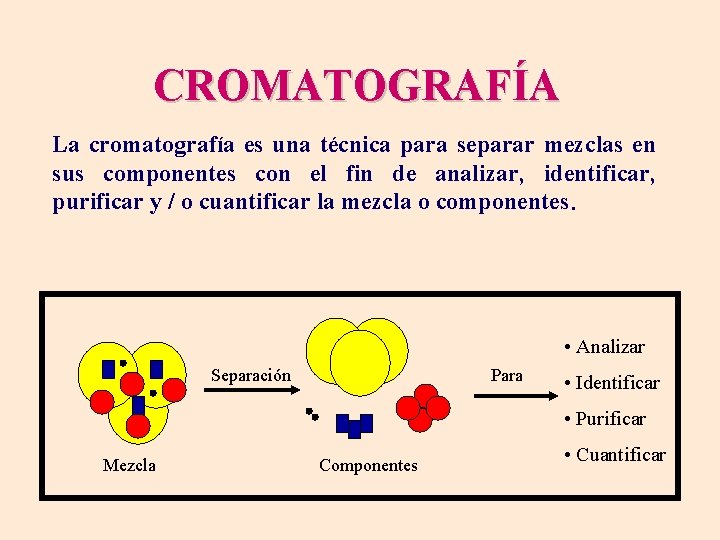
CROMATOGRAFÍA La cromatografía es una técnica para separar mezclas en sus componentes con el fin de analizar, identificar, purificar y / o cuantificar la mezcla o componentes. • Analizar Separación Para • Identificar • Purificar Mezcla Componentes • Cuantificar

SE USA PARA: • Analizar – examinar una mezcla, sus componentes relaciones entre ellos • y las Identificar – determinar la identidad de una mezcla o componentes, basados en componentes conocidos • Purificar – separar los componentes con el fin de aislar uno, para estudiarlo de forma particular • Cuantificar – determinar la cantidad de una mezcla y /o la cantidad de componentes presentes en la mezcla

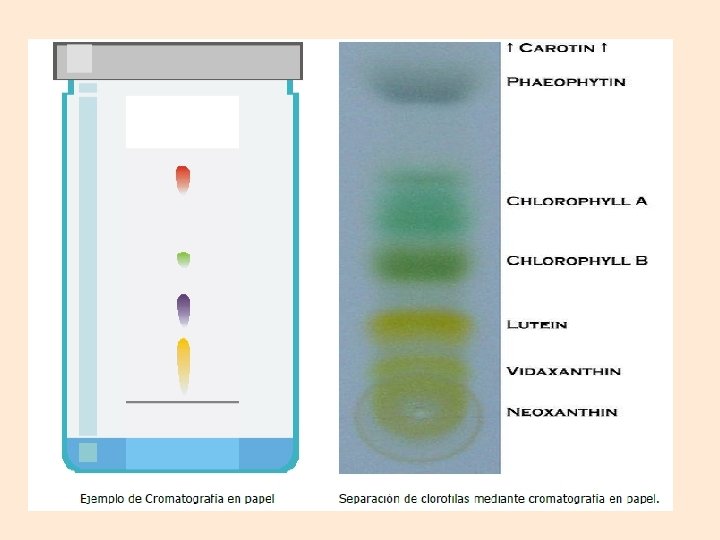
Ejemplos: • Separar los colorantes de un caramelo • Obtener los tintes de una tinta • Separar los pigmentos de una hoja • Separar los aminoácidos de una proteína

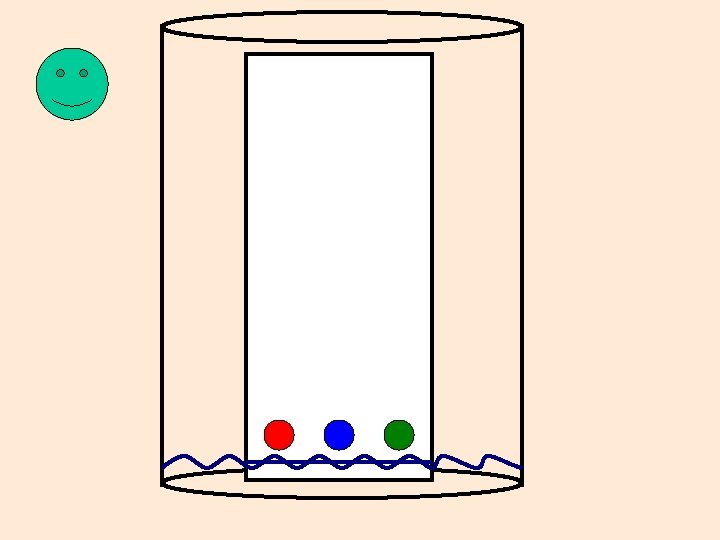
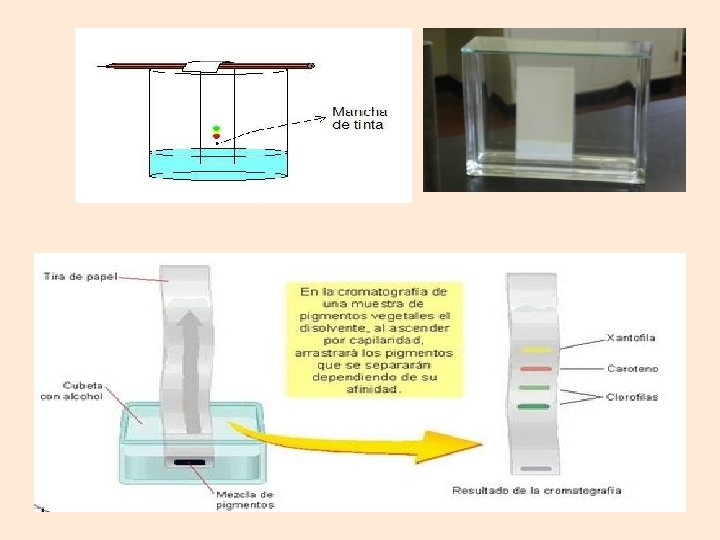
• La cromatografía es un procedimiento que se emplea para separar los distintos componentes de una mezcla homogénea aprovechando su diferente afinidad por un solvente. • En todas las técnicas cromatográficas hay una fase movil, puede ser un líquido o un gas, y una fase estacionaria, que suele ser un sólido. Los componentes de la mezcla interaccionan en distinta forma con la fase estacionaria. De este modo, los componentes atraviesan la fase estacionaria a distintas velocidades y se van separando

Procedimiento para separar los tintes de una tinta Se pone una gota de la muestra de tinta en el papel cromatográfico. Se pone papel en la cámara cromatográfica provista de solvente de arrastre.
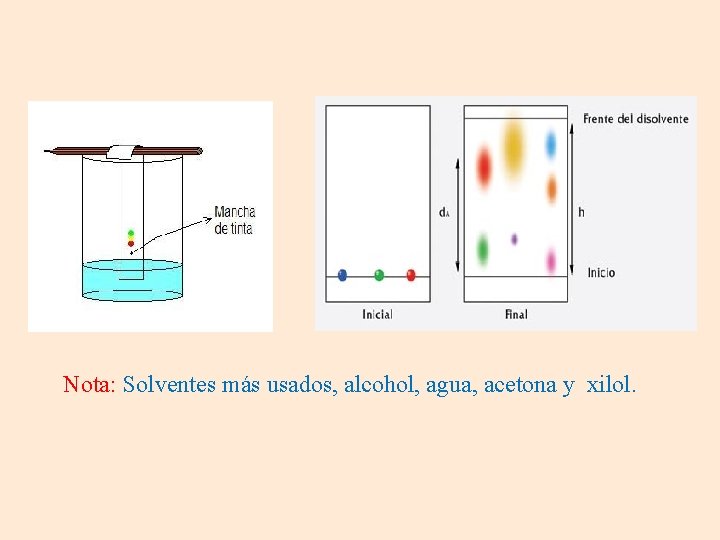
Nota: Solventes más usados, alcohol, agua, acetona y xilol.
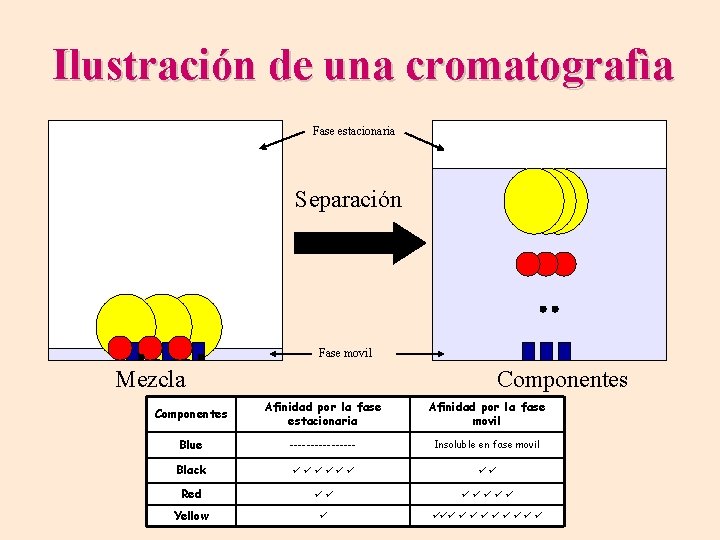
Ilustración de una cromatografìa Fase estacionaria Separación Fase movil Mezcla Componentes Afinidad por la fase estacionaria Afinidad por la fase movil Blue -------- Insoluble en fase movil Black Red Yellow


CRISTALIZACIÓN

• La cristalización es un procedimiento que se emplea para separar mezclas homogéneas de un sólido disuelto en un líquido. • Esta técnica consiste en hacer que cristalice un soluto sólido con objeto de separarlo del disolvente en el que está disuelto. Para ello es conveniente evaporar parte del disolvente o dejar que el proceso ocurra a temperatura ambiente.

• Si la evaporación es rápida se obtienen cristales pequeños y, si es lenta, se formarán cristales de mayor tamaño
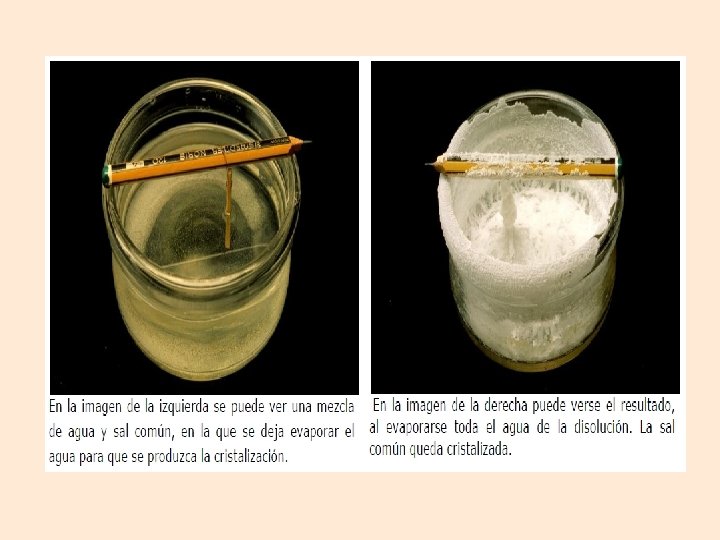

• Si la evaporación es rápida se obtienen cristales pequeños y, si es lenta, se formarán cristales de mayor tamaño
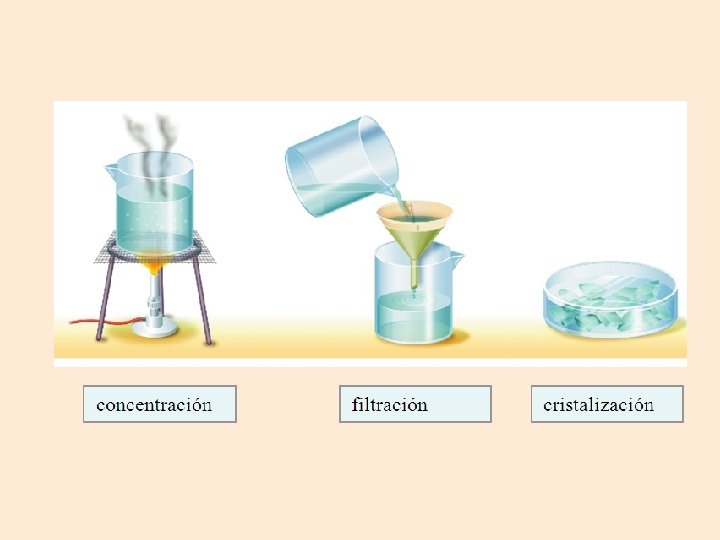
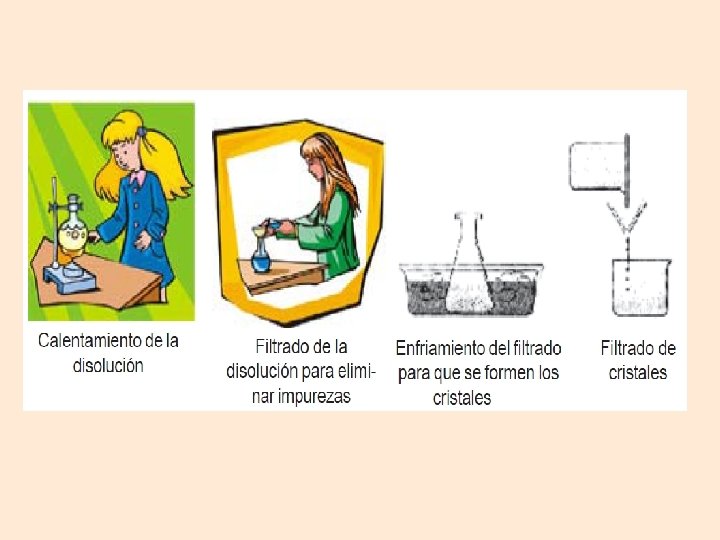
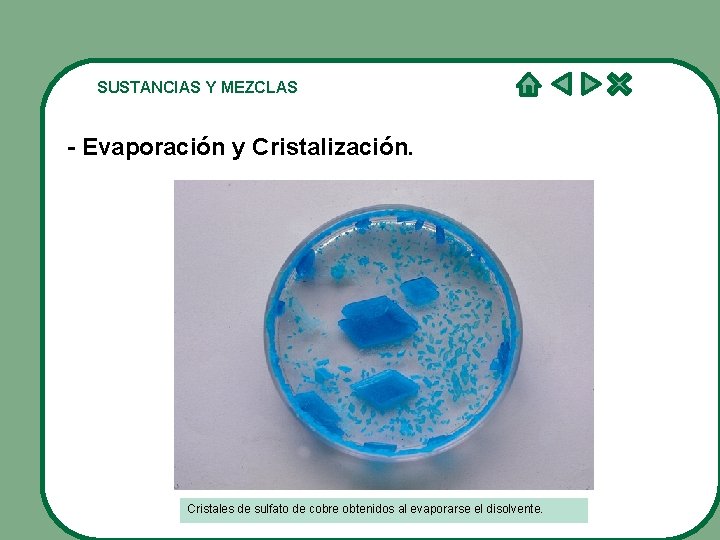
SUSTANCIAS Y MEZCLAS - Evaporación y Cristalización. Cristales de sulfato de cobre obtenidos al evaporarse el disolvente.

SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA Evaporación y Cristalización En las salinas encontramos un claro ejemplo de evaporación. Sulfato de cobre obtenido por cristalización.

Se utiliza para separar un soluto sólido disuelto en un disolvente. Se Se deja Se disuelve evaporar eliminan en el las caliente impurezas. disolvente. todo el disolvent e posible. Se obtienen cristales muy puros.

Cristal de fosfato monoamónico presentado en el I Concurso de Cristalización Ciencia sobre Ruedas

EVAPORACIÓN • Este proceso separa las mezclas de sólidos con líquidos. Al colocar la mezcla al fuego, se calienta el líquido y pasa a estado gaseoso (se evapora) y el sólido permanece en el fondo del recipiente. • El procedimiento de evaporación consiste en separar los componentes más volátiles exponiendo una gran superficie de la mezcla. Al aplicar calor y una corriente de aire seco acelera el proceso.
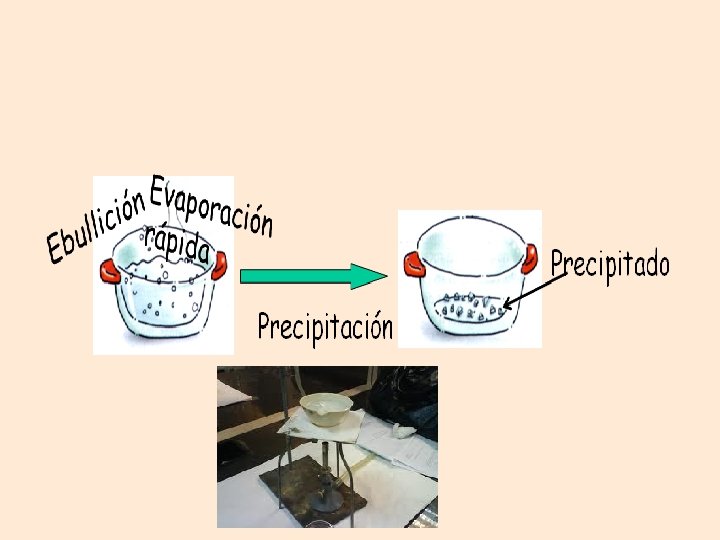

En algunas caletas del sur de Chile, aprovechan la marea alta para apozar el agua en piscinas artificiales y obtener por calentamiento del Sol sales no refinadas.

SALAR EN IQUIQUE

Evaporación y cristalización
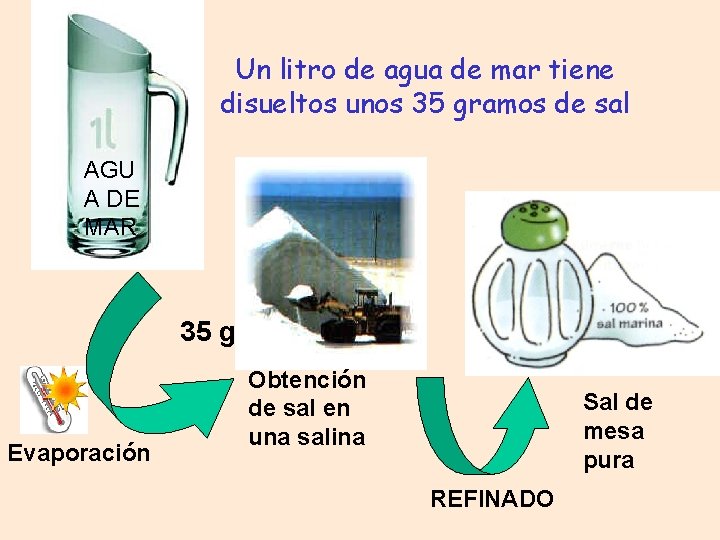
Un litro de agua de mar tiene disueltos unos 35 gramos de sal AGU A DE MAR 35 g Evaporación Obtención de sal en una salina Sal de mesa pura REFINADO

DESTILACIÓN • Existen dos tipos: Simple y fraccionada • Se basa en utilizar la diferencia en los puntos de ebullición de las sustancias mezcladas En este proceso ocurren dos cambios físicos: la evaporación y la condensación. La mezcla se calienta hasta el punto de ebullición y los vapores se enfrían en el condensador o refrigerante
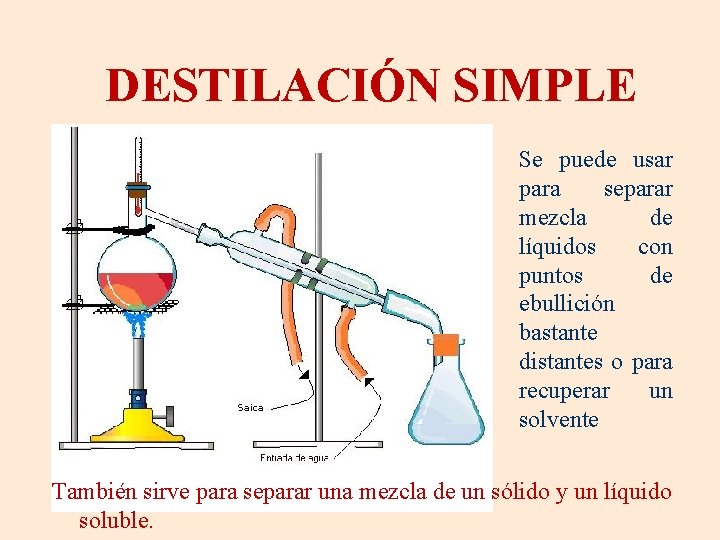
DESTILACIÓN SIMPLE Se puede usar para separar mezcla de líquidos con puntos de ebullición bastante distantes o para recuperar un solvente También sirve para separar una mezcla de un sólido y un líquido soluble.
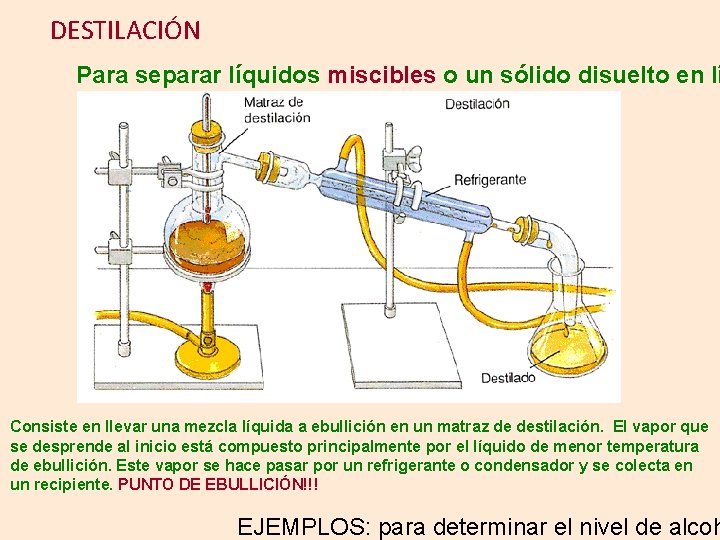
DESTILACIÓN Para separar líquidos miscibles o un sólido disuelto en lí Consiste en llevar una mezcla líquida a ebullición en un matraz de destilación. El vapor que se desprende al inicio está compuesto principalmente por el líquido de menor temperatura de ebullición. Este vapor se hace pasar por un refrigerante o condensador y se colecta en un recipiente. PUNTO DE EBULLICIÓN!!! EJEMPLOS: para determinar el nivel de alcoh
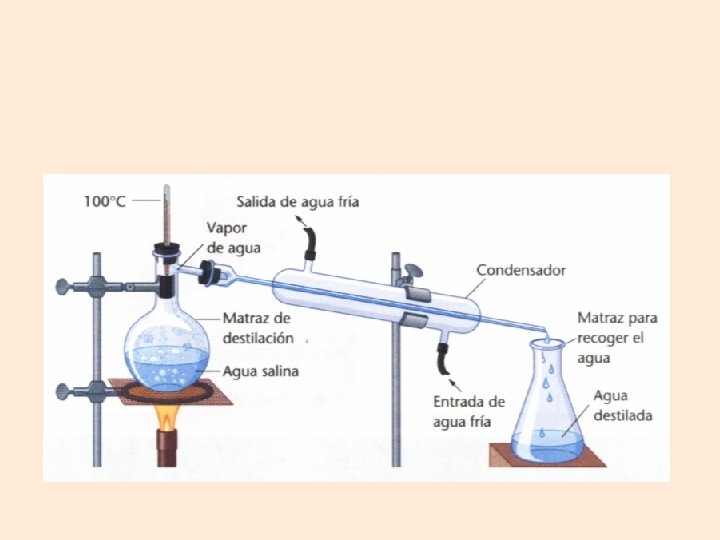
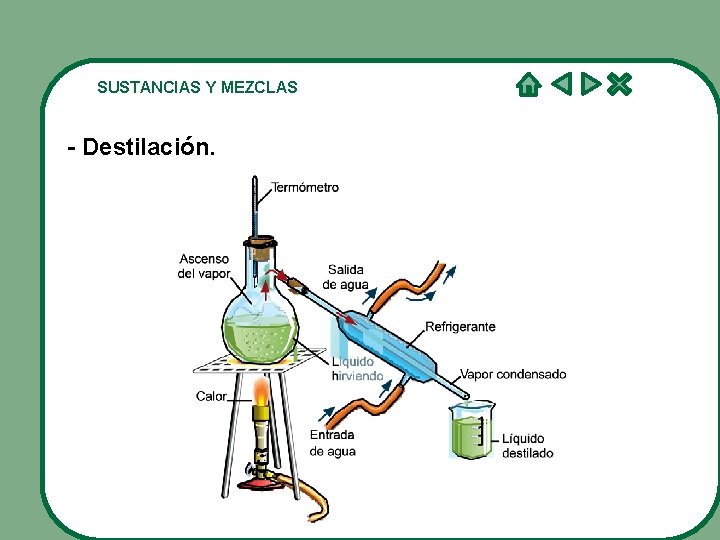
SUSTANCIAS Y MEZCLAS - Destilación.
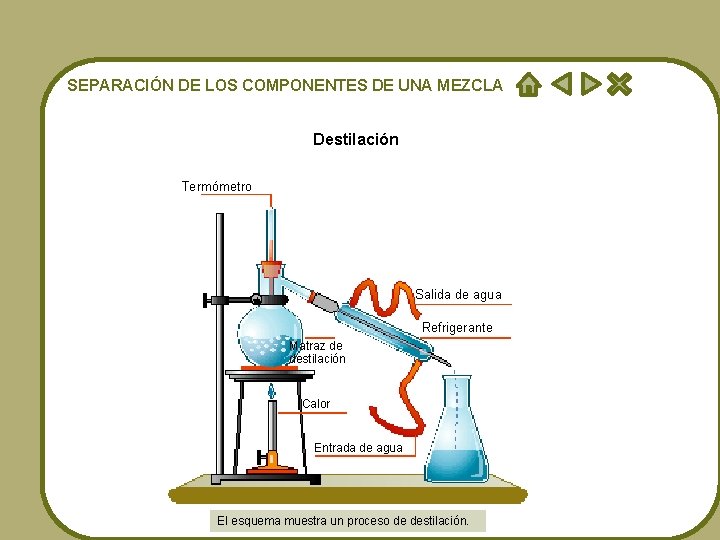
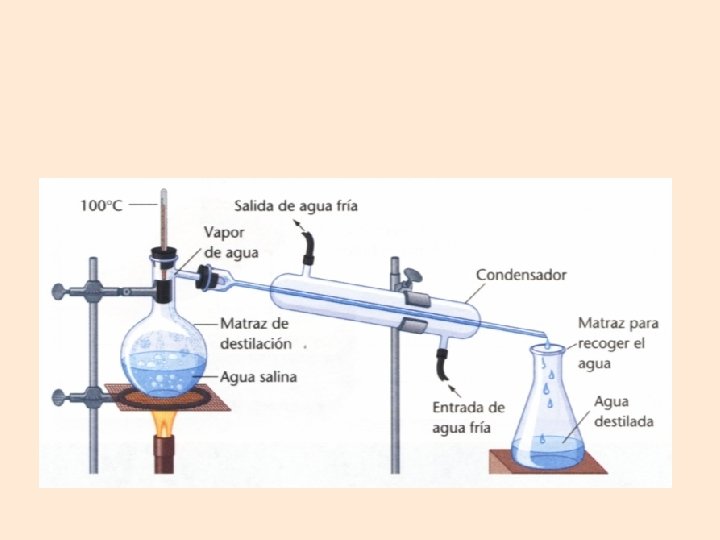
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA Destilación Termómetro Salida de agua Refrigerante Matraz de destilación Calor Entrada de agua El esquema muestra un proceso de destilación.
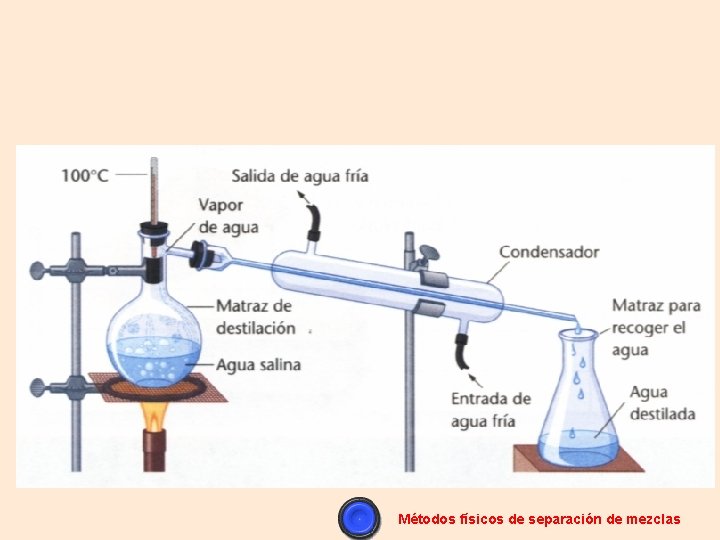
Métodos físicos de separación de mezclas
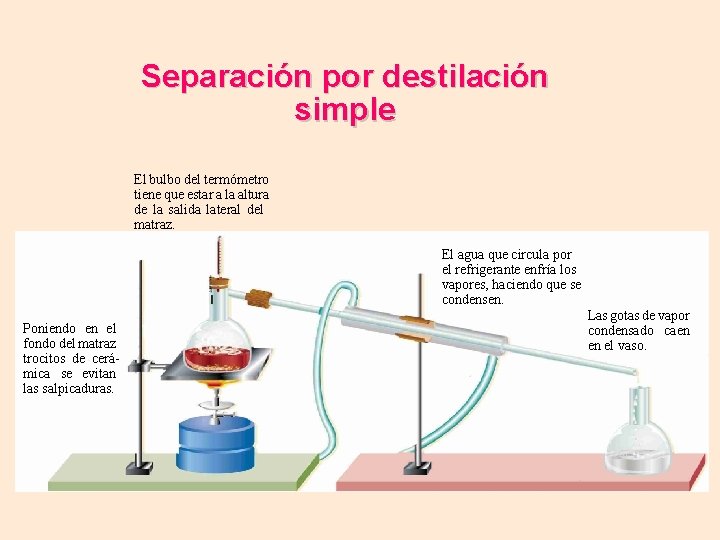
Separación por destilación simple El bulbo del termómetro tiene que estar a la altura de la salida lateral del matraz. El agua que circula por el refrigerante enfría los vapores, haciendo que se condensen. Poniendo en el fondo del matraz trocitos de cerámica se evitan las salpicaduras. Las gotas de vapor condensado caen en el vaso.
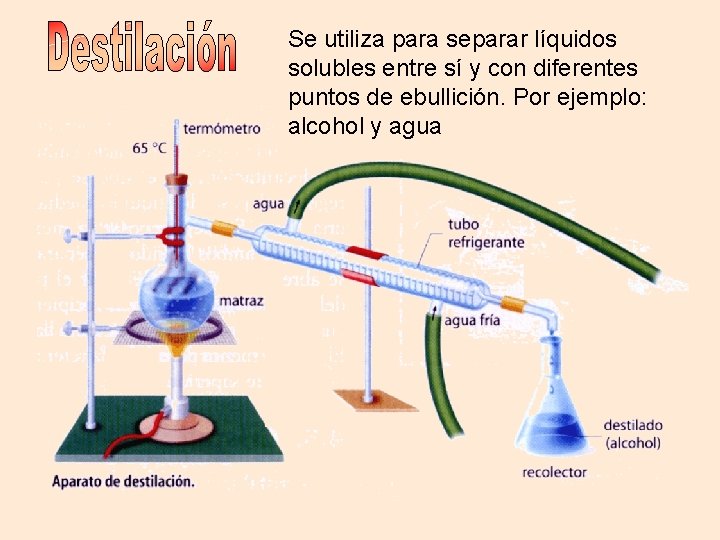
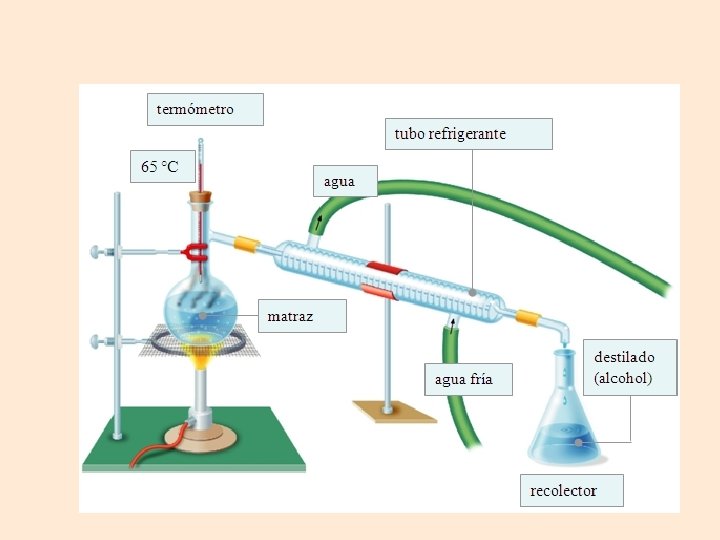
Se utiliza para separar líquidos solubles entre sí y con diferentes puntos de ebullición. Por ejemplo: alcohol y agua

§ Este método se usa para obtener el solvente de una solución o bien como método de purificación. Por ejemplo se puede obtener agua pura ( agua destilada) a partir de agua de la llave o bien agua pura a partir de agua de mar. Ejemplo: separar el agua de una solución de agua con sal. Procedimiento: • Se pone la mezcla en el matraz de destilación. • Se arma el aparataje de destilación simple.

• Se calienta suavemente evitando que se realice una ebullición violenta. • Finalmente se obtendrá en el vaso precipitado o matraz Erlenmeyer el líquido puro y en el matraz de destilación quedará la sal posiblemente con un poco de agua.
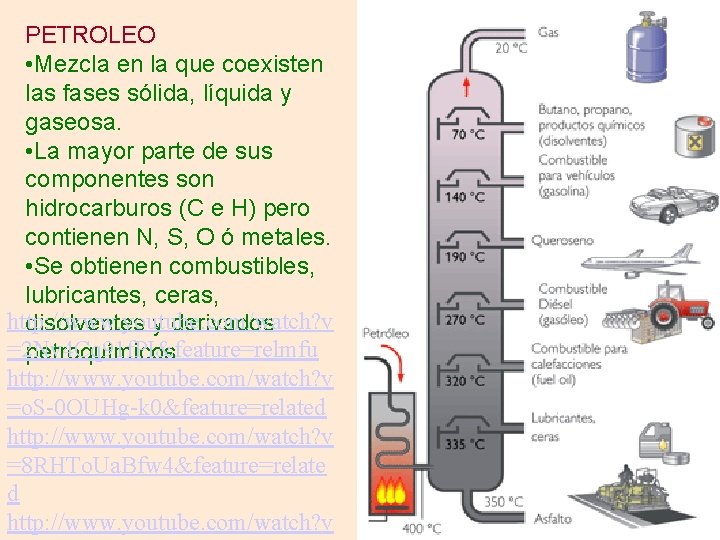
PETROLEO • Mezcla en la que coexisten las fases sólida, líquida y gaseosa. • La mayor parte de sus componentes son hidrocarburos (C e H) pero contienen N, S, O ó metales. • Se obtienen combustibles, lubricantes, ceras, http: //www. youtube. com/watch? v disolventes y derivados =2 Nv 4 Cq 91 f. PI&feature=relmfu petroquímicos. http: //www. youtube. com/watch? v =o. S-0 OUHg-k 0&feature=related http: //www. youtube. com/watch? v =8 RHTo. Ua. Bfw 4&feature=relate d http: //www. youtube. com/watch? v
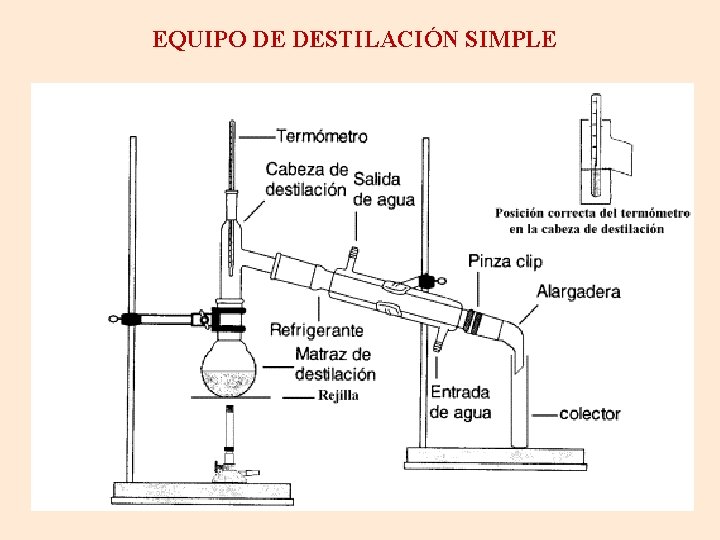
EQUIPO DE DESTILACIÓN SIMPLE

DESTILACIÓN FRACCIONADA

§ Este método se usa para separar líquidos miscibles (que se mezclan) y que tienen diferentes puntos de ebullición, aunque éstos estén muy próximos. Ejemplos más comunes: - separar las diferentes porciones del petróleo - separar el alcohol del vino Ejemplo: separar el alcohol del agua de una mezcla de agua con alcohol.

Procedimiento: • Se pone la mezcla en el matraz de destilación. • Se arma el aparataje de destilación fraccionada. • Se calienta suavemente la mezcla hasta llegar al punto de ebullición del líquido con menor punto de ebullición, momento en que se comienza a destilar el alcohol el cual ebulle a los 76, 5 ºC. La temperatura se mantiene constante hasta que todo el alcohol se destile. • Cuando la temperatura comience a subir significará que comenzará a destilar el agua.

• Cuando la disolución se calienta y comienza a hervir, los líquidos se separan porque tienen puntos de ebullición distintos, es decir, hierven a diferentes temperaturas. El líquido que hierve primero se evapora antes; los vapores se recogen en el tubo refrigerante, donde se enfrían y vuelven a condensarse pasando de nuevo al estado líquido. Este líquido, que se denomina destilado, se recoge luego en un vaso (recolector).
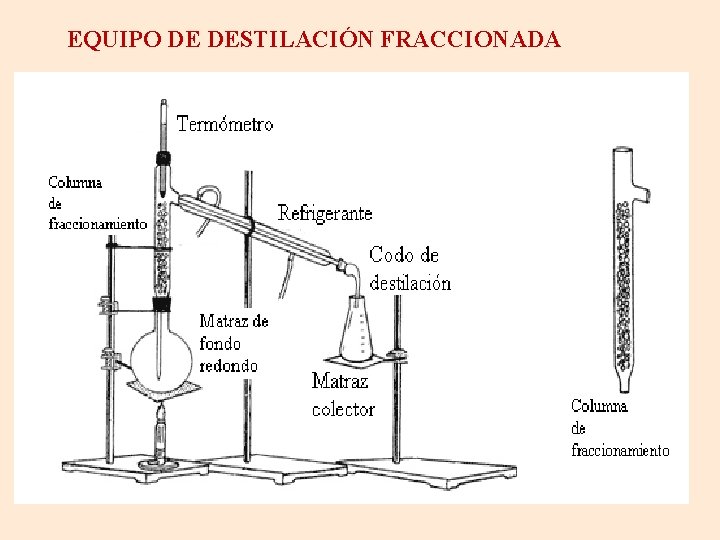
EQUIPO DE DESTILACIÓN FRACCIONADA

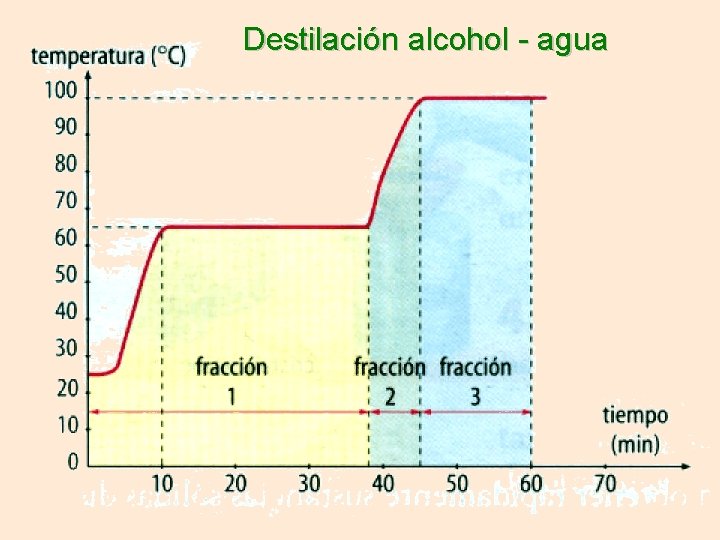
Destilación alcohol - agua
- Slides: 54