Mtabolisme microbien Gnralits sur les Archaea Halophiles Toute

Métabolisme microbien Généralités sur les Archaea Halophiles

ØToute cellule vivante qu'elle provienne d'organismes unicellulaires « primitifs» ou fasse partie d'organes très évolués comme le cerveau, baigne dans une solution saline qui contient essentiellement du chlorure de sodium (Na. Cl) et renferme une concentration équivalente en chlorure de potassium (KCl). ØDe nombreuses fonctions vitales (le battement du cœur, la transmission nerveuse, etc. ) dépendent étroitement des gradients de concentration en Na. Cl et en KCl de part et d'autre de la membrane cellulaire. A faible concentration, le sel est donc indispensable au fonctionnement de la cellule. ØMais à fortes doses il empêche la vie. Voilà pourquoi la salaison est traditionnellement utilisée pour conserver des aliments : la plupart des micro organismes responsables de pourriture ne peuvent se développer dans un environnement très salin. En effet ; une différence importante de concentration en sel entre l'intérieur et le milieu extérieur provoque la sortie de l'eau.

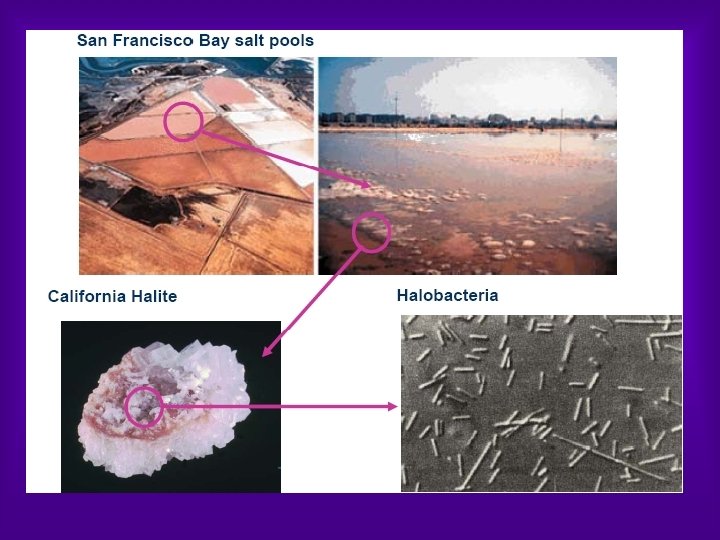
ØTrop de sel entraîne la mort des cellules : on pourrait donc légitimement s'attendre à ce que les milieux hypersalés soient absolument stériles. Il n'en est rien, Ø Des communautés de micro organismes prolifèrent dans les écosystèmes où le sel (essentiellement du Na. Cl) a été concentré par évaporation à la limite de sa solubilité (360 g/l), soit plus de dix fois la concentration de l'eau de mer. ØCes «microbes du sel » représentent la seule forme de vie possible dans les grands lacs salés de l'Ouest américain, le lac Rose au Sénégal, la mer Morte en Palestine ou dans les marais salants des côtes de France.

Métabolisme microbien Environnements Hypersalins

Les milieux hypersalés Ø On appelle plus généralement milieu hypersalé ou sursalé, les milieux dont la teneur en sels dissout est supérieure à celle de l'eau de mer. Lorsque l'on dépasse 100 g/l en sels, les milieux deviennent extrêmes et inhibent la croissance d'une grande majorité de micro organismes. Ø Parmi ces milieux, on trouve divers lacs continentaux des zones désertiques ou sub désertiques, des lagunes maritimes, les marais salants etc. Les eaux sont souvent riches en chlorure de sodium mais il existe également des milieux où dominent les carbonates ou les sulfates. Ces milieux, bien que restreints à la surface de la planète, sont habités par des formes microbiennes très bien adaptées.

s e l i h alop H Lac rose au Sénégal

Les marais salants

Origine des milieux hypersalés Ø En ce qui concerne les "eaux salées", l'origine des sels est, le plus souvent, l'eau de mer. Ø La quantité de sels dissout dans les mers ou océans a été estimée à 4, 26 1016 tonnes. On y trouve principalement 11 ions différents: Na*, K+, Mg 2+, Ca 2+, Sr 2+ Cl , S 042 , HCO 3 , Br , F et BO 3. Ø Pour ces écosystèmes, la concentration maximale en sels totaux observée est de 350 g/l. A partir de cette limite le Na. Cl commence à précipiter et le magnésium devient le composé prépondérant. De tels systèmes peuvent être issus de l'activité humaine comme par exemple, les marais salants qui sont des systèmes artificiels assez largement répandus à travers le monde. Ø De par leur origine, ces lacs ou mers hypersalés présentent la particularité de posséder une composition chimique dont les rapports en ions sont comparables à ceux trouvés dans l'eau de mer.

Ø La deuxième catégorie des systèmes hypersalés est d'origine continentale puisqu'elle provient de la dissolution, par action des eaux de pluies ou des eaux de ruissellements, des sels contenues dans les roches ou les couches géologiques traversées. Ø Ces sels sont alors concentrés par évaporation comme dans le cas précédant, lorsque ces eaux se trouvent accumulées dans des bassins imperméables. Dans ce cas chaque lac salé est unique par sa composition chimique. Ø On peut cependant classer ces lacs en 2 catégories selon l'anion qui prédomine : les lacs sulfateux et les lacs contenant du carbonate (lacs alcalin de l'est africain). Ø Si dans les premiers environnements une flore ubiquiste peut être trouvée, les seconds présentent souvent une biodiversité restreinte et spécifique de son biotope.
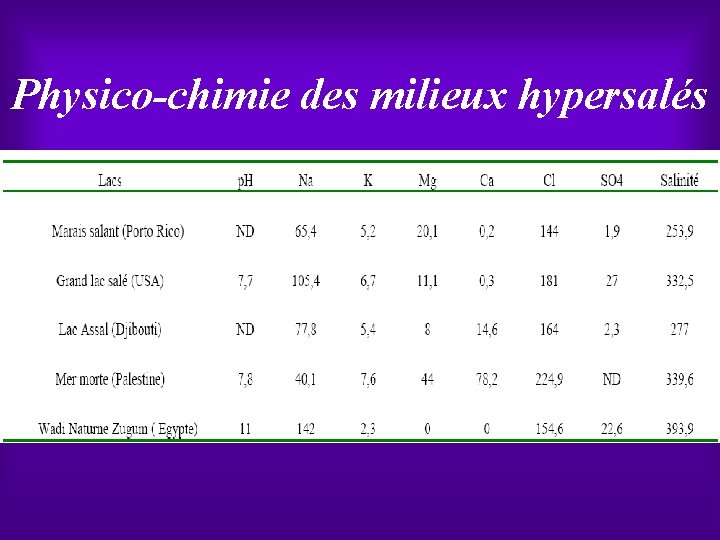
Physico-chimie des milieux hypersalés

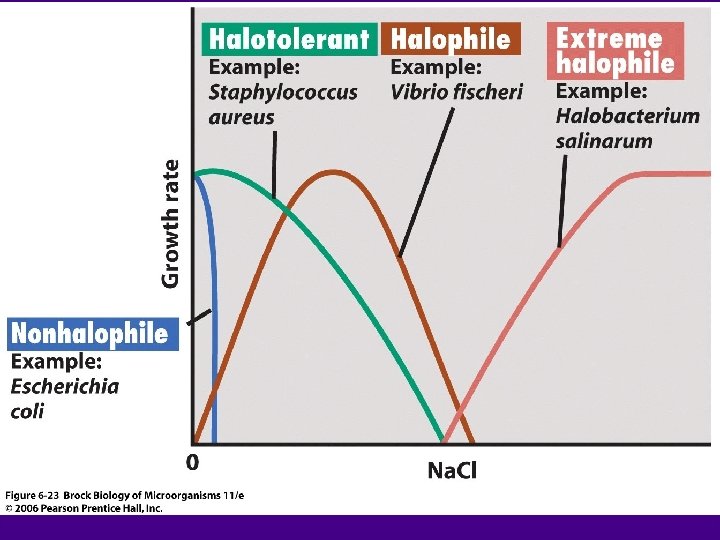
Les organismes des milieux hypersalés Ø Le terme "halophile" est utilisé pour des organismes poussant obligatoirement en présence de sels (généralement le Na. Cl). Ø On doit tout d'abord faire une distinction entre les organismes halophiles et les organismes qui peuvent tolérer le sel même s'il est présent en grande quantité (halotolérance). Les bactéries nécessitant moins de 20 g/l de sels pour une croissance optimale ne sont pas considérées comme des organismes halophiles. Ø Larsen (1986) définit 3 catégories de bactéries halophiles selon la concentration en sels qui amène à une croissance optimale des micro organismes (Figure 1. 3). Ø La limite séparant les deux derniers groupes n'étant pas très claire, certains auteurs avaient quelques difficultés à classer les organismes. Ø Kushner en 1999, modifia la définition de Larsen en incluant une nouvelle catégorie : les bactéries halophiles extrêmes limites "Borderline extrême halophile" dont l'optimum de croissance se situe entre 180 et 240 g/l.
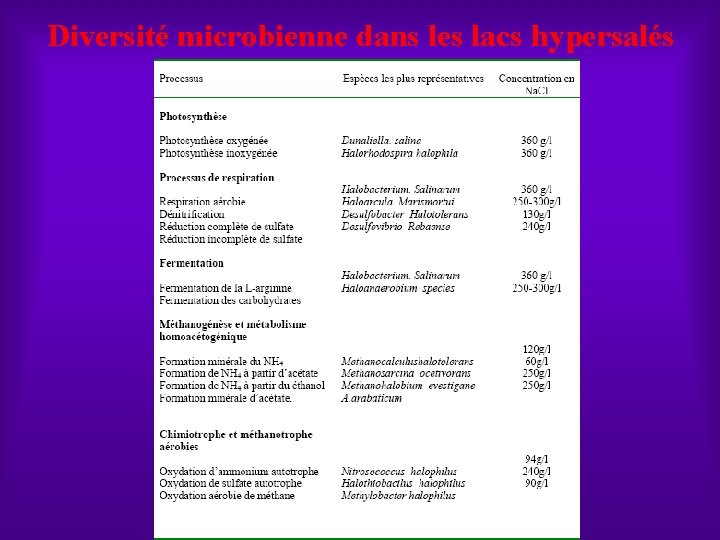
Diversité microbienne dans les lacs hypersalés


Osmorégulation Ø En condition de forte salinité, l'eau contenue dans la cellule se déplace vers le milieu externe en provoquant une diminution du volume cellulaire qui, lorsqu'elle est trop importante, peut provoquer la dormance ou la mort de la cellule. Ø Si par contre, la cellule baigne dans un milieu à faible osmolarité le flux d'eau se fera en sens inverse en provoquant une turgescence de la cellule pouvant aller jusqu'à son éclatement si l'on dépasse le seuil d'élasticité de ses enveloppes. Ø La cellule doit toujours ajuster la pression osmotique intracytoplasmique par rapport à celle de son environnement immédiat. Ø Dans ce but, elle élabore des mécanismes de transports actifs à travers la membrane en mettant en oeuvre des processus endergoniques, dont la pompe à sodium qui refoule hors de la cellule les ions Na+ toxiques.
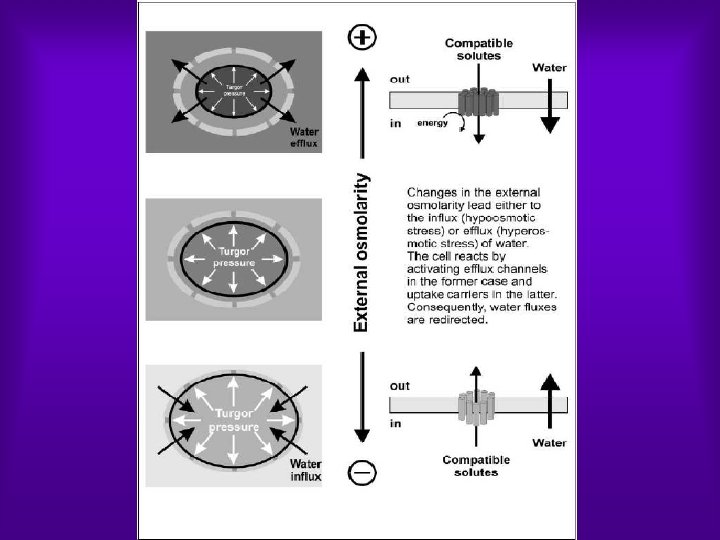

Osmorégulation chez les microorganismes Ø La composition ionique des milieux hypersalés change au cours du temps en fonction de l'évaporation ou d'assèchement d'eaux (précipitations). Ø Ces brusques variations ioniques conduisent les micro organismes à s'adapter rapidement à ces nouvelles conditions. Ø L'ensemble des mécanismes qui permettent aux cellules de contrôler cette pression osmotique interne représente l'osmorégulation. Ø Dans certains cas, la capacité d'une bactérie à croître dans un milieu hypertonique est fonction de la résistance de ses enveloppes, Ø Il existe aujourd'hui deux mécanismes qui préviennent les chocs osmotiques du milieu. v le transport d'ions à travers la membrane par des pompes ioniques v (b) la synthèse ou l'accumulation de molécules organiques.


Métabolisme microbien Halo enzymes

Adaptation des protéines à l’hypersalinité Ø Une protéine est naturellement constituée d’une chaîne d’acides aminés qui doit se replier de façon précise dans l’espace pour assurer la stabilité de l’ensemble. Ce repliement permet à la protéine de remplir sa fonction dans la cellule. Or pour qu’une protéine puisse se replier convenablement, elle doit être hydratée à sa surface. Ø Lorsqu’une protéine normale (non halophile) est plongée dans un solvant très salé. La couche d’hydratation nécessaire au repliement ne peut se former car les molécules d’eau sont toutes piégées par le sel du solvant. Résultat : la protéine devient insoluble et précipite. Ø Les organismes halophiles ne semblent pas connaître ce stress cellulaire : leurs protéines sont non seulement solubles et fonctionnent dans des fortes concentrations en KCl, mais elles se dénaturent dés que la concentration en sel diminue. En ce sens, on peut dire que ces protéines sont elles même halophiles.

Ø Pour expliquer la solubilité des protéines halophiles, on a d’abord pensé que ces dernières possédaient une couche d’hydratation renforcée. Ø il a été démontré qu’au contraire, les protéines halophiles concentraient fortement le sel prés de leur surface. Une protéine halophile associe environ 10% de sa masse en KCl et de 40% en eau. Ø Des mesures équivalentes sur des protéines non halophiles donnent 0% de KCl, et 20% à 40% d’eau. Ø Ainsi, au lieu de se protéger du sel, comme les protéines conventionnelles, elles l’associent à leur structure et l’utilisent pour capturer les molécules d’eau nécessaire à leur repliement, leur stabilisation et leur solubilité. Ø Cette couche de sel et d’eau forme une sorte de cage qui empêche la protéine de se déplier. Mais comment cette dernière attire t elle le sel à sa surface ?

Ø En 1995, Eisenberg a obtenu la première structure cristallographique de protéines halophiles issues de la mer Morte, la malate déshydrogénase de Halorcula marismortui et la ferrédoxine du même organisme. Ø Ces deux protéines se distinguent de leurs homologues non halophiles principalement par la nature chimique des acides aminés situés à leur surface. Elles sont en effet recouvertes d’acides aminés « acides » c’est à dire chargés négativement. Ø Les études ultérieures ont montré que ce phénomène est généralisé à l’ensemble des protéines halophiles. Or ces groupements d’acides aminés acides sont connus pour interagir fortement avec les molécules d’eau et les ions positifs comme le K+
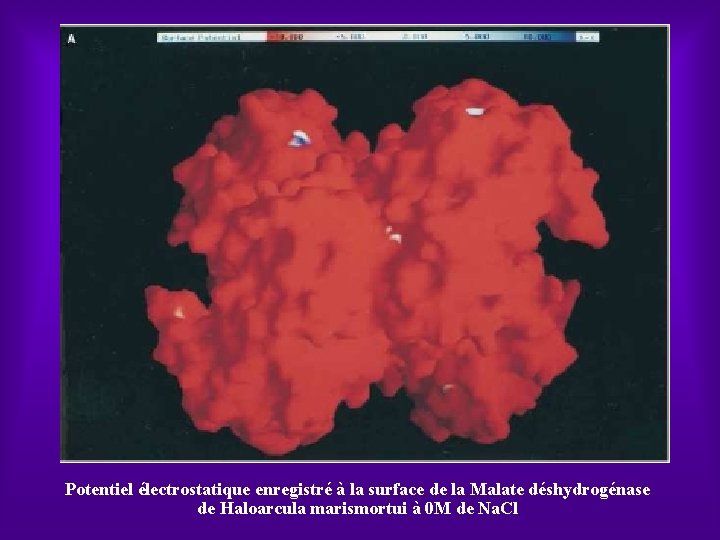
Potentiel électrostatique enregistré à la surface de la Malate déshydrogénase de Haloarcula marismortui à 0 M de Na. Cl
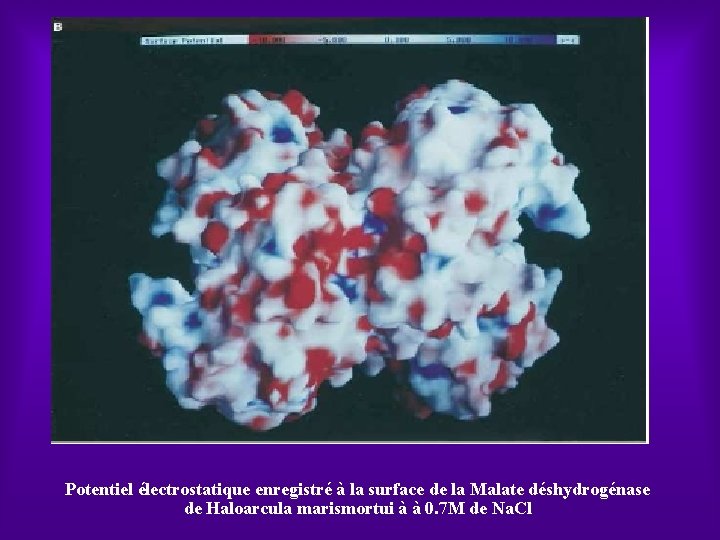
Potentiel électrostatique enregistré à la surface de la Malate déshydrogénase de Haloarcula marismortui à à 0. 7 M de Na. Cl
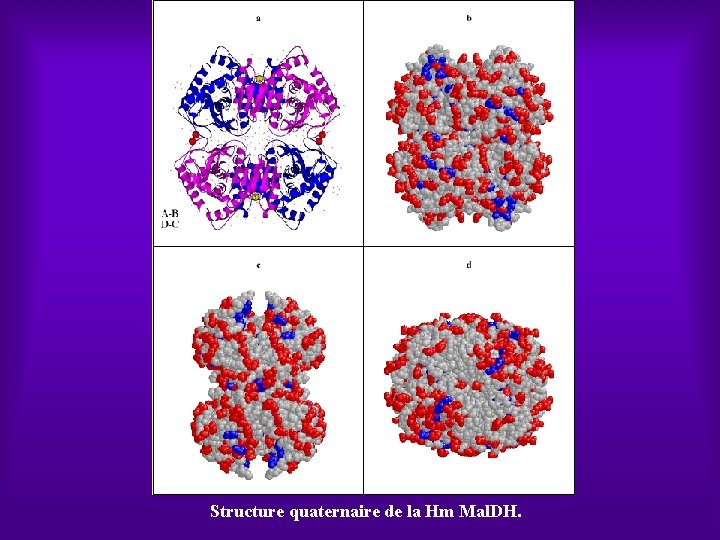
Structure quaternaire de la Hm Mal. DH.

Intérêt des holoenzymes en biotechnologie Ø La synthèse des produits d’intérêt par voie chimique est souvent entravée par le coût élevé et la faible sélectivité du processus de production ; ce qui génère des sous produits souvent Polluants. Ø Les enzymes mésophiles ne sont pas souvent bien adaptées aux conditions dures des réactions exigées dans les processus industrielles en raison du manque de la stabilité enzymatique. Ø Ceci explique pourquoi l’utilisation des biocatalyseurs dans les réactions organiques a représenté seulement une petite fraction du marché industriel potentiel du passé. Ø La découverte de nouveaux microorganismes extrêmophiles et de leurs enzymes avait un grand impact sur le domaine de la biocatalyse.

Ø Les organismes halophiles produisent de nombreux enzymes présentant un intérêt potentiel en bio industrie tels que les amylases , les protéases, Les glycosidases et les lipases. Cependant les seules haloenzymes disponibles à l’échelle industrielle sont des endonucléases de restriction. Ø Du fait que le Na. Cl diminue la Aw, Les enzymes issues d’organismes halophiles pourraient êtres utiles pour la biocatalyse en milieux organiques. En effet la Aw du Na. Cl saturée est de 0. 75 ; ce qui correspond à une concentration de DMSO de 60 % (v/v). Ø Un travail récent sur la catalase Halobacterium cutirubrum a montré que cette enzyme est très stable en milieu organique et présente un maximum d’activité à 2. 5 M de glycérol, éthylène glycol ou de DMSO. Ces solvants organiques dénaturent la catalase bovine.

Métabolisme microbien Biotechnologie des Archaea

Utilisation de cellules entières d’Archaea en biotechnologie Ø L’une des premières applications possibles est la biolixiviation utilisée essentiellement pour concentrer les métaux (cuivre, or et uranium) lorsque les concentrations initiales de minerai sont faibles et les procédés chimiques conventionnels non rentables. Ø Cette approche, développée en Afrique du Sud, au Brésil et en Australie, fait en général appel à des cultures de bactéries mésophiles des genres Thiobacillus, Acidithiobacillus et Leptospirillum. Toutefois, différents travaux ont mis en évidence l’intérêt des archées Pyrobaculum, Pyrococcus, Sulfolobus et Metallosphaera. Ø Un second type d’application est directement lié aux caractéristiques de certaines archées halophiles extrêmes. Seules espèces vivantes capables de se développer dans des saumures proches de la saturation, elles sont aussi les seules aptes à être utilisées en bioremédiation en cas de contamination par divers produits chimiques, métaux lourds, radionucléides ou composés halogénés. Ainsi, Haloferax mediterranei est capable d’utiliser le pétrole brut, Halobacterium sp.

Utilisation des lipides d’Archaea Ø Les lipides d’archées sont caractérisés notamment par la présence de liaisons éthers entre le glycérol et les chaînes d’acides gras et par les propriétés originales des lipides tétraéther bipolaires leur permettant de générer des films monocouches stables. Ø Ces lipides bipolaires atypiques jouent un rôle important dans l’adaptation aux conditions extrêmes des milieux où prolifèrent les archées. Ils ont également suscité un intérêt marqué pour leurs propriétés singulières et leurs applications biotechnologiques potentielles pour la réalisation de films lipidiques monocouches particuliers ou la production de liposomes d’archées (archaeosomes). Ø La stabilité des archaeosomes aux hautes températures, aux p. H alcalins, aux phospholipases, aux estérases et aux sels biliaires est très élevée : certains archaeosomes peuvent être stérilisés par autoclavage sans altération de structure. Ils présentent de plus un profil de toxicité acceptable chez la souris par voie orale et en injection intraveineuse, et ciblent naturellement les cellules phagocytiques mononucléaires avec une efficacité 50 fois supérieure à celle de liposomes à liaisons esters

Polymères d’Archaea • Deux types de molécules présentent un intérêt particulier : Ø les polyhydroxyalkanoates (PHA), intracellulaires, peuvent être utilisés comme plastiques biodégradables. Ø les exopolysaccharides (EPS) ont de multiples applications dans l’agroalimentaire, la cosmétique et la santé. Ø Plusieurs espèces d’archées peuvent synthétiser des PHA, dont Natrialba aegyptiaca et Haloferax mediterranei, chez qui l’accumulation peut atteindre 60 % du poids sec cellulaire et pour laquelle la récupération est effectuée par simple lyse cellulaire en milieu dessalé. Haloferax peut également produire des EPS dans certaines conditions.

Enzymes d’Archaea Enzymes des acides nucléiques ØLes technologies de l’ADN recombinant reposent sur l’utilisation d’enzymes très diverses : enzymes de restriction, ADN polymérases, ADN ligases, etc. ØLes ADN polymérases thermostables jouent un rôle fondamental dans les techniques d’ingénierie du vivant grâce à leur aptitude à amplifier un gène donné à des millions de copies in vitro par PCR(7), amplification isotherme, etc. ØL’enzyme la plus utilisée en PCR est la Taq polymérase, isolée de la bactérie Thermus aquaticus. Les ADN polymérases des archées hyperthermophiles Pyrococcus et Thermococus occupent le deuxième rang, avec 30 % du marché. ØElles ont, à l’inverse de la Taq, une activité exonucléasique 3’ 5’ et donc une fonction de correction d’erreurs, et sont, de fait, plus fidèles. Les ADN polymérases d’archées constituent donc les enzymes de référence dès lors que la fidélité du produit final est essentielle, comme pour la production de protéines recombinantes.

ØMais si les polymérases de Thermococcales ont une excellente thermostabilité et une fidélité élevée, leur processivité*4, leurs paramètres cinétiques et les tailles des fragments amplifiés en PCR sont plus variables. En outre, utilisées en combinaison avec la Taq, les ADN polymérases de Pyrococcus et de Thermococcus peuvent produire des fragments de grande taille en PCR longue distance jusqu’à 20 kb à partir d’ADN génomique. ØPlusieurs domaines sont plus particulièrement demandeurs de nouvelles ADN polymérases : le bioterrorisme, avec l’objectif de disposer d’ADN polymérases fonctionnelles dans des conditions drastiques (présence de solvants et autres inhibiteurs), la médecine légale et les recherches sur les ADN anciens ou fossiles, caractérisés par une fréquence élevée de lésions dans les ADN génomiques récupérés.

Lipases et estérases Ø Les estérases se distinguent des lipases par leur préférence pour les chaînes carbonées courtes et ne sont pas actives sur les substrats qui forment des micelles. Ø Elles ne requièrent pas de cofacteur, présentent de bonnes chimiosélectivité, régiosélectivité et énantiosélectivité. Elles ont trouvé de multiples applications dans les industries médicales, agroalimentaires, de production d’énergie, grâce à leurs propriétés en synthèse organique (d’arômes, de détergents, de biodiesel notamment), etc. Ø Depuis la caractérisation de la première carboxylestérase de Sulfolobus acidocaldarius, en 1988, de nombreuses estérases d’archées ont été isolées. La première lipase ne l’a été que récemment, chez l’archée hyperthermophile Archaeoglobus fulgidus. Ø Les p. H optimaux s’échelonnent entre 6 et 9, mais celui de la lipase d’A. fulgidus atteint 11. La majorité des carboxypeptidases issues d’archées hyperthermophiles affiche une excellente thermostabilité et une activité optimale à des températures comprises entre 70 et 100 °C.



Enzymes dégradant les polysaccharides ØLes enzymes de la famille des glycosylases, impliquées dans le métabolisme des glucides, revêtent un intérêt industriel important. En particulier, celles qui convertissent l’amidon et celles capables de dégrader la cellulose et la lignocellulose sont fondamentales dans les procédés de production de biocarburants respectivement de première et deuxième générations. ØLes archées constituent un gisement extrêmement varié d’enzymes intéressantes pour la dégradation de l’amidon : amylases, glucoamylases et a glucosidases. ØLes a amylases de plusieurs espèces d’archées hyperthermophiles appartenant aux genres Sulfolobus, Thermococcus, Pyrococcus et Methanocaldococcus sont caractérisées par leur thermostabilité extrême et leur optimum de température compris entre 80 et 100 °C. Certaines, comme celles de Pyrococcus et Methanocaldococcus, sont actives jusqu’à 130 °C. ØDans un autre registre, les a amylases de certaines halophiles telles que Haloarcula sont actives en solutions à concentrations élevées en Na. Cl ainsi que dans des solvants (benzène, toluène, chloroforme, etc. ). De même, il existe des amylases issues d’alcaliphiles fonctionnelles à p. H 10.

Solutés compatibles et extrêmolytes ØLes extrêmolytes sont des composés organiques solubles synthétisés par les extrêmophiles pour protéger leurs constituants cellulaires des conditions environnementales. ØLes archées produisent une grande diversité d’extrêmolytes originaux applications nombreuses : vstabilisation des enzymes vprotection des protéines et des anticorps vprotection contre les dommages congélation/ décongélation, etc. ØLe plus connu est l’ectoïne, produite industriellement à partir des halophiles.
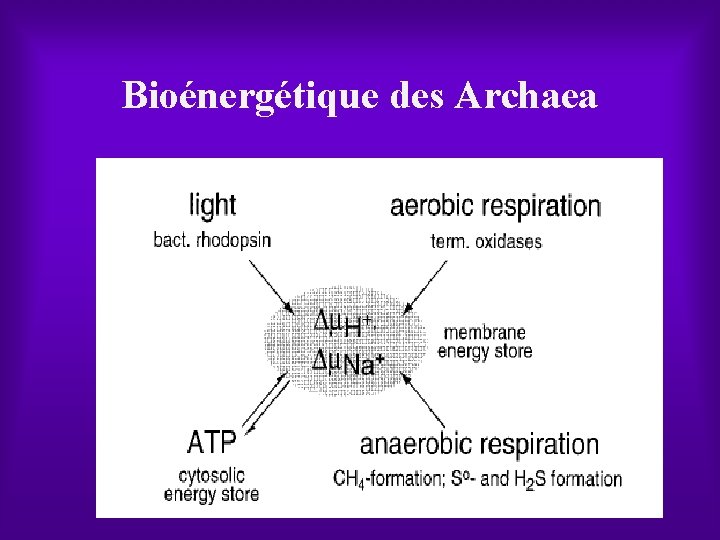
Bioénergétique des Archaea

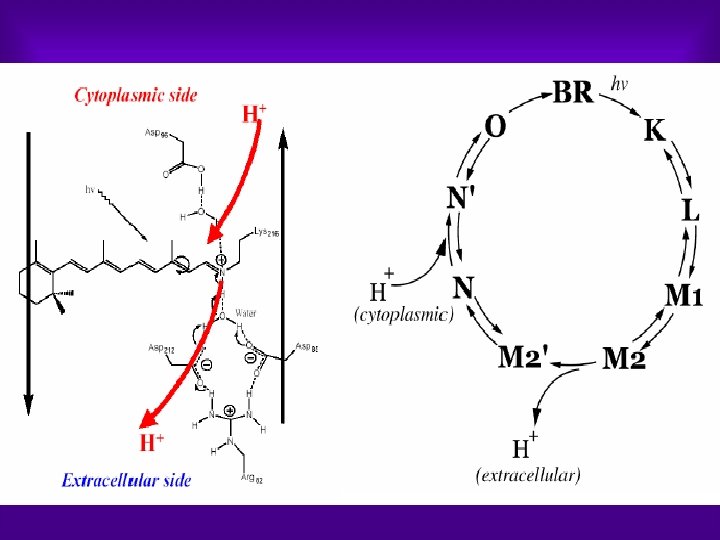
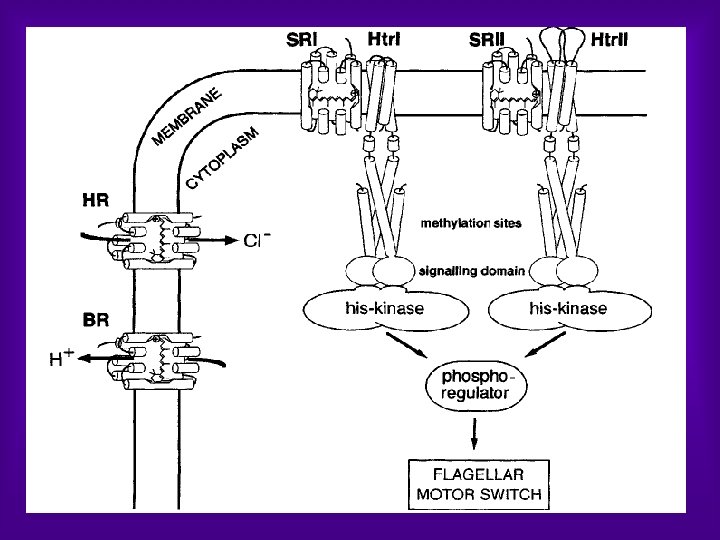
LIGHT DRIVEN ENERGETICS Ø In the early 1970 s, the so called purple membrane from H. Salinarum was found to contain only a single protein Ø It was later demonstrated that a retinal chromophore attached to this protein gives rise to the purple color Ø Because of the obvious resemblance to vertebrate rhodopsins, the authors named this retinylidene protein bacteriorhodopsin (BR) Ø During the elucidation of the proton pumping mechanism of BR and the physiology of H. salinarum, three other bacterial rhodopsins were discovered Ø These pigments are functionally quite distinct. HR, like BR an ion pump, is an inwardly directed chloride pump. The two other bacterial rhodopsins turned out to be photoreceptors that trigger the photophobic and/or photoattractive response of bacteria
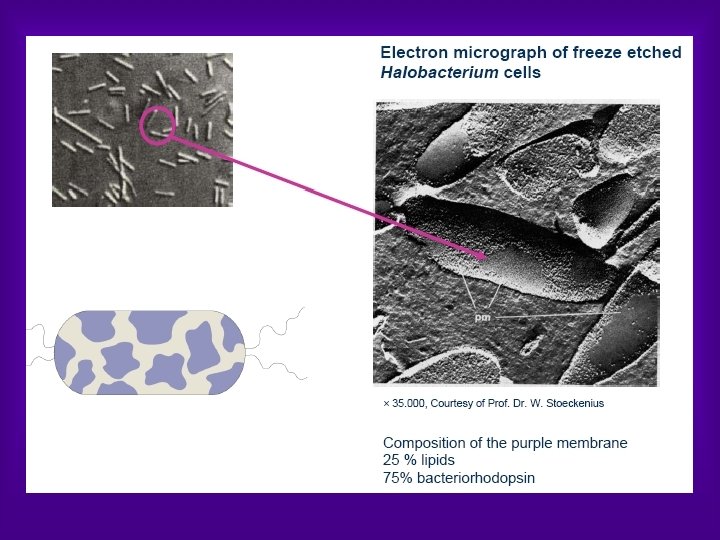


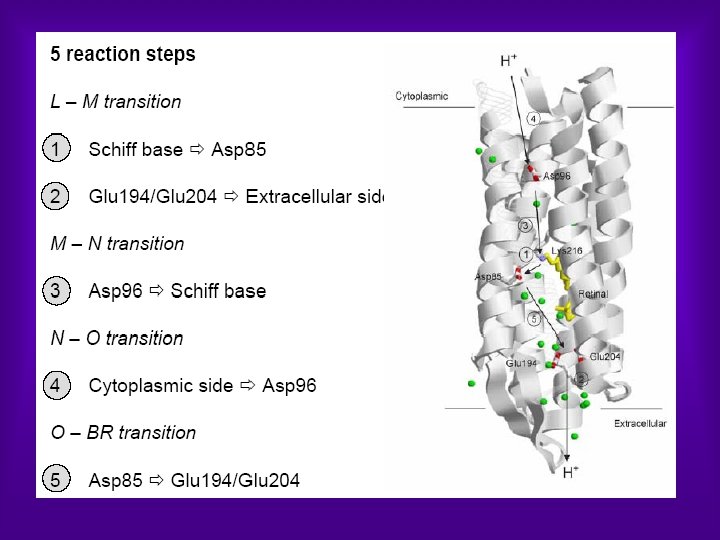
Bacterio. Rhodopsin (BR) Ø From the primary structure of BR; it became evident that the protein is a chain of 248 amino acids, which folds into a bundle of seven helices with short non helical interconnecting loops. Ø Several potentially charged amino acids are found in the hydrophobic interior of the protein. Two Asp residues (Asp 85 and Asp 96) were located in helix C, Asp 115 was in helix D, and finally Asp 212 and Lys 216 were in helix G.
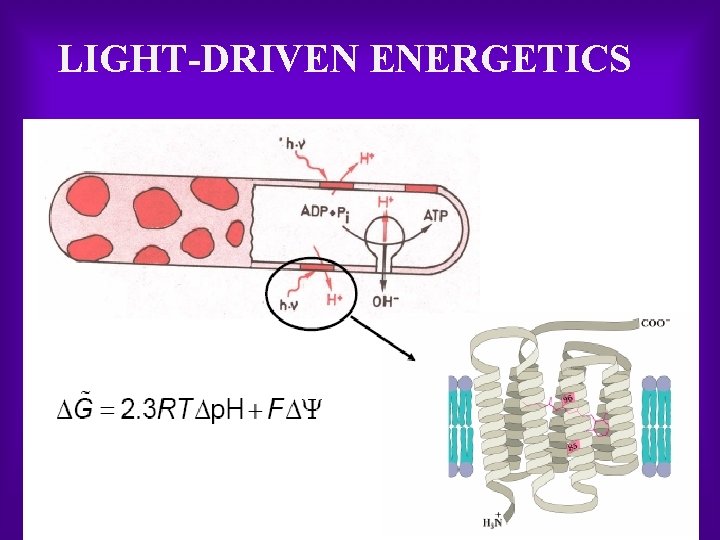
LIGHT DRIVEN ENERGETICS
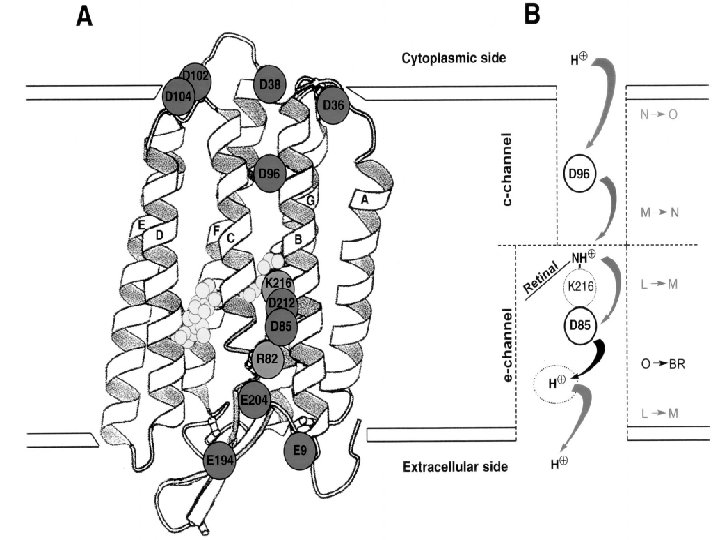
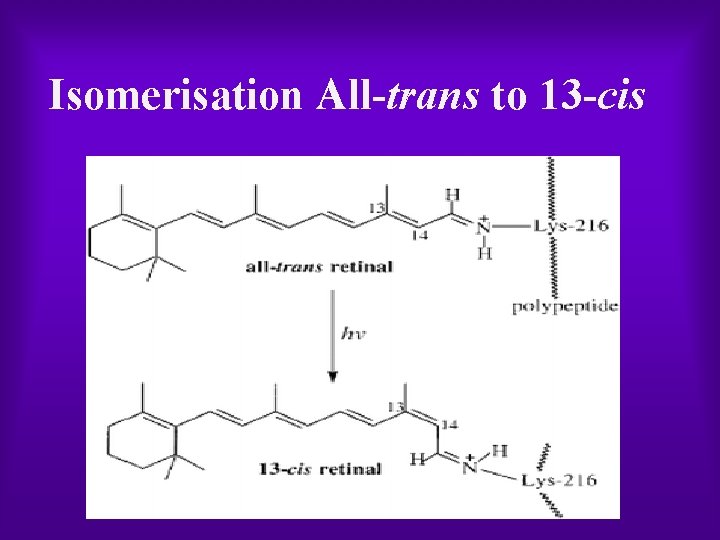
Isomerisation All trans to 13 cis
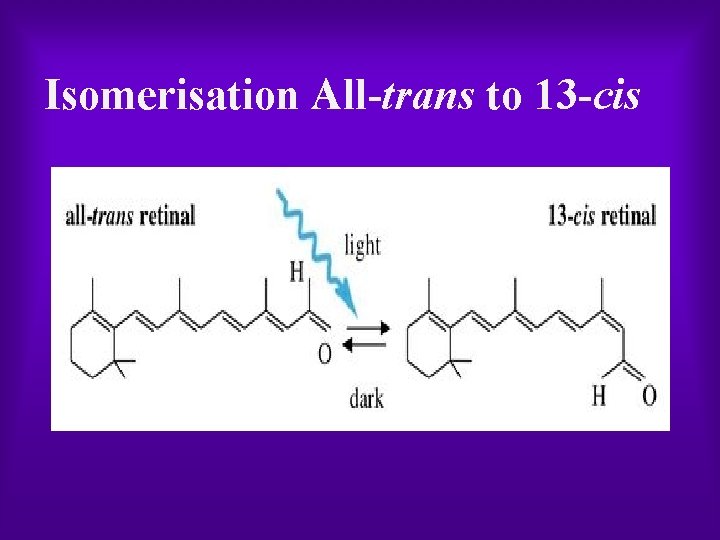
Isomerisation All trans to 13 cis

Merci pour votre bonne attention Dr/ Boutaiba Saad
- Slides: 52