MSIH EN UNA AMPLIA VARIEDAD DE TUMORES CUNDO















- Slides: 50

MSI-H EN UNA AMPLIA VARIEDAD DE TUMORES: ¿CUÁNDO ES UN SÍNDROME DE LYNCH? , ¿CÓMO ACTUAR EN LA PRÁCTICA Lastra Aras CLÍNICA? Enrique Unidad de Consejo Genético Sº Oncología Médica H. Universitario de Burgos

Disclosure Information q Employment: Medical Oncologist and Genetic Counselor. Hospital Universitario de Burgos. q Consultant or Advisory Role: No. q Stock Ownership: No. q Research Funding: Asociación La Concepción. Universidad de Burgos. q Speaking: Guardant Health, Inc. Speaker Agreement. q Grant support: FIS. Gerencia Regional de Salud SACYL. q Other: No.

GUIÓN • MSI en la asistencia oncológica actual • Nuevos escenarios de diagnóstico en S. Lynch • Cómo inferir S. Lynch desde estudios moleculares en tumor • Actitud en la práctica clínica

MSI EN LA ASISTENCIA ONCOLÓGICA ACTUAL • Estrategia universal en diagnóstico Síndrome Lynch • Oncología de precisión agnóstica de histología

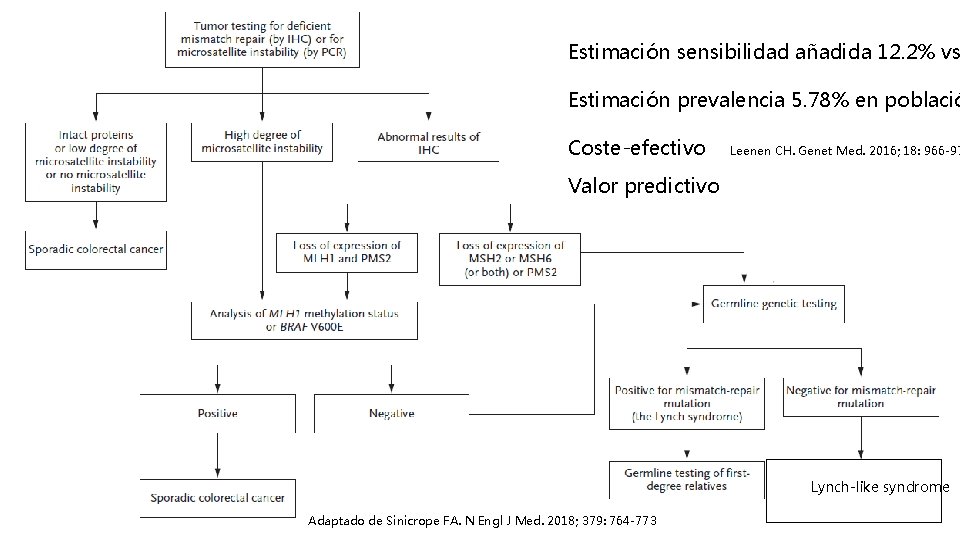
Estimación sensibilidad añadida 12. 2% vs Estimación prevalencia 5. 78% en població Coste-efectivo Leenen CH. Genet Med. 2016; 18: 966 -97 Valor predictivo Lynch-like Lu syndrome Adaptado de Sinicrope FA. N Engl J Med. 2018; 379: 764 -773

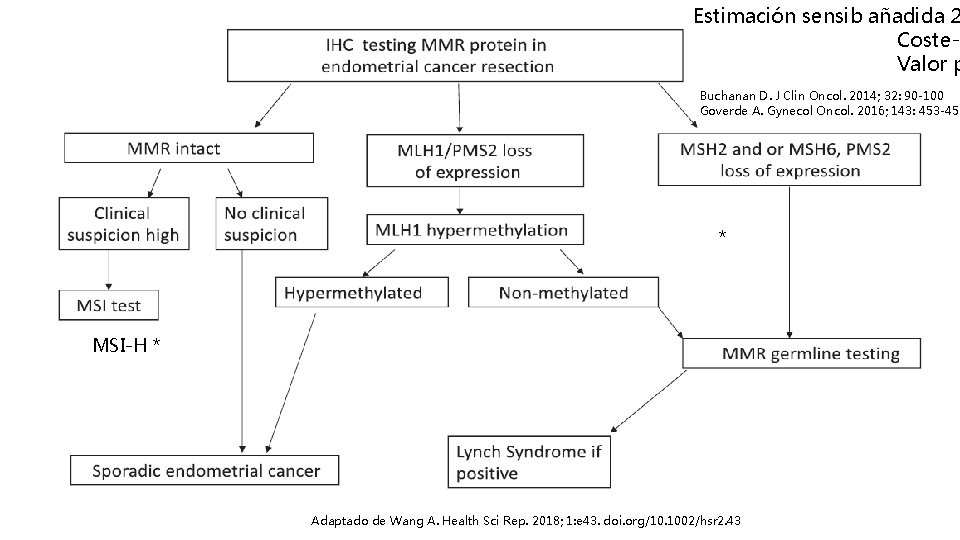
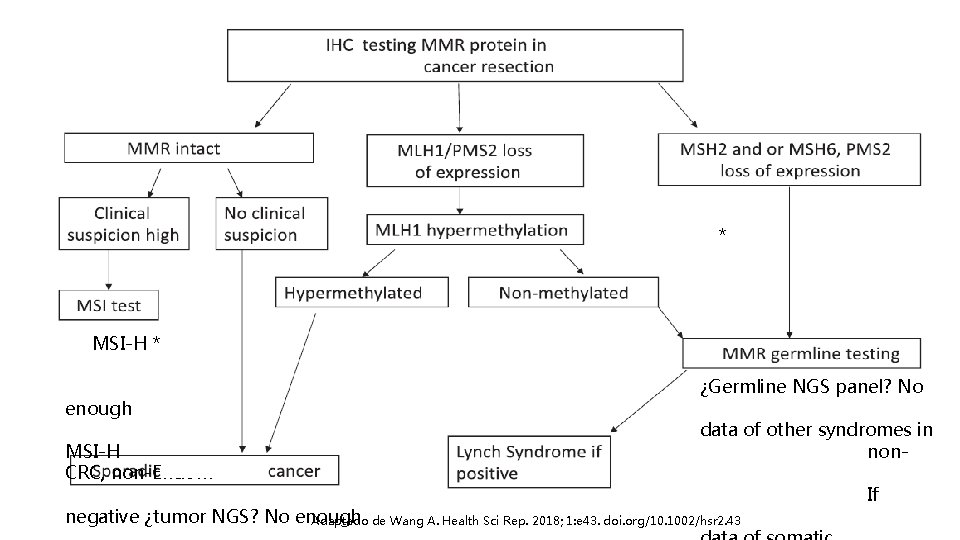
Estimación sensib añadida 2 Coste-e Valor p Buchanan D. J Clin Oncol. 2014; 32: 90 -100 Goverde A. Gynecol Oncol. 2016; 143: 453 -459 * MSI-H * Adaptado de Wang A. Health Sci Rep. 2018; 1: e 43. doi. org/10. 1002/hsr 2. 43

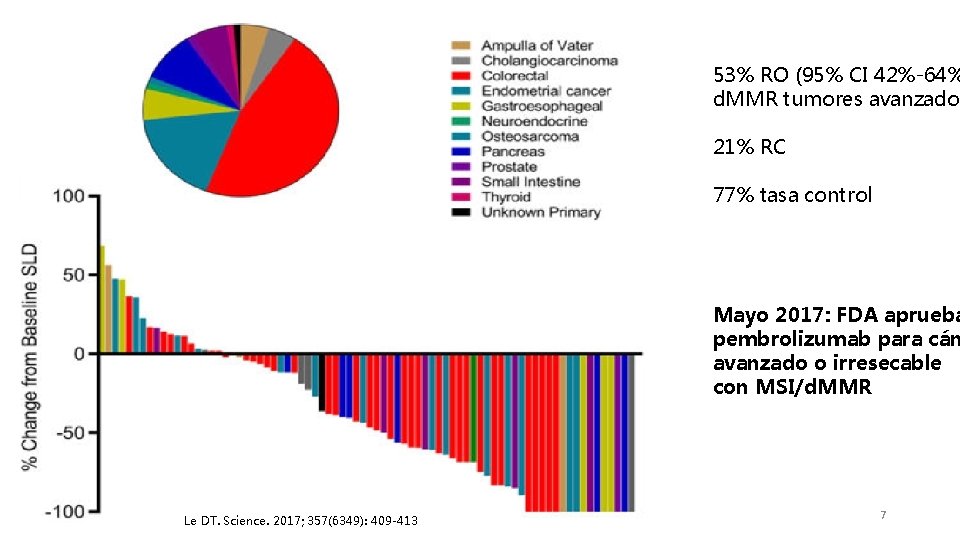
53% RO (95% CI 42%-64% d. MMR tumores avanzados 21% RC 77% tasa control Mayo 2017: FDA aprueba pembrolizumab para cán avanzado o irresecable con MSI/d. MMR Le DT. Science. 2017; 357(6349): 409 -413 7

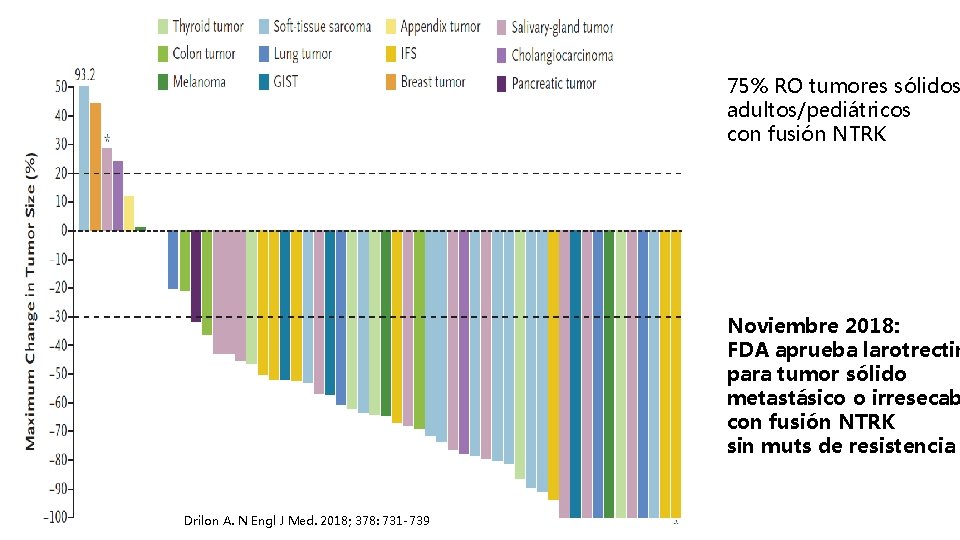
75% RO tumores sólidos adultos/pediátricos con fusión NTRK Noviembre 2018: FDA aprueba larotrectin para tumor sólido metastásico o irresecab con fusión NTRK sin muts de resistencia Drilon A. N Engl J Med. 2018; 378: 731 -739

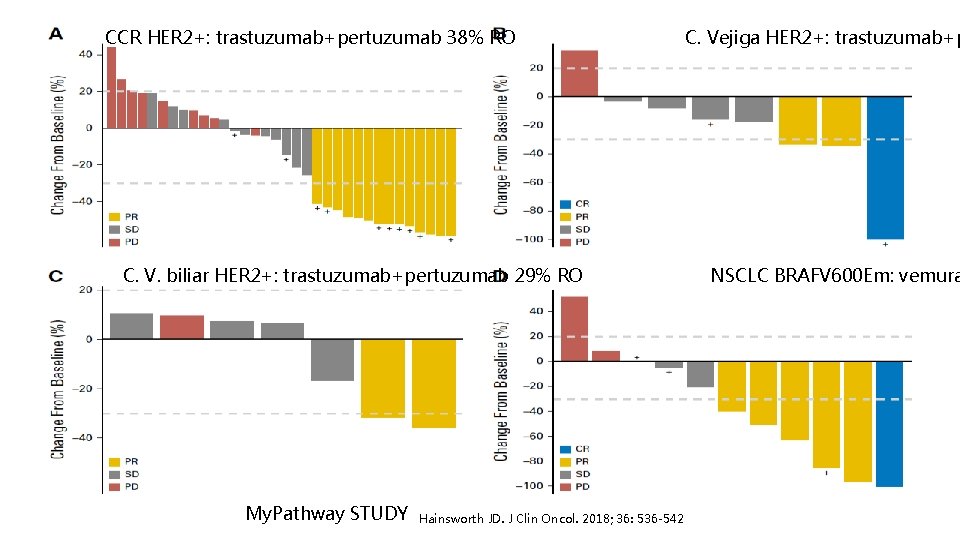
CCR HER 2+: trastuzumab+pertuzumab 38% RO C. V. biliar HER 2+: trastuzumab+pertuzumab 29% RO My. Pathway STUDY Hainsworth JD. J Clin Oncol. 2018; 36: 536 -542 C. Vejiga HER 2+: trastuzumab+p NSCLC BRAFV 600 Em: vemura

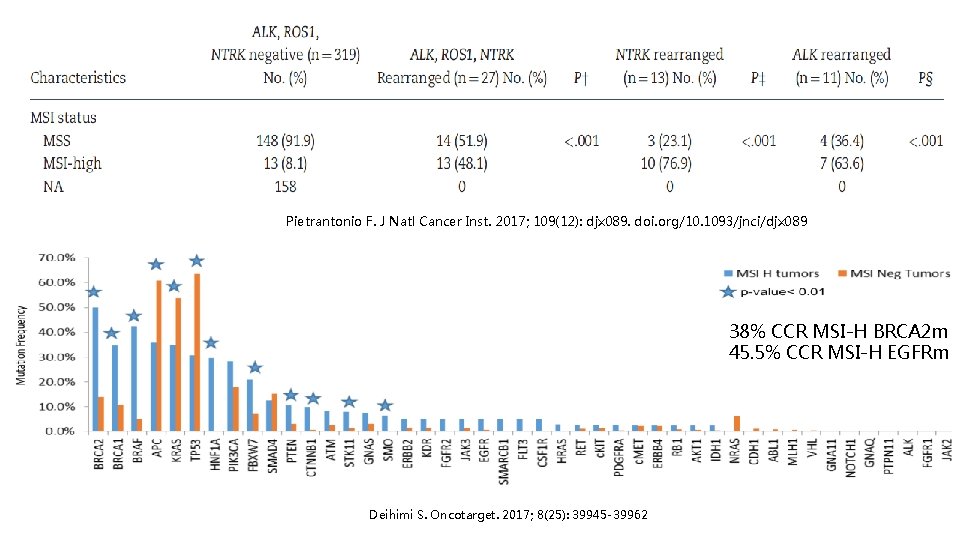
Pietrantonio F. J Natl Cancer Inst. 2017; 109(12): djx 089. doi. org/10. 1093/jnci/djx 089 38% CCR MSI-H BRCA 2 m 45. 5% CCR MSI-H EGFRm Deihimi S. Oncotarget. 2017; 8(25): 39945 -39962

* Análisis computacional microsatélites para determinar MSI * TMB: Tumor Mutational Burden * HRD: Perfiles moleculares para Homologous Recombination Deficiency * Otros perfiles moleculares: PDL 1 Haraldsdottit S. JCO Precision Oncology. Oct. 2017. JCO Precis Oncol 10. 1200/PO. 17. 00189 Lastra E, Robles L. Cáncer Hereditario 3ª Edició

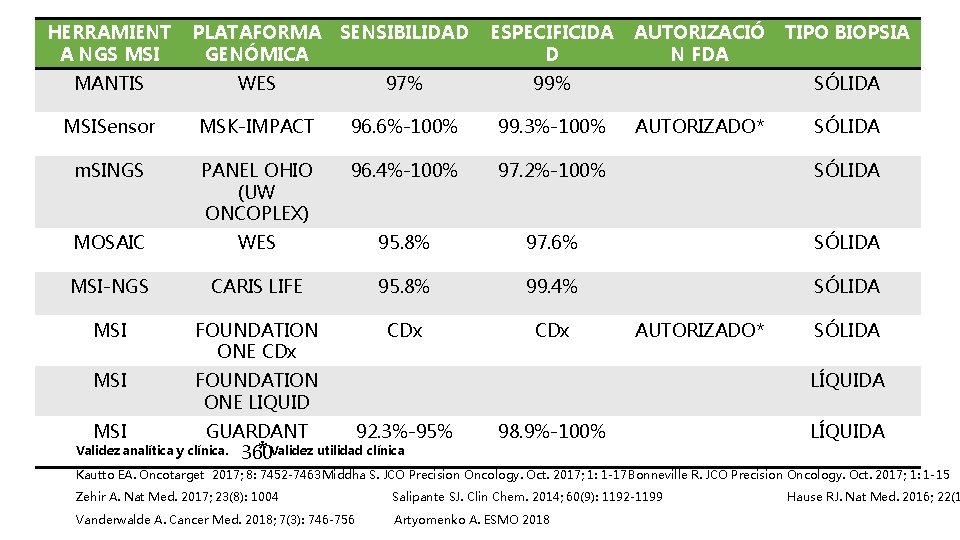
HERRAMIENT A NGS MSI PLATAFORMA GENÓMICA SENSIBILIDAD ESPECIFICIDA D MANTIS WES 97% 99% MSISensor MSK-IMPACT 96. 6%-100% 99. 3%-100% m. SINGS PANEL OHIO (UW ONCOPLEX) 96. 4%-100% 97. 2%-100% SÓLIDA MOSAIC WES 95. 8% 97. 6% SÓLIDA MSI-NGS CARIS LIFE 95. 8% 99. 4% SÓLIDA MSI FOUNDATION ONE CDx CDx MSI FOUNDATION ONE LIQUID MSI AUTORIZACIÓ N FDA TIPO BIOPSIA SÓLIDA AUTORIZADO* SÓLIDA LÍQUIDA GUARDANT 92. 3%-95% Validez analítica y clínica. 360 * Validez utilidad clínica 98. 9%-100% LÍQUIDA Kautto EA. Oncotarget 2017; 8: 7452 -7463 Middha S. JCO Precision Oncology. Oct. 2017; 1: 1 -17 Bonneville R. JCO Precision Oncology. Oct. 2017; 1: 1 -15 Zehir A. Nat Med. 2017; 23(8): 1004 Salipante SJ. Clin Chem. 2014; 60(9): 1192 -1199 Vanderwalde A. Cancer Med. 2018; 7(3): 746 -756 Artyomenko A. ESMO 2018 Hause RJ. Nat Med. 2016; 22(1

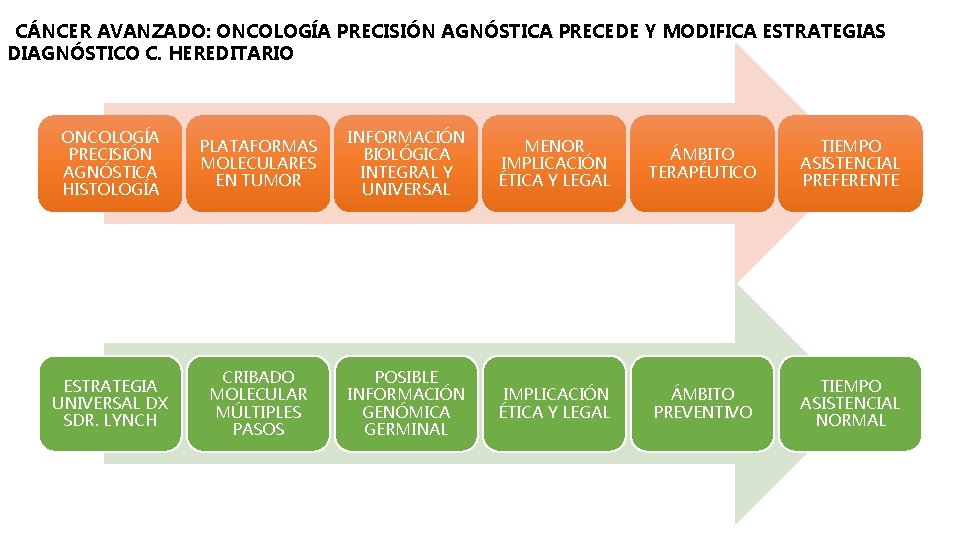
CÁNCER AVANZADO: ONCOLOGÍA PRECISIÓN AGNÓSTICA PRECEDE Y MODIFICA ESTRATEGIAS DIAGNÓSTICO C. HEREDITARIO ONCOLOGÍA PRECISIÓN AGNÓSTICA HISTOLOGÍA PLATAFORMAS MOLECULARES EN TUMOR INFORMACIÓN BIOLÓGICA INTEGRAL Y UNIVERSAL MENOR IMPLICACIÓN ÉTICA Y LEGAL ÁMBITO TERAPÉUTICO TIEMPO ASISTENCIAL PREFERENTE ESTRATEGIA UNIVERSAL DX SDR. LYNCH CRIBADO MOLECULAR MÚLTIPLES PASOS POSIBLE INFORMACIÓN GENÓMICA GERMINAL IMPLICACIÓN ÉTICA Y LEGAL ÁMBITO PREVENTIVO TIEMPO ASISTENCIAL NORMAL

NUEVOS ESCENARIOS DE DIAGNÓSTICO EN S. LYNCH • Limitaciones de la estrategia universal • Evolución estrategia universal • Paneles NGS germinal en pacientes con CCR • Paneles NGS en CCR • Paneles NGS oncología de precisión agnóstica

• Limitaciones estrategia universal: MSS y S. Lynch-like • Falsos negativos en CCR MSS: 13%-23% S. Lynch con MSS • Pierde Cáncer Colon Familiar tipo X (CCF-X)/otras causas CCR MSS • Detecta S. Lynch: 24%-67% CCR MSI-H, 16%-80% C. endometrio MSI-H • No identifica inactivación somática (49. 8%-69% tumores MSI-H) • Pierde muts. germ atípicas genes MMR/muts otros genes en CCR MSI-H • Pérdida metilación MLH 1 germinal/2º hit Hampel H. J Clin Oncol. 2008; 26: 5783 -5788; Buchanan DD. Appl Clin Genet. 2014; 7: 183 -193; Haraldsdottir S. Gastroenterology. 2014; 147: 1308 -1316. e 1; Mensenkamp AR. Gastroenterology. 2014; 146: 643 -646. e 8 ; Sourrouille I. Fam Cancer. 2013; 12: 27 -33; Palomaki GE. Genet Med. 2009; 11(1): 42 -65; Hampel H, JAMA Oncol. 2018; 4(6): 806 -813; Castillejo A. Eur J Cancer. 2014; 50(13): 2241 -2250; Morak M. Eur J Hum Genet. 2014; 22(11): 1334 -1337; Vargas-Parra GM. Int J Cancer. 2017; 144(7): 1365 -1380; Valle L. Hum Mol Genet. 2014; 23(13): 3506 -3512; Ferrer-Avargues R. J Gene Med. 2017; 19(4). doi: 10. 1002/jgm. 2951

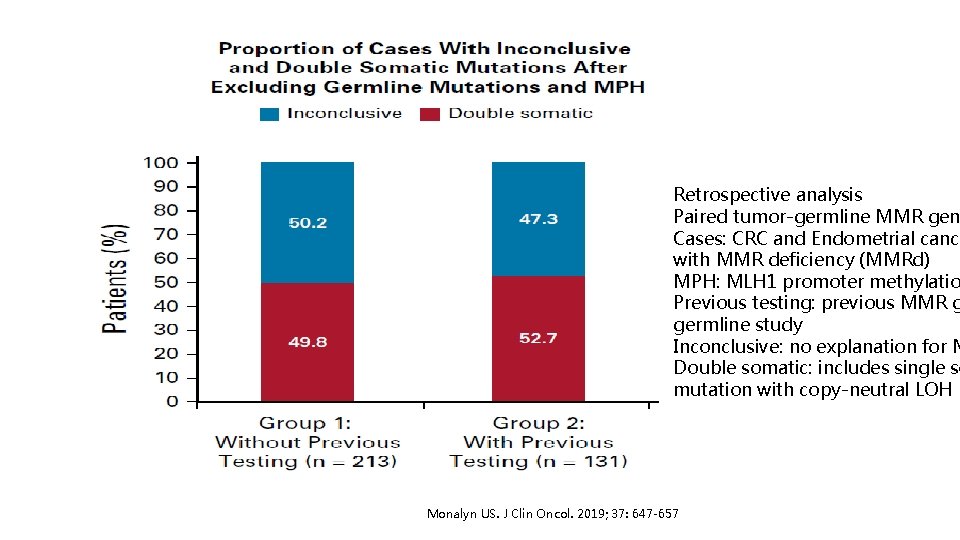
Retrospective analysis Paired tumor-germline MMR gen Cases: CRC and Endometrial cance with MMR deficiency (MMRd) MPH: MLH 1 promoter methylatio Previous testing: previous MMR g germline study Inconclusive: no explanation for M Double somatic: includes single so mutation with copy-neutral LOH Monalyn US. J Clin Oncol. 2019; 37: 647 -657

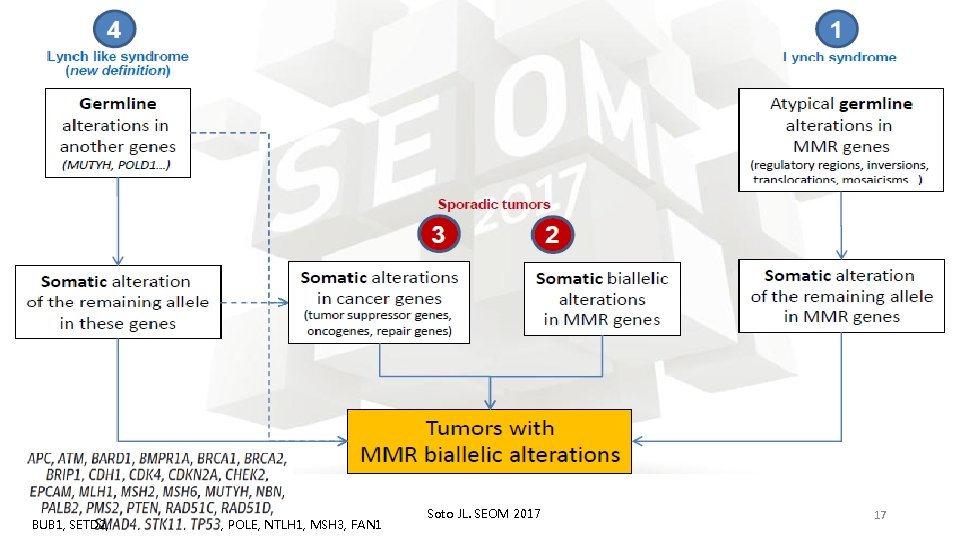
BUB 1, SETD 2, , POLE, NTLH 1, MSH 3, FAN 1 Soto JL. SEOM 2017 17

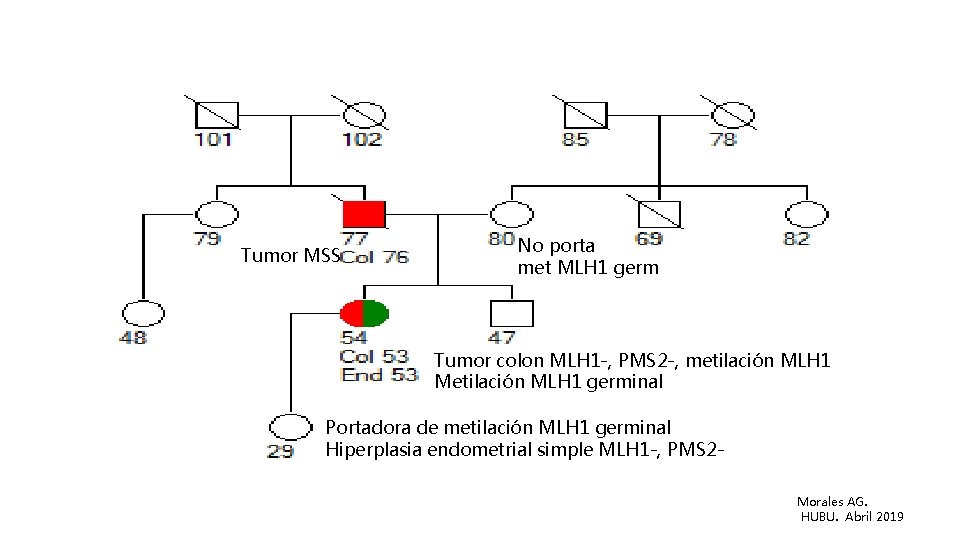
Tumor MSS No porta met MLH 1 germ Tumor colon MLH 1 -, PMS 2 -, metilación MLH 1 Metilación MLH 1 germinal Portadora de metilación MLH 1 germinal Hiperplasia endometrial simple MLH 1 -, PMS 2 Morales AG. HUBU. Abril 2019

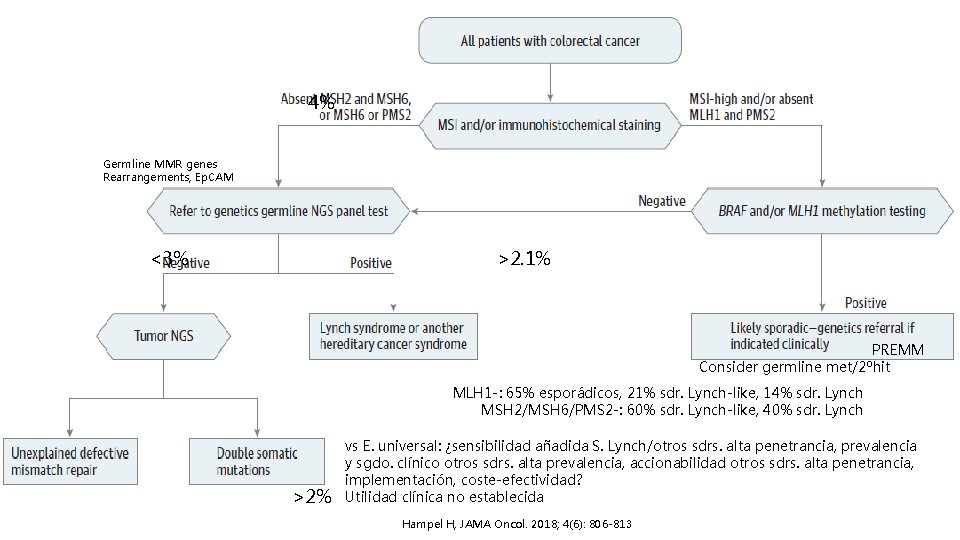
4% Germline MMR genes Rearrangements, Ep. CAM <3% >2. 1% PREMM Consider germline met/2ºhit MLH 1 -: 65% esporádicos, 21% sdr. Lynch-like, 14% sdr. Lynch MSH 2/MSH 6/PMS 2 -: 60% sdr. Lynch-like, 40% sdr. Lynch >2% vs E. universal: ¿sensibilidad añadida S. Lynch/otros sdrs. alta penetrancia, prevalencia y sgdo. clínico otros sdrs. alta prevalencia, accionabilidad otros sdrs. alta penetrancia, implementación, coste-efectividad? Utilidad clínica no establecida Hampel H, JAMA Oncol. 2018; 4(6): 806 -813

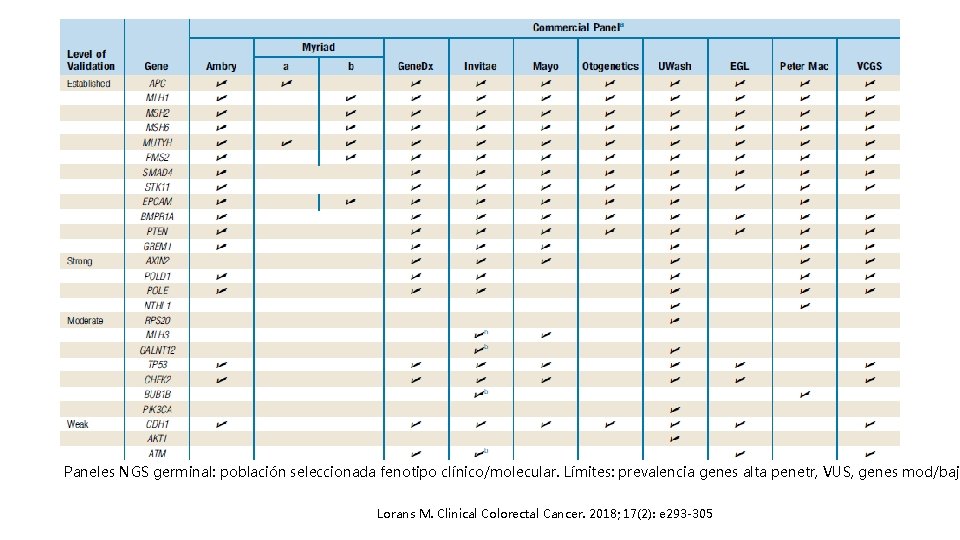
Paneles NGS germinal: población seleccionada fenotipo clínico/molecular. Límites: prevalencia genes alta penetr, VUS, genes mod/baja Lorans M. Clinical Colorectal Cancer. 2018; 17(2): e 293 -305

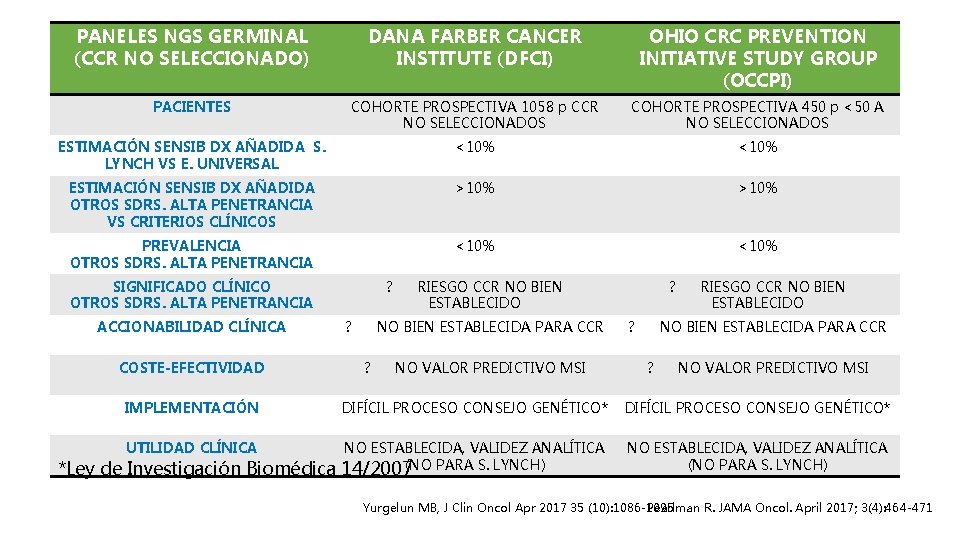
PANELES NGS GERMINAL (CCR NO SELECCIONADO) DANA FARBER CANCER INSTITUTE (DFCI) OHIO CRC PREVENTION INITIATIVE STUDY GROUP (OCCPI) PACIENTES COHORTE PROSPECTIVA 1058 p CCR NO SELECCIONADOS COHORTE PROSPECTIVA 450 p <50 A NO SELECCIONADOS ESTIMACIÓN SENSIB DX AÑADIDA S. LYNCH VS E. UNIVERSAL <10% ESTIMACIÓN SENSIB DX AÑADIDA OTROS SDRS. ALTA PENETRANCIA VS CRITERIOS CLÍNICOS >10% PREVALENCIA OTROS SDRS. ALTA PENETRANCIA <10% SIGNIFICADO CLÍNICO OTROS SDRS. ALTA PENETRANCIA ACCIONABILIDAD CLÍNICA COSTE-EFECTIVIDAD ? ? RIESGO CCR NO BIEN ESTABLECIDO NO BIEN ESTABLECIDA PARA CCR ? NO VALOR PREDICTIVO MSI IMPLEMENTACIÓN DIFÍCIL PROCESO CONSEJO GENÉTICO* UTILIDAD CLÍNICA NO ESTABLECIDA, VALIDEZ ANALÍTICA 14/2007(NO PARA S. LYNCH) NO ESTABLECIDA, VALIDEZ ANALÍTICA (NO PARA S. LYNCH) *Ley de Investigación Biomédica Yurgelun MB, J Clin Oncol Apr 2017 35 (10): 1086 -1095 Pearlman R. JAMA Oncol. April 2017; 3(4): 464 -471

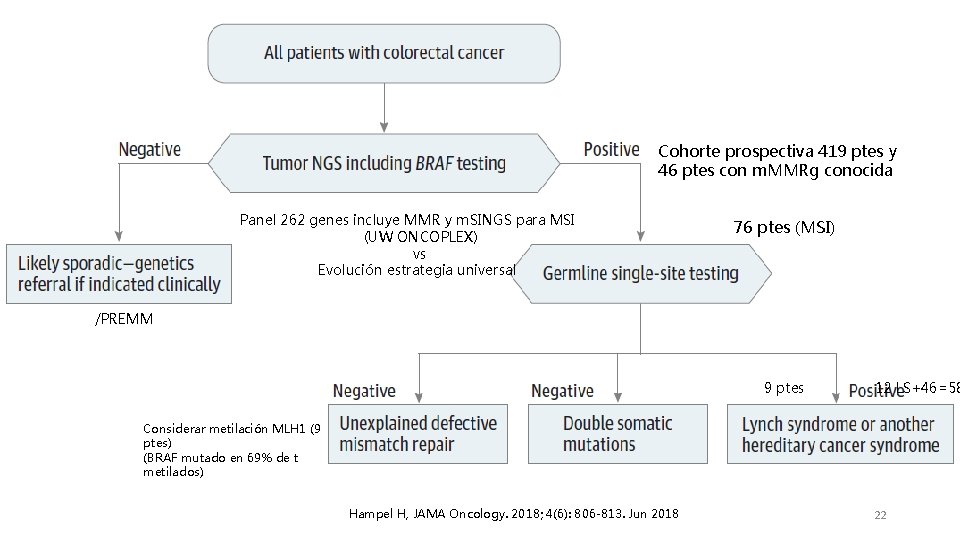
Cohorte prospectiva 419 ptes y 46 ptes con m. MMRg conocida Panel 262 genes incluye MMR y m. SINGS para MSI (UW ONCOPLEX) vs Evolución estrategia universal 76 ptes (MSI) /PREMM 9 ptes 12 LS+46=58 Considerar metilación MLH 1 (9 ptes) (BRAF mutado en 69% de t metilados) Hampel H, JAMA Oncology. 2018; 4(6): 806 -813. Jun 2018 22

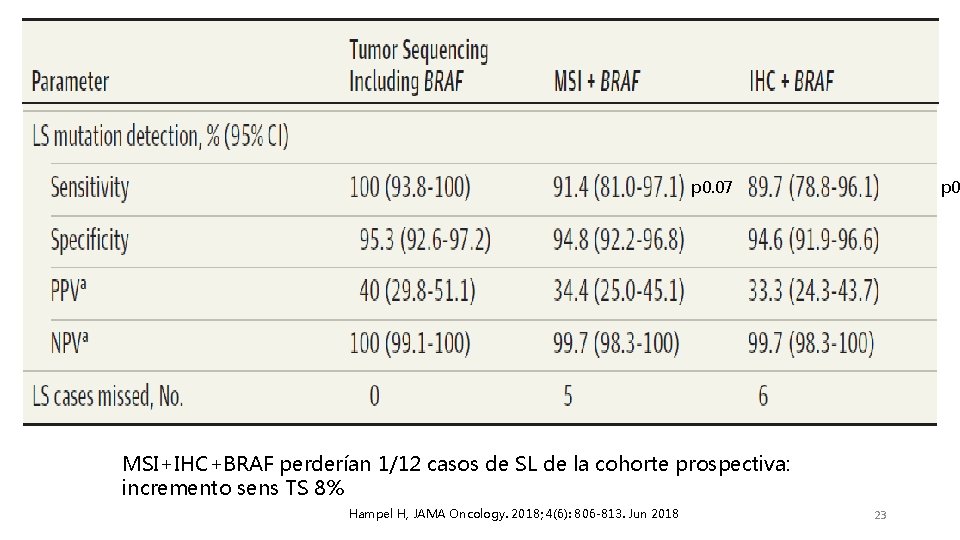
p 0. 07 p 0 MSI+IHC+BRAF perderían 1/12 casos de SL de la cohorte prospectiva: incremento sens TS 8% Hampel H, JAMA Oncology. 2018; 4(6): 806 -813. Jun 2018 23

PANELES NGS TUMORAL (CCR NO SELECCIONADO) OHIO CRC PREVENTION INITIATIVE STUDY GROUP (OCCPI) PACIENTES COHORTE PROSPECTIVA 419 p CCR NO SELECCIONADOS Y 46 P m. MMRg ESTIMACIÓN SENSIB DX AÑADIDA S. LYNCH VS E. UNIVERSAL >10% (vs IHQ+BRAF) PÉRDIDA DELECIONES (CORREGIBLE X NUEVOS PANELES) Y METILACIÓN MLH 1 ESTIMACIÓN SENSIB DX AÑADIDA OTROS SDRS. ALTA PENETRANCIA VS CRITERIOS CLÍNICOS ? PROBABLE NO OBJETIVO DEL ESTUDIO COSTE-EFECTIVIDAD ? VALOR PREDICTIVO MSI (m. SINGS) ESTUDIO GERMINAL DIRIGIDO IMPLEMENTACIÓN CRIBADO MOLECULAR EN DOS PASOS, FÁCIL PROCESO CONSEJO GENÉTICO (2º PASO ORIENTADO AL SÍNDROME SOSPECHADO) UTILIDAD CLÍNICA VALIDEZ ANALÍTICA, VALIDEZ CLÍNICA, VALIDEZ UTILIDAD CLÍNICA MANEJO SDR. LYNCH, VALIDEZ UTILIDAD CLÍNICA PREDICITVA (MSI) Hampel H, JAMA Oncology. 2018; 4(6): 806 -813. Jun 2018

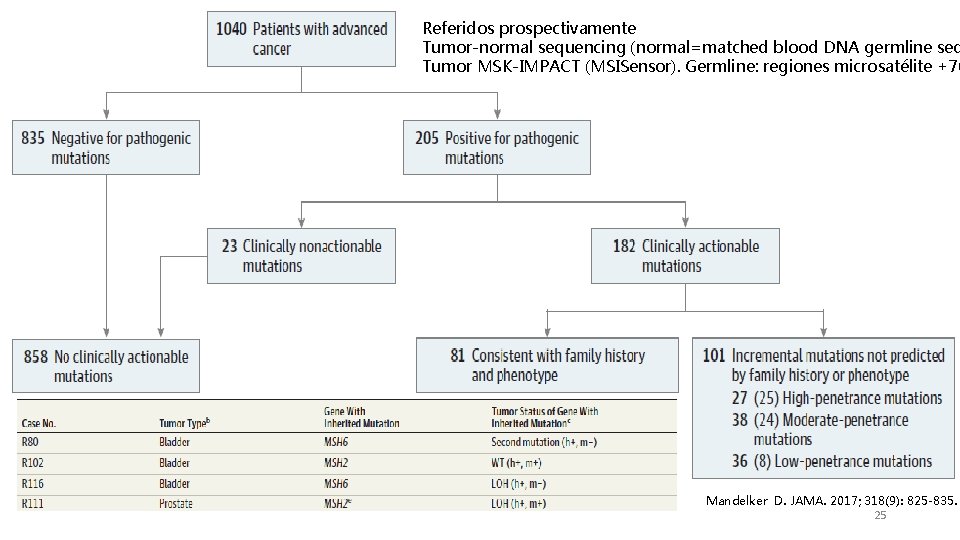
Referidos prospectivamente Tumor-normal sequencing (normal=matched blood DNA germline seq Tumor MSK-IMPACT (MSISensor). Germline: regiones microsatélite +76 Mandelker D. JAMA. 2017; 318(9): 825 -835. 25

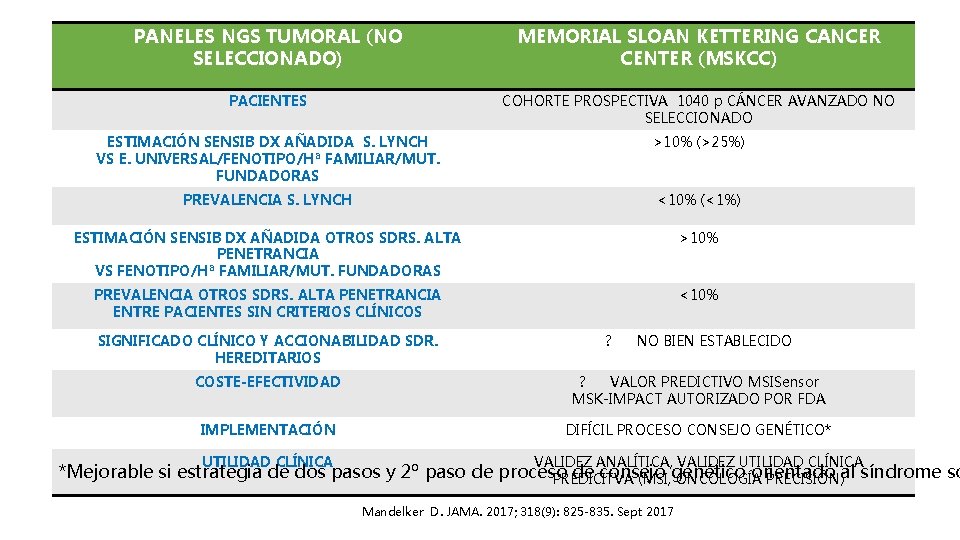
PANELES NGS TUMORAL (NO SELECCIONADO) MEMORIAL SLOAN KETTERING CANCER CENTER (MSKCC) PACIENTES COHORTE PROSPECTIVA 1040 p CÁNCER AVANZADO NO SELECCIONADO ESTIMACIÓN SENSIB DX AÑADIDA S. LYNCH VS E. UNIVERSAL/FENOTIPO/Hª FAMILIAR/MUT. FUNDADORAS >10% (>25%) PREVALENCIA S. LYNCH <10% (<1%) ESTIMACIÓN SENSIB DX AÑADIDA OTROS SDRS. ALTA PENETRANCIA VS FENOTIPO/Hª FAMILIAR/MUT. FUNDADORAS >10% PREVALENCIA OTROS SDRS. ALTA PENETRANCIA ENTRE PACIENTES SIN CRITERIOS CLÍNICOS <10% SIGNIFICADO CLÍNICO Y ACCIONABILIDAD SDR. HEREDITARIOS ? NO BIEN ESTABLECIDO COSTE-EFECTIVIDAD ? VALOR PREDICTIVO MSISensor MSK-IMPACT AUTORIZADO POR FDA IMPLEMENTACIÓN DIFÍCIL PROCESO CONSEJO GENÉTICO* UTILIDAD CLÍNICA VALIDEZ ANALÍTICA, VALIDEZ UTILIDAD CLÍNICA *Mejorable si estrategia de dos pasos y 2º paso de proceso de consejo orientado PREDICITVA (MSI, genético ONCOLOGÍA PRECISIÓN)al síndrome so Mandelker D. JAMA. 2017; 318(9): 825 -835. Sept 2017

CÓMO INFERIR S. LYNCH DESDE ESTUDIOS MOLECULARES EN TUMOR • Oncología de precisión agnóstica precede y modifica estrategias de diagnóstico en cáncer hereditario • Paneles NGS en CCR: validez analítica, clínica y utilidad clínica en S. Lynch

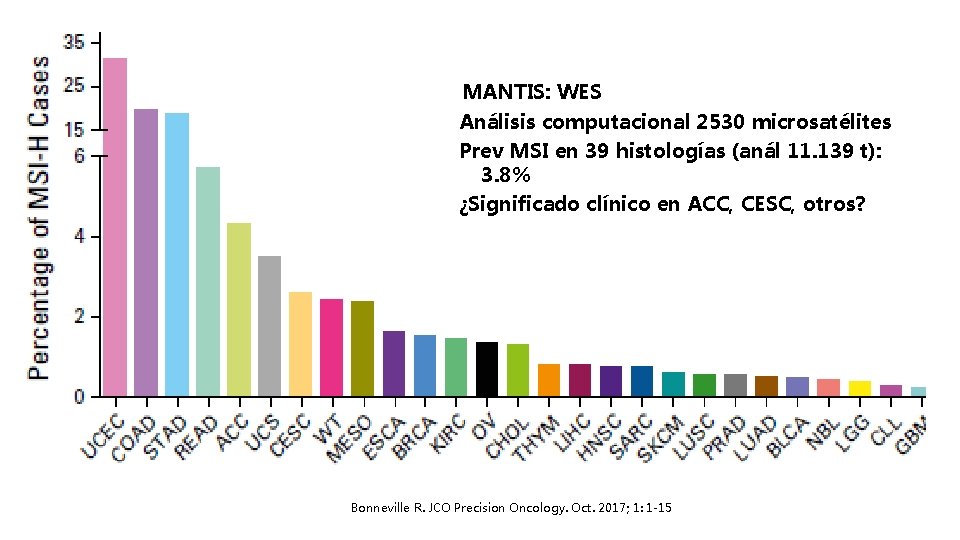
MANTIS: WES Análisis computacional 2530 microsatélites Prev MSI en 39 histologías (anál 11. 139 t): 3. 8% ¿Significado clínico en ACC, CESC, otros? Bonneville R. JCO Precision Oncology. Oct. 2017; 1: 1 -15

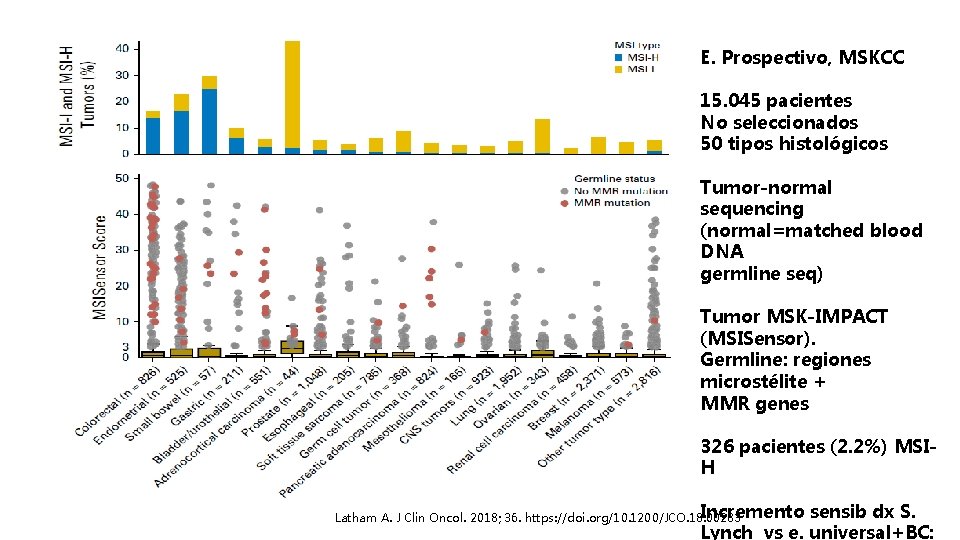
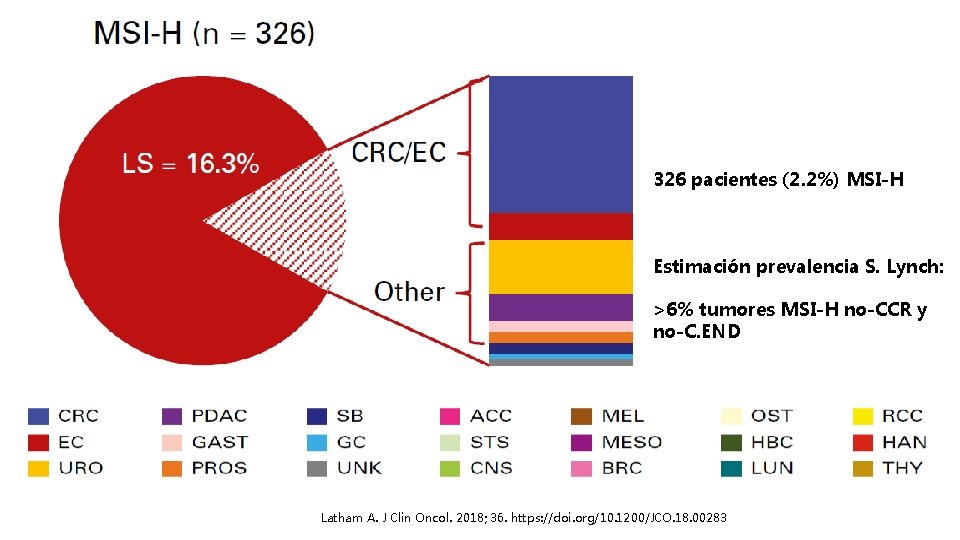
E. Prospectivo, MSKCC 15. 045 pacientes No seleccionados 50 tipos histológicos Tumor-normal sequencing (normal=matched blood DNA germline seq) Tumor MSK-IMPACT (MSISensor). Germline: regiones microstélite + MMR genes 326 pacientes (2. 2%) MSIH Incremento Latham A. J Clin Oncol. 2018; 36. https: //doi. org/10. 1200/JCO. 18. 00283 sensib dx S. Lynch vs e. universal+BC:

326 pacientes (2. 2%) MSI-H Estimación prevalencia S. Lynch: >6% tumores MSI-H no-CCR y no-C. END Latham A. J Clin Oncol. 2018; 36. https: //doi. org/10. 1200/JCO. 18. 00283

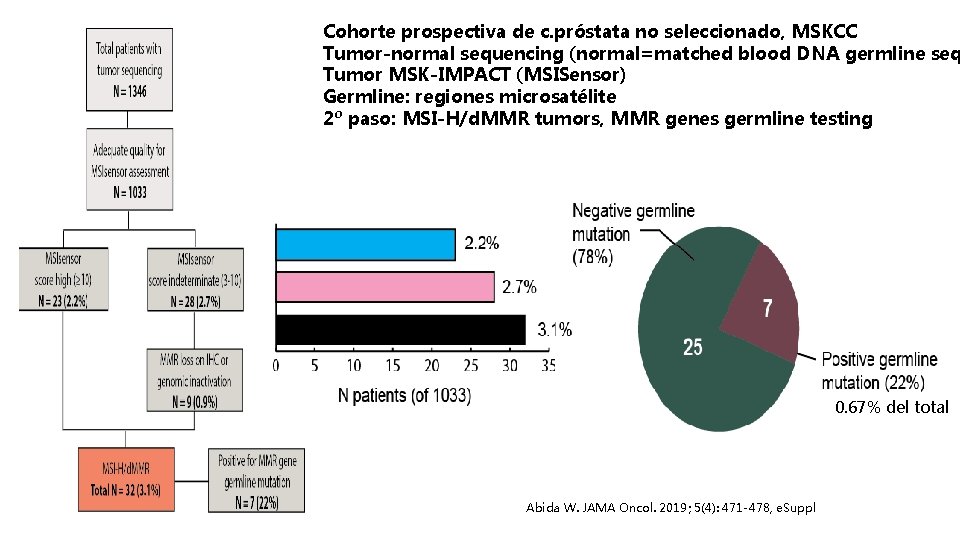
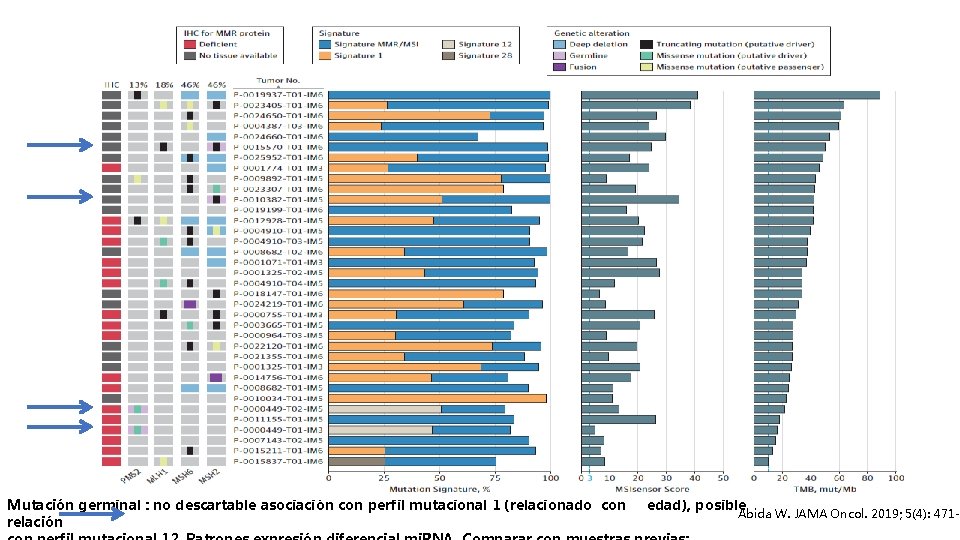
Cohorte prospectiva de c. próstata no seleccionado, MSKCC Tumor-normal sequencing (normal=matched blood DNA germline seq Tumor MSK-IMPACT (MSISensor) Germline: regiones microsatélite 2º paso: MSI-H/d. MMR tumors, MMR genes germline testing 0. 67% del total Abida W. JAMA Oncol. 2019; 5(4): 471 -478, e. Suppl

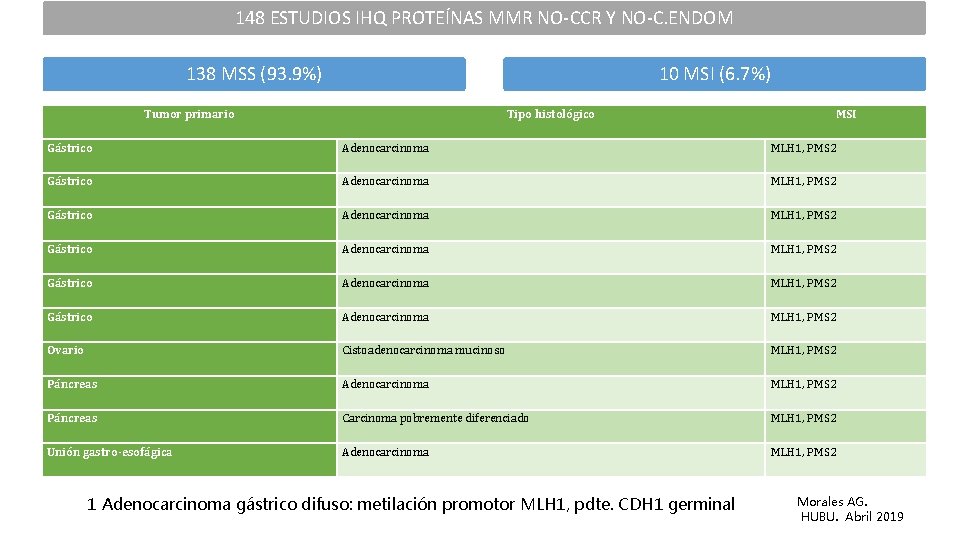
148 ESTUDIOS IHQ PROTEÍNAS MMR NO-CCR Y NO-C. ENDOM 138 MSS (93. 9%) 10 MSI (6. 7%) Tumor primario Tipo histológico MSI Gástrico Adenocarcinoma MLH 1, PMS 2 Gástrico Adenocarcinoma MLH 1, PMS 2 Ovario Cistoadenocarcinoma mucinoso MLH 1, PMS 2 Páncreas Adenocarcinoma MLH 1, PMS 2 Páncreas Carcinoma pobremente diferenciado MLH 1, PMS 2 Unión gastro-esofágica Adenocarcinoma MLH 1, PMS 2 1 Adenocarcinoma gástrico difuso: metilación promotor MLH 1, pdte. CDH 1 germinal Morales AG. HUBU. Abril 2019

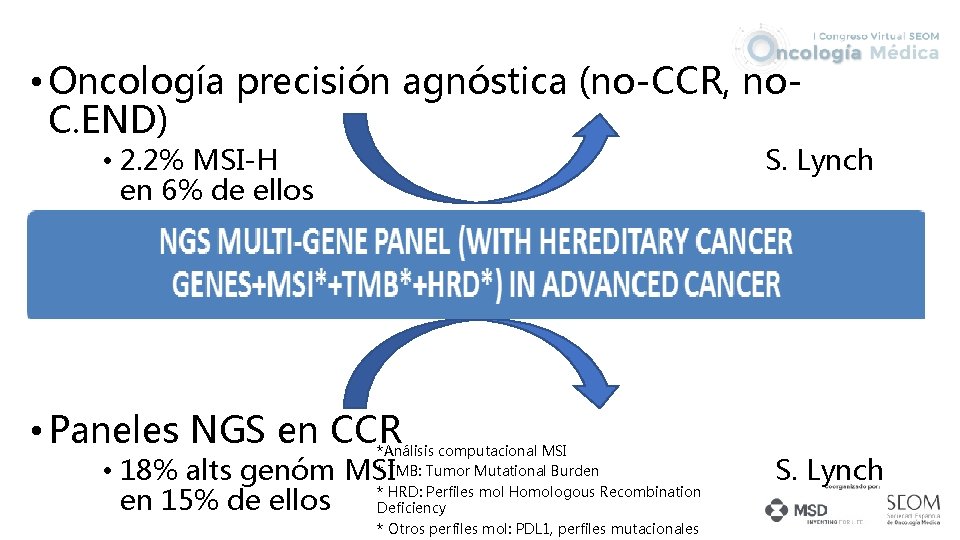
• Oncología precisión agnóstica (no-CCR, no. C. END) • 2. 2% MSI-H en 6% de ellos S. Lynch • Paneles NGS en CCR *Análisis computacional MSI * TMB: Tumor Mutational Burden * HRD: Perfiles mol Homologous Recombination Deficiency * Otros perfiles mol: PDL 1, perfiles mutacionales • 18% alts genóm MSI en 15% de ellos S. Lynch

Mutación germinal : no descartable asociación con perfil mutacional 1 (relacionado con relación edad), posible Abida W. JAMA Oncol. 2019; 5(4): 471 -

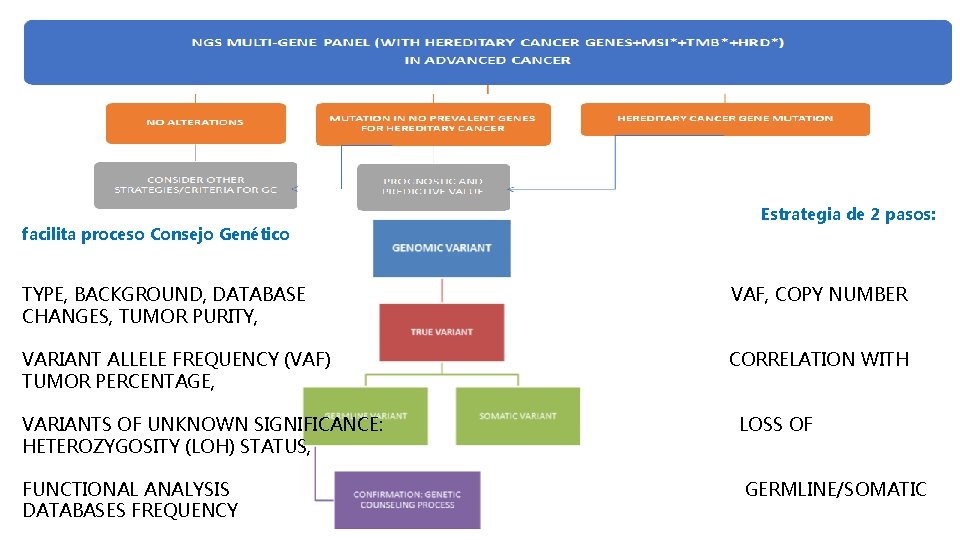
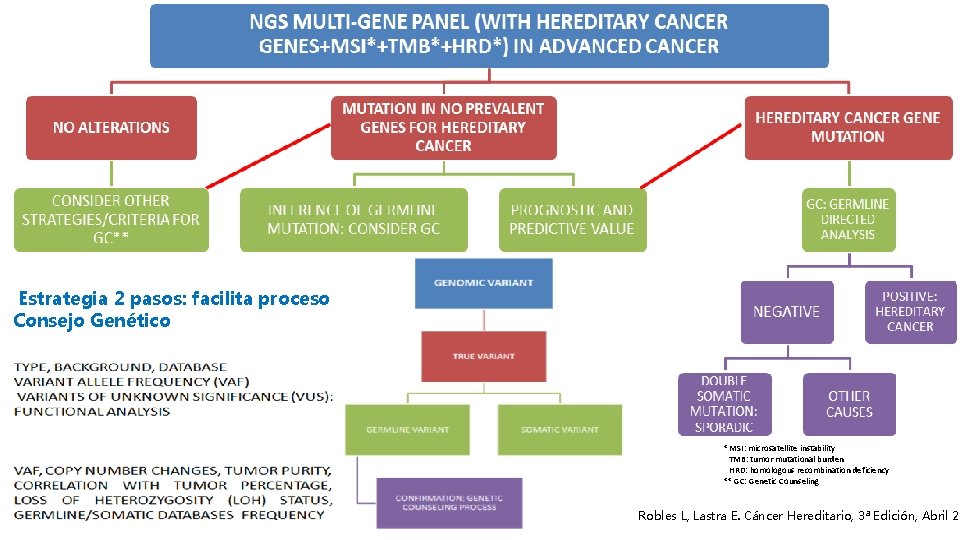
facilita proceso Consejo Genético Estrategia de 2 pasos: TYPE, BACKGROUND, DATABASE CHANGES, TUMOR PURITY, VAF, COPY NUMBER VARIANT ALLELE FREQUENCY (VAF) TUMOR PERCENTAGE, CORRELATION WITH VARIANTS OF UNKNOWN SIGNIFICANCE: HETEROZYGOSITY (LOH) STATUS, FUNCTIONAL ANALYSIS DATABASES FREQUENCY LOSS OF GERMLINE/SOMATIC

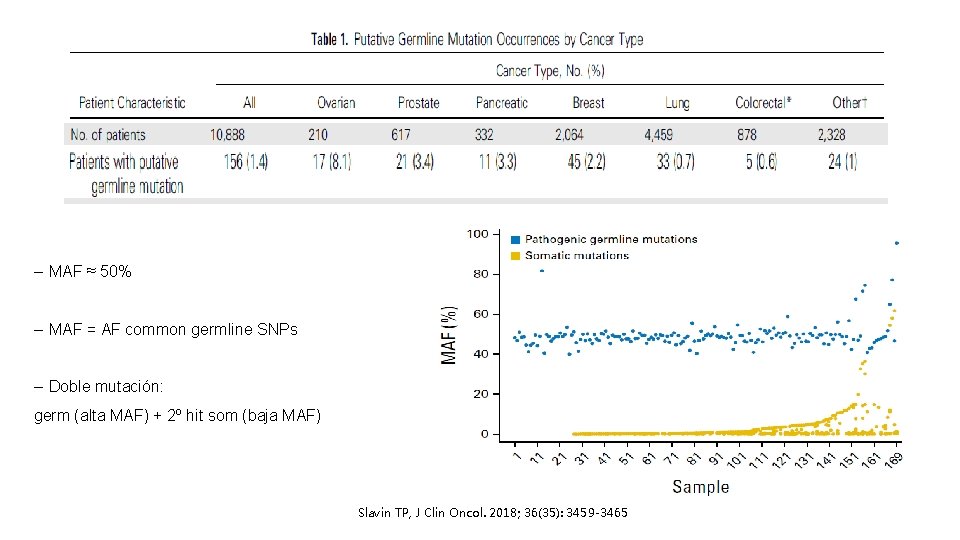
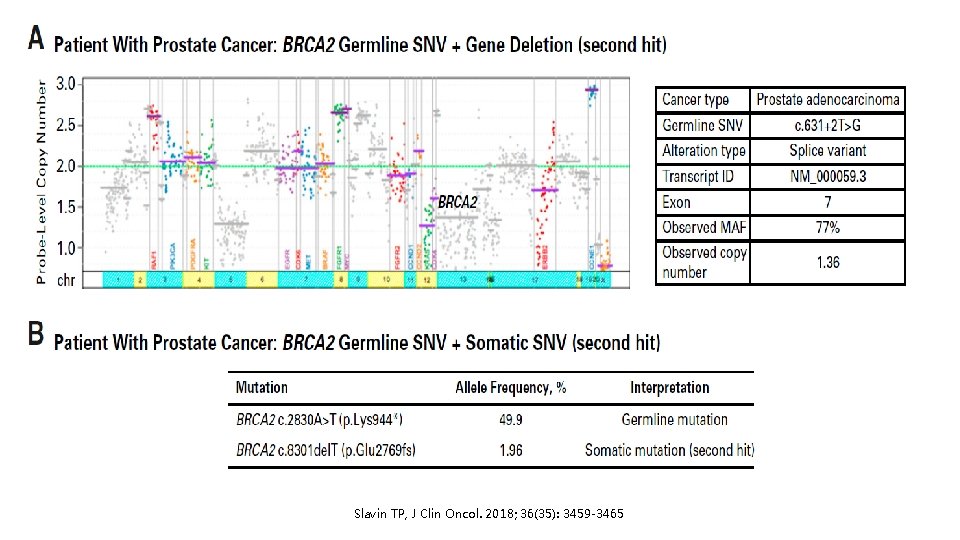
– MAF ≈ 50% – MAF = AF common germline SNPs – Doble mutación: germ (alta MAF) + 2º hit som (baja MAF) Slavin TP, J Clin Oncol. 2018; 36(35): 3459 -3465

Slavin TP, J Clin Oncol. 2018; 36(35): 3459 -3465

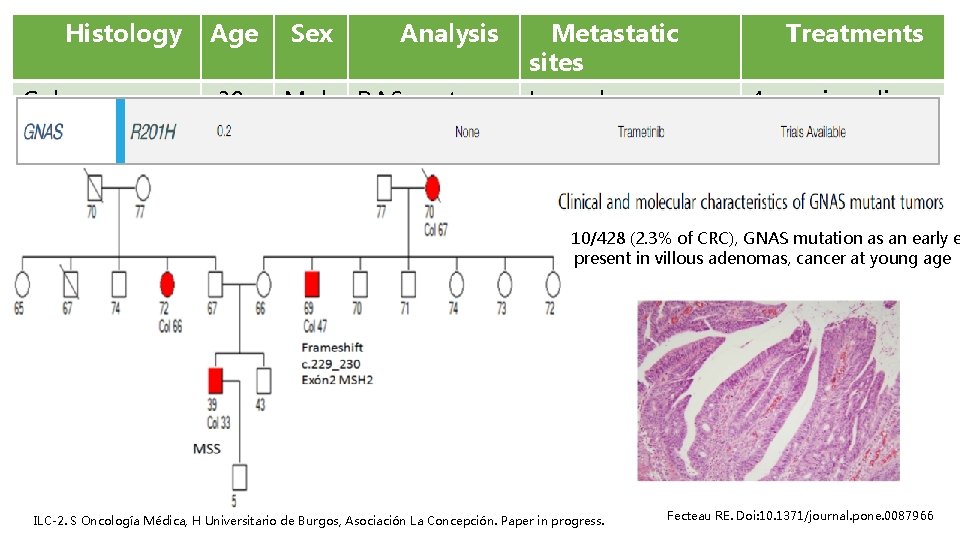
Histology Colon adenoca. Age Sex 39 Mal e Analysis RAS mut, MSS Metastatic sites Lung, bone, nodal Treatments 4 previous lines 10/428 (2. 3% of CRC), GNAS mutation as an early e present in villous adenomas, cancer at young age ILC-2. S Oncología Médica, H Universitario de Burgos, Asociación La Concepción. Paper in progress. Fecteau RE. Doi: 10. 1371/journal. pone. 0087966

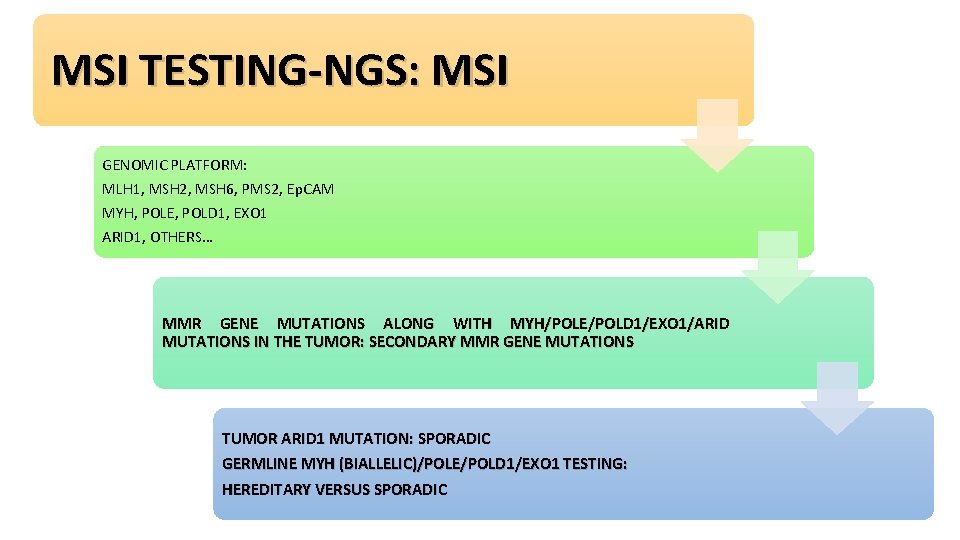
MSI TESTING-NGS: MSI GENOMIC PLATFORM: MLH 1, MSH 2, MSH 6, PMS 2, Ep. CAM MYH, POLE, POLD 1, EXO 1 ARID 1, OTHERS… MMR GENE MUTATIONS ALONG WITH MYH/POLE/POLD 1/EXO 1/ARID MUTATIONS IN THE TUMOR: SECONDARY MMR GENE MUTATIONS TUMOR ARID 1 MUTATION: SPORADIC GERMLINE MYH (BIALLELIC)/POLE/POLD 1/EXO 1 TESTING: HEREDITARY VERSUS SPORADIC

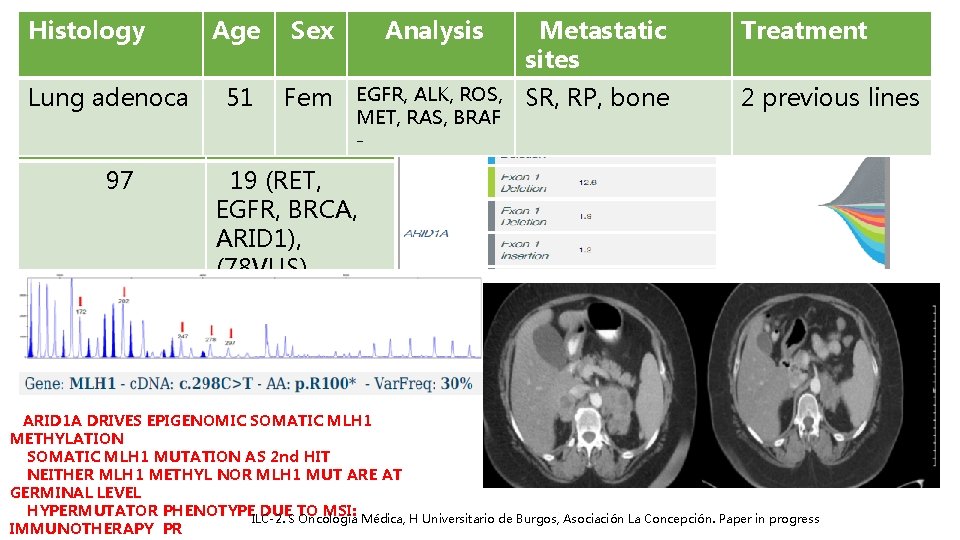
Histology Lung adenoca Genomic alts 97 Age Sex Analysis Metastatic sites Treatment 51 Fem EGFR, ALK, ROS, MET, RAS, BRAF - SR, RP, bone 2 previous lines Actionable 19 (RET, EGFR, BRCA, ARID 1), (78 VUS) ARID 1 A DRIVES EPIGENOMIC SOMATIC MLH 1 METHYLATION SOMATIC MLH 1 MUTATION AS 2 nd HIT NEITHER MLH 1 METHYL NOR MLH 1 MUT ARE AT GERMINAL LEVEL HYPERMUTATOR PHENOTYPE DUE TO MSI: ILC-2. S Oncología Médica, H Universitario de Burgos, Asociación La Concepción. Paper in progress IMMUNOTHERAPY PR

MSI TESTING-NGS: MSI GENOMIC PLATFORM: MLH 1, MSH 2, MSH 6, PMS 2, Ep. CAM MYH, POLE, POLD 1, EXO 1 ARID 1, OTHERS… DOUBLE MMR GENE MUTATION IN THE TUMOR SUSPECT SOMATIC BIALLELIC IF PIK 3 CA MUT GERMLINE TESTING: LYNCH SYNDROME VERSUS SPORADIC

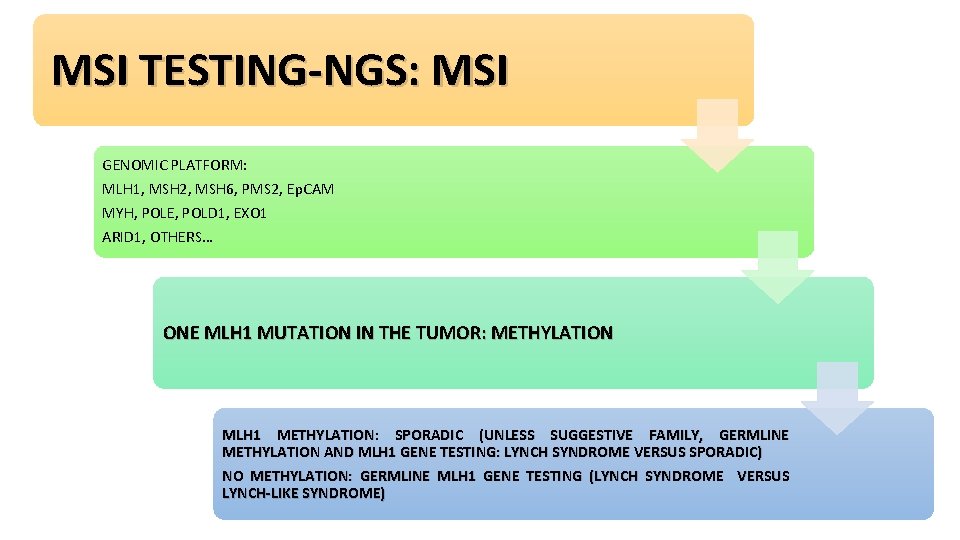
MSI TESTING-NGS: MSI GENOMIC PLATFORM: MLH 1, MSH 2, MSH 6, PMS 2, Ep. CAM MYH, POLE, POLD 1, EXO 1 ARID 1, OTHERS… ONE MLH 1 MUTATION IN THE TUMOR: METHYLATION MLH 1 METHYLATION: SPORADIC (UNLESS SUGGESTIVE FAMILY, GERMLINE METHYLATION AND MLH 1 GENE TESTING: LYNCH SYNDROME VERSUS SPORADIC) NO METHYLATION: GERMLINE MLH 1 GENE TESTING (LYNCH SYNDROME VERSUS LYNCH-LIKE SYNDROME)

MSI TESTING-NGS: MSI GENOMIC PLATFORM: MLH 1, MSH 2, MSH 6, PMS 2, Ep. CAM MYH, POLE, POLD 1, EXO 1 ARID 1, OTHERS… ONE MMR GENE MUTATION IN THE TUMOR (NO MLH 1) GERMLINE MMR GENE TESTING: LYNCH SYNDROME VERSUS LYNCH-LIKE SYNDROME

MSI TESTING-NGS: MSI GENOMIC PLATFORM: MLH 1, MSH 2, MSH 6, PMS 2, Ep. CAM MYH, POLE, POLD 1, EXO 1 ARID 1, OTHERS… NO MMR GENE MUTATIONS IN THE TUMOR: IHQ FOR MMR GENES DEFFICIENT PROTEIN GUIDES SUBSEQUENT STUDY AS IF A TUMOR MUTATION IN THE CODING MMR GENE HAD BEEN FOUND

ACTITUD EN LA PRÁCTICA CLÍNICA • Oncología de precisión agnóstica precede y modifica estrategias de diagnóstico en cáncer hereditario • No prevalencia elevada de MSI-H ni de S. Lynch en población no-CCR y no-C. END • Prevalencia S. Lynch >5% en MSI-H no-CCR y no-C. END • Paneles NGS-MSI: información integral conjunta perfiles moleculares y alteraciones genómicas • Estrategia 2 pasos: orientar proceso Consejo Genético desde la información molecular tumoral • Paneles NGS en CCR: validez analítica, clínica y

* MSI-H * enough MSI-H CRC, non-Endom ¿Germline NGS panel? No data of other syndromes in non- negative ¿tumor NGS? No enough Adaptado de Wang A. Health Sci Rep. 2018; 1: e 43. doi. org/10. 1002/hsr 2. 43 If

Estrategia 2 pasos: facilita proceso Consejo Genético * MSI: microsatellite instability TMB: tumor mutational burden HRD: homologous recombination deficiency ** GC: Genetic Counseling Robles L, Lastra E. Cáncer Hereditario, 3ª Edición, Abril 20

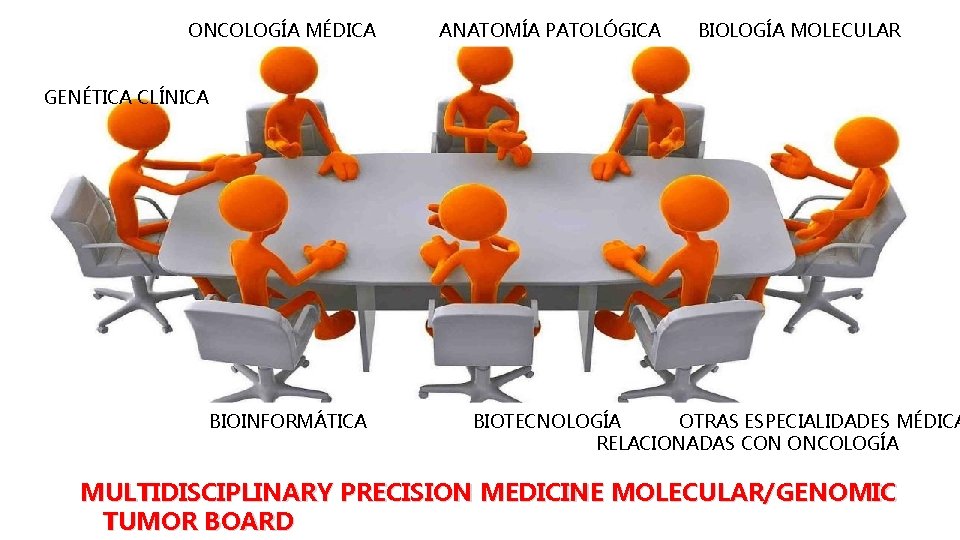
To ensure adequate interpretation, recommendation, and communication of tumor sequencing results, an MGTB should include professionals with knowledge and experience in clinical translation of tumor sequencing, testing methodology, molecular pathology, cancer biology, genomic pathways, germline variant interpretation, evaluation of family history, and application of professional recommendations for germline testing after tumor-only sequencing. These skills may not be held by a single professional on an MGTB. Fishler KP. JCO Precision Oncology. 2019; 3: 1 -8. https: //doi. org/10. 1200/PO. 18. 00216

ONCOLOGÍA MÉDICA ANATOMÍA PATOLÓGICA BIOLOGÍA MOLECULAR GENÉTICA CLÍNICA BIOINFORMÁTICA BIOTECNOLOGÍA OTRAS ESPECIALIDADES MÉDICA RELACIONADAS CON ONCOLOGÍA MULTIDISCIPLINARY PRECISION MEDICINE MOLECULAR/GENOMIC TUMOR BOARD

GRACIAS POR SU ATENCIÓN